Bài viết Áp lực đẩy và tử vong trong bệnh viện ở bệnh nhân không ARDS được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Driving Pressure and Hospital Mortality in Patients Without ARDS: A Cohort Study
TÓM TẮT
Tổng quan
Áp lực đẩy (ΔP) có liên quan đến tử vong ở bệnh nhân ARDS và với biến chứng phổi ở những bệnh nhân đang gây mê tổng quát. Nhưng ΔP có liên quan với kết cục của bệnh nhân không có ARDS đã được thông khí trong ICU không rõ. Mục tiêu của chúng tôi là xác định mối liên hệ độc lập giữa ΔP và kết cục ở bệnh nhân thở máy không có ARDS vào ngày 1 của thông khí cơ học.
Phương pháp
Đây là một phân tích hồi cứu của một nhóm gồm 622 bệnh nhân người lớn thông khí cơ học không có ARDS vào ngày 1 thở máy từ 5 ICU ở trung tâm đại học ở Hoa Kỳ. Kết quả chính là tử vong trong bệnh viện. Sự có mặt của ARDS đã được xác định sử dụng tỷ lệ tối thiểu PaO2/FiO2 (PF) hàng ngày và tìm kiếm tự động các báo cáo chụp X quang ngực. Bộ dữ liệu được xác nhận bằng cách thử nghiệm mô hình đầu tiên trong 543 bệnh nhân với ARDS.
Kết quả
Ở những bệnh nhân không có ARDS vào ngày 1 của thông khí cơ học, ΔP không liên quan độc lập với tử vong của bệnh viện (OR, 1,01, 95% CI, 0,97-1,05). Các kết quả của phân tích chính đã được khẳng định trong một loạt các phân tích độ nhạy trước.
Kết luận
Trong nhóm nghiên cứu của bệnh nhân không có ARDS vào ngày 1 của thông khí cơ học và trong giới hạn của thiết lập thông khí thông thường được sử dụng bởi các bác sĩ lâm sàng, ΔP không liên quan đến tử vong bệnh viện. Nghiên cứu này cũng khẳng định mối liên quan giữa ΔP và tỷ lệ tử vong ở bệnh nhân ARDS không tham gia thử nghiệm và ở những bệnh nhân thiếu oxy không có ARDS.
Việc sử dụng chiến lược thở máy có thể tích khí lưu thông thấp làm giảm tử vong ở bệnh nhân ARDS.[1,2] Chiến lược “bảo vệ phổi” này cũng liên quan đến việc giảm mức độ các dấu hiệu viêm và giảm các biến chứng về phổi sau khi gây mê tổng quát ở bệnh nhân không có ARDS.[3,4,5,6,7,8] Tuy nhiên, cách thức tối ưu để thiết lập máy thở để tránh thương tích phổi ở bệnh nhân không có ARDS vẫn còn đang tranh cãi.
Thông khí bảo vệ phổi bao gồm việc sử dụng VT giữa 4 và 8 mL/kg trọng lượng cơ thể dự đoán, tránh áp lực cao nguyên (PPLAT) cao, và sử dụng PEEP. Tuy nhiên, lựa chọn VT dựa trên trọng lượng cơ thể dự đoán và PPLAT là vấn đề đáng nghi ngờ.[9] Hơn nữa, cách tốt nhất để thiết lập PEEP còn gây tranh cãi.[10,11] Ngoài ra, chế độ thông khí khác nhau trong các nghiên cứu khác nhau.[2,12]
Một phương pháp hấp dẫn để thiết lập VT bao gồm việc bình thường hóa nó theo độ giãn nở của hệ thống hô hấp của bệnh nhân (CRS), thay đổi theo từng cá nhân và trong cùng một người theo số lượng phổi được tuyển dụng.[13] VT chia cho CRS là áp lực lái (ΔP). Các nghiên cứu gần đây cho thấy ΔP có liên quan đến tử vong ở bệnh nhân ARDS trong các thử nghiệm lâm sàng và cũng có liên quan đến biến chứng phổi sau khi gây mê tổng quát ở bệnh nhân không có ARDS.[14,15]
Khám phá mối liên quan giữa ΔP và tử vong ở bệnh nhân không có ARDS có hai mục đích. Thứ nhất, có những dữ liệu mâu thuẫn liên quan đến hiệu quả của thông khí bảo vệ phổi ở bệnh nhân không có ARDS.[16] Một mối liên quan giữa ΔP và tỷ lệ tử vong sẽ hỗ trợ cho một lập luận sử dụng một chiến lược hạn chế ΔP trong quần thể này. Thứ hai, phân tích dân số trong đó sự tuân thủ không liên quan đến tử vong có thể giải quyết vấn đề tiềm ẩn mối quan hệ giữa ΔP và tử vong bằng cách tuân thủ.
Phương pháp
Chọn dữ liệu
Nghiên cứu đoàn hệ này sử dụng giám sát thông minh đa điểm trong cơ sở dữ liệu Critical Care II.[17] Đây là một cơ sở dữ liệu lâm sàng có sẵn công khai có chứa thông tin về các thông số sinh lý của bệnh nhân, kết quả xét nghiệm trong phòng thí nghiệm và phóng xạ, thông số máy thở, và ghi chú văn bản miễn phí từ các nhà cung cấp dịch vụ chăm sóc. Nó bao gồm > 37,000 bệnh nhân ICU nằm từ 5 cơ sở chăm sóc đặc biệt tại một trung tâm y tế của Trung tâm Y tế Deaconess, Boston, MA từ năm 2001 đến năm 2008. Protocol cho nghiên cứu hiện tại đã được Hội đồng Đạo đức Nghiên cứu Trung tâm Khoa học Y tế Sunnybrook (số 068-2015).
Nhóm nghiên cứu
Chúng tôi bao gồm tất cả các bệnh nhân từ 15 tuổi trở lên đã tiếp nhận thông khí trong ít nhất 48 giờ trong khoảng thời gian thở máy đầu tiên. Chúng tôi đã phân tích dữ liệu từ ngày đầu tiên của ngày thông khí cơ học (ngày 1), kể từ khi thông khí cơ học được khởi động (ngày 0) có thời lượng biến đổi. Bệnh nhân được loại trừ khỏi tất cả các phân tích nếu họ đã được chuyển từ các bệnh viện khác và có thể đã nhận được thông khí cơ học trước khi chuyển bệnh, nếu họ thiếu thông tin nhập viện, nếu họ được thông khí với bất kỳ phương thức nào khác ngoài thông khí kiểm soát thể tích (VCV) hoặc thông khí kiểm soát áp lực (PCV) trong bất kỳ khoảng thời gian nào vào ngày 1 hoặc nếu họ nhận được thông khí với VCV và không có PPLAT đo được vào ngày thứ 1. Để phân tích có chứa VT, chúng tôi phải loại trừ bệnh nhân không đo chiều cao, do chúng tôi có thể không tính trọng lượng cơ thể dự đoán.
Chúng tôi áp dụng định nghĩa Berlin để loại trừ bệnh nhân có ARDS vào ngày 1 thở máy, sử dụng một công cụ đã được kiểm chứng trước đó mà chúng tôi thích nghi với dân số của chúng tôi.[18,19] Các công cụ kết hợp tỷ lệ PF hàng ngày với kết quả tìm kiếm X quang ngực, các báo cáo đã được thực hiện trong vòng 1 ngày theo lịch. Bệnh nhân thiếu thông tin được phân loại là có ARDS được coi là không có ARDS. Chúng tôi đề cập đến tiềm năng thiên vị đối với giả thuyết khác có thể phát sinh từ quyết định này trong các phân tích độ nhạy được mô tả thêm.
Biến tiếp xúc
Biến tiếp xúc chính là đo ΔP theo thời gian vào ngày 1 của thông khí cơ học, được tính trung bình kết quả của PPLAT – PEEP trong ngày 1 của thông khí. Trung bình, năm (khoảng interquartile [IQR], 4-6) đo PPLAT cho mỗi bệnh nhân vào ngày 1 của thông khí cơ học trong cơ sở dữ liệu. Ở những bệnh nhân đã được thông khí bằng PCV, chúng tôi sử dụng áp lực đỉnh làm đại diện cho PPLAT. Ở bệnh nhân thông khí với hai chế độ trong ngày 1, chúng tôi tính toán trung bình của PPLAT mỗi lần dành cho mỗi chế độ thở máy. Chúng tôi loại trừ giá trị không thể, chẳng hạn như PPLAT ít hơn PEEP.
Ngoài ra, chúng tôi đã kiểm tra VT trung bình theo thời gian được hiệu chỉnh với trọng lượng cơ thể dự đoán và CRS trung bình theo thời gian như các biến số phơi nhiễm. Chúng tôi tính trọng lượng cơ thể dự đoán dựa trên chiều cao và giới tính của bệnh nhân.[2] Chúng tôi tính toán độ giãn nở từ VT và ΔP (VT/ΔP).
Trùng biến
Đối với phân tích đa biến, chúng tôi bao gồm các biến số dự báo về tử vong, những yếu tố có thể ảnh hưởng đến việc lựa chọn các thiết lập thông khí và các thông số thông khí quan trọng khác không đồng nhất với ΔP. Những điều này đã được chỉ định trước. Mô hình bao gồm điểm số sinh lý học cấp tính giản đơn (SAPS) khi nhập viện, tuổi tác, chỉ số kết hợp Elixhauser khi nhập viện, chẩn đoán khi nhập viện, PaCO2 cao nhất vào ngày 1 và tỷ lệ PF thấp nhất trong ngày 1.[20,21,22] Chúng tôi không bao gồm các biến được kết nối toán học với nhau, chẳng hạn như ΔP và VT hoặc độ giãn nở trong cùng một mô hình.
Kết quả
Kết quả chính là tử vong trong bệnh viện. Để kiểm tra tính nhất quán của kết quả của chúng tôi, chúng tôi đã kiểm tra tỷ lệ tử vong ICU và tỷ lệ tử vong 6 tháng là kết cục thứ phát.
Xác nhận phân loại ARDS
Để xác nhận tính phân loại ARDS tự động của chúng tôi, chúng tôi đã sử dụng mô hình của Amato và cộng sự [14] ở các bệnh nhân được phân loại có ARDS. Chúng tôi dự kiến sẽ tìm thấy một mối liên kết độc lập giữa ΔP và tử vong ở những bệnh nhân này.
Phân tích thống kê
Để kiểm tra mối liên kết độc lập giữa ΔP và tỷ lệ tử vong ở bệnh viện, chúng tôi đã thực hiện hồi quy logistic đa biến. Sau đó chúng tôi lặp lại phân tích cho mỗi kết quả thứ cấp. Chúng tôi lặp lại các phân tích tương tự cho CRS và VT một cách riêng biệt. Chúng tôi bao gồm các biến số nhiễu tương tự trong mỗi phân tích và thực hiện phân tích trường hợp hoàn chỉnh (những bệnh nhân bị thiếu các giá trị của các biến số liên quan trong mô hình đã được loại trừ khỏi các phân tích).
Một số phân tích độ nhạy đã được xác định đã được tiến hành để kiểm tra tính mạnh mẽ của các phát hiện của chúng tôi. Trước tiên, chúng tôi đã kiểm tra hiệu quả của các nỗ lực thở tự phát bằng cách xác định những bệnh nhân đã kích hoạt máy thở, trong đó PPLAT có thể không phải là một đại diện hợp lệ cho áp lực phổi, sử dụng sự khác biệt giữa tổng và tỷ lệ hô hấp được thiết lập. Chúng tôi đánh giá biến này với một thuật ngữ tương tác để kiểm tra xem sự liên quan giữa phơi nhiễm ban đầu và kết quả đã được sửa đổi bằng cách thông khí tự phát.
Thứ hai, chúng tôi đã kiểm tra nếu bệnh nhân không được phân loại là có ARDS nhưng thiếu thông tin cần thiết để phân loại chắc chắn là không có ARDS (phân loại tương đối) cư xử khác với những người có tất cả các thông tin cần thiết bằng cách thêm một thuật ngữ tương tác với mô hình. Chúng tôi tiến hành kiểm tra chỉ những bệnh nhân có các tiêu chí để xác định chắc chắn ARDS đang vắng mặt bằng cách loại trừ những người có phân loại tương đương.
Cuối cùng, chúng tôi chia cho tất cả các bệnh nhân là thiếu oxy máu (PF ratio ≤ 300) hoặc không thiếu oxy máu (PF ratio > 300) bất kể kết quả chụp X quang phổi. Chúng tôi đã làm điều này vì có sự khác biệt đáng kể trong việc giải thích chụp X quang ngực, ngay cả khi được đánh giá bởi các chuyên gia.[23] Chúng tôi đã cân nhắc việc thực hiện phân tích hòa giải (mediation analysis); phân tích như vậy nên được thực hiện chủ yếu trong một thử nghiệm đối chứng ngẫu nhiên khi một mối quan hệ nhân quả đã được thiết lập.[24]
Các biến phân loại được mô tả như là tỷ lệ (%) và các biến liên tục là trung vị (IQR) đối với các biến hoặc các phương tiện phân phối không bình thường (SD) cho các biến phân phối bình thường. χ2 test, t-test hoặc các bài kiểm tra tổng hợp hạng Wilcoxon đã được sử dụng cho các biến liên tục phân loại phân bố, bình thường phân bố và không bình thường.
Chúng tôi đã phân tích và báo cáo nghiên cứu này theo Strengthening the Reporting of Observational Studies in Epidemiology guidelines.[25] Chúng tôi thực hiện tất cả các phân tích thống kê sử dụng Stata, phiên bản 13 (StataCorp LLC).
Kết quả
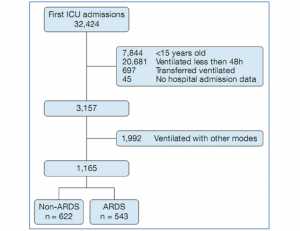
Trong số 3.899 bệnh nhân đáp ứng được tiêu chí thu nhận, có 45 bệnh nhân thiếu thông tin nhập viện, 697 người có thể đã được thông khí trước khi chuyển và 1.992 đã nhận được các phương thức thông khí ngoài VCV hoặc PCV vào ngày 1 và đã bị loại trừ (Hình 1). Trong số 1.165 bệnh nhân còn lại, 543 được phân loại là có ARDS, để lại 622 bệnh nhân cho phân tích ban đầu (Bảng 1). Trong số những bệnh nhân không có ARDS, 151 người không có tỷ số PF vào ngày 1 (n = 1) hoặc chụp X quang phổi trong vòng 1 ngày lịch (trước hoặc sau) hoặc đo khí máu động mạch (n = 137) hoặc kết hợp (n = 13). Chúng tôi tóm tắt sự khác biệt giữa bệnh nhân với ARDS và những người không có để cung cấp cái nhìn sâu sắc hơn về độ chính xác của việc phát hiện tự động của chúng tôi (e-Bảng 1).
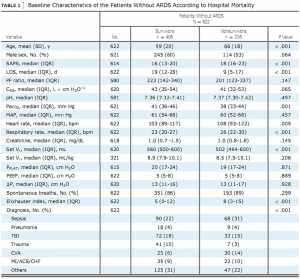
Trong các biến được sử dụng trong phân tích sơ cấp, tỷ lệ PF là tỷ lệ thiếu nhất (e-Bảng 2). Kiểm tra hiệu quả của VT theo trọng lượng cơ thể dự đoán bị cản trở bởi nhiều phép đo chiều cao bị thiếu trong bộ dữ liệu.
Phương thức thông khí phổ biến nhất là VCV, và 608 bệnh nhân nhận duy nhất VCV. Chỉ có 8 bệnh nhân nhận PCV riêng và sáu người khác đã nhận được kết hợp cả hai chế độ trong cung ngày 1.
Xác nhận trong bệnh nhân ARDS
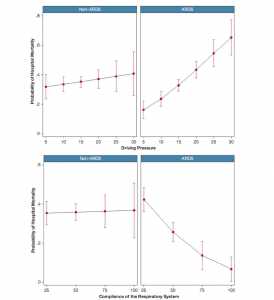
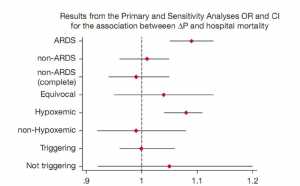
Ở bệnh nhân ARDS, ΔP được kết hợp độc lập với tử vong trong bệnh viện (OR 1,09, 95% CI, 1,05- 1,13) (Hình 2, e-Bảng 3), tử vong trong ICU (OR 1,10, 95% CI, 1,06-1,14) và tử vong 6 tháng (OR, 1,09, 95% CI, 1,05-1,14). CRS cũng có liên quan đến tử vong ở bệnh nhân ARDS (OR, 0,97, 95% CI, 0,96-0,99). Không có sự liên quan đáng kể giữa VT được điều chỉnh với dự đoán trọng lượng cơ thể và tử vong ở bệnh nhân ARDS (OR, 1,06, 95% CI, 0,92-1,22).
Kết cục chính và phụ
Ở những bệnh nhân không có ARDS vào ngày 1 thở máy, ΔP không liên quan độc lập với tử vong trong bệnh viện (OR, 1,01, 95% CI, 0,96-1,05) (Hình 2, Bảng 2), tử vong trong ICU (OR, 1,05; 95% CI, 0.99-1.10), hoặc tử vong trong 6 tháng (OR, 1.02, 95% CI, 0.97-1.06).
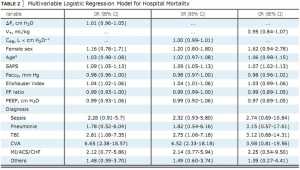
CRS (OR, 1,00, 95% CI, 0,99-1,01) và VT không điều chỉnh (OR, 0,95, 95% CI, 0,85-1,07) (Bảng 2) cũng không liên quan đến tử vong trong bệnh viện ở bệnh nhân không có ARDS.
Phân tích độ nhạy
Không có sự tương tác có ý nghĩa thống kê giữa các bệnh nhân kích hoạt máy thở và mối liên quan giữa ΔP và tử vong. Chúng tôi cũng thấy không có sự tương tác giữa phân loại ARDS tương đồng và ΔP (P = 0,89 tương tác). Khi chúng tôi loại trừ các bệnh nhân có phân loại tương đương, chúng tôi đã có kết quả tương tự cho mối liên hệ giữa ΔP và tỷ lệ tử vong ở bệnh viện (OR, 0,99, 95% CI, 0,94-1,05) (Hình 3).
Khi kiểm tra tất cả bệnh nhân, có một sự tương tác đáng kể giữa tỷ lệ ΔP và PF (P = .007 đối với sự tương tác). Ở bệnh nhân có tỷ lệ PF ≤ 300, ΔP có liên quan độc lập với tử vong trong bệnh viện (OR = 1.08, 95% CI, 1.04-1.11), nhưng ở nhóm có tỷ lệ PF > 300 thì không có (OR, 0.99, 95% CI, 0.92- 1.08). CRS có liên quan đến tỷ lệ tử vong ở bệnh nhân thiếu oxy máu (OR, 0.99, 95% CI, 0.97-0.99) nhưng không thấy ở bệnh nhân không thiếu oxy máu (OR, 1.01, 95% CI, 0.99-1.03). Cuối cùng, chia dữ liệu thành các phần tứ phân không mang lại kết quả khác và không chứng minh sự không tuyến tính.
Bàn luận
Trong nghiên cứu này, chúng tôi đã chỉ ra rằng ΔP vào ngày 1 không liên quan đến tử vong ở bệnh viện trong một nhóm bệnh nhân nặng mà không có ARDS đã được thông khí trong 48 giờ hoặc nhiều hơn. Theo hiểu biết của chúng tôi, đây là nghiên cứu đầu tiên để giải quyết câu hỏi này. Chúng tôi cũng đã xác nhận quan sát trước rằng ΔP có liên quan đến tử vong ở bệnh nhân ARDS trong một mẫu bệnh nhân không tham gia vào một thử nghiệm lâm sàng.[14] Hơn nữa, chúng tôi thấy rằng ΔP ảnh hưởng đến các bệnh nhân có tỷ lệ PF ≤ 300 bất kể kết quả của chụp X quang ngực hoặc, do đó, chẩn đoán ARDS.
Có một số giải thích có thể cho việc thiếu liên kết giữa ΔP và tử vong ở bệnh viện ở bệnh nhân không có ARDS. Thứ nhất, ΔP là một cách để đại diện cho VT được điều chỉnh cho độ giãn nở và có thể được tính toán từ những con số này.[26] Vì vậy, nó nên được kết hợp với tử vong ở bệnh nhân ARDS, vì nó thể hiện cả mức độ tổn thương phổi và mức độ VT cung cấp. Không có bằng chứng cho thấy độ giãn nở là yếu tố nguy cơ chính cho tử vong ở bệnh nhân không có ARDS, và trong nghiên cứu của chúng tôi, nó không liên quan đến tỷ lệ tử vong trong bệnh viện trong phân tích điều chỉnh. Vì vậy, không nên ngạc nhiên khi một “VT điều chỉnh theo độ giãn nở” không liên quan đến tử vong.
Trên thực tế, hiệu quả có lợi của thở máy VT thấp ở bệnh nhân không có ARDS vẫn được thể hiện rõ ràng. Phân tích gộp của Serpa Neto và cộng sự,[27] thường được coi là bằng chứng về mối liên quan giữa VT và tử vong cao, bao gồm các nghiên cứu quan sát hoặc bán ngẫu nhiên, và khi phân tích tỷ lệ tử vong dựa nhiều vào dữ liệu từ một nghiên cứu đồng thời giảm VT và truyền máu.
Một phân tích gộp khác của các nhà nghiên cứu đã tìm ra mối liên quan giữa VT và biến chứng phổi ở bệnh nhân không có ARDS.[28] Các nghiên cứu khác đã tìm ra mối liên quan giữa VT tuyệt đối lớn và sự phát triển của ARDS, và gần đây hơn trong một phân tích gộp khác, Neto và cộng sự sự kết hợp giữa cao ΔP trong gây mê toàn thân và nhiều biến chứng phổi sau khi phẫu thuật.[29,30] Những nghiên cứu này có điểm chung là sự liên kết không xảy ra với tử vong nhưng có với các biến chứng khác. Ngoài ra, nghiên cứu duy nhất kiểm tra ΔP đã làm như vậy trong một quần thể hoàn toàn khác nhau và, một lần nữa, sử dụng một kết quả khác.
Thứ hai, chỉ có 11% bệnh nhân không có ARDS và 18% bệnh nhân ARDS không có tần số thở tự phát lớn hơn tần số thở được thiết lập. Trong một hít thở có trợ giúp, bệnh nhân tạo ra một phần trong tổng số công thở, và PPLAT đo được có thể là một đại diện kém cho áp lực phổi. Mặc dù báo cáo gần đây của Bellani và cộng sự cho thấy PPLAT có thể được đo lường một cách tin cậy ở những bệnh nhân được thở hỗ trợ áp lực, nhưng chúng tôi không có cách nào để xác định tính chính xác của các phép đo có trong tập dữ liệu. Ngoài ra, mối liên quan giữa tỷ lệ tử vong và ΔP ở bệnh nhân ARDS được xác định ở những bệnh nhân mà họ tin rằng không có nỗ lực về hô hấp.
Thứ ba, bệnh nhân không có ARDS nhận được mức PEEP đồng đều. Muscedere et al [32] cho thấy phổi thông khí có thể tích nhỏ hơn và PEEP ít hơn điểm uốn dưới của đường cong áp lực thể tích dẫn đến tổn thương phổi do thở máy gây ra. Sự kết hợp giữa PEEP thấp và ΔP thấp có thể có những tác động tương tự trong tập dữ liệu này. Sự khác biệt rất nhỏ trong PEEP ở bệnh nhân không có ARDS đã cản trở việc thăm dò thêm sự tương tác giữa PEEP và VT trong quần thể này.
Cuối cùng, bộ dữ liệu của chúng tôi có thể không có khả năng phát hiện mối liên hệ giữa ΔP và tử vong hoặc có thể, như trong bất kỳ cơ sở dữ liệu lâm sàng, chứa các phép đo giả mạo, làm tăng nhiễu và can thiệp vào việc tìm ra mối liên hệ thực tế. Kết quả từ dữ liệu của chúng tôi tương thích với một sự khác biệt kéo dài sự giảm 4% đến tăng 5% tỷ lệ chết cho mỗi centimet H2O tăng trung bình ΔP vào ngày đầu tiên của thông khí cơ học. Tuy nhiên, chúng ta phải lưu ý rằng sự khác biệt thật sự có xu hướng hướng tới trung tâm của khoảng đó.[33]
Những hạn chế quan trọng của nghiên cứu của chúng tôi là khả năng phân loại sai ARDS và thực tế là dữ liệu để đưa ra quyết định đó đã mất đi ở khoảng 13% bệnh nhân. Để giảm thiểu những hạn chế tiềm ẩn này, chúng tôi đã tiến hành các phân tích độ nhạy cảm cho thấy sự thiếu liên kết giữa ΔP và tỷ lệ tử vong ở bệnh nhân có tỷ lệ PF > 300, rõ ràng không có ARDS, và những người có dữ liệu đầy đủ. Hơn nữa, sự không chắc chắn trong phân loại X quang ngực không chỉ dừng lại ở nghiên cứu cơ sở dữ liệu hoặc nghiên cứu hồi cứu.[23] Một hạn chế nữa là khả năng đo PPLAT sai trong dữ liệu, điều này sẽ ảnh hưởng đến ΔP được quan sát. Tuy nhiên, các phép đo này được thực hiện và ghi lại bởi các nhà trị liệu về hô hấp được huấn luyện trong một trung tâm học thuật lớn. Việc giải thích kết quả của chúng ta nên lưu ý rằng những dữ liệu này đến từ một trung tâm duy nhất, làm giới hạn khả năng khái quát hóa. Cuối cùng, kết quả của chúng tôi chỉ áp dụng cho bệnh nhân nhận được các chế độ thông khí kiểm soát, và chúng tôi loại trừ hơn một nửa số bệnh nhân không có ARDS nhận được các chế độ thông khí tự phát.
Nghiên cứu của chúng tôi có một số điểm mạnh. Đây là nghiên cứu đầu tiên tìm hiểu mối liên quan giữa ΔP và tỷ lệ tử vong ở bệnh nhân không ARDS. Chúng tôi xác nhận tập dữ liệu của chúng tôi bằng cách đầu tiên phân tích bệnh nhân có ARDS và chỉ sau đó phân tích bệnh nhân không có ARDS. Hơn nữa, một số phân tích độ nhạy đã được thực hiện để giải thích cho sự khác biệt có thể xảy ra trong các phân nhóm, tôn trọng giới hạn tiềm năng của các phân tích nhóm phân nhóm.[34,35,36]
Sử dụng ΔP để cài đặt máy thở là một khái niệm thú vị xứng đáng để khám phá thêm. Rõ ràng, các bệnh nhân khác nhau có thể tích phổi khác nhau theo giới tính và chiều cao của họ nhưng cũng theo các quá trình bệnh lý và đặc điểm cá nhân của họ.[13] ΔP, như là một VT điều chỉnh theo độ giãn nở, có thể cung cấp một cách cá nhân hoá các thiết lập của máy thở cho mỗi bệnh nhân. Tuy nhiên, một số câu hỏi cần phải được trả lời trước khi áp dụng nó vào thực tiễn lâm sàng. Kết hợp với tỷ lệ tử vong ở bệnh nhân ARDS có thể không chuyển thành kết quả tốt hơn nếu nó được sử dụng như là một mục tiêu của máy thở, như thường xảy ra với các thông số sinh lý.[37] Ngoài ra, không biết liệu thiết lập máy thở bằng cách nhắm mục tiêu một ΔP nhất định sẽ dẫn đến những thay đổi đáng kể trong chính nó.
Một chiến lược khác có thể bao gồm việc sử dụng ΔP để thiết lập PEEP, nhằm mục tiêu một VT đã cho thấy giảm tử vong. Thật không may, các chiến lược tại giường mà PEEP đặt mục tiêu để cải thiện độ giãn nở không cải thiện việc tuyển dụng phổi khi được đo bằng hình ảnh CT.[11]
Nghiên cứu của chúng tôi cho thấy rằng thông khí ΔP ở những bệnh nhân không có ARDS đặt ra nhiều câu hỏi hơn so với bệnh nhân ARDS, vì không có mối liên quan giữa ΔP và kết cục bệnh nhân trong dữ liệu của chúng tôi. Chúng tôi tin rằng điều quan trọng là nhấn mạnh rằng nghiên cứu của chúng tôi đã kiểm tra mối liên hệ giữa tử vong và “thực tế” ΔP. Nó không mâu thuẫn với những phát hiện ban đầu rằng thể tích hoặc áp lực rất cao gây tổn hại phổi cho phổi lành tính, vì áp lực và thể tích trong bộ dữ liệu không đạt được mức độ thí nghiệm đầu tiên để đạt được hiệu quả đó.[38] Các kết quả cần phải được giải thích một cách nhẹ nhàng của phạm vi hẹp của PEEP và phạm vi CRS tương đối hẹp.
Kết luận
ΔP không liên quan đến tỷ lệ tử vong ở bệnh viện trong một nhóm bệnh nhân có thở máy mà không bị ARDS, trong đó độ giãn nở hệ hô hấp cũng không liên quan đến tử vong. Phát hiện của chúng tôi cần phải được nhân rộng trong các nhóm bệnh nhân khác.





