Tác giả: Bác sĩ Đặng Thanh Tuấn
Tóm tắt
Chế độ thông khí tiên tiến cho trẻ sơ sinh cố gắng giảm tổn thương phổi do thể tích gây ra, để giảm áp lực đường thở và sự tiếp xúc với oxy, và cải thiện sự thoải mái của bệnh nhân. Thông khí nhắm mục tiêu theo thể tích dẫn đến thể tích khí lưu thông phù hợp hơn, cho phép tự động cai áp lực đường thở, có thể tránh được giảm PaCO2 máu và có thể liên quan đến giảm tỷ lệ mắc bệnh lý lâm sàng mãn tính. Thông khí hỗ trợ áp lực cho phép bệnh nhân kiểm soát thời gian của nhịp thở cơ học. Nó đòi hỏi một trung tâm kiểm soát hô hấp ổn định hoặc dự phòng cho ngưng thở. Thông khí hỗ trợ áp lực có thể có hiệu quả cho cai máy thở. Thông khí hỗ trợ theo tỷ lệ được nghiên cứu ở các loài động vật nhỏ. Ở trẻ sinh non mắc bệnh phổi cấp tính và mãn tính, yêu cầu áp lực máy thở thấp hơn so với các so sánh ngắn hạn chéo với thông khí kích thích thông thường. Hỗ trợ thông khí được điều chỉnh theo thần kinh mang đến áp lực máy thở theo tỷ lệ và đồng bộ với hoạt động điện cơ hoành được thực hiện từ các điện cực trong thực quản. Các thử nghiệm lâm sàng đa trung tâm lớn được yêu cầu để chứng minh lợi ích lâm sàng lâu dài của các chế độ mới này.
Giới thiệu
Suy hô hấp thường gặp ở trẻ non tháng rất nhẹ cân (ELBW) và có liên quan với tỷ lệ mắc bệnh cao bao gồm loạn sản phế quản phổi (BPD, bronchopulmonary dysplasia).[1] Sinh bệnh học của BPD là đa yếu tố. Các nguyên nhân bao gồm chấn thương phổi do thở máy.[2] Gần đây Sharma và Greenough [3] đã khảo sát tất cả 228 đơn vị sơ sinh ở Anh. Ở đó, chế độ thông khí cơ học thường sử dụng nhất cho trẻ sinh non trong giai đoạn cấp của hội chứng suy hô hấp (RDS) là thông khí áp lực dương ngắt quãng thông thường (73% đơn vị ICU sơ sinh), tức là thông khí giới hạn áp lực theo chu kỳ thời gian (TCPLV, time – cycled pressure – limited ventilation). Ngược lại, khi cai máy thở, chế độ ưu tiên (73% đơn vị ICU sơ sinh) là sử dụng thông khí bắt buộc ngắt quãng đồng bộ (SIMV, synchronised intermittent mandatory ventilation). It ưu tiên hơn là hỗ trợ/kiểm soát (A/C, 15%) và thông khí đảm bảo thể tích (VGV, 5%).
Trong chương này, chúng tôi xem xét các bằng chứng cho các lợi ích lâm sàng của các chế độ thông khí được giới thiệu gần đây so với các chế độ truyền thống cho trẻ sơ sinh. Thông khí nhắm mục tiêu theo thể tích, thông khí hỗ trợ áp lực (PSV) và thông khí hỗ trợ tỷ lệ (PAV) về mặt lý thuyết có thể làm giảm tổn thương phổi do máy thở gây ra và cải thiện kết cục lâm sàng lâu dài. Chúng tôi cũng xem xét trợ giúp thông khí được điều chỉnh theo thần kinh (NAVA).[4] NAVA đã được thử nghiệm ở người lớn và đã được cung cấp cho trẻ sơ sinh ở châu Âu.
Các phương pháp thông khí giới hạn áp lực, chu kỳ thời gian (TCPLV)
Trong TCPLV, bác sĩ lâm sàng đặt áp lực dương cuối thì thở ra (PEEP) để huy động phế nang và duy trì dung tích cặn chức năng.
Thể tích khí lưu thông của nhịp thở cơ học phụ thuộc vào sự khác biệt giữa PEEP và áp lực đỉnh thì hít vào (PIP) cài đặt, thời gian hít vào (Tin) và các đặc tính cơ học của hệ hô hấp. Tin được kết hợp với thời gian thở ra (Tex) xác định tốc độ thông khí. Chế độ này được gọi là thông khí áp lực dương ngắt quãng (IPPV). Các chế độ A/C và SIMV sử dụng các thiết bị kích hoạt để đồng bộ hóa sự khởi đầu của các nỗ lực hô hấp tự phát và làm tăng áp lực máy thở lên. A/C đáp ứng tất cả các nhịp thở tự phát được phát hiện bằng cách cung cấp một nhịp thở cơ học đầy đủ. SIMV cho phép thời gian thở tự phát giữa nhịp thở hỗ trợ của máy thở. Mức độ tổn thương phổi do máy thở gây ra thường là do áp lực cuối thì hít vào.
Tuy nhiên, các nghiên cứu thực nghiệm cho thấy rằng mức độ của thể tích khí lưu thông cao (volutrauma) có liên quan chặt chẽ hơn với tổn thương phổi do máy thở gây ra hơn là áp lực cuối thì hít vào cao. Một thử nghiệm ngẫu nhiên có đối chứng đa trung tâm (RCT) ở người lớn bị hội chứng suy hô hấp cấp cho thấy thể tích khí lưu thông 6 mL/kg khi so sánh với thể tích khí lưu thông lớn hơn (12 mL/kg) có liên quan đến tỷ lệ tử vong thấp hơn.[6]
Các trẻ sơ sinh, khi so sánh với các đối tượng lớn tuổi, có thành ngực đàn hồi hơn làm tăng độ giãn nở (compliance) hệ thống hô hấp và kéo dài hằng số thời gian (time constant) hệ thống hô hấp. Áp lực áp dụng cho phổi sơ sinh sẽ dễ dàng dẫn đến quá căng phổi và gây ra volutrauma hơn là có thể xảy ra ở những người lớn tuổi hơn. Hơn nữa, trong TCPLV, một phương pháp thông khí áp lực nhắm mục tiêu, thể tích khí lưu thông có thể thay đổi nhanh chóng khi các đặc tính cơ học hô hấp thay đổi. Những thay đổi này có thể xảy ra nhanh chóng trong và sau khi dùng surfactant ngoại sinh. Trẻ sơ sinh sinh non do nỗ lực hô hấp thay đổi nhanh chóng sẽ ảnh hưởng nhiều đối với áp lực phổi thay đổi. Điều này dẫn đến thể tích khí lưu thông biến thiên cao.
Do đó, việc cung cấp một lượng khí lưu thông phù hợp giới hạn trong phạm vi sinh lý thấp có thể làm giảm volutrauma và tạo nên lợi ích về lâm sàng.
Các phương pháp thông khí hướng mục tiêu thể tích khí lưu thông
Đặc điểm của chế độ đặc biệt
Các chế độ này đã được xem xét chi tiết ở nơi khác.[7] Tất cả đều nhằm mục đích cung cấp phù hợp thể tích khí lưu thông do người vận hành cài đặt. Lý tưởng nhất, thể tích cung cấp là một tham số độc lập trong khi PIP phụ thuộc vào độ giãn nở hệ thống hô hấp.
Thuật ngữ ‘thông khí kiểm soát thể tích’ hoặc ‘thông khí chu kỳ thể tích’ (VCV, volume- cycled ventilation) mô tả các kỹ thuật thông khí trong đó máy thở cung cấp thể tích hít vào định sẵn hằng định vào bộ dây máy thở (ventilator circuit) và phổi. Tuy nhiên, một số lượng khí cung cấp có thể không đến phổi. Thể tích ‘bị mất’ (compressible volume) bằng cách nén bên trong bộ dây máy thở và buồng tạo độ ẩm cao hơn khi thể tích bộ dây máy thở lớn và PIP cao hơn. Một cảm biến lưu lượng (flow sensor) đặt giữa đoạn nối Y của bộ dây máy thở và ống nội khí quản có thể làm giảm bớt vấn đề này. Một rò rỉ xung quanh ống nội khí quản là một nguồn mất thể tích khác trong thì hít vào. Tuy nhiên, phép đo cả thể tích khí lưu thông trong hít vào và thở ra cho phép máy thở để tính toán thể tích rò rỉ và bù cho tổn thất thể tích.
Kiểm soát thể tích điều chỉnh áp lực (PRVC, Pressure-regulated volume control) là một chế độ cung cấp ban đầu một thể tích thử nghiệm. Độ giãn nở hệ thống hô hấp sau đó được tính toán dựa trên sự thay đổi đo được trong áp lực đường thở. Nó được sử dụng để ước tính áp lực cao nguyên cần thiết để đạt được thể tích khí lưu thông mục tiêu. Sau đó, áp lực cao nguyên được điều chỉnh theo từng nhịp thở được cung cấp. Các kiểu lưu lượng hít vào là lưu lượng giảm. Thời gian hít vào được cài đặt bời người vận hành.
Hỗ trợ áp lực được đảm bảo bằng thể tích (VAPS, Volume-assured pressure support) cung cấp một áp lực hít vào đặt trước. Ngoài ra, thể tích khí lưu thông được đo trong từng nhịp thở. Nếu nó không đạt được mục tiêu vào cuối thì hít vào, thể tích sẽ được thiết bị bổ sung. Có rất ít dữ liệu về việc sử dụng lâm sàng ở trẻ sơ sinh về áp dụng phương thức thở PRVC và VAPS.
Thông khí đảm bảo thể tích (VGV) sử dụng các phép đo thể tích khí lưu thông trong vòng phản hồi để điều chỉnh áp lực cao nguyên. Các điều chỉnh được dựa trên thể tích khí lưu thông thở được đo của nhịp thở trước đó. Nếu thể tích khí lưu thông đo được nhỏ hơn thể tích khí lưu thông mục tiêu được thiết lập bởi nhà lâm sàng, áp lực cao nguyên được tăng theo thời gian từng bước, theo thuật toán của nhà sản xuất, cho đến khi đạt đến thể tích khí lưu thông mục tiêu hoặc giới hạn an toàn áp lực. Nếu thể tích khí lưu thông thở ra được đo tăng lên trên thể tích khí lưu thông mục tiêu, áp lực cao nguyên sẽ giảm. Chế độ thông khí này có thể duy trì thể tích khí lưu thông phù hợp khi thay đổi các đặc tính cơ học của hệ hô hấp và nỗ lực của bệnh nhân xảy ra. VGV đòi hỏi một số nhịp thở cơ học để điều chỉnh PIP đến cấp độ mới. Các nhà điều hành cần lưu ý có một thời gian trễ khi bù đắp cho những thay đổi nhanh chóng trong cơ học phổi và/hoặc nỗ lực của bệnh nhân.
Hơn nữa, thở nấc (brake) và các tình trạng gián đoạn ngắn của thì thở ra do chất tiết, không đồng bộ, hoặc hoạt động cơ hô hấp có thể gây giảm thể tích khí lưu thông thở ra do đo sai. Việc điều chỉnh PIP không phù hợp có thể xảy ra sau đó.[8]
Cảm biến lưu lượng được đặt giữa đoạn nối Y và ống NKQ. Việc sử dụng thể tích khí thở ra trái ngược với thể tích khí lưu thông hít vào cần tránh trong chế độ VGV do thể tích khí lưu thông thực sự sẽ cao khi có rò rỉ khí hít vào. Sự rò rỉ ống NKQ quá mức tồn tại ngay cả ở áp lực đường thở thấp trong thời gian thở ra có thể làm hạn chế sử dụng VGV.
Các nghiên cứu ngắn hạn đã chứng minh tính khả thi của việc sử dụng VGV ở trẻ non tháng.[9–11] PIP và áp lực đường thở trung bình có thể giảm so với các chế độ giới hạn áp lực thông thường.[10] Các cytokine tiền viêm trong dịch hút khí quản cho thấy giảm trong nhóm sử dụng VG của một nghiên cứu khác.[12] Hơn nữa, hai nghiên cứu cho rằng VG, khi so với các chế độ giới hạn áp lực thông thường, có thể làm giảm hiện tượng giảm PaCO2 vô ý.[13,14] Giảm PaCO2 đã được kết hợp với nhuyễn hóa chất trắng quanh não thất [15] (leucomalacia periventricular) và bại não.[16]
Thử nghiệm ngẫu nhiên có đối chứng về thông khí nhắm mục tiêu theo thể tích
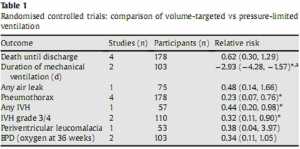
Tổng quan Cochrane dựa trên bốn RCT của chế độ thông khí nhắm mục tiêu theo thể tích đã được xuất bản vào năm 2005.[17] Hai nghiên cứu sử dụng VCV,[18,19] hai nghiên cứu khác sử dụng VGV.[12,14] Bốn thử nghiệm đã huy động trẻ sơ sinh trong 72 giờ đầu đời. Họ đã nghiên cứu tổng cộng 178 trẻ non tháng. Không có sự khác biệt về tỷ lệ tử vong, rò rỉ khí, nhuyễn hóa chất trắng quanh não thất hoặc BPD (Bảng 1). Nhóm nhắm mục tiêu theo thể tích có thời gian thở máy ngắn hơn và tỷ lệ tràn khí màng phổi thấp hơn, xuất huyết não thất (IVH, intraventricular haemorrhage) nhiều mức độ và IVH độ 3-4 (Bảng 1). Sự khác biệt trong IVH là trong số của một nghiên cứu với tỷ lệ cao hơn tổng thể.[19]
Gần đây, Singh và cộng sự [20] nghiên cứu ngẫu nhiên các trẻ sinh non từ 24–31 tuần tuổi thai vào nhóm VCV (57 trẻ) hoặc TCPLV truyền thống (52 trẻ). Trẻ sơ sinh VCV đạt được các chỉ tiêu thành công đã được xác định trước đó so với nhóm trẻ có nhóm chứng (23 so với 58 giờ; P <0,05). Không có sự khác biệt về bệnh suất hô hấp nhưng có xu hướng giảm tỷ lệ tử vong ở nhóm thông khí kiểm soát thể tích.
D’Angio và cộng sự [21] nghiên cứu ngẫu nhiên trên trẻ non tháng có cân nặng khi sinh từ 500-1249 g vào lô thở chế độ PRVC (104 trẻ) và so sánh với SIMV truyền thống. Không có sự khác biệt về tỷ lệ tử vong, thời gian thở máy, hoặc bệnh suất hô hấp ở tuổi sau 36 tuần. Không có sự khác biệt giữa các nhóm trong kết quả phát triển thần kinh như được đánh giá ở 6-18 tháng tuổi được điều chỉnh trong một nhóm phụ của 128 người tham gia nghiên cứu (64 trẻ sử dụng PRVC).
Thông khí nhắm mục tiêu theo thể tích với các đợt thiếu oxy ở trẻ non tháng
Thông khí nhắm mục tiêu theo thể tích và SIMV được so sánh trong một nghiên cứu chéo của 15 trẻ sơ sinh có các đợt thiếu oxy nghiêm trọng và thường xuyên.[22]
Không có sự khác biệt trong kết quả chính (tổng thời gian với SpO2 <80%). VCV duy trì thể tích khí lưu thông tốt hơn trong các đợt thiếu oxy và các cơn nhịp tim chậm thường ít xảy ra hơn. Polimeni và cộng sự [23] nghiên cứu VGV ở trẻ non tháng thở máy với các đợt thiếu oxy thường xuyên. Tần suất của các sự kiện này không giảm khi sử dụng thể tích khí lưu thông 3,5 mL/kg. Một lượng khí lưu thông mục tiêu tăng lên 6.0 mL/kg đã rút ngắn thời lượng nhưng không phải là tần số của các đợt thiếu oxy máu.
Tóm lại, thông khí nhắm mục tiêu theo thể tích dẫn đến thể tích khí lưu thông phù hợp hơn, cho phép tự động cai áp lực đường thở, có thể giúp tránh giảm PaCO2 máu và có thể liên quan đến các tác động lâm sàng ngắn hạn. Trẻ sơ sinh non tháng thở máy với các đợt giảm oxy máu thường xuyên dường như không có lợi ích từ thông khí nhắm mục tiêu theo thể tích. Rõ ràng, các RCT lớn hơn được yêu cầu để đánh giá các lợi ích lâu dài.
Phương pháp thông khí hỗ trợ áp lực
Định nghĩa và đặc điểm
Thông khí hỗ trợ áp lực (PSV) nhằm hỗ trợ các nỗ lực hô hấp tự phát. Một cảm biến áp lực, hoặc thường xuyên hơn, là một cảm biến lưu lượng sẽ bắt đầu kích hoạt nhịp thở cơ học. Các nhà điều hành cài đặt một áp lực bình nguyên hít vào của máy thở và giới hạn thời gian hít vào tối đa. So với A/C có Tin cố định, thì Tin trong PSV phụ thuộc vào đặc trưng của lưu lượng hít vào. Càng đến cuối thì hít vào, lưu lượng hít vào càng giảm và sẽ chấm dứt sự hỗ trợ cơ học. Điểm kết thúc xảy ra khi lưu lượng hít vào cắt qua ngưỡng đặt trước hoặc giới hạn của thời gian hít vào. Người vận hành thiết lập ngưỡng nhịp thở kết thúc như một tỷ lệ phần trăm của lưu lượng hít vào đỉnh đo được. Điều này cũng được gọi là “chu kỳ lưu lượng”.[24]
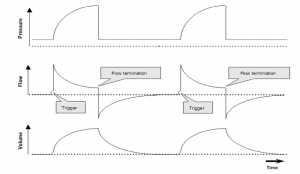
Bệnh nhân kiểm soát tần số thở và thời gian hít vào của hỗ trợ cơ học. Điều này cải thiện sự đồng bộ và sự thoải mái của bệnh nhân. Hình 1 cho thấy sự gia tăng nhanh chóng của lưu lượng hít vào sau khi ngưỡng kích hoạt được vượt qua. Khi tín hiệu lưu lượng hít vào vượt qua ngưỡng kết thúc, máy thở sẽ chuyển chu kỳ sang thì thở ra, giảm áp lực đường thở xuống đến mức PEEP.
PSV hỗ trợ nỗ lực hô hấp của bệnh nhân bằng cách tăng áp lực xuyên phổi và làm giảm công thở của bệnh nhân. Khi giảm tần số thở trong giai đoạn cai máy thở của SIMV, PSV có thể được sử dụng để hỗ trợ nhịp thở tự phát. PSV bù cho các kháng lực áp đặt bởi ống nội khí quản và tải trọng hô hấp liên quan đến bệnh, chẳng hạn như các lực đàn hồi liên quan đến bệnh phổi đang mắc hoặc sức cản đường thở tăng ở trẻ bị BPD.[25]
Khi sử dụng SIMV với PSV song song, SIMV cung cấp dự phòng trong trường hợp ngưng thở và/hoặc nỗ lực hô hấp kém. Ở bệnh nhân có trung khu kiểm soát hô hấp ổn định và nỗ lực, PSV có thể được sử dụng như một chế độ thông khí độc lập không có SIMV. Bệnh nhân kiểm soát tần số thở khi PSV được sử dụng một mình. Có sự phụ thuộc vào trung tâm hô hấp của bệnh nhân để đảm bảo thông khí đầy đủ.
Khi trung khu hô hấp kiểm soát kém có thể dẫn đến giảm thông khí phế nang, giảm oxy máu và ứ CO2, trừ khi có chế độ thông khí dự phòng được cung cấp.
Nghiên cứu ngắn hạn lâm sàng về thông khí hỗ trợ áp lực
Osorio et al.[26] nghiên cứu hiệu quả ngắn hạn của hai mức PSV (3 và 6 cm H2O) như là một hỗ trợ cho SIMV về trao đổi khí và nỗ lực hô hấp. Mười lăm trẻ sơ sinh rất nhẹ cân đã được thử thách bằng cách giảm tần số SIMV trong giai đoạn cai máy thở. Trong khi trao đổi khí vẫn không thay đổi, thông khí phút, nhịp thở và áp lực đường thở trung bình cao hơn trong quá trình giảm SIMV + PSV. Mức hỗ trợ áp lực cao hơn đã làm giảm sự gia tăng nỗ lực thở, được đo bằng áp lực thực quản.
PSV là hỗ trợ hô hấp liên kết với hỗ trợ hô hấp không xâm lấn đã được nghiên cứu trong một thử nghiệm chéo ngẫu nhiên ngắn hạn trong 15 VLBW được hỗ trợ với CPAP.[27] Giảm nỗ lực hô hấp của bệnh nhân và đồng bộ ngực-bụng được cải thiện, cho thấy giảm tải hô hấp hiệu quả và giảm sự biến dạng thành ngực.
Olson et al.[28] nghiên cứu ảnh hưởng ngắn hạn của PSV với VGV (5 mL/kg) trên các biến đổi sinh lý, cơ học và trao đổi khí so với SIMV trong ở 14 trẻ non tháng với tuổi thai từ 30–37 tuần phục hồi từ RDS. Mặc dù không có sự khác biệt về trao đổi khí, tần số hô hấp, thông khí phút và áp lực đường thở trung bình cao hơn, và thể tích thở cuối thì thở ra thấp hơn trong nhóm PSV-VGV, cho thấy xu hướng hướng dẫn đến xẹp phổi hơn. Hơn nữa, sự biến thiên của thông khí phút và áp lực đường thở trung bình có xu hướng lớn hơn trong quá trình PSV + VGV, điều này có thể tái xác định biến số hô hấp của quần thể nghiên cứu này. Các tác giả kết luận, dựa trên nghiên cứu của họ, rằng việc sử dụng thường quy PSV-VGV không được khuyến cáo. Trong các nghiên cứu khác, PSV kết hợp với VGV đã được chứng minh là làm giảm áp lực đường thở trung bình và sự biến thiên của thể tích khí lưu thông so với PSV với PIP cố định.[11,29]
Thử nghiệm ngẫu nhiên có đối chứng về thông khí hỗ trợ áp lực
Một thử nghiệm ngẫu nhiên nhỏ (34 trẻ sơ sinh VLBW) so sánh PSV + VGV là chế độ thông khí duy nhất với nhóm kiểm soát dùng chề độ SIMV.[30] Mặc dù không có sự khác biệt về kết quả lâm sàng tổng thể giữa các nhóm, áp lực đường thở trung bình giảm nhanh hơn trong nhóm SIMV, trong khi tần số lấy mẫu máu động mạch đã giảm trong nhóm PSV + VGV. Việc giảm lấy mẫu khí máu động mạch có lẽ liên quan đến việc sử dụng bổ sung VGV.
Reyes et al.[31] nghiên cứu trên trẻ sơ sinh được phân ngẫu nhiên có trọng lượng cơ thể từ 500–1000 g yêu cầu thông khí cơ học từ <7 ngày vào lô PSV + SIMV hoặc SIMV. Trong nhóm thử nghiệm, tần số SIMV giảm 10 lần/phút. PSV sau đó được bắt đầu từ 30-50% sự khác biệt giữa PIP và PEEP của nhịp thở SIMV. Trong cả hai nhóm, giao thức cai máy thở chi tiết được thiết lập trong 28 ngày đầu tiên. Trẻ sơ sinh của nhóm PSV + SIMV đạt đến thông số cài đặt máy thở tối thiểu và được rút sớm hơn trẻ sơ sinh trong nhóm SIMV. Tổng thời gian thở máy, thời gian phụ thuộc oxy và tỷ lệ BPD và tử vong không khác nhau giữa các nhóm. Phân tích sau nghiên cứu cho thấy trẻ sơ sinh trong khoảng 700-2100 g cân nặng khi sinh được tiếp xúc với oxy bổ sung trong một thời gian ngắn hơn. Kết quả nghiên cứu cho thấy việc thêm vào PSV như một bổ sung hiệu quả cho SIMV có thể cải thiện việc cai máy thở của trẻ ELBW khỏi thở máy và có thể làm giảm sự tiếp xúc oxy trong một nhóm nhỏ trẻ sơ sinh.
Tóm lại, PSV là một chế độ mới của thông khí do bệnh nhân kích hoạt cho phép bệnh nhân kiểm soát thời gian nhịp thở cơ học. Nó giúp giảm tải hô hấp của nhịp thở tự phát. Các nghiên cứu lâm sàng sơ bộ cho thấy rằng PSV đòi hỏi một trung tâm kiểm soát hô hấp ổn định hoặc nên được cài đặt dự phòng với SIMV. PSV có thể là một phương pháp hữu ích để cai máy thở. Tuy nhiên, các thử nghiệm lâm sàng lớn được yêu cầu để chứng minh các lợi ích lâm sàng lâu dài.
Phương pháp khuếch đại tỷ lệ (Proportional amplification methods)
Các khía cạnh chung và khái niệm cơ bản
Các kỹ thuật khuếch đại tỷ lệ không cố định chu kỳ của máy thở như là một dữ kiện thời điểm duy nhất, chẳng hạn như khởi đầu hoặc kết thúc của thì hít vào. Trong các phương thức này, máy thở liên tục nhạy cảm với nỗ lực hô hấp tức thời của bệnh nhân. Máy thở điều chỉnh áp lực hỗ trợ theo cách tương đối và liên tục. Điều này có thể đạt được sự đồng bộ gần hoàn hảo giữa máy thở và nỗ lực thở tự phát với việc giảm đồng thời từ công thở cơ học tăng lên liên quan đến bệnh.
Bộ điều khiển servo điều khiển áp lực máy thở áp dụng, dựa trên đầu vào liên tục từ bệnh nhân. Tín hiệu đầu vào này một mình điều khiển áp lực thông khí tức thời, được điều chỉnh liên tục theo biểu đồ dạng sóng tín hiệu đầu vào, hầu như không bị trễ thời gian. Tín hiệu đầu vào phản ánh hoạt động hô hấp tự phát của trẻ. Nó cuối cùng phản ánh đầu ra của trung tâm hô hấp. Do đó, về mặt lý thuyết, nó có thể thu được ở bất cứ nơi nào dọc theo con đường từ trung tâm hô hấp đến cơ quan cuối, ví dụ: được ghi nhận là hoạt động điện dây thần kinh hoành hoặc cơ hoành, hoặc như thể tích khí lưu thông và lưu lượng khí từ các đầu dò bên trong đường hô hấp hoặc từ phép đo plethysmography.[32] Cung lượng áp lực của máy thở tỷ lệ thuận với tín hiệu đầu vào và sẽ nâng cao hiệu quả thông khí của hoạt động của trung tâm hô hấp.[33]
Điều này có nghĩa là:
1. Các kỹ thuật khuếch đại tương ứng làm tăng lượng thông khí trên một đơn vị hoạt động hô hấp tự phát theo tỷ lệ với cường độ tức thời của nỗ lực. Ngược lại, thông khí do bệnh nhân kích hoạt sẽ thêm một lượng áp lực hoặc thể tích khí lưu thông vào nhịp thở tự phát bất cứ khi nào phát hiện thấy nỗ lực hô hấp, bất kể mức độ của nỗ lực hô hấp và thời gian của nó.
2. Máy thở trở nên hoàn toàn bị làm nô lệ, cho phép bệnh nhân kiểm soát thời gian, độ sâu, thể tích khí lưu thông và các kiểu thở.
3. Các bác sĩ lâm sàng đặt ‘gain’ của sự tăng cường này. Mức tăng là tỷ lệ giữa áp lực của máy thở áp dụng cho mỗi ‘đơn vị đầu ra của trung tâm hô hấp’, tức là áp lực cho mỗi đơn vị tín hiệu đầu vào. Độ “gain” càng cao, càng ít công thở cơ học của bệnh nhân được yêu cầu để duy trì sự thông khí đầy đủ.
4. Các chế độ này dựa vào chức năng chủ yếu của việc kiểm soát sinh học của nhịp thở. Các chế độ này không khởi động các nỗ lực thở tự phát. Họ không thể phục hồi một trung tâm kiểm soát hô hấp suy yếu. Trong các giai đoạn ngừng thở tự nhiên hoặc giảm thông khí, cần phải có thông khí cơ học thông thường để dự phòng. Khi trẻ tiếp tục thở tự phát, máy thở phải tự động ngưng thông khí dự phòng.[34]
Độ khuếch đại theo tỷ lệ dựa trên thể tích khí lưu thông và các tín hiệu không khí của nhịp thở tự phát
- Thông khí hỗ trợ tỷ lệ theo thể tích (volume- proportional assist ventilation) và
- Thông khí hỗ trợ tỷ lệ theo lưu lượng (flow- proportional assist ventilation)
- Cũng được gọi là dỡ tải đàn hồi và sức cản đường thở
Cài đặt thông khí
Một cài đặt tỷ lệ “khuếch đại” cho thông khí hỗ trợ tỷ lệ thể tích (PAV) cho phép các bác sĩ lâm sàng để thiết lập tỷ lệ áp lực máy thở được cung cấp cho mỗi đơn vị thể tích khí lưu thông trong cm H2O/mL trên một quy mô liên tục trên bảng điều khiển phía trước máy thở.
Với tính năng này, áp lực máy thở tăng lên tương ứng với thể tích khí lưu thông thì hít vào, và trở về PEEP đã đặt trong khi thở ra (Hình 2A). Các dạng sóng áp lực tỷ lệ nghịch với sự tăng áp lực đàn hồi phổi (lung elastic recoil pressure) trong mỗi thì hít vào. Do đó, nó tạo ra hiệu ứng dỡ tải lực đàn hồi (elastic unloading effect) đặc biệt làm giảm công thở của lực đàn hồi.[35]
Một điều khiển riêng biệt đặt độ “khuếch đại” cho hỗ trợ tỷ lệ theo lưu lượng. Hỗ trợ tỷ lệ lưu lượng cung cấp các dạng sóng áp lực của máy thở theo tỷ lệ lưu lượng không khí khí lưu thông (cm H2O/L/s) (Hình 2 B). Việc cung cấp áp lực máy thở này đặc biệt chống lại các lực trở kháng dòng khí (airflow resistive forces) bởi vì nó thay đổi tỷ lệ với tín hiệu dòng khí hít vào. Nó tạo ra hiệu ứng dỡ tải trở kháng (resistive unloading effect) giúp giảm công thở của trở kháng.[36] Nếu tính năng này được kích hoạt trong cả thì hít vào và thở ra (dỡ tải trở kháng toàn chu kỳ), tạo điều kiện cho thở ra, rút ngắn hằng số thời gian thở ra, và giúp tránh PEEP nội sinh ở trẻ có sức cản đường thở cao.
Các giai đoạn giảm thông khí và ngừng thở kích hoạt thông khí dự phòng thông thường. Nhà điều hành thiết lập các thông số thông khí dự phòng thông thường và giới hạn an toàn áp lực.
Các nghiên cứu về thông khí hỗ trợ tỷ lệ thể tích và lưu lượng trong các loài động vật nhỏ và các nghiên cứu ngắn hạn lâm sàng ở trẻ nhỏ
PAV thể tích và lưu lượng đã được nghiên cứu rộng rãi ở những động vật nhỏ trưởng thành và mới sinh có phổi bình thường và trong các mô hình bệnh phổi sơ sinh khác nhau, như là thiếu chất hoạt động bề mặt (surfactant) và hít phân su.[37–39]
Một nghiên cứu thiết kế chéo của 36 trẻ sinh non (trọng lượng cơ thể 600-1200 g) với bệnh hô hấp cấp tính nhẹ đến trung bình so sánh PAV hỗ trợ kiểm soát và thông khí cơ học thông thường (TCPLV).[39] Các biến kết quả sinh lý ngắn hạn được đánh giá. Trong thời gian PAV, yêu cầu áp lực đường thở trung bình và áp lực xuyên phổi thấp hơn khi tiếp xúc với mức oxy tương đương, với sự hấp thụ oxy của phổi tương đương và với tỷ lệ thanh thải CO2 tương tự. PAV an toàn trong các điều kiện kiểm soát chặt chẽ của nghiên cứu. PAV ít nhất cũng hiệu quả như các chế độ thông thường khi so sánh. Khi áp dụng cho trẻ, PAV thường cho thấy một kiểu hô hấp ‘nhanh và nông’, với tần số hô hấp giữa khoảng 50 và 80 lần/phút. Thể tích khí lưu thông thường nhỏ hơn 5 ml/kg. Trẻ sinh non có chức năng thận chưa trưởng thành và thường có toan máu nhẹ. Người ta nghĩ rằng trẻ sơ sinh có thể tăng thông khí hỗ trợ với PAV. Sự tăng thông khí không được chứng minh. PAV sau đó được điều tra ở 22 trẻ sinh non phụ thuộc thở máy mạn tính (trọng lượng sơ sinh trung bình 705 g) trong thiết kế nghiên cứu chéo với thông khí thông thường cho bệnh nhân (SIMV hoặc A/C).[40] Áp lực của thông khí thấp hơn đáng kể trong PAV so với chế độ điều khiển kích hoạt thông thường. Các chiến lược thông khí dự phòng thích ứng cho các đợt ngưng kiểm soát của trung tâm hô hấp và sự mất độ bão hòa oxy trong PAV đã được chứng minh là có hiệu quả ở trẻ sinh non.[34]
Ngoài ra, PAV đã được sử dụng trong các nghiên cứu điều tra các khía cạnh khác nhau của việc điều chỉnh nhịp thở tự phát ở trẻ non tháng.[41–43] Cho đến nay, PAV chưa được đánh giá chính thức như là phương thức thông khí ban đầu và duy nhất ở trẻ sinh non trong các giai đoạn khác nhau của bệnh lý hô hấp. Ngoài ra, tiện ích của nó ở trẻ sơ sinh với các loại bệnh phổi hoặc tim khác chưa được nghiên cứu.
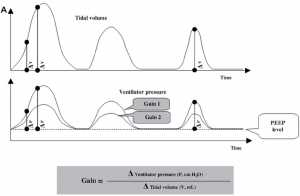
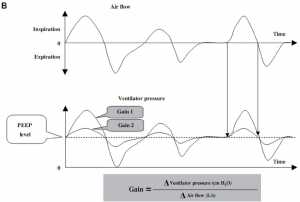
”(A) Biểu diễn sơ đồ của nhịp thở tự phát trong hỗ trợ tỷ lệ thể tích (dỡ tải đàn hồi) ở hai cài đặt khác nhau (gain 1 và gain 2) của mức tăng hỗ trợ. Các đường thẳng đứng chứng minh rằng độ khuếch đại (tỷ lệ thay đổi áp suất của máy thở trên một đơn vị thay đổi trong thể tích khí lưu thông) được duy trì liên tục theo thời gian trong khi kiểu thở thì thay đổi. Thiết lập độ khuếch đại 2 thể hiện mức hỗ trợ thấp hơn. (B) Sơ đồ thể hiện nhịp thở tự phát trong hỗ trợ tỷ lệ lưu lượng (dỡ tải trở kháng toàn chu kỳ) ở hai cài đặt khác nhau (gain 1 và gain 2) của mức tăng hỗ trợ. Các đường thẳng đứng cho thấy thay đổi áp lực của máy thở hầu như không xảy ra trễ thời gian với tín hiệu lưu lượng khí. Độ khuếch đại (tỷ số thay đổi áp suất của máy thở trên một đơn vị lưu lượng khí) được duy trì liên tục theo thời gian trong khi kiểu thở thay đổi. Gain 2 đại diện cho một mức độ thấp hơn của sự hỗ trợ.”
Khuếch đại theo tỷ lệ được điều khiển dựa trên hoạt động điện của cơ hoành
Các khía cạnh chung
Hỗ trợ thông khí được điều chỉnh theo thần kinh (NAVA, Neurally adjusted ventilatory assist) là một chế độ thông khí cơ học được hỗ trợ sử dụng hoạt động điện của cơ hoành (Eadi, electrical activity of the diaphragm) để điều khiển máy thở.[4] Người ta cho rằng hoạt động điện của cơ hoành là một chỉ số của hoạt động cơ hô hấp toàn phần trong khi thở. [44]
EAdi thô thu được từ một mảng điện cực gắn vào ống thông mũi và được đặt ở thực quản dưới. Thuật toán xử lý tín hiệu thô, loại bỏ điện tâm đồ và làm giảm sự ảnh hưởng của các nhiễu loạn chuyển động điện cực, nhu động thực quản và nhiễu nền để tạo ra phasic EAdi.[45] Phasic EAdi kích hoạt máy thở ở thì hít vào ban đầu, thúc đẩy áp lực bơm phồng phổi tương ứng với mức tăng EAdi trong khi nỗ lực thì hít vào, và chuyển chu kỳ giảm áp lực máy thở ở cuối thì hít vào. Tầm quan trọng của trợ giúp hô hấp có thể điều chỉnh bởi nhà điều hành bằng cách thiết lập một hằng số tỷ lệ, được gọi là ‘NAVA gain’ hoặc ‘NAVA level’. Nó xác định sự gia tăng áp lực của máy thở trên mỗi đơn vị tăng trong EAdi trong thì hít vào.
Các nghiên cứu thực nghiệm trên NAVA
Hỗ trợ thông khí được điều chỉnh theo thần kinh (NAVA) ở các đối tượng người lớn khỏe mạnh có thể dỡ tải công cơ hô hấp một cách an toàn theo các mức khác nhau tùy thuộc vào mức tăng NAVA được áp dụng. Mức tăng NAVA từng bước làm giảm EAdi. Do đó, thể tích khí lưu thông và thông khí phút không thay đổi đáng kể giữa mức zero và mức NAVA cao trong khi thở ở mức nghỉ ngơi.[46]
Gần dỡ tải hoàn toàn của cơ hoành với gần như bãi bỏ áp lực thực quản hít vào đã đạt được ở mức khuếch đại cao của NAVA. Ngay cả ở các cấp độ này, EAdi vẫn có mặt và có khả năng kiểm soát việc cung cấp tỷ lệ áp lực hỗ trợ của máy thở. Chấm dứt áp lực hô hấp vẫn còn đủ.[46]
Tình trạng áp lực máy thở tự duy trì có thể xảy ra trong quá trình PAV với cài đặt tăng quá mức vô ý khi chế độ được điều khiển bởi tín hiệu thể tích không khí hoặc khí lưu thông của nhịp thở tự phát.[47] Hiện tượng như vậy đã không được quan sát thấy trong NAVA. Khi tăng lên đến ‘mức siêu cao’ mức tăng NAVA gây ra một mô hình thở định kỳ trong đó mô hình thở phasic bị gián đoạn bởi các giai đoạn ngừng thở ở thỏ trưởng thành bị tổn thương phổi cấp tính.[48] Trong cùng một mô hình động vật, kích hoạt tỷ lệ thất bại trong PSV tăng ở mức áp lực máy thở cao hơn, trong khi đồng bộ giữa các nỗ lực hô hấp tự phát và chu kỳ của máy thở được duy trì tốt ở mức NAVA cao. Với sự suy giảm của suy hô hấp, giả định rằng các tín hiệu cần thiết cho thông khí do bệnh nhân kích hoạt trở nên yếu dần dần trong khi tín hiệu EAdi được điều chỉnh.[49] NAVA duy trì trao đổi khí hô hấp và áp lực thông khí đồng bộ thông qua ngạnh mũi ở thỏ bị chấn thương phổi cấp tính khi có rò rỉ khí lớn ở giao diện máy thở-bệnh nhân.[50]
Chưa có nghiên cứu nào về NAVA ở trẻ non tháng được công bố. Có thể nhận được tín hiệu EAdi có chất lượng tốt trong trẻ sơ sinh sinh non.[51,52] Nó vẫn được thiết lập cho dù các tín hiệu này có đủ ổn định trong một khoảng thời gian dài hay không và liệu trễ kích hoạt và chu kỳ có đủ ngắn ở trẻ sơ sinh để điều khiển máy thở một cách an toàn và hiệu quả hay không.
| Điểm thực hành |
|
| Hướng nghiên cứu |
|





