Tác giả: Nguyễn Thái Minh Trận, Tiến sĩ Võ Đức Duy.
Bài viết dài thời gian đọc 20 phút, thích hợp cho người có hứng thú với bệnh ung thư vú và cách điều trị.
Fulvestrant là thuốc gì?
Fulvestrant là thuốc được Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (Food and Drug Administration-FDA) công nhận để điều trị ung thư vú di căn dương tính với thụ thể hormone ở phụ nữ sau mãn kinh mà bệnh vẫn tiến triển sau khi điều trị bằng liệu pháp đối kháng estrogen (antiestrogen therapy).
Với cơ chế hoạt động độc đáo, fulvestrant gắn lên và thúc đẩy hoàn toàn sự thoái hóa của thụ thể estrogen, cho thấy khả năng vượt trội so với các liệu pháp hormone khác như tamoxifen.
Bài viết này sẽ so sánh cơ chế hoạt động của tamoxifen và fulvestrant để cho thấy khả năng vượt trội của fulvestrant trong điều trị ung thư vú. Đồng thời, bàn luận về giới hạn của fulvestrant và hướng đi mới trong điều trị ung thư vú.
Vai trò của Estrogen trong ung thư vú
Estrogen là một hormone quan trọng cho sự phát triển sinh dục và sinh sản, đặc biệt là ở phụ nữ. Thông qua việc cho phép các tế bào phát triển khi thích hợp, estrogen rất cần thiết cho giai đoạn dậy thì ở trẻ nhỏ và ngay cả trong cuộc sống của người trưởng thành, chẳng hạn như trong sự phát triển của xương, nồng độ estrogen thấp có thể dẫn đến chứng loãng xương. Tuy nhiên, trong trường hợp ung thư, estrogen có thể làm tăng sự tăng sinh khối u và do đó làm cho bệnh tiến triển nặng hơn.
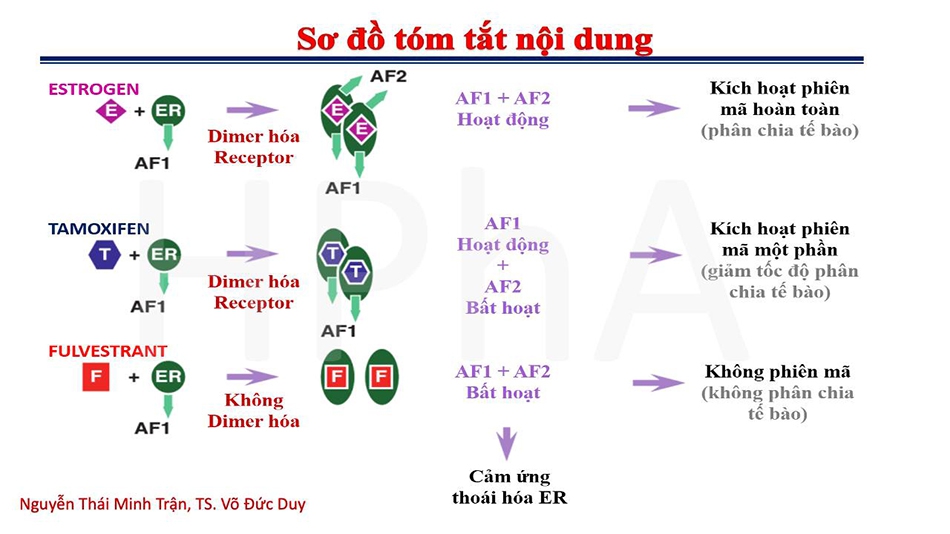
Ở phụ nữ, sau khi được tạo ra tại buồng trứng, estrogen sẽ di chuyển vào máu và hoạt động ở khắp mọi nơi trong cơ thể. Bởi vì có tính chất kỵ nước, estrogen muốn di chuyển trong máu phải liên kết với một loại protein vận chuyển gọi là hormone giới tính gắn globulin (Sex Hormone Binding Globulin), giúp làm tăng khả năng ưa nước của estrogen. Tuy nhiên, cũng nhờ tính chất kỵ nước này mà estrogen có thể dễ dàng đi qua màng tế bào khi chúng di chuyển được đến tế bào mục tiêu. Bên trong tế bào mục tiêu, estrogen sẽ liên kết với thụ thể estrogen (Estrogen Receptor-ER). Điều này làm thay đổi hình dạng của ER, cho phép 2 ER bắt cặp lại với nhau tạo dimer và đồng thời làm lộ diện 2 vùng chức năng hoạt động (Activation Function-AF) trên ER là AF1 và AF2 giúp tuyển dụng các nhân tố hỗ trợ phiên mã (coactivators-CoA). Sau khi hình thành dimer, vùng liên kết DNA (DNA‐binding domain) trên ER sẽ cho phép nó liên kết với DNA tại một vùng trình tự đặc biệt nằm ở vùng khởi động phiên mã gọi là yếu tố đáp ứng estrogen (Estrogen Response Element). Sau đó, thông qua AF1 và AF2, ER sẽ tuyển dụng CoA để kích hoạt phiên mã một số gen liên quan đến con đường tăng sinh tế bào (Hình 2).
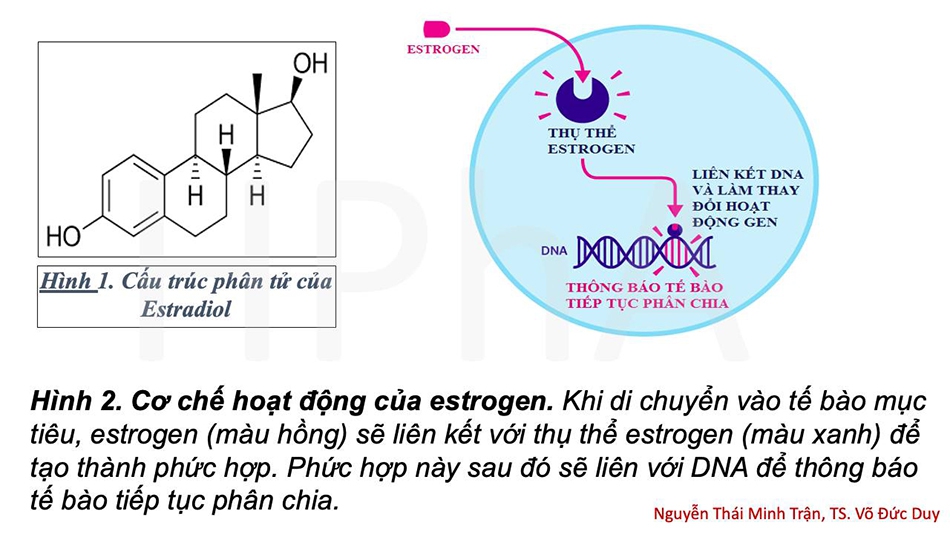
Thông thường, quá trình này sẽ được tiến hành để phát triển tử cung khi người phụ nữ mang thai hoặc duy trì hệ thống ngăn ngừa loãng xương.
Tamoxifen – Chất đối kháng và chủ vận một phần
Trong các liệu pháp đối kháng estrogen để điều trị ung thư vú, tamoxifen là loại thuốc lâu đời nhất được sử dụng, bởi vì tính an toàn và khả năng dung nạp tốt (Hình 3).
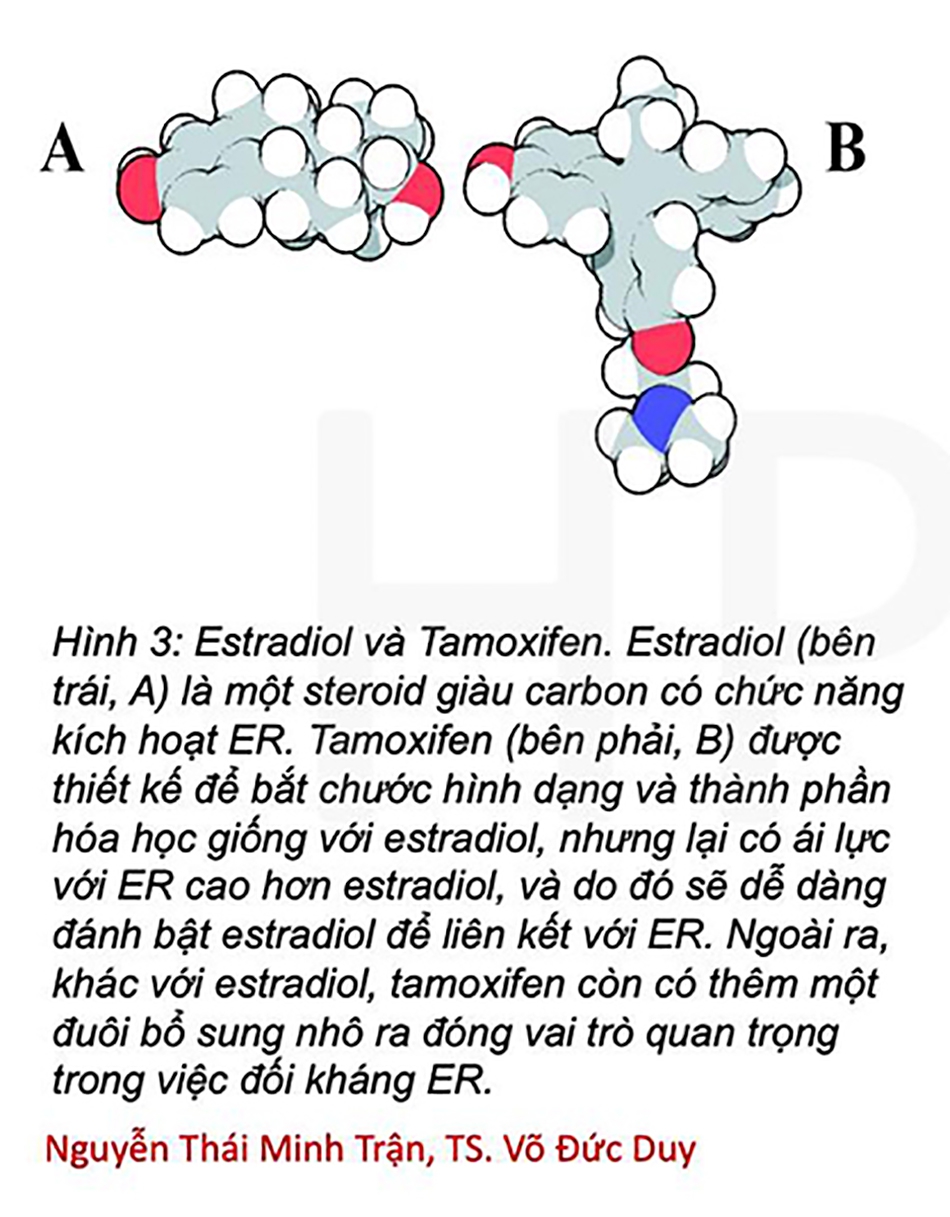
Tamoxifen là tác nhân điều biến thụ thể estrogen chọn lọc (Selective Estrogen Receptor Modulator), vừa có tính chất đối kháng ER một phần thông qua ức chế AF2, vừa có tính chất chủ vận ER một phần thông qua kích hoạt AF1 (Hình 4).
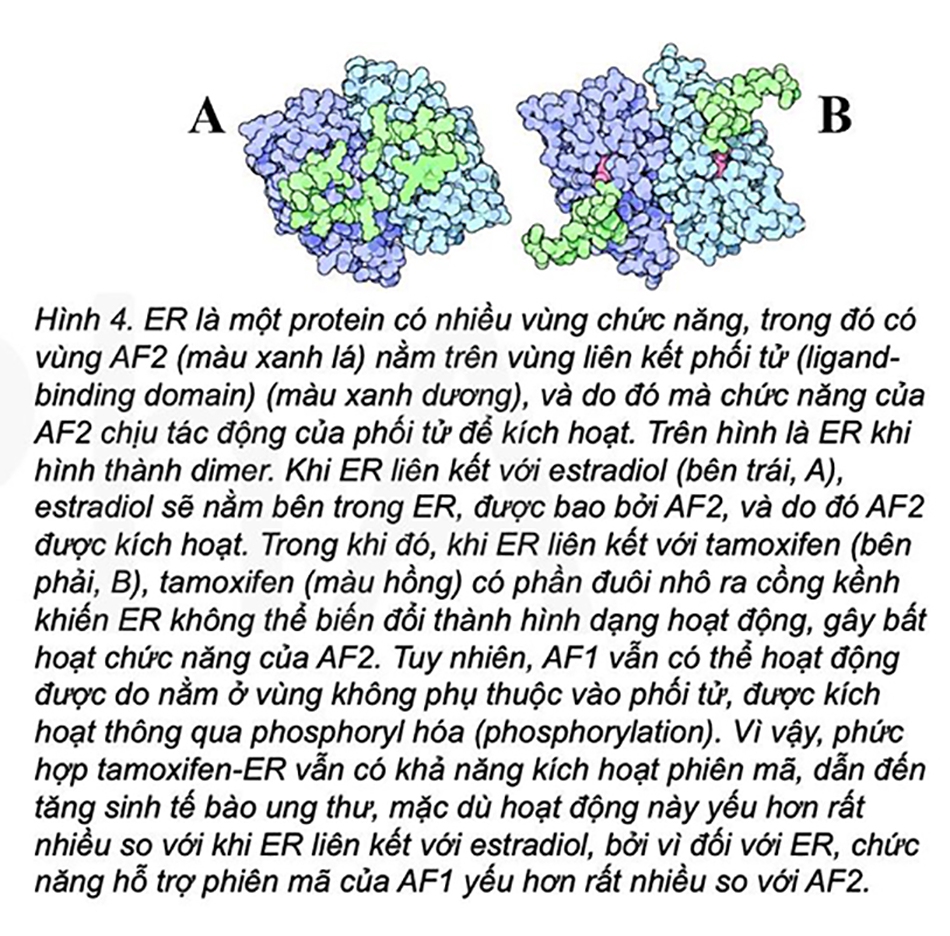
Tính chất chủ vận và đối kháng một phần của tamoxifen phụ thuộc vào từng loại mô. Đối với mô tuyến vú, tamoxifen cho thấy khả năng đối kháng mạnh mẽ. Tuy nhiên, ở mô nội mạc tử cung và trong hệ thống máu, tính chủ vận của tamoxifen thể hiện rõ rệt thông qua có khả năng làm tăng nguy cơ bị ung thư nội mạc tử cung, thiếu máu cục bộ và tạo huyết khối tĩnh mạch. Đặc tính chủ vận một phần của tamoxifen thỉnh thoàng cũng được ghi nhận ở các bệnh nhân ung thư vú di căn khi các bệnh nhân này xuất hiện đề kháng với tamoxifen và cho thấy sự tăng sinh khối u vú trở lại. Vì vậy, để điều trị ung thư vú hiệu quả, cần thiết tìm kiếm một loại thuốc mới có ái lực cao với ER, có tính chất đối kháng hoàn toàn và đặc biệt phải có cơ chế hoạt động hoàn toàn khác với các cơ chế đã biết trước đó để ngăn chặn sự kháng chéo giữa các thuốc [2].
Fulvestrant – Chất thoái hoá và đối kháng hoàn toàn
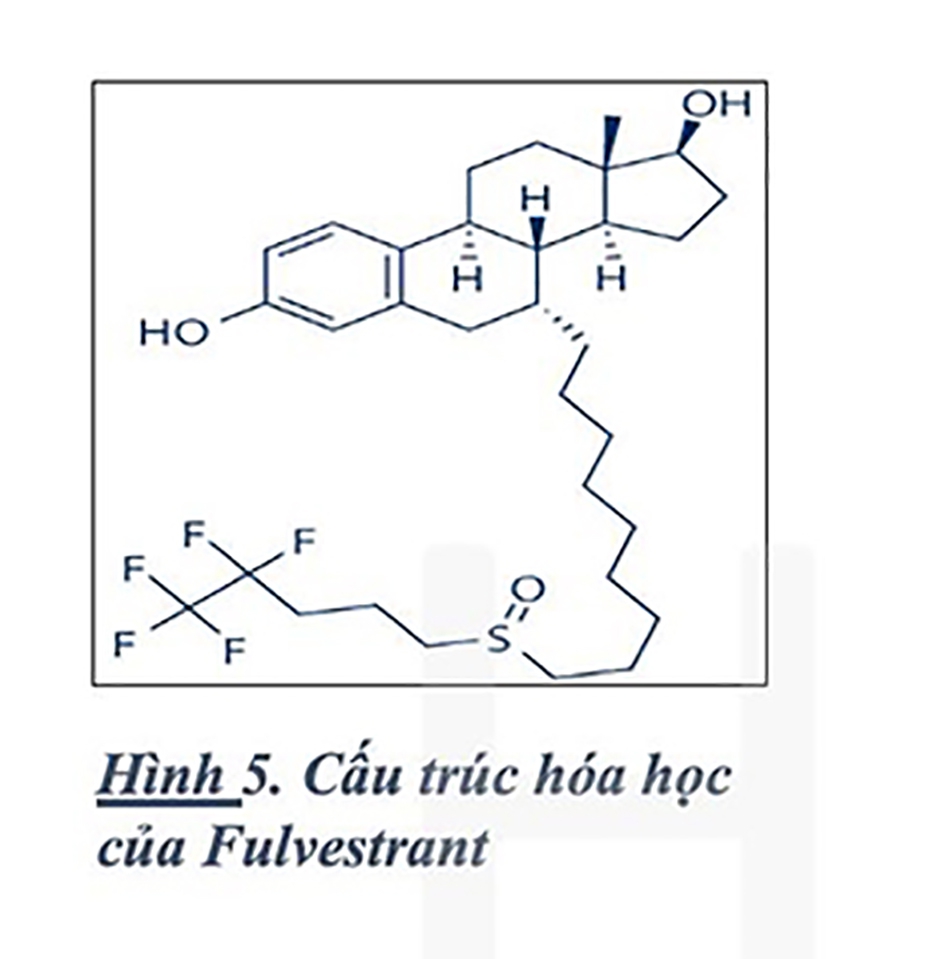
(1) Một chiến lược phát triển thuốc để tìm ra loại thuốc hoàn toàn không có tính chất chủ vận và có cơ chế hoạt động khác với tamoxifen đã được tiến hành trong một khoảng thời gian dài. Kết quả của cuộc tìm kiếm này là sự xuất hiện của loại thuốc fulvestrant, được phát hiện và phát triển bởi AstraZeneca và được bán dưới thương hiệu Faslodex. Fulvestrant là chất điều hòa làm giảm thụ thể estrogen chọn lọc (Selective Estrogen Receptor Down-regulator) với cấu trúc gồm có 2 phần: phần đầu được thiết kế để giống với estradiol cho phép fulvestrant liên kết được với ER và có ái lực với ER cao hơn rất nhiều so với tamoxifen; phần đuôi là một chuỗi fluoroalkyl kỵ nước cồng kềnh gây cảm ứng thoái hóa ER thông qua hiệu ứng kỵ nước (Hình 5).
Fulvestrant hoạt động theo cơ chế gắn nhãn kỵ nước (Hydrophobic Tagging) (Hình 6).
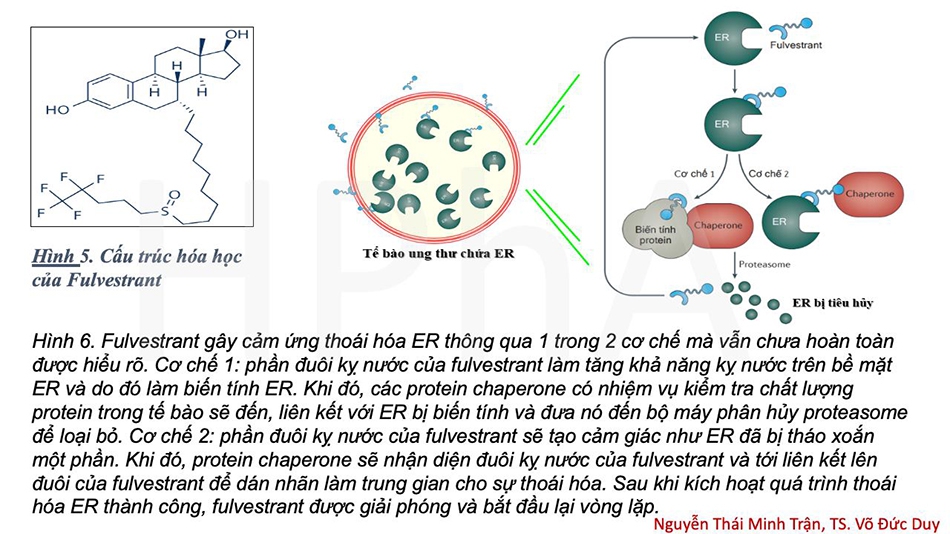
Tác động của fulvestrant lên ER bao gồm: thứ nhất, khi liên kết với ER, fulvestrant sẽ làm suy yếu sự hình thành dimer của ER và con đường vận chuyển giữa tế bào chất và nhân cần năng lượng (energy- dependent nucleo-cytoplasmic shuttling). Từ đó, ức chế khả năng định vị nhân (nuclear localisation) của ER, giúp ngăn chặn ER đi vào nhân để phiên mã; thứ hai, ngay cả khi phức hợp fulvestrant-ER đi vào nhân và liên kết được với DNA, sự phiên mã vẫn không xảy ra được do thiếu CoA, bởi vì cả AF1 và AF2 đều đã bị ức chế do fulvestrant, tính chất đối kháng hoàn toàn; thứ ba, phức hợp fulvestrant-ER thường không ổn định, dẫn đến cảm ứng thoái hóa ER trong tế bào. Như vậy, fulvestrant sẽ liên kết, khóa và tăng tốc độ thoái hóa của ER, dẫn đến ức chế hoàn toàn tín hiệu của estrogen thông qua ER[2].
Bàn luận
Fulvestrant là loại thuốc duy nhất được FDA công nhận (2002) trong chiến lược phát triển thuốc có khả năng đối kháng ER hoàn toàn. Với cơ chế hoạt động độc đáo, fulvestrant đã cho thấy các đặc tính vượt trội hơn so với tamoxifen. Thứ nhất, fulvestrant là chất đối kháng hoàn toàn, cho thấy khả năng chống ung thư vượt trội hơn nhiều so với tamoxifen, đặc biệt là trong mô nội mạc tử cung khi không làm tăng nguy cơ ung thư. Thứ hai, ngoài con đường điều khiển phiên mã thông qua liên kết với DNA, ER còn có thể điều hòa phiên mã gián tiếp mà không cần gắn lên DNA bằng cách sử dụng các thụ thể trên bề mặt màng tế bào để tạo các tín hiệu nội bào. Do đó, với khả năng làm suy giảm ER trong tế bào, fulvestrant đã đồng thời ức chế con đường gián tiếp này. Thứ ba, việc làm suy giảm ER trong tế bào thay vì ức chế như tamoxifen cho thấy khả năng điều trị ung thư bền vững của fulvestrant, bởi vì sẽ mất một khoảng thời gian để lượng ER có thể phục hồi và hoạt động. Thứ tư, với cơ chế hoạt động độc đáo khác với các cơ chế trước đó, fulvestrant sẽ không kháng chéo với các loại thuốc khác. Điều này rất có giá trị vì sẽ cung cấp thêm một lựa chọn điều trị, giúp kéo dài thời gian chữa trị ung thư vú di căn đối với những phụ nữ sau mãn kinh đã điều trị bằng tamoxifen nhưng bệnh vẫn tiến triển, trước khi phải sử dụng hóa trị liệu (Chemotherapy) mà có thể gây độc tế bào [2].
Tuy nhiên, fulvestrant vẫn còn một số hạn chế. Thứ nhất, bởi vì có độ hòa tan kém nên sử dụng theo đường uống sẽ cho hiệu quả kém, vì vậy thuốc fulvestrant hiện nay phải sử dụng theo dạng tiêm dưới bắp, dẫn đến hạn chế liều lượng và thể tích có thể sử dụng [3], giảm khả năng sử dụng rộng rãi và phải mất tới 3 tháng để đạt nồng độ ổn định trong huyết thanh [4]. Thứ hai, khả năng thoái hóa ER vẫn còn kém, gần 50% lượng ER vẫn còn tồn tại sau sáu tháng sử dụng fulvestrant khi so với ban đầu [5].
Nhằm khắc phục các hạn chế của fulvestrant, công ty Arvinas đã phát triển loại thuốc có tên ARV-471 sử dụng kỹ thuật sinh học mới, PROteolysis TArgeting Chimeras (PROTACs). ARV-471 là một chất thoái hóa ER mạnh mẽ đã được chứng minh ức chế các khối u vú trong các mô hình tiền lâm sàng. Hiện tại, ARV-471 đang trong giai đoạn thử nghiệm lâm sàng, hứa hẹn sẽ đem đến một bước tiến mới trong điều trị ung thư vú ER dương tính [5].
Tài liệu tham khảo
[1] 2017, “Hormone Therapy for Breast Cancer“, National Cancer Institute, 11/07/2020.
[2] C K Osborne, A Wakeling & R I Nicholson, 2004, ”Fulvestrant: an oestrogen receptor antagonist with a novel mechanism of action”, British Journal of Cancer, 11/07/2020.
[3] Mark R. Nathan, Peter Schmid, 2017, “A Review of Fulvestrant in Breast Cancer”, Oncology and Therapy, 11/07/2020.
[4] Jiawang Liu, et al., 2016, “Fulvestrant-3 Boronic Acid (ZB716): An Orally Bioavailable Selective Estrogen Receptor Downregulator (SERD)”, Journal of Medicinal Chemistry, 11/07/2020.
[5] Arvinas Inc., 2019, “Arvinas Announces the Initiation of Patient Dosing in a First-in-Human Phase 1 Study of ARV-471, an Estrogen Receptor-Targeting PROTAC® Protein Degrader ”, GlobeNewswire, 11/07/2020.
[6] Emma Smith, 2015, “Solving a breast cancer mystery – why do ‘double-positive’ women do better?”, Cancer Research UK, 11/07/2020.
[7] David S. Goodsell, 2002, “The Molecular Perspective: Tamoxifen and the Estrogen Receptor”, The Oncologist, 11/07/2020.
[8] Charles Swanton, Stephen R. D. Johnston, 2006, “Handbook of Metastatic Breast Cancer 2nd Edition”, CRC Press, 11/07/2020.
[9] Mark R. Nathan & Peter Schmid, 2017, “A Review of Fulvestrant in Breast Cancer“, Oncology and Therapy, 11/07/2020.
[10] Ashton C. Lai, Craig M. Crews, 2016, “Induced protein degradation: an emerging drug discovery paradigm”, Nature Reviews Drug Discovery, 11/07/2020.


![[REVIEW] An Nữ Đan có tốt không? Công dụng, Giá bao nhiêu Hình ảnh sản phẩm An Nữ Đan](https://www.healcentral.org/wp-content/uploads/2021/07/an-nu-dan-2-218x150.jpg)


