Tác giả: Bác sĩ Đặng Thanh Tuấn
1. Mở đầu
Tần suất thở máy > 48 giờ sau phẫu thuật lồng ngực lên đến 9,3% [1]. Nhu cầu và thời gian thở máy sau khi phẫu thuật ngực tương quan có ý nghĩa với tình trạng bệnh lý sau phẫu thuật [2, 3]. Trong meta-analysis gần đây, đã chứng minh được rằng tỉ lệ “tổn thương phổi cấp” (ALI) sau phẫu thuật lồng ngực là 4,3%. Mặc dù tỷ lệ này tương đương với phẫu thuật bụng (3,4%), tử vong do tổn thương phổi sau phẫu thuật cao hơn ở bệnh nhân sau can thiệp ngực (26,5% so với 12,2%) [4].
Chương này sẽ tập trung vào một số thách thức đặc biệt của thông khí cơ học ở bệnh nhân sau mổ.
2. Thông khí hỗ trợ sau phẫu thuật ngực
Phẫu thuật ngực là duy nhất theo ý nghĩa là cơ quan đích của cả hai việc: phẫu thuật và thông khí cơ học. Không chỉ các bác sĩ phẫu thuật có thể loại bỏ được phần phổi bệnh lý, mà họ cũng thường làm tổn thương các phần của mô phổi khỏe mạnh còn lại và cũng có thể làm hỏng các cơ hô hấp. Hơn nữa, vết mổ lồng ngực là một trong những vết mổ gây đau nhất, có thể làm giảm sự thông khí. Người ta có thể cho rằng tổn thương phổi sau phẫu thuật sẽ nhiều hơn do chấn thương phẫu thuật. Người ta thấy rằng mức độ tăng mật độ phóng xạ là có ý nghĩa lớn hơn ở vùng phổi không phẫu thuật so với vùng phổi phẫu thuật, sau khi cắt thùy phổi [5].
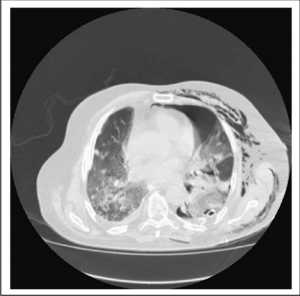
Hầu như tất cả các biến chứng (cả hô hấp và không hô hấp) sau phẫu thuật lồng ngực dẫn đến suy hô hấp (Hình 1.1). Bệnh cảnh lâm sàng thường là hỗn hợp chứ không phải là tình trạng giảm oxy máu hoặc giảm CO2 máu đơn thuần:
- Giảm thể tích phổi chức năng có thể là hậu quả của việc cắt bỏ nhu mô, xẹp phổi, phù phổi, và hạn chế di động lồng ngực sau mổ do đau.
- Giảm dung tích cặn chức năng và thể tích phổi, rối loạn chức năng cơ hoành và cơ liên sườn, và tăng kháng lực đường thở có thể gây ra tình trạng giảm thông khí.
- Bất tương xứng thông khí – tưới máu và giảm thông khí phút có thể dẫn đến trao đổi khí không hiệu quả [6].
Thêm vào đó, truyền dịch tĩnh mạch và truyền máu có thể trực tiếp gây hại hoặc làm trầm trọng thêm nguy hại cho phổi.
Trên thực tế, cần tránh thông khí cơ học trong PACU hoặc ICU nếu có thể, vì nó có thể gây ra tổn thương phổi “liên quan đến máy thở hoặc gây ra do thở máy” hoặc làm trầm trọng thêm. Mọi nỗ lực thông khí cơ học xâm lấn có liên quan đến nguy cơ làm cho mọi thứ tồi tệ hơn trong khi ta đang cố gắng cải thiện tình trạng của bệnh nhân. Nguy cơ này cao hơn ở bệnh nhân sau khi mở ngực vì phổi (cả phổi đang phẫu thuật và phổi đang thông khí) đã bị tiếp xúc với “cơn đau đầu tiên” trong quá trình phẫu thuật. Ngoài ra, kinh nghiệm lâm sàng cho thấy rằng thông khí áp suất dương có thể làm tổn thương các chổ nối còn mới hoặc gốc phế quản đã khâu mõm cụt (fresh anastomoses or bronchial stump), mặc dù không có bằng chứng cho giả định hợp lý này.
3. Những gợi ý thực hành
Các quy tắc thực dụng có thể giúp làm giảm khả năng xảy ra các sự kiện không có lý do khi quyết định tiếp tục thở máy sau khi phẫu thuật ngực:
- Một mặt, các chuyên gia gây mê, bác sĩ phẫu thuật và BS hồi sức phải tránh thông khí cơ sau sau phẫu thuật ngực. Mặt khác, bệnh nhân phải tăng công thở gấp nhiều lần, sau đó anh ta sẽ hồi phục lại sau khi bị suy hô hấp.
- Thở tự nhiên tốt hơn là thông khí cơ học, và thông khí hỗ trợ tốt hơn so với thông khí kiểm soát. Tuy nhiên, nhu cầu tái đặt nội khí quản có thể coi như là một tình huống xấu nhất.
- Quyết định thông khí phải được thực hiện trong khi phẫu thuật, và dự đoán trước phẫu thuật nên được tái đánh giá liên tục.
- Nếu cần tiếp tục thông khí cơ học, nên thay ống nội khí quản hai nòng (DLT, double-lumen tubes) vào cuối phẫu thuật bằng ống nội khí quản đơn thông thường. Tuy nhiên, ở những bệnh nhân có ý định rút nội khí quản trong vòng hai giờ sau phẫu thuật, DLT có thể vẫn giữ với bóng chèn phế quản được xả xẹp xuống.
- Việc chuyển tiếp sang một ống nội khí quản đơn (SLT, single-lumen tube) phải được thực hiện thông qua một bộ trao đổi ống (tube exchanger) có chiều dài chính xác (DLT dài hơn SLT). Nên nhớ rằng đặt nội khí quản “dễ” khi bắt đầu phẫu thuật có thể trở nên “khó” do nhiều nguyên nhân khác nhau như phù nề đường thở.
- Ở bệnh nhân có kế hoạch thông khí sau mổ, có thể chỉ định sử dụng nút chặn phế quản (BB, bronchial blocker) bởi vì nó tránh được quá trình chuyển đổi từ ống đôi sang ống đơn. Vì vậy, BB chỉ cần được gỡ bỏ.
- Ống Univent® (LMA) có thể vẫn dùng để thông khí hậu phẫu, nhưng bộ phận chặn phải được lôi lại vào nòng ống thông chính.
- Cuối cùng, cai máy từ thông khí cơ học là một quá trình nên bắt đầu khi bệnh nhân nhập vào ICU có đặt khí quản.
4. Protective Lung Ventilation
Trên thực tế, khái niệm “thông khí bảo vệ phổi ” (PLV, protective lung ventilation) đã được xác nhận và xác định trong các bệnh nhân ARDS [7], nhưng phương pháp này trở nên quan trọng hơn ở phổi dễ bị tổn thương của bệnh nhân sau khi phẫu thuật ngực. PLV bao gồm:
- Thể tích khí lưu thông thấp, 6–8 ml/kg
- Cài đặt PEEP thích hợp
- Thủ thuật huy động phế nang – (Recruitment maneuvers, RM)
Các meta-analysis đã tìm thấy PLV có hiệu quả và bảo vệ ở cả ARDS ở ICU và OLV [8-10]. Thể tích khí lưu thông 6-8 ml/kg trong phòng mổ, có liên quan đến giảm tần suất suy phổi sau khi phẫu thuật [11]. Mặc dù không có bằng chứng cho thấy lập luận tương tự cũng có giá trị trong giai đoạn hậu phẫu, nhưng có bằng chứng rõ ràng về việc sử dụng các hướng dẫn này ở các bệnh nhân ICU tổng quát. Tình huống này có nghĩa là giảm nhu mô phổi chức năng giống như “baby lung” trong ARDS [12].
Các chi tiết của chiến lược này được thảo luận ở những nơi khác trong cuốn sách này; các tác giả sẽ chỉ tập trung vào một số tình huống khó khăn sau đây:
1. Có bất kỳ thành phần đặc biệt nào “quan trọng hơn” thành phần khác không? Gần đây, người ta đã báo cáo rằng áp lực đẩy (DP, driving pressure) xác định bởi VT/compliance, là một biến số thở máy thường dùng, nhưng giúp phân loại tốt nhất bệnh nhân ARDS có nguy cơ mắc ALI [13]. Sự thay đổi trong DP đóng một vai trò quan trọng hơn so với PEEP hoặc áp lực đỉnh hít vào (PIP). Vấn đề đặt ra là liệu nó có phù hợp hơn để xác định PLV với “DP thấp” (ít hơn khoảng 20 cmH2O) chứ không phải là “VT thấp”.
2. Một VT 6 mL/kg có đủ bảo vệ không ? Xem xét phẫu thuật lồng ngực thường liên quan đến việc giảm thể tích phổi, ví dụ như ở bệnh nhân sau khi cắt bỏ phổi, 6 ml/kg sẽ có nghĩa là quá cao và có thể không còn bảo vệ nữa. Trong một nghiên cứu trên động vật, áp dụng cùng VT với một phổi so với hai phổi đã gây tổn thương phổi lớn hơn rõ rệt trong kết quả đánh giá điểm “tổn thương phế nang” về mặt mô học [14]. Mặt khác, giảm một nửa VT xuống còn 3-4 mL/kg, nghĩa là giảm xuống dưới thông khí khoảng chết. Theo kinh nghiệm, một VT 4-6 mL/kg có vẻ hợp lý, nhưng cần phải được chứng minh và kiểm tra trên cơ sở cá nhân.
3. Điều gì sẽ xảy ra nếu DP vẫn còn cao mặc dù VT vẫn giữ ở mức thấp? Trong trường hợp giảm compliance phổi nặng và/hoặc thể tích phổi hiệu quả giảm nghiêm trọng, áp lực đẩy rất cao có thể là cần thiết ngay cả đối với VT thấp. Mặc dù đây là một tình trạng rất hiếm hoi, việc gọi là thông khí cực kỳ bảo vệ (ultraprotective ventilation), việc áp dụng hệ thống trợ giúp phổi ngoài cơ thể (ECLA, extracorporeal lung assist) có thể trở nên cần thiết. Nó đã được hiển thị trong hai nghiên cứu (một nghiên cứu trên động vật [15] và một nghiên cứu lâm sàng [16]) rằng ECLA giúp giảm VT xuống rất thấp để tránh áp lực cao trong thông khí cơ học trong giai đoạn hậu phẫu. Tỷ lệ sống sót cao hơn nhiều so với ở cách thông khí thông thường (100% trong nghiên cứu trên động vật và 86% (sáu trong số bảy bệnh nhân) ở người). ECLA được thảo luận trong một chương khác trong cuốn sách này.
4. “Làm thế nào để áp dụng PEEP?” PEEP là “tốt” không chỉ để cải thiện oxy hóa mà còn (và có thể quan trọng hơn) để cải thiện mối tương quan V/Q trong phổi phụ thuộc và ngăn ngừa xẹp phế nang cuối thì thở ra bằng cách tăng dung tích cặn chức năng (Hình 1.2) [17]. Tuy nhiên, PEEP quá mức cũng có thể dẫn đến sự dịch chuyển thông khí của đường cong áp suất và thể tích sang bên phải và không cần thiết (Hình 1.3). Hơn nữa, mặc dù không phải là bằng chứng và thậm chí có thể là không hợp lý, “kinh nghiệm lâm sàng” cũng có thể gợi ý rằng thông khí áp lực dương có thể làm tổn thương các chổ nối còn mới hoặc gốc phế quản đã khâu mõm cụt. Một cách tiếp cận để giữ cho PEEP “cao khi cần thiết” và “càng thấp càng tốt” có thể giúp vượt qua cả xẹp phổi và căng phế nang quá mức [18]; nhưng thực tế, vấn đề này phức tạp hơn nhiều so với cái trước. Một “thử nghiệm giảm dần” sau khi thực hiện thủ thuật huy động phế nang (RM) (bước giảm PEEP từ 20 cm H2O) để điều chỉnh tìm compliance tốt nhất có thể là thích hợp nhất [19].
5. Làm thế nào để huy động phế nang? Trong khi PEEP có thể giữ phổi mở, nó không có khả năng mở vùng phổi đang bị xẹp. Để mở vùng phổi xẹp, một thủ thuật huy động phế nang (RM) là cần thiết [20]. Tuy nhiên, ở bệnh nhân bị rò rỉ khí (air leak), RM là chống chỉ định; Hơn thế nữa, ở những bệnh nhân không bị rò rỉ khí (hoặc rò rỉ khí ít), có một “nỗi sợ hãi” chung của áp lực cao do RM tạo ra, và PEEP có thể làm hỏng các chổ nối mới và mõm cụt phế quản. RM sau khi phẫu thuật lồng ngực là một vấn đề, trong đó ưu và khuyết điểm phải được kiểm tra trong các thiết lập lâm sàng cá nhân.
![Hình 11.2 Liên quan giữa FRC (functional residual capacity) và CC (closing capacity) ở các cách cài đặt thông số thở máy khác nhau. Bên phải: FRC nằm dưới CC trong khi thở máy; thể tích khí lưu thông lớn có thể có trao đổi khí tốt hơn (diện tích vùng nằm trên đường CC); tuy nhiên việc đóng mở chu kỳ phế nang không thể tránh khỏi. Bên trái: áp dụng PEEP trong khi giữ VT thấp: PEEP làm cho FRC nằm trên CC. Đóng mở phế nang chu kỳ tránh được; và việc thông khí (bây giờ nằm trên FRC “mới”) vẫn tốt hơn là không có PEEP (Adapted from [17] (with permission))](https://www.healcentral.org/wp-content/uploads/2020/10/nhung_thach_thuc_dac_biet_trong_thong_khi_co_hoc_sau_phau_thuat_long_nguc_la_gi_2-300x152.jpg)
![Hình 1.3 Liên quan giữa PEEP và LIP (lower inflection point, điểm uốn dưới). Ghi nhận LIP có thể khác nhau ở mỗi người và có thể là zero. A, B, và C là điểm có thể của PEEP total (PEEP intrinsic + external). Mức PEEP cài ngoài phải điều chỉnh càng gần mức LIP. Nếu PEEP ngoài chuyển từ A đến B, oxygen hóa sẽ tốt hơn, nhưng nếu PEEP ngoài làm cho PEEP total từ B sang C, oxygen hóa sẽ xấu đi; nếu LIP = 0, oxygen hóa tốt nhất là ở A (Adapted from [17] (with permission)](https://www.healcentral.org/wp-content/uploads/2020/10/nhung_thach_thuc_dac_biet_trong_thong_khi_co_hoc_sau_phau_thuat_long_nguc_la_gi_3-300x199.jpg)
5. Permissive Hypercapnia
Các bác sĩ lâm sàng có xu hướng bù đắp cho việc giảm VT bằng việc tăng tần số để duy trì thể tích thông khí phút. Tuy nhiên, điều này có thể là sai:
1. Thời gian hít vào ngắn hơn có thể làm áp suất đường thở cao hơn, và kết quả của thời gian thở ra ngắn hơn có thể là bẫy khí và auto-PEEP.
2. Về mặt vật lý, “power” đóng vai trò trong chấn thương phổi (chứ không phải “work”), và do đó “số lần nhát búa trong 1 đơn vị thời gian” cũng rất quan trọng (trích dẫn của Luciano Gattinoni). Tăng tần số hô hấp (= nhát búa) làm tăng năng lượng gây tổn thương phổi.
3. Quan trọng hơn, tăng CO2 máu nhẹ không chỉ được cho phép trong nhiều trường hợp [21], nó cũng có thể được kéo dài thậm chí trong nhiều giờ [22]. Sự tăng CO2 máu cho phép có thể bảo vệ phổi và cải thiện việc oxy hóa mô do sự gia tăng cung lượng tim và sự dịch chuyển sang phải của đường cong bão hòa oxy (O2) [23].
4. Mặt khác, cần lưu ý rằng tăng CO2 máu sẽ làm trầm trọng thêm tình trạng co thắt phế quản phổi, và do đó, nó không được đề cập trong tăng áp phổi, thường xảy ra ở bệnh nhân sau khi phẫu thuật ngực. Ngoại trừ người tăng áp phổi, tăng CO2 máu cho phép được xem như là một quy trình chuẩn của thông khí bảo vệ phổi.
6. FiO2 (Inspired Oxygen Fraction)
Tăng mức tiêu thụ O2 ở những bệnh nhân sau mổ đã dẫn đến việc sử dụng O2 bổ sung. Tuy nhiên, cách tiếp cận này có thể có hại hơn so với có lợi [24]. Mặc dù nghiên cứu này đã được thực hiện trong trường hợp cấp cứu, cơ chế của sang chấn do FiO2 cao có thể được xem là có giá trị cho bệnh nhân sau khi phẫu thuật lồng ngực. Đây là những con đường được giả định về những tổn thương có thể xảy ra do hyperoxia:
1. Sự co thắt mạch vành và mạch máu hệ thống dẫn đến giảm thể tích nhát bóp.
2. Thậm chí một thời gian ngắn của FiO2 là 100% có thể dẫn đến xẹp phổi do kết quả của các phế nang bị xẹp do oxygen thay thế nitơ [25].
Rõ ràng, giảm oxygen máu ở bệnh nhân hậu phẫu nên được điều trị, nhưng vẫn phải tránh hyperoxia: giảm oxygen máu nên được điều trị bằng tăng FiO2 từng bước, chỉ cao đến mức cần thiết để tránh tình trạng hyperoxia [24].
Gần đây, việc tăng FiO2 trước khi áp dụng gói “VT thấp-PEEP-RM” thấp đã được ủng hộ: cái gọi là xẹp phổi cho phép. Mặc dù gợi ý này chỉ giới hạn trong việc thông khí cơ học trong gây mê của phổi “lành mạnh”, nhưng cần phải kiểm tra ngoại suy cho bệnh nhân sau mổ [18].
7. Mode thở (Ventilation Mode)
Nếu xem “áp lực đẩy” (DP) là nguyên nhân chính gây thương tích phổi, dường như có ít hoặc thậm chí không có ý nghĩa áp dụng cùng DP với kiểm soát áp suất (PCV) hay kiểm soát thể tích (VCV). Các nghiên cứu trước đây ủng hộ PCV vì “kiểu lưu lượng giảm” giống như thở tự nhiên sinh lý ở OLV [26] đã không được khẳng định trong những nghiên cứu gần đây với các thiết lập tương tự [27]. Tác dụng trong giai đoạn hậu phẫu cũng tương tự như vậy.
Sự khác biệt duy nhất giữa các chế độ thông khí này có lẽ là áp lực đỉnh thấp hơn (không phải là áp lực bình nguyên), đóng góp ít hơn (nếu có) vào ALI. Gần đây, trong OLV cho thấy PCV có liên quan nhiều hơn với sự cải thiện chức năng tâm thất trái so với VCV. [28] Chức năng tâm thất phải là điều quan trọng đối với bệnh nhân sau phẫu thuật lồng ngực; và trong giai đoạn hậu phẫu cũng vẫn được đánh giá.
Nhịp thở sinh lý là không đều trong tất cả các thành phần của nó (VT, tần số, thở dài (sigh), …). Nó đã được hiển thị trong một nghiên cứu ALI thử nghiệm rằng một cái gọi là thông khí hỗ trợ áp lực “noisy” có liên quan với một sự cải thiện oxy hóa và tái phân phối lưu lượng máu phổi [29].
8. Bệnh nhân cần thông khí cơ học, nhưng có rò rỉ khí
Thách thức “đặc biệt” nhất của việc thông khí cơ sau khi mổ là bệnh nhân bị rò rỉ khí liên tục và cần thông khí cơ học. Cả hai điều kiện đều xấu đi: khí rò rỉ làm nặng thêm tình trạng suy hô hấp và tăng nhu cầu thông khí cơ học, thông khí áp lực dương và làm trầm trọng thêm sự rò rỉ khí. Ở những bệnh nhân này, thông khí không xâm lấn có thể được thử (được thảo luận trong chương khác). Trong một số trường hợp, có thể cần phải áp dụng thông khí cao tần hoặc thông khí phổi tách biệt (2 phổi thông khí riêng).
9. High-Frequency Jet Ventilation (HFJV) sau phẫu thuật ngực
Thông khí máy thở tần số cao (HFJV) đóng vai trò cận biên trong việc thông khí sau phẫu thuật khi có sự hiện diện của lỗ rò khí quản – màng phổi [30]. Đặc điểm cơ bản của thông khí dạng phụt nói chung, thường tạo ra áp suất đường thở thấp hơn thông khí cổ điển. Trong trường hợp lỗ rò khí quản – màng phổi, có hai lỗ mở để cho khí thoát ra: (1) đường thở trên (ví dụ, thông qua ống nội khí quản hoặc ống nội phế quản) và (2) qua qua lỗ rò. Tuyến không khí qua lỗ rò vẫn là một hiệu ứng không mong muốn vì nó ngăn cản việc đóng lỗ rò và lành vết thương.
Do đó, mục tiêu của liệu pháp giảm thiểu lưu lượng khí càng sớm càng tốt. Điều này có thể được tạo điều kiện bằng cách làm áp suất đường thở thấp hơn so với thông khí cổ điển. Ngoài ra, một lượng lớn khí mất qua lỗ rò thậm chí sẽ cản trở việc áp dụng thông khí áp suất dương. Những tình huống này dẫn đến việc xem xét HFJV như một phương tiện tốt hơn để thông khí phổi bị bệnh lý nếu thông khí phổi đơn một bên phổi (unilateral single-lung ventilation) được coi là không đủ để duy trì sự trao đổi khí. Thông thường, lỗ rò khí quản – màng phổi là một bên và có thể xảy ra ở bên phổi phẫu thuật. Nếu sự rò rỉ là nhỏ thì nên duy trì hô hấp tự nhiên, do áp suất đường thở thấp. Tuy nhiên, nếu cần thiết phải thở máy, cần xem xét thông khí hai phổi khác biệt.
Trong quá trình vận hành, bệnh nhân được đặt ống nội khí quản đôi (DLT). Nếu lỗ rò trở nên rõ ràng sau khi rút nội khí quản, và bệnh nhân cần thông khí hỗ trợ, thì giao điện được chọn là ống nội khí quản đôi để phân biệt hai phổi. Việc này cho phép thông khí cổ điển ở phổi bình thường, trong khi phổi bệnh sẽ nhận HFJV [31, 32].
Các thiết lập của HFJV đối với phổi bị bệnh có thể được điều chỉnh theo nhu cầu chuyển hóa của bệnh nhân. Mục đích để áp dụng HFJV có khi cần thiết (để duy trì sự trao đổi khí đầy đủ) và giảm nó xuống mức thấp nhất có thể (để có được lượng khí thải thấp nhất có thể qua hệ thống). Các yếu tố quyết định chính của lượng HFJV là áp lực đẩy (DP), dẫn đến các thông số kết quả như lượng khí, thể tích khí lưu thông và áp suất đường thở. Hoàn toàn cần thiết để điều chỉnh DP theo từng bước đến độ lớn tối ưu đã đề cập.
Cài đặt này phải được điều chỉnh thường xuyên với những thay đổi về độ lớn của rò rỉ khí. Các cài đặt khác là nồng độ oxy, thời gian hít vào, và tần số. Nồng độ ôxy cần được thiết lập theo kết quả các tham số oxy hóa; thời gian hít vào có tầm quan trọng thứ nhì và nên được đặt ở mức 40 hoặc 50%, trong khi tần số thông khí có thể dao động từ 120 đến 300 lần/phút. Áp suất đường thở thấp nhất có thể chọn một tần số thở cao, trong khi sự thải carbon dioxide có thể đòi hỏi tần số thở thấp; cần có sự cân bằng lý tưởng giữa hai lợi ích này. Trong hầu hết các trường hợp, người ta sẽ bắt đầu HFJV với oxy 100%, DP ở 1,5 bar, thời gian hít vào 40% và tần số 150 lần/phút. Các kết quả khí máu có thể chỉ ra thời điểm khi DP có thể được giảm xuống theo từng bước cũng như tần số có thể tăng lên. Sự điều chỉnh này mong muốn hiện tượng rò rỉ càng nhanh chóng cải thiện hơn. Khi đạt đến DP < 0,8 bar và tần số 300 lần/phút, sự đóng góp của HFJV đối với việc oxy hóa và thải bỏ khí cácbon sẽ trở nên nhỏ và có thể ngưng. Điều này cũng sẽ cho phép rút ống và ngưng hỗ trợ hô hấp.
10. Thông khí phổi khác biệt (Differential Lung Ventilation)
Đối với bác sĩ gây mê lồng ngực, thông khí phổi khác nhau (DLV) dường như quen thuộc như một biến thể của OLV. Đối với bệnh nhân sau phẫu thuật lồng ngực, DLV có hai chỉ định chính: phẫu thuật phổi 1 bên và rò rỉ khí [33]. Lý do là để thông khí cả hai phổi – đồng bộ hay không đồng bộ – với VT và/hoặc PEEP khác nhau. Trong ARDS, phương pháp này đã được sử dụng chủ yếu trong bệnh lý phổi 1 bên; tuy nhiên, nó có thể được sử dụng thành công trong ARDS ở tư thế nằm nghiêng 1 bên, nơi phân bố không đồng đều của thông khí có thể được chia cho cả hai phổi thông qua tư thế này, DLV cho phép chuẩn độ và áp dụng “PEEP tối ưu chọn lọc” cho cả hai phổi [34].
Mục đích của DLV ở bệnh nhân có rò rỉ khí/dò phế quản – màng phổi là thúc đẩy việc lành phổi bệnh với một DP thấp đồng thời giảm nguy cơ làm trầm trọng thêm tình trạng oxy hóa và trao đổi khí. Nó cũng có thể bảo vệ phổi lành chống lại các quá trình bệnh lý của phổi khác bao gồm ho ra máu một bên, chứng giãn phế quản và áp xe phổi.
Trong DLV, có thể sử dụng hai máy thở kết hợp (“master” và “slave”) với hít vào và thở ra đồng bộ. Hai quạt máy thở cũng có thể được sử dụng theo cách không đồng bộ, nhưng điều này có thể gây ra sự dịch chuyển trung thất. Phổi “lành mạnh” được thông khí với các cài đặt thông thường (để tiếp nhận trao đổi khí); phổi có chỗ rò rỉ được thông khí với VT ít hơn, PEEP thấp hơn hoặc zero, và không bao giờ làm huy động phế nang.
Một giải pháp dễ dàng hơn là thông khí một phổi (phổi bình thường) với các cài đặt thông thường, trong khi áp dụng CPAP hoặc thông khí tần số cao (HFV) có thể được áp dụng cho phổi “bệnh”.
Rõ ràng, việc sử dụng DLV trong ICU trong một thời gian kéo dài có thể liên quan đến một số vấn đề (như ống sai vị trí, giãn cơ bắt buộc, …). Do đó, việc sử dụng DLV ở bệnh nhân sau mổ vẫn còn hạn chế, chỉ định đối với bệnh nhân cần thông khí cơ học nhưng vẫn còn rò rỉ khí.
11. Cai máy
Một nguyên tắc thiết yếu của thông khí cơ học là (hoặc nên) cai máy nên bắt đầu – ít nhất là trong tâm trí của bác sĩ – khi thông khí cơ học bắt đầu. Cai máy thở cơ nên được thực hiện càng nhanh càng tốt nhưng không nhanh quá để không thành công. Một số tiêu chuẩn nên được thực hiện để rút nội khí quản không biến chứng, cho dù thời gian thở máy là bao lâu:
- Nhiệt độ bình thường
- Hợp tác
- Ho đủ mạnh
- Thở tự nhiên với các thông số khí máu pH, PaCO2, và PaO2 ở mức chấp nhận được
Một trong những điểm chính của cai máy thành công là theo một protocol tốt [35]. Các phương pháp cai máy nên phân biệt rõ ràng bệnh nhân cần phải thử, phương pháp và chiến lược cai máy, và tiêu chuẩn cai máy thành công (Hình 1.5).
Một số quy tắc cho việc cai máy thành công bao gồm:
- Các thử nghiệm tự thở hằng ngày: nên được thực hiện ở mỗi bệnh nhân thở máy hơn 24 giờ để tránh tình trạng “không nhận ra được” bệnh nhân có thể cai máy
- Tìm kiếm và điều trị lý do của thử nghiệm tự thở thất bại
- Một protocol cai máy hướng từ thông khí có kiểm soát đến hỗ trợ và từ thông khí xâm lấn đến thông khí không xâm lấn
- Ngăn ngừa an thần quá mức (và cũng như thiếu an thần)
12. Tracheostomy
Trong trường hợp thông khí cơ học kéo dài, hoặc thậm chí dự báo thông khí cơ học kéo dài hơn 7 ngày cùng với các thử nghiệm cai máy không thành công, cần phải xem xét mở khí quản. Ngay cả việc bỏ ống nội khí quản và các băng keo khác cũng có thể giảm liều thuốc an thần. Quan trọng hơn, nó giúp huy động đàm dễ hơn và tạo điều kiện cho việc loại bỏ chất tiết khí quản. Bệnh nhân có thể ăn, uống, và thậm chí nói chuyện. Mặc dù có một số nghiên cứu trái ngược, nhưng nhìn chung phẫu thuật mở khí quản sớm có liên quan đến việc cai sữa dễ dàng hơn và giảm nhiễm trùng.
Đối với những bệnh nhân phẫu thuật lồng ngực, bác sĩ phẫu thuật có khuynh hướng thực hiện mở khí quản trong phòng mổ. Nhưng được xem như là thủ thuật thông thường của ICU, phẫu thuật mở khí quản qua da là dễ dàng, an toàn hơn và rẻ hơn, ít nhất là trong các trường hợp không biến chứng.

13. Xử trí ống dẫn lưu ngực
Đối với phẫu thuật lồng ngực, đặt ống ngực là một thủ tục thường quy và gần như bắt buộc. Vì vậy, bác sĩ chịu trách nhiệm chăm sóc sau mổ cũng nên làm quen với việc chăm sóc ống dẫn lưu ngực bao gồm cả chẩn đoán và điều trị các biến chứng của nó. Ống ngực cho phép dẫn lưu không khí và/hoặc dịch. Do đó, mục tiêu của bác sĩ là theo dõi, phòng ngừa, hoặc điều trị rò rỉ khí và quá trình dẫn lưu dịch màng phổi [36]. Thông qua hệ thống dẫn lưu ngực cổ điển ba bình (Hình 11.6), không khí từ màng phổi có thể được dẫn lưu thụ động hoặc chủ động bằng cách gắn vào nguồn hút chân không. Có những báo cáo gây tranh cãi về những ảnh hưởng của sự hút chủ động hoặc thụ động và/hoặc xen kẽ [37, 38]. Một hệ thống dẫn lưu ngực cân bằng có thể là chiến lược hợp lý nhất để duy trì trung thất ở vị trí trung lập. Nếu chọn hút chủ động, áp suất âm không nên vượt quá 15-20 cm H2O. Nên tránh áp lực âm sau khi cắt bỏ phổi, bởi vì nó có thể gây ra sự dịch chuyển trung thất. Ống không bao giờ được kẹp, ví dụ, trong quá trình vận chuyển bệnh nhân, do nguy cơ tràn khí màng phổi.
![Hình 1.6 Hệ thống dẫn lưu 3 bình. Bình đầu tiên (drainage collection) có thể làm tăng kháng lực với dẫn lưu nếu mức dịch/máu dâng lên cao trong bình. Thêm bình thứ hai (water seal) cho phép dịch dẫn lưu chứa trong bình thứ nhất và khí đi qua bình thứ hai, cũng ngăn ngửa tạo thành bọt khí. Tuy nhiên tăng thêm chiều dài ống có thể làm tăng khoảng chết và kháng lực thêm nữa, có thể làm dịch đi ngược lại ống và có thể vài lại khoang màng phổi. Vì vậy bình thứ ba (suction control) cho phép hút áp lực âm chủ động, ngăn dịch từ bình đi ngược vào bệnh nhân (Adapted from [40] (with permission))](https://www.healcentral.org/wp-content/uploads/2020/10/nhung_thach_thuc_dac_biet_trong_thong_khi_co_hoc_sau_phau_thuat_long_nguc_la_gi_5-300x168.jpg)
14. Kết luận
Ngày nay, chỉ có một số bệnh nhân sau phẫu thuật lồng ngực đòi hỏi thông khí cơ học kéo dài trong các ICU. Tuy nhiên, cần phải luôn luôn lưu ý rằng việc thông khí cơ học sau phẫu thuật có thể dẫn đến các biến chứng thêm. Các vấn đề khác, như rối loạn nhịp tim, quá tải dịch … có thể làm trầm trọng thêm tình trạng bệnh nhân. Thông khí cơ học chỉ nên được xem xét khi cần thiết, nhưng ngưng thông khí càng sớm càng tốt. Trong quá trình thông khí cơ học, mô phổi mới bị tổn thương cần được bảo vệ; tránh làm trầm trọng thêm sự rò rỉ khí và dò khí quản – màng phổi, ảnh hưởng đến sự trao đổi khí ít nhất. Cai máy nên được xem xét càng sớm càng tốt.





