Biên soạn: Nguyễn Thái Minh Trận, Tiến sĩ Võ Đức Duy, Tiến sĩ – Dược sĩ Phạm Đức Hùng.
RIBOnuclease-TArgeting Chimeras (RIBOTACs), chất phân huỷ RNA, hứa hẹn mở đường cho các loại thuốc điều trị các loại ung thư khó điều trị và các bệnh rối loạn di truyền.
Từ khóa: Chất thoái hóa RNA, RIBOTACs. Chuyên mục: Công nghệ.
RIBOTACS – CHẤT THOÁI HÓA RNA
Kể từ khi dự án ENCODE (Encyclopedia of DNA Elements) được hoàn thành năm 2010, nó đã cho thấy chỉ có ~2% bộ gen của chúng ta là được dịch mã thành protein, còn lại phần lớn là được phiên mã thành các RNA không mã hóa (non coding RNA-ncRNA). ncRNA, sau đó, đã được chứng minh là có tác động đáng kể đến gần như toàn bộ hệ thống sinh học của con người từ điều hòa phiên mã đến cắt nối (splicing), dịch mã và xúc tác phản ứng. Điều này đã làm bùng nổ lên nhiều dự án phát triển thuốc chuyển hướng đối tượng từ protein sang RNA. Tuy nhiên, với nhiều đặc điểm độc đáo khác xa so với protein, chẳng hạn như kích thước nhỏ, thiếu tính ổn định, thiếu thông tin về các con đường nhắm tới RNA một cách đặc hiệu và chọn lọc, bề mặt có độ âm điện cao giúp dễ dàng liên kết với các phân tử tích điện dương không đặc hiệu (như kháng sinh nhóm aminoglycoside) và chỉ được cấu thành từ 4 loại nucleotide A, T, G và C thay vì nhiều loại acid amin như protein, RNA đã được biết đến như một đối tượng “undruggable” và phát triển thuốc nhắm tới RNA đã trở thành một lĩnh vực đầy thách thức.
Ngày 24/5/2018, các nhà khoa học tại viện nghiên cứu Scripps, đứng đầu bởi tiến sĩ Matthew D. Disney, đã công bố một công nghệ mới, RIBOTACs, cho phép tiêu hủy chọn lọc RNA liên quan tới ung thư trên tạp chí Hiệp hội Hóa học Hoa Kỳ (Journal of the American Chemical Society). RIBOTACs là các tiểu phân tử được thiết kế để bám đặc hiệu và phá hủy các RNA gây bệnh thông qua tuyển dụng enzyme phân giải RNA. Bởi vì RIBOTACs là các tiểu phân tử thay vì protein, nên nó có thể dễ dàng được đóng gói thành một viên thuốc thuận tiện sử dụng được qua đường miệng.
RIBOTACS – CƠ CHẾ HOẠT ĐỘNG
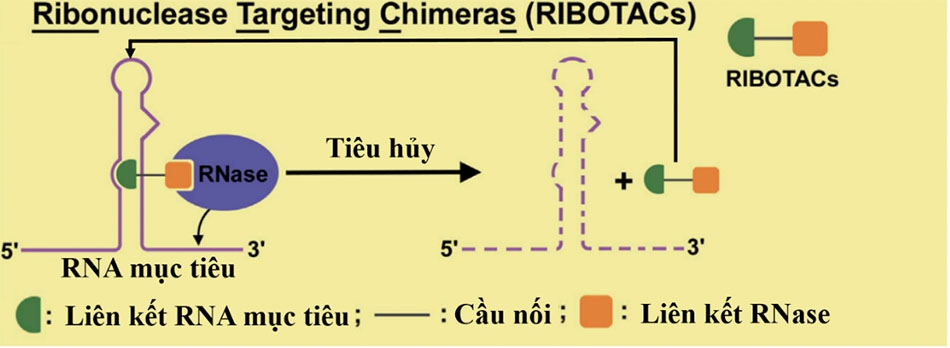
RIBOTACs là tiểu phân tử có 2 đầu ái lực cao: một đầu giúp liên kết đặc hiệu với RNA mục tiêu, đặc biệt là các RNA có cấu trúc bậc 2 và bậc 3; đầu còn lại là tetra-adenylate cho phép tuyển dụng và kích hoạt enzyme phân giải RNA L (RNase L) cho sự tiêu hủy RNA mục tiêu (Hình 1).
KẾT LUẬN
Hiện tại, nhóm nghiên cứu của Matthew D. Disney sẽ tập trung phát triển RIBOTACs cho các loại ung thư khó điều trị như ung thư vú bộ ba âm tính (Triple negative breast cancer), các bệnh rối loạn di truyền được gây ra bởi các RNA độc hại và các loại bệnh có tiên lượng xấu mà bây giờ vẫn chưa có cách điều trị. “Phạm vi ứng dụng của RIBOTACS sẽ trải rộng từ các bệnh ung thư cho đến các bệnh nan y. Về cơ bản là bất kỳ căn bệnh nào mà RNA là yếu tố chính”, theo Matthew D. Disney.
TÀI LIỆU THAM KHẢO
[1] Amanda L Garner, 2019, “RNA-targeted drug discovery: moving beyond promiscuous small-molecule scaffolds“, Future Medicinal Chemistry.
[2] Sourav K. Dey and Samie R. Jaffrey, 2019, “RIBOTACs: Small Molecules Target RNA for Degradation”, Cell Chemical Biology Previews ,07/07/2020.
[3] Amirah Al Idrus, 2018, “Small molecule silences cancer-driving RNA, opens up previously undruggable targets”, Fiercebiotech ,07/07/2020.