Bài viết Tổng kết năm 2018: Thông khí cơ học trẻ em được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Year in Review 2018: Pediatric Mechanical Ventilation
Tóm tắt
Thông khí cơ học thường được sử dụng ở bệnh nhân nhi để đảm bảo trao đổi khí đầy đủ, cải thiện suy hô hấp và cho phép giải quyết các bệnh lý phổi hoặc các bệnh lý nơi khác. Tuy nhiên, vẫn còn một số thách thức quan trọng trong cộng đồng nhi khoa vì có rất ít thử nghiệm ngẫu nhiên có đối chứng quy mô lớn để tạo dữ liệu và thông báo thực hành lâm sàng. Đánh giá này tóm tắt một số khám phá và tiến bộ đã được thực hiện trong thở máy cho trẻ em từ tháng 6 năm 2017 đến tháng 12 năm 2018.
Giới thiệu
Thông khí cơ học thường được sử dụng ở bệnh nhân nhi để đảm bảo trao đổi khí đầy đủ, cải thiện tình trạng suy hô hấp và cho phép giải quyết các bệnh lý phổi hoặc các bệnh lý nơi khác. Một số thách thức quan trọng vẫn còn trong dân số nhi. Vì nhiều lý do thực tế, đã có một số ít các thử nghiệm ngẫu nhiên có đối chứng quy mô lớn để tạo dữ liệu để thông báo thực hành lâm sàng trong thở máy. Trong nhiều trường hợp, cần phải ngoại suy từ các nghiên cứu được thực hiện ở dân số người lớn, nhưng có nhiều khác biệt tồn tại giữa người lớn và trẻ em thở máy. Đánh giá này tóm tắt một số khám phá và tiến bộ trong lĩnh vực thở máy cho trẻ em đã được triển khai từ tháng 6 năm 2017 đến tháng 12 năm 2018.
ARDS nhi
Có một số điểm tương đồng trong sinh lý bệnh của ARDS ở người lớn và trẻ em; cả hai biểu hiện với việc giảm độ giãn nở hệ hô hấp và nhu cầu thở máy, và có tỷ lệ tử vong cao. Tuy nhiên, mô hình thực hành đặc hiệu cho trẻ em, bệnh đi kèm và sự khác biệt về kết cục đòi hỏi phải có một định nghĩa cụ thể về nhi khoa và thậm chí là khác biệt trong các chiến lược điều trị. ARDS ở trẻ em được đặc trưng bởi khởi phát cấp tính, bệnh nhu mô phổi cấp tính trên X quang phổi và chỉ số oxygen hóa ≥ 4 (chỉ số oxygen hóa = [MAP × FIO2]/PaO2) hoặc chỉ số bão hòa oxy ≥ 5 (chỉ số bão hòa oxy = [MAP × FIO2]/SpO2, với điều kiện SpO2 là ≤ 97%). ARDS nhi được phân tầng thành nhẹ, trung bình hoặc nặng. Bệnh nhân mắc ARDS ở trẻ em nặng có khả năng tử vong cao nhất. Nhìn chung, tỷ lệ tử vong ở trẻ em mắc ARDS ở trẻ em là ~ 18%.
Các yếu tố liên quan đến nguy cơ tử vong trong ARDS ở trẻ em
Khemani et al1 đã tìm cách đánh giá mối quan hệ giữa PEEP và tỷ lệ tử vong trong ARDS ở trẻ em. Đó là một nghiên cứu hồi cứu đa trung tâm, kết hợp dữ liệu của 1.134 trẻ thở máy với ARDS ở trẻ em từ 4 cuộc điều tra trước đó. Tỷ lệ tử vong chung được quan sát trong nghiên cứu là 18,6%. 1 Vì rõ ràng việc áp dụng nồng độ oxy khí hít vào và PEEP cao có liên quan đến mức độ nghiêm trọng của ARDS ở trẻ em, các nhà nghiên cứu đã khéo léo tính toán sự khác biệt giữa PEEP được áp dụng (bằng cách sử dụng giá trị trung bình trong ngày đầu tiên của ARDS ở trẻ em) và PEEP được đề xuất từ nhánh dưới bảng PEEP- FIO2 của ARDS network. 1,2 Thật thú vị, các nhà nghiên cứu đã mô tả xu hướng áp đảo để áp dụng PEEP là 6-10 cm H2O và rất ít khi áp dụng mức > 10 cm H2O (Hình 1). Các nhà nghiên cứu lưu ý phát hiện chính của nghiên cứu, bởi vì sự khác biệt giữa PEEP được áp dụng và PEEP được đề xuất bởi ARDSnet tăng lên, do đó, khả năng tử vong cũng tăng.1 Sau khi điều chỉnh nhiều yếu tố lâm sàng, bao gồm mức độ thiếu oxy, cài đặt máy thở, mức độ nghiêm trọng của bệnh tật, sử dụng thuốc tăng co bóp, tỷ lệ mắc bệnh, PEEP thấp hơn mức khuyến nghị có liên quan độc lập với tỷ lệ tử vong cao hơn (tỷ lệ chênh 2.05, CI 95% 1.32- 3.17).1
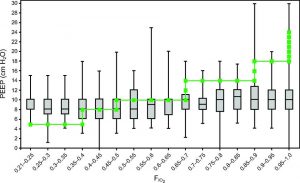
”Giá trị PEEP thực tế là một hàm của các mức FIO2 thực tế (trung vị [bar] và phạm vi liên vùng [hộp]) cho tất cả các đối tượng mắc ARDS ở trẻ em trong ngày đầu tiên thở máy sau khi chẩn đoán ARDS ở trẻ em. Dòng xếp chồng biểu thị các kết hợp mục tiêu giao thức Mạng ARDS của PEEP-FIO2. Nói chung, các bác sĩ lâm sàng sử dụng nhiều PEEP hơn mức khuyến nghị khi FIO2 < 0,4 và sử dụng PEEP ít hơn so với khuyến nghị khi FIO2 > 0,5. PEEP trung bình không vượt quá 10 cm H2O, bất kể FIO2. Từ tài liệu tham khảo 1, với sự cho phép.”
Ngoài ra, các nhà nghiên cứu phân tích đường cong sống sót cho toàn bộ các nhóm đối tượng và nhóm đối tượng dựa trên phạm vi PaO2/FIO2. 1 Nhìn chung, PEEP thấp hơn so với đề xuất của giao thức cho một FIO2 nhất định có liên quan đến tỷ lệ tử vong cao hơn (P < .001). Tuy nhiên, khi phân nhóm theo PaO2/FIO2 ban đầu, phát hiện có ý nghĩa thống kê duy nhất là trong khoảng từ 100 đến 200 (P = .004). 1 Phát hiện này chỉ ra rằng các bệnh nhân trong phạm vi PaO2/FIO2 ban đầu giữa 100-200 có thể thấy lợi ích lớn nhất từ việc sửa đổi ứng dụng PEEP và các nghiên cứu trong tương lai không chỉ tập trung vào việc đánh giá các khái niệm chung mà có lẽ nên đặc biệt quan tâm nhóm này.
Khi nói đến việc đánh giá và tính toán phương sai trong quản lý máy thở, nghiên cứu là quan sát, và do đó, thiết kế nghiên cứu không cho phép giao thức hóa chăm sóc lâm sàng.1 Do đó, cần đặt ra câu hỏi quan trọng về kiểm soát sự phù hợp các yếu tố gây nhiễu, chẳng hạn như các mục tiêu trao đổi khí, thể tích khí lưu thông và các mục tiêu áp lực; sử dụng thuốc an thần và thuốc liệt cơ; chẩn đoán; sự áp dụng và thời gian của các liệu pháp bổ trợ, như nitric oxide dạng hít (INO) và các yếu tố khác. Các nhà nghiên cứu đã áp dụng một thử nghiệm thống kê chính thức để tính đến sự tương tác giữa các bệnh viện, nhưng kết quả này là âm tính (P= .4).1
Tuy nhiên, các nhà nghiên cứu đã khám phá thêm câu hỏi này bằng cách lấy riêng mô hình rủi ro tử vong cho 2 tổ chức chính đóng góp dữ liệu (Bệnh viện Nhi đồng Los Angeles và Bệnh viện Nhi đồng Philadelphia). Sau khi kiểm soát các yếu tố gây nhiễu tiềm ẩn, nguy cơ tử vong liên quan đến sự khác biệt trong PEEP và ARDSnet được khuyến nghị chỉ dành cho bộ dữ liệu của Bệnh viện Nhi đồng Los Angeles (tỷ lệ chênh 2,09, KTC 95% 1,26-3,46); dữ liệu của Bệnh viện Nhi đồng Philadelphia đã chứng minh giảm nguy cơ tử vong (tỷ lệ chênh 0,87, KTC 95% 0,32-2,35), mặc dù CI rộng, nên rất khó để đưa ra kết luận cụ thể. 1 Nhìn chung, nghiên cứu của Khemani et al1 là một đóng góp quan trọng cho tài liệu ARDS nhi khoa và nêu bật các mô hình thực hành thú vị có liên quan đến việc tăng nguy cơ tử vong. Mặc dù những phát hiện này chắc chắn sẽ cung cấp các thử nghiệm lâm sàng trong tương lai, rất khó để chỉ định mối quan hệ nhân quả giữa sự khác biệt của PEEP và tỷ lệ tử vong và do đó, ngoại suy những phát hiện này để sửa đổi thực hành lâm sàng hiện tại sẽ không thận trọng.
Điều trị phụ trợ: INO
Lý do sinh lý để áp dụng INO cho trẻ em mắc ARDS ở trẻ em xuất phát từ thực tế rằng INO là thuốc giãn mạch phổi và là bộ điều biến của chức năng nội mô. Có thể hình dung, làm giãn mạch máu phổi có thể cải thiện sự phù hợp thông khí-tưới máu, giúp cải thiện oxygen hóa và khả năng rút bệnh nhân ra khỏi máy thở. Tuy nhiên, tác dụng oxygen hóa được ghi nhận là chỉ thoáng qua và nhiều nghiên cứu ở cả người lớn và trẻ em đã chứng minh không có lợi ích tử vong khi áp dụng INO trong ARDS.3-5 Tuy nhiên, INO vẫn được áp dụng để cải thiện tình trạng thiếu oxy lên đến 13% trẻ em bị ARDS. 6 Một mặt, sẽ hợp lý khi một nhà khoa học lâm sàng đặt câu hỏi tại sao nhiều nghiên cứu đánh giá lợi ích tử vong của INO trong ARDS ở trẻ em là cần thiết. Mặt khác, một bác sĩ lâm sàng thực tế trên giường có thể lập luận rằng một thử nghiệm INO nói chung là lành tính, dễ thực hiện và có thể được sử dụng như một cầu nối cho các liệu pháp hỗ trợ khác, như thở máy tần số cao hoặc bắt đầu oxygen hóa qua màng ngoài cơ thể. Thật vậy, việc áp dụng INO trong ICU nhi là điều mà nhiều bác sĩ lâm sàng phải vật lộn.
Cuối cùng, Bhalla et al7 đã công bố một nghiên cứu đoàn hệ hồi cứu đa trung tâm của 499 trẻ em thở máy với ARDS ở trẻ em, và tiến hành phân tích phân nhóm 143 đối tượng đã nhận INO. Họ đã áp dụng phương pháp so khớp điểm xu hướng, một phương pháp thống kê nhằm ước tính hiệu quả của việc điều trị bằng cách tính toán các đồng biến có liên quan đến việc điều trị ở vị trí đầu tiên.7 Các hiệp phương sai này bao gồm tuổi, cân nặng, kích hoạt ARDS ở trẻ em và/hoặc nguyên nhân, tỷ lệ tử vong, chỉ số oxygen hóa ban đầu, hỗ trợ vận mạch, nguy cơ tử vong (PRISM III), tổn thương thần kinh cấp tính, ngừng tim và nhập viện. Khi so sánh giữa một đoàn hệ đã nhận được INO và một đoàn hệ không có, chẩn đoán chính là viêm phổi, chỉ số oxygen hóa ban đầu cao hơn và hỗ trợ nhiều thuốc vận mạch hơn, có liên quan đến việc bắt đầu INO.7 Trong phân tích không xác định, lưu ý là tỷ lệ tử vong cao hơn trong nhóm điều trị INO (25,2 so với 16,3%, P = 0,02) và cũng có ngày không thở máy trong 28 ngày trở nên tồi tệ hơn (10 so với 17 ngày, P <0,001). 7
Tuy nhiên, vì những dữ liệu này không được điều chỉnh và INO thường chỉ được bắt đầu ở trẻ em bị thiếu oxy nặng hơn, các nhà nghiên cứu đã áp dụng phân tích phù hợp với điểm số. Điều quan trọng là, trong đoàn hệ phù hợp này, INO không liên quan đến tỷ lệ tử vong (tỷ lệ chênh 1,3, 95% CI 0,56-3,0) hoặc ngày không thở máy trong 28 ngày (tỷ lệ mới mắc 0,91, 95% CI 0,80 – 1,04). 7 Nhìn chung, không có lợi ích gì đối với tỷ lệ tử vong hoặc ngày không có máy thở trong 28 ngày đầu ở những đối tượng sử dụng INO. Tuy nhiên, những đối tượng có đáp ứng oxygen hóa tích cực với INO thì sao? Trong một phân tích thứ cấp, tỷ lệ tử vong không liên quan đến đáp ứng oxygen hóa phân tầng (P = 0,52); tuy nhiên, trong trường hợp trẻ em không thể hiện đáp ứng với INO, các nhà nghiên cứu đã ghi nhận nguy cơ gia tăng số ngày không có máy thở (tỷ lệ chênh 6.1, 95% CI 1.4 -26.3; P = .02). 7 Phát hiện này là lợi ích khoa học nhưng ít lợi ích lâm sàng. Mặc dù việc xác định một nhóm bệnh nhân có sự khác biệt về kết quả dựa trên đáp ứng lâm sàng với một liệu pháp, việc áp dụng INO chỉ để tìm hiểu có bao nhiêu ngày không thở máy là không thực tế hoặc khôn ngoan.
Một trong những hạn chế quan trọng nhất của nghiên cứu hiện tại là thực tế là các nhà nghiên cứu chỉ có thể so khớp 61,5% trẻ em nhận được INO với những người không nhận được INO.7 Sự khác biệt lớn về tỷ lệ tử vong và ngày thở máy. Với một đoàn hệ lớn hơn, có thể xác định được kích thước hiệu ứng nhỏ hơn. Nhìn chung, INO trong nghiên cứu của Bhalla et al7 chứng minh rằng điều trị INO ở ARDS ở trẻ em không liên quan đến sự cải thiện đáng kể về tỷ lệ tử vong hoặc ngày không thở máy. Đây là một trong những nghiên cứu đầu tiên chứng minh tác hại tiềm tàng khi áp dụng INO cho trẻ em mắc ARDS; tuy nhiên, kết luận này dựa trên phân tích chưa được điều chỉnh, vì vậy tiện ích lâm sàng không rõ ràng.
An thần trong ICU và trong quá trình thông khí cơ học Mê sảng
Mê sảng
được đặc trưng bởi sự thay đổi cấp tính về tình trạng tâm thần với sự nhầm lẫn hoặc mức độ thay đổi ý thức không giải thích được xảy ra thường xuyên ở bệnh nhân nhi bị bệnh nặng, bao gồm cả những bệnh nhân đang thở máy.8 Mê sảng có thể là triệu chứng của bệnh hiểm nghèo hoặc tác dụng phụ của các can thiệp được sử dụng trong quá trình chăm sóc, ví dụ, an thần.8 Mối liên quan giữa mê sảng và thở máy có liên quan đến bác sĩ lâm sàng, và phương pháp giảm cả hai điều này là mong muốn.
Traube et al8 đã thực hiện một nghiên cứu hợp tác theo chiều dọc tiền cứu đánh giá mê sảng ở các đối tượng nhi khoa bị bệnh nặng. Họ đã phát hiện ra rằng cả việc điều trị bằng benzodiazine và thở máy đều là những yếu tố dự đoán phụ thuộc của mê sảng ở những đối tượng bị bệnh nặng. Họ cũng phát hiện ra rằng mê sảng có liên quan đến yêu cầu và thời gian thở máy và tử vong ở bệnh nhân này, điều này cho biết giảm thiểu nhu cầu sử dụng thuốc benzodiazepine có thể làm giảm mê sảng, thời gian thở máy và tử vong ở bệnh nhân nhi bệnh nặng, nhưng các thử nghiệm tiền cứu tương lai là cần thiết.
Quản lý máy thở
Chuẩn độ PEEP
Ở trẻ em bị suy hô hấp do thiếu oxy và thở máy, PEEP được chuẩn độ để cải thiện oxy thông qua việc huy động và ổn định phế nang. Tuy nhiên, PEEP có thể làm trầm trọng thêm hoặc làm giảm mức độ tổn thương phổi.9 Thật không may, có rất ít hướng dẫn trong tài liệu nhi khoa để thông báo cho bác sĩ lâm sàng tại giường biết cách điều chỉnh PEEP. Trong hầu hết các trường hợp, lý do để tăng PEEP là cải thiện oxy và giảm tổn thương phổi bằng cách cải thiện thể tích và độ giãn nở của phổi cuối thì hít vào, bằng cách giảm các tỷ lệ khoảng chết và shunt, và mức độ không phù hợp của thông khí-tưới máu.10-12 Trong thực tế, việc sử dụng PEEP ở mức độ trung bình và thậm chí cao đã được chứng minh là an toàn trong dân số trẻ em.13-16 Tuy nhiên, việc áp dụng rộng rãi và nhất quán không được khuyến nghị. 17,18 Các quyết định vốn là không đồng nhất và khác nhau bởi tổ chức và đơn vị y tế, và giữa các bác sĩ lâm sàng.19
Nhóm của chúng tôi đã tìm cách định lượng lượng thời gian cần thiết cho quá trình oxygen hóa và độ giãn nở phổi để cân bằng sau khi tăng hoặc giảm PEEP.20 Nghiên cứu đã được hồi cứu và tổng cộng 200 đối tượng đã đăng ký và bao gồm 1.150 thay đổi PEEP; tuy nhiên, chỉ có 54 trong số các đối tượng này và 171 thay đổi PEEP được đưa vào phân tích dựa trên tiêu chuẩn hoàn thành dữ liệu và chất lượng.20 Đối với mỗi thay đổi PEEP, dữ liệu được thu thập trong 90 phút sau khi tăng.20 Thời gian tới 90% cải thiện oxygen hóa và độ giãn nở phổi đã được tính toán; điều này đã được thực hiện để bình thường hóa sự cải thiện và so sánh tất cả các kết quả với nhau. Trường hợp thay đổi PEEP được phân loại là đáp ứng (cải thiện oxy) hoặc không đáp ứng (không cải thiện hoặc xấu đi trong quá trình oxygen hóa).
Ở những người đáp ứng, thời gian đến 90% cần 38 phút cho việc cải thiện độ giãn nở và 71 phút cho quá trình cải thiện oxygen hóa (Hình 2). 20 Thực tế là cải thiện độ giãn nở trước những thay đổi trong oxygen hóa trong điều trị suy hô hấp do thiếu oxy có ý nghĩa. Sau khi cải thiện độ giãn nở, cần thêm thời gian để mang oxy đến màng mao mạch phế nang.20 Phân phối lại lưu lượng máu trong hệ thống phổi có thể giải thích cho việc cải thiện quá trình oxygen hóa bị trì hoãn. Ngoài ra, chúng tôi quan sát thấy rằng thời gian để đạt được oxy cao điểm sau khi tăng PEEP phụ thuộc vào mức độ nghiêm trọng của suy hô hấp do thiếu oxy; rối loạn chức năng phổi có liên quan đến thời gian cân bằng dài hơn (P = 0,001). 20 Ở những người không đáp ứng, cả hai đều bị suy giảm và oxygen hóa về cơ bản cùng một lúc (65 phút đối với oxy và 64 phút đối với oxygen hóa). 20
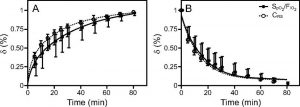
”Giá trị trung bình ± SD được biểu thị bằng các vòng tròn và râu; 6 (%) là thay đổi về chỉ số bão hòa oxy (OSI) (OSI = FIO2 × P × 100/SpO2) hoặc độ giãn nở hệ hô hấp (CRS) so với cực đại tại mỗi thời điểm. A: Người đáp ứng (những người đã tăng oxy sau khi tăng PEEP), OSI được cải thiện 13% và CRS được cải thiện 14% trong khung thời gian theo dõi ở người đáp ứng. B: Người không đáp ứng (không thay đổi oxy hoặc xấu đi sau khi tăng PEEP). Từ tài liệu tham khảo 20, với sự cho phép.”
Những hạn chế của nghiên cứu bao gồm những điều sau đây: nó được thực hiện tại một trung tâm duy nhất, nó đã được hồi cứu, nguyên nhân để tăng PEEP không được kiểm soát và mức độ mà PEEP được chuẩn độ chỉ là 1-3 cm H2O.20 Cung lượng tim cũng không được đo và có thể đã được một yếu tố gây nhiễu. Tuy nhiên, nhịp tim, huyết áp động mạch trung bình, loại bỏ CO2 và tần số thở được ghi lại trong suốt thời gian 90 phút và báo cáo không có thay đổi nào ngoại trừ nhịp tim, giảm khi nhịp từ 120 xuống còn 118 nhịp/phút (P = .02). 20 Nếu cung lượng tim đã tham gia vào thay đổi oxygen hóa, thì sự gia tăng sẽ được dự đoán là huyết áp và nhịp tim. Bởi vì đây không phải là trường hợp trong nghiên cứu hiện tại, không chắc điều này đóng vai trò quan trọng. Thật khó để đề xuất rằng những phát hiện này cho việc “wait and see” và tiếp cận quản lý PEEP, nhưng tiếp tục đánh giá những phát hiện này tiền cứu được chỉ định. Nếu được xác nhận, những phát hiện này có thể giúp các bác sĩ lâm sàng bên giường xác định thời gian tối ưu cần thiết giữa các thay đổi PEEP.
Hỗ trợ thông khí điều chỉnh theo thần kinh sau phẫu thuật tim nhi
Trẻ em thở máy sau phẫu thuật tim cần được chăm sóc đặc biệt và chiến lược thở máy thường khác với thở máy bảo vệ phổi. Áp lực trong lồng ngực có thể làm giảm trở lại tĩnh mạch và tăng hậu tải tâm thất phải, và như vậy, chiến lược thể tích khí lưu thông cao hơn, nhịp thở thấp hơn được áp dụng để giảm áp lực đường thở trung bình trong khi vẫn duy trì được thông khí phút thích hợp.21,22 – Hỗ trợ thông khí điều chỉnh theo thần kinh (NAVA, Neurally-Adjusted Ventilatory Assist) là một chế độ thông khí sử dụng hoạt động điện của cơ hoành, được đặt bởi một ống thông đặt trong thực quản, để kích hoạt máy thở cơ học và cung cấp áp lực dương dựa trên mức độ phát hiện của hoạt động điện. 23 Nhờ cơ chế kích hoạt, không phụ thuộc vào mạch thở, NAVA có thể mang lại lợi ích tiềm năng cho những bệnh nhân có hoạt động tim tăng cường hoặc những người được hỗ trợ với thiết bị hỗ trợ tâm thất. Do tim nằm rất gần khí quản, hoạt động của tim tăng cường có thể gây ra dao động dòng chảy trong mạch thở và dẫn đến tự động kích hoạt với kích hoạt dòng và áp lực truyền thống.
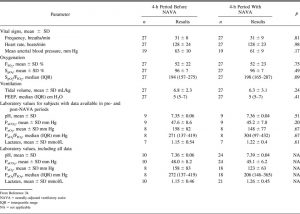
Crulli et al24 đã báo cáo kinh nghiệm lâm sàng với NAVA áp dụng cho trẻ em sau phẫu thuật tim. Nghiên cứu đã được hồi cứu và bao gồm dữ liệu dấu hiệu sinh tồn, các thông số máy thở, trao đổi khí và dữ liệu khí máu động mạch. Tổng cộng có 28 đối tượng đã tham gia vào nghiên cứu, bao gồm cả những người đang sử dụng NAVA24 không xâm lấn hoặc xâm lấn, các nhà nghiên cứu báo cáo giảm áp lực hít vào đỉnh từ 20,9 cm H2O khi thở máy áp lực hoặc thể tích xuống đến 15,1 cm H2O trong khi sử dụng NAVA (P <0,001). 24 Các nhà nghiên cứu không báo cáo áp lực đường thở trung bình, nhưng có thể giả định rằng nó giảm vì tần số thở tương tự trước và trong khi dùng NAVA. Cần lưu ý rằng thể tích khí lưu thông là 0,5 ml/kg thấp hơn trong NAVA so với đường cơ sở, nhưng kết quả này không có ý nghĩa thống kê (Bảng 1). Không có yếu tố nào khác được ghi nhận là khác nhau trong nghiên cứu trước đây so với trong NAVA.24 Khó có thể đưa ra bất kỳ khuyến nghị lâm sàng nào dựa trên các kết quả này bởi vì thiết kế nghiên cứu đã loại trừ một khả năng đánh giá lưu lượng mạch máu phổi hoặc một thông số thay thế nó. Các nhà nghiên cứu lưu ý rằng về tổng thể, NAVA được dung nạp tốt và một số tình huống NAVA có thể chứng minh là có lợi; tuy nhiên, như các nhà nghiên cứu kết luận, các thử nghiệm tiền cứu là cần thiết để đánh giá hiệu quả của NAVA đối với các kết quả chức năng ngắn hạn, như sức cản của mạch máu phổi và lưu lượng máu, mà cả về kết quả lâm sàng, bao gồm cả thời gian thở máy, thời gian ICU ở lại, và tỷ lệ tử vong.24
Thông khí tại nhà
Những cải tiến trong công nghệ và thay đổi trong các chiến lược thông khí cơ học đã dẫn đến sự gia tăng thông khí dài hạn bên ngoài ICU. Thông khí cơ học tại một cơ sở dài hạn hoặc tại nhà giúp giảm gánh nặng điều tra dân số đối với ICU và chi phí tài chính cho các đợt lưu trú ICU dài. Nó cũng cho phép bệnh nhân cần thở máy để sống thoải mái trong nhà và có thể giảm gánh nặng bệnh viện trong một số trường hợp. Amirnovin et al25 đã tiến hành phân tích hồi cứu trong khoảng thời gian 26 năm đánh giá xu hướng của các đối tượng nhi khoa cần thở máy tại nhà sau khi nhập viện. Họ tìm thấy sự gia tăng tần suất của các đối tượng được xuất viện với thông khí tại nhà trong khoảng thời gian đó; họ cũng báo cáo sự gia tăng độ phức tạp của những năm gần đây, mà họ có thể là do công nghệ máy thở tiên tiến hơn, đặc biệt là sự ra đời của van PEEP bên trong máy thở gia đình.25 Mặc dù báo cáo này chỉ dựa trên một đánh giá sơ đồ hồi cứu, nó cho thấy sự gia tăng về tỷ lệ thông khí tại nhà, có lẽ do những thay đổi trong công nghệ và tiêu chuẩn thông khí đòi hỏi phải nhập học ICU. Khi việc theo dõi và điều trị từ xa và tự động từ xa trở nên khó khăn hơn, khả năng thông khí tại nhà của bệnh nhân nhi sẽ tiếp tục tăng.
Chất lượng và an toàn
Trọng lượng cơ thể lý tưởng
Tiện ích của trọng lượng cơ thể lý tưởng (IBW) như một phương pháp bình thường hóa thể tích khí lưu thông khi thở máy đã được thiết lập tốt ở trẻ sơ sinh và ở bệnh nhân nhi và người lớn. Thật vậy, IBW chỉ đơn giản là một thông số thay thế thô cho tổng thể tích phổi vì bệnh nhân cao hơn hoặc nam có xu hướng có dung tích phổi lớn hơn. Mặc dù vậy, một phương pháp phổ biến để tính toán IBW vẫn chưa được thiết lập trong dân số nhi khoa.
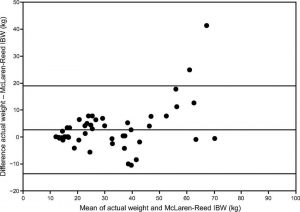
Bilharz et al26 đã nghiên cứu 58 đối tượng nhi khoa được thở máy và so sánh 3 phương pháp tính toán IBW với trọng lượng cơ thể thực tế. Họ đã sử dụng phân tích Bland-Altman để định lượng cá nhân giữa mỗi phương pháp và trọng lượng cơ thể thực tế (Hình 3).26 Họ cũng báo cáo số lượng đối tượng sẽ có một lỗi quan trọng về mặt lâm sàng, nghĩa là một chênh lệch ≥ 10% giữa trọng lượng cơ thể thực tế và IBW. Phân tích Bland-Altman cho thấy sự khác biệt giữa trọng lượng cơ thể thực tế và IBW tăng ở những đối tượng lớn hơn và rõ ràng nhất ở những người > 25 kg.26 Ngoài ra, phần lớn các đối tượng (51,7-56,9%) đã chứng minh một lỗi quan trọng về mặt lâm sàng. Phân tích các dữ liệu này nhấn mạnh tầm quan trọng của các phép đo chiều cao và tính toán IBW để tạo điều kiện cho các phép đo thể tích khí lưu thông chính xác trong ICU nhi. Các nhà nghiên cứu cũng lưu ý rằng một phương pháp sử dụng dữ liệu chỉ số khối cơ thể được chỉ định cho bệnh nhân > 2 tuổi. 26
Trong một phân tích post-hoc lớn, đa trung tâm, Ward et al27 đã kiểm tra sự thay đổi trong tính toán IBW ở trẻ em và kiểm tra 4 phương pháp. Các nhà nghiên cứu đã tìm cách xác định phương pháp tính toán tốt nhất cho tính toán IBW, được định nghĩa là (1) có thể được tính trong phần lớn các đối tượng, (2) thể hiện sự đồng thuận tốt với các phương pháp khác và (3) sẽ dẫn đến việc sử dụng khí lưu thông thấp hơn.27 Lưu ý rằng các phương pháp khác để tính toán IBW có phương sai lớn, đặc biệt là trong các đối tượng > 10 tuổi. Các nhà nghiên cứu khuyến nghị sử dụng phương pháp McLaren vì nó có thể được áp dụng ở > 90% dân số và thể hiện sự đồng thuận tốt với các phương pháp khác.27
Sự kiện liên quan đến máy thở và bệnh viêm phổi
Vào năm 2013, Trung tâm kiểm soát và phòng ngừa dịch bệnh đã đưa ra một định nghĩa giám sát quốc gia thay thế viêm phổi liên quan đến máy thở (VAP) bằng một sự kiện liên quan đến máy thở (VAE) và đặc biệt phác thảo một định nghĩa về VAE nhi khoa. VAE ở trẻ em được xác định bằng tình trạng suy giảm tình trạng hô hấp sau một thời gian ổn định hoặc cải thiện khi thở máy. Thời gian thông khí ổn định được xác định là 2 ngày theo lịch trong đó áp suất đường thở trung bình tối thiểu hàng ngày và FIO2 không thay đổi hoặc giảm. Nếu, sau 2 ngày ổn định này được theo sau bởi sự gia tăng áp lực đường thở trung bình ≥ 4 cm H2O hoặc FIO2 ≥ 25% trong 2 ngày, thì đã xảy ra VAE. Tỷ lệ mắc VAE chung ở trẻ em là ~ 3 trên 1.000 ngày thở máy và có liên quan đến nguy cơ tử vong và bệnh tật nghiêm trọng.
Chomton et al30 đã thực hiện một cuộc điều tra hồi cứu một trung tâm duy nhất của 284 trẻ em về thở máy. Trong đoàn hệ này, 10,6% đối tượng đáp ứng các tiêu chí của Trung tâm kiểm soát và phòng ngừa dịch bệnh đối với VAP, 7 trên 1.000 ngày tiêm tĩnh mạch.30 VAP có liên quan đến thời gian thở máy và thời gian lưu lại ICU lâu hơn. Sử dụng nội soi phế quản (P = 0,03), cho ăn đường ruột liên tục (P = 0,02) và tỷ lệ mắc ARDS ở trẻ em (P = 0,03) cao hơn ở những trẻ mắc bệnh VAP so với những người không có.30 Thao tác đường thở trong quá trình nội soi phế quản và nuôi dưỡng đường ruột có thể liên quan đến VAP vì cả hai đều cung cấp một cơ chế gây ô nhiễm mạch thở hoặc hít sặc dịch dạ dày. Tuy nhiên, vì cả hai không được đo trực tiếp trong nghiên cứu, rất khó để chỉ định nguyên nhân. Thật không may, các nhà nghiên cứu đã không báo cáo số lượng đối tượng được phân loại là VAE trong nhóm thuần tập lớn hơn nhưng lưu ý rằng, trong số 30 đối tượng có VAP, 17 cũng đáp ứng các tiêu chí cho VAE người lớn (ngưỡng PEEP và FIO2 khác nhau).30
VAE nhi là một công cụ sàng lọc quan trọng trong kích hoạt thông khí ở nhi khoa. Nó tạo điều kiện cho việc xác định khách quan các sự kiện có liên quan đến việc tăng thời gian lưu lại ICU ở trẻ em, sử dụng thông khí cơ học và tử vong. Bước tiếp theo sẽ là thực hành nhằm mục đích giảm xác suất VAE trong ICU nhi khoa và cố gắng đưa tỷ lệ đó về 0.
Cai máy thở và ngưng thở máy
Kể từ khi phát triển các thử nghiệm thở tự phát được tiêu chuẩn hóa và chứng minh giá trị của chúng ở bệnh nhân cai thở máy, việc phát triển các giao thức để tạo điều kiện cho các thử nghiệm này đã được đề xuất tại nhiều trung tâm ở nhiều định dạng31,32 được đánh giá chủ yếu dựa trên kết quả bệnh nhân đã được chứng minh. Tuy nhiên, việc các kết quả chưa được cải thiện có thể là dấu hiệu cho thấy độ tuân thủ kém với giao thức hơn là cho thấy giao thức đó không hiệu quả.
Krawiec et al 33 đã khởi xướng một giao thức điều trị hô hấp được thiết kế để tăng đánh giá sớm sự sẵn sàng thử nghiệm hơi thở tự phát ở các đối tượng nhi khoa thở máy bằng cách cho phép các nhà trị liệu hô hấp bắt đầu các thử nghiệm hơi thở tự phát nếu các đối tượng đáp ứng các tiêu chí cho thấy sự ổn định của tim phổi và giảm thuốc an thần. Sau đó, họ đã tiến hành xem xét biểu đồ hồi cứu để đánh giá hiệu quả của giao thức này đối với kết quả của bệnh nhân, bao gồm thời gian thở máy, thời gian ở lại ICU và thời gian nằm viện. Họ cũng báo cáo sự tuân thủ với giao thức. Không có sự khác biệt trong kết quả đã được tìm thấy sau khi bắt đầu giao thức điều trị hô hấp; tuy nhiên, họ đã báo cáo độ tuân thủ 56% về thể chế với giao thức mới, điều này có thể cho thấy rằng giao thức không được thực thi hiệu quả thay vì không hiệu quả trong việc thay đổi kết quả bệnh nhân.33 Lưu ý, họ đã báo cáo sự gia tăng sử dụng thông khí không xâm lấn sau khi bắt đầu giao thức, có thể là do vai trò của nhà trị liệu hô hấp tăng lên hoặc sự hiện diện trong quá trình cai máy của bệnh nhân.33
Kết luận
Từ tháng 6 năm 2017 đến tháng 12 năm 2018, các báo cáo đánh giá liên quan đến thở máy ở trẻ em đã được công bố để đánh giá việc quản lý và tử vong của ARDS ở trẻ em, việc sử dụng INO, sự liên quan của mê sảng, chuẩn độ PEEP, sử dụng NAVA, những tiến bộ trong điều trị thông khí tại nhà, tính toán IBW, sàng lọc VAEs ở trẻ em và hiệu quả của các phác đồ cai máy theo phương pháp trị liệu hô hấp. Nghệ thuật và khoa học về thở máy nhi khoa không có nghĩa là đã được giải quyết, và sự cải thiện hiểu biết của chúng tôi tiếp tục tăng lên. Điều cần thiết là các bác sĩ lâm sàng hô hấp cần phải thông tin về thực tiễn lâm sàng của họ bằng cách đánh giá các tài liệu có sẵn và lập kế hoạch nghiên cứu trong tương lai dựa trên nhu cầu rất lớn trong lĩnh vực này.





