Bài viết Dùng thuốc chẹn thần kinh cơ sớm trong Hội chứng suy hô hấp cấp tính được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Early Neuromuscular Blockade in the Acute Respiratory Distress Syndrome
Tóm tắt
Bối cảnh
Những lợi ích của thuốc phong bế thần kinh cơ liên tục sớm ở những bệnh nhân mắc hội chứng suy hô hấp cấp tính (ARDS) đang được thở máy vẫn chưa rõ ràng.
Phương pháp
Chúng tôi đã chỉ định ngẫu nhiên các bệnh nhân mắc ARDS từ trung bình đến nặng (được xác định bằng tỷ lệ áp suất riêng phần của oxy động mạch với tỷ lệ oxy khí hít vào < 150 mm Hg với áp lực dương cuối thì thở ra [PEEP] 8 cm nước) truyền cisatracurium liên tục trong 48 giờ với thuốc an thần sâu đồng thời (nhóm can thiệp) hoặc phương pháp chăm sóc thông thường mà không cần thuốc phong bế thần kinh cơ thông thường và với mục tiêu an thần nhẹ hơn (nhóm đối chứng). Các chiến lược thông khí cơ học giống nhau đã được sử dụng trong cả hai nhóm, bao gồm cả chiến lược liên quan đến PEEP cao. Điểm cuối chính là tử vong tại bệnh viện do bất kỳ nguyên nhân nào sau 90 ngày.
Các kết quả
Thử nghiệm đã dừng lại ở phân tích tạm thời lần thứ hai vì không hiệu quả. Chúng tôi đã đăng ký 1006 bệnh nhân sớm sau khi bắt đầu điều trị ARDS từ trung bình đến nặng (trung bình, 7,6 giờ sau khi khởi phát). Trong 48 giờ đầu sau khi ngẫu nhiên, 488 trong số 501 bệnh nhân (97,4%) trong nhóm can thiệp bắt đầu truyền cisatracurium liên tục (thời gian truyền trung bình, 47,8 giờ; liều trung bình, 1807 mg) và 86 trong số 50 bệnh nhân ( 17,0%) trong nhóm đối chứng nhận được một thuốc phong bế thần kinh cơ (liều trung bình, 38 mg). Sau 90 ngày, 213 bệnh nhân (42,5%) trong nhóm can thiệp và 216 (42,8%) trong nhóm đối chứng đã chết trước khi xuất viện (chênh lệch giữa các nhóm, -0,3 điểm phần trăm; khoảng tin cậy 95%, −6,4 đến 5,9; P = 0,93). Khi ở trong bệnh viện, bệnh nhân trong nhóm can thiệp ít hoạt động thể chất và có nhiều biến cố tim mạch bất lợi hơn so với bệnh nhân trong nhóm điều trị. Không có sự khác biệt giữa các nhóm trong các điểm cuối được xác định vào lúc 3, 6 và 12 tháng.
Kết luận
Trong số những bệnh nhân mắc ARDS từ trung bình đến nặng được điều trị bằng chiến lược liên quan đến PEEP cao, không có sự khác biệt đáng kể về tỷ lệ tử vong ở 90 ngày giữa những bệnh nhân được tiêm truyền cisatracurium sớm và liên tục và những người được điều trị chăm sóc thông thường tiếp cận với các mục tiêu an thần nhẹ hơn. (Được tài trợ bởi Viện Tim, Phổi và Máu Quốc gia; thử nghiệm ROSE ClinicalTrials.gov, NCT02509078.)
Mở đầu
Hội chứng suy hô hấp cấp tính (ARDS) là một dạng viêm của tổn thương phổi dẫn đến suy hô hấp do thiếu oxy, giảm độ giãn nở phổi và hình mờ phế nang hai bên trên hình ảnh x quang ngực.[1] Các phương pháp được sử dụng để áp dụng thở máy ở những bệnh nhân mắc ARDS có thể ảnh hưởng đến sự sống còn và kết quả sau khi xuất viện từ khoa chăm sóc đặc biệt (ICU). Ví dụ, thuốc phong bế thần kinh cơ làm giảm sự không đồng bộ máy thở của bệnh nhân, công thở và sự tích tụ của dịch phế nang; bệnh nhân mắc ARDS có thể được hưởng lợi từ những kết quả này.[2] Tuy nhiên, việc sử dụng thuốc phong bế thần kinh cơ kéo dài có liên quan đến yếu cơ thần kinh sau đó.[3,4] Thử nghiệm đa trung tâm lớn nhất cho đến nay (thử nghiệm ARDS et Curarisation Systematique [ACURASYS]) đã được tiến hành một thập kỷ trước đây và thực tiễn ICU đã thay đổi kể từ đó. Các nhà điều tra của cuộc thử nghiệm đó đã báo cáo rằng việc truyền thuốc phong bế thần kinh cơ trong 48 giờ ở những bệnh nhân mắc ARDS từ trung bình đến nặng (được xác định bằng tỷ lệ áp suất một phần của oxy động mạch [PaO2] với tỷ lệ oxy khí hít vào [FiO2] <150 mm Hg với áp lực dương cuối thì thở ra [PEEP] ≥5 cm nước) dẫn đến tỷ lệ tử vong thấp hơn so với chiến lược an thần sâu mà không cần thuốc phong bế thần kinh cơ thường xuyên.[5] Mặc dù những kết quả đáng khích lệ này, thuốc phong bế thần kinh cơ sớm không được áp dụng rộng rãi và chỉ được khuyến nghị yếu trong các hướng dẫn hiện hành.[6-9] Mối quan tâm tiềm ẩn bao gồm thiếu nghiên cứu so sánh thuốc phong bế thần kinh cơ và an thần sâu với thực hành hiện nay (thúc đẩy các mục tiêu an thần nhẹ hơn [8,10-12]), ảnh hưởng của thuốc phong bế thần kinh cơ đối với chức năng thần kinh cơ và các kết quả lâu dài khác.[2,13] Ngoài ra, phong bế thần kinh cơ đòi hỏi phải dùng thuốc an thần sâu, chính nó có thể dẫn đến kết quả tiêu cực.[6,12,14]
Mạng lưới thử nghiệm lâm sàng phòng ngừa và điều trị sớm chấn thương phổi cấp tính (PETAL) của Viện Tim, Phổi và Máu Quốc gia (NHLBI) đã tiến hành đánh giá lại thử nghiệm ức chế thần kinh cơ sớm (ROSE) toàn thân – một thử nghiệm ngẫu nhiên với ARDS từ trung bình đến nặng – để xác định hiệu quả và an toàn của thuốc phong bế thần kinh cơ sớm với thuốc an thần nặng đồng thời so với chiến lược chăm sóc thông thường với các mục tiêu an thần nhẹ hơn. Chúng tôi đã đưa ra giả thuyết rằng việc sử dụng thuốc phong bế thần kinh cơ sớm sẽ dẫn đến tỷ lệ tử vong do hít phải do mọi nguyên nhân thấp hơn ở 90 ngày so với chăm sóc thông thường.
Phương pháp
Thiết kế thử nghiệm và giám sát
Chúng tôi đã thiết kế thử nghiệm ROSE phù hợp với một số yếu tố của thử nghiệm ACURASYS.[5,15] Điểm tương đồng bao gồm việc sử dụng cùng một thuốc phong bế thần kinh cơ (cisatracurium) với cùng chế độ điều trị và thời gian điều trị. Một sự khác biệt chính là việc chúng tôi sử dụng các mục tiêu an thần nhẹ hơn trong nhóm kiểm soát để phù hợp với các khuyến nghị thực hành hiện tại.[6,8,9] Để giảm thiểu sự khác biệt có thể gây nhiễu trong việc sử dụng các quy tắc, chúng tôi đã chỉ định cách tiếp cận thông khí cơ học trong giao thức, bao gồm sử dụng chiến lược liên quan đến PEEP cao và chúng tôi khuyến nghị sử dụng chiến lược dịch truyền hạn chế.[16-18] Để nắm bắt những khác biệt tiềm ẩn trong di chứng muộn, những người đánh giá không biết về sự phân công nhóm đã phỏng vấn các bệnh nhân còn sống hoặc người đại diện của họ vào lúc 3, 6 và 12 tháng sau khi ngẫu nhiên. Chúng tôi đã xuất bản giao thức và gửi kế hoạch phân tích thống kê (có sẵn toàn văn của bài viết này tại NEJM.org) cho NHLBI trước khi phân tích dữ liệu.[15] Một hội đồng đánh giá thể chế trung tâm và một ban giám sát dữ liệu và an toàn do NHLBI chỉ định cung cấp giám sát. Trung tâm điều phối của chúng tôi đã thu thập và phân tích dữ liệu, và ủy ban giao thức đã viết bản thảo đầu tiên của bản thảo. Chúng tôi bảo đảm tính chính xác và đầy đủ của dữ liệu và tính trung thực của thử nghiệm với giao thức. Chúng tôi đã nhận được sự đồng ý bằng văn bản từ đại diện của tất cả các bệnh nhân.
Bệnh nhân
Chúng tôi đã ghi danh những bệnh nhân được thông khí thông qua ống nội khí quản và có các tiêu chí sau trong vòng dưới 48 giờ: PaO2: FiO2 dưới 150 mm Hg với PEEP từ 8 cm trở lên; các hình ảnh tổn thương phổi hai bên trên X quang phổi hoặc trên chụp cắt lớp vi tính không thể thực hiện được do tràn dịch, xẹp phổi hoặc nốt; và suy hô hấp không thể giải thích được do suy tim hoặc quá tải dịch truyền. Nếu không có kết quả phân tích khí máu động mạch, PaO2 được suy ra từ độ bão hòa oxy được đo bằng phương pháp độ bão hòa oxy mạch đập (SpO2) và được sử dụng để ước tính PaO2:FiO2 ở mức PEEP 8 cm trở lên. Danh sách đầy đủ các tiêu chí loại trừ được cung cấp trong phần Phương pháp bổ sung trong Phụ lục bổ sung, có sẵn tại NEJM.org.
Cách ngẫu nhiên và điều trị
Chúng tôi đã chỉ định ngẫu nhiên các bệnh nhân theo tỷ lệ 1:1 để nhận được 48 giờ thuốc phong bế thần kinh cơ liên tục với thuốc an thần sâu đồng thời (nhóm can thiệp) hoặc được chăm sóc thông thường mà không cần thuốc phong bế thần kinh cơ thông thường và với các mục tiêu an thần nhẹ (nhóm đối chứng). Bệnh nhân trong nhóm can thiệp chưa được an thần sâu tại điểm cơ sở đã được an thần sâu trong vòng 4 giờ sau khi ngẫu nhiên. Sau đó, những bệnh nhân trong nhóm này đã nhận được một liều thuốc tiêm tĩnh mạch 15 mg cisatracurium, sau đó là truyền tĩnh mạch liên tục 37,5 mg mỗi giờ trong 48 giờ. Mặc dù điều trị không được thực hiện một cách mù đôi, chúng tôi đã chọn không điều chỉnh liều thuốc phong bế thần kinh cơ theo kích thích thần kinh ngoại biên để điều chỉnh lại chế độ dùng thuốc trong thử nghiệm ACURASYS và để tạo điều kiện tuân thủ giao thức của thử nghiệm. Thuốc phong bế thần kinh cơ có thể được dừng lại sớm nếu bệnh nhân đáp ứng các tiêu chí cai thở máy (FiO2 40% và PEEP ≤ 8 cm nước) trong ít nhất 12 giờ. Chúng tôi đề nghị sử dụng thuốc an thần nhẹ trong nhóm kiểm soát. Thuốc an thần nhẹ được xác định bằng điểm số trên Thang điểm an thần của thang điểm Kích thích- An thần của Richmond ở 0 hoặc −1 (điểm số từ 4 [combative] đến -5 [unresponsive], với điểm 0 cho thấy bệnh nhân tỉnh táo và bình tĩnh), điểm số trên thang điểm Kích thích-An thần của Riker, 3 hoặc 4 (điểm số từ 1 [Riker] đến 7 [dangerous agitation], với điểm số 4 cho thấy bệnh nhân bình tĩnh và hợp tác), hoặc điểm trên Thang đo an thần Ramsay từ 2 hoặc 3 (điểm số nằm trong khoảng từ 1 [anxious, restless] đến 6 [unresponsive], với điểm 2 cho thấy bệnh nhân hợp tác và có định hướng).[21-23]
Thủ tục thử nghiệm chung
Tất cả các bệnh nhân được điều trị bằng chiến lược thông khí thể tích khí lưu thông thấp trong vòng 2 giờ sau khi ngẫu nhiên hóa và chiến lược PEEP cao trong tối đa 5 ngày sau khi ngẫu nhiên.[16,24,25] Chúng tôi cho phép PEEP thấp hơn nếu bác sĩ lâm sàng nghi ngờ rằng PEEP cao hơn làm xấu đi tình trạng oxy hóa, hạ huyết áp, áp lực cao nguyên cao (> 30 cm nước) hoặc toan máu (pH <7,15) mặc dù giảm thể tích khí lưu thông, tiêm dịch truyền hoặc tăng tần số hô hấp. PEEP thấp hơn cũng được cho phép nếu viêm phổi phát triển hoặc nếu bệnh nhân có nguy cơ cao mắc bệnh barotrauma. Việc sử dụng tư thế nằm sấp theo ý của bác sĩ lâm sàng, mặc dù chúng tôi khuyên các bác sĩ lâm sàng nên đợi ít nhất 12 giờ sau khi bắt đầu điều trị ARDS, như được đề xuất bởi bằng chứng hiện tại,[26] và tránh sử dụng tự động thuốc phong bế thần kinh cơ. Chúng tôi cho phép tiêm bolus tiêm tĩnh mạch mở 20 mg cisatracurium ở cả hai nhóm nếu bệnh nhân đáp ứng các tiêu chí được chỉ định trước (xem phần Phương pháp bổ sung trong Phụ lục bổ sung). Sau thời gian can thiệp thử nghiệm kéo dài 48 giờ, các quyết định liên quan đến việc sử dụng thêm thuốc phong bế thần kinh cơ, bao gồm cả việc lựa chọn tác nhân, được để lại cho bác sĩ điều trị. Để tạo điều kiện so sánh, chúng tôi báo cáo tất cả các sử dụng thuốc phong bế thần kinh cơ như liều cisatracurium tương đương.[27]
Điểm cuối
Điểm cuối chính là tử vong tại bệnh viện do bất kỳ nguyên nhân nào sau 90 ngày (tại bệnh viện được coi là thời gian ở bệnh viện thử nghiệm cộng với chuyển đến bệnh viện khác, bao gồm cả thời gian ở các cơ sở chăm sóc cấp tính dài hạn). Điểm cuối phụ là rối loạn chức năng nội tạng (được đánh giá dựa trên điểm số SOFA [Sequential Organ Failure], điểm số từ 0 đến 4 cho mỗi sáu hệ thống cơ quan, với điểm số cao hơn cho thấy rối loạn chức năng cơ quan nghiêm trọng hơn), tử vong tại bệnh viện ngày 28, ngày không bị rối loạn chức năng nội tạng, ngày không ở ICU, ngày không thở máy và ngày không ở bệnh viện vào ngày 28. Điểm cuối được đánh giá ở 3, 6 và 12 tháng là sống sót, khuyết tật, chất lượng cuộc sống liên quan sức khỏe, sức khỏe được báo cáo của bệnh nhân, can thiệp đau, các triệu chứng giống như căng thẳng sau chấn thương, chức năng nhận thức và trở lại làm việc.[29-33] Điểm cuối an toàn bao gồm phục hồi tê liệt (đánh giá bằng bảng câu hỏi Brice đã sửa đổi), yếu cơ mắc phải-ICU cho đến ngày 28 (được đánh giá theo thang điểm của Hội đồng nghiên cứu y tế, bao gồm điểm số cho sức mạnh cơ ở 6 nhóm cơ ở mỗi bên của cơ thể, cho tổng số 12 nhóm cơ; nhóm cơ có thể từ 0 [không có chuyển động quan sát được] đến 5 [các cơ co lại bình thường chống lại toàn bộ sức đề kháng], với tổng điểm từ 0 đến 60), các hạn chế về hoạt động thể chất (được đánh giá theo Thang đo di động ICU; điểm số dao động từ 0 [không cử động] đến 10 [đi bộ mà không cần hỗ trợ]), rung tâm nhĩ mới khởi phát hoặc nhịp nhanh trên thất, barotrauma và các tác dụng phụ được báo cáo của điều tra viên.[34-38] Chúng tôi không thể đảm bảo rằng các giám định viên trong bệnh viện đã kết thúc các điểm không biết về nhóm điều trị, nhưng tất cả các điểm cuối sau khi xuất viện được đánh giá bởi các nhân viên thử nghiệm, những người không biết về sự phân công của nhóm.
Phân tích thống kê
Theo giả định rằng 27% bệnh nhân trong nhóm can thiệp và 35% trong nhóm đối chứng sẽ chết, chúng tôi đã tính toán rằng 1408 bệnh nhân sẽ cần phải đăng ký để cung cấp thử nghiệm với 90% sức mạnh để từ chối giả thuyết khống không có sự khác biệt giữa các nhóm về hiệu quả điều trị, ở mức độ alpha hai mặt 0,05.[5,25,39] Thử nghiệm được thiết kế để dừng lại nếu tính ưu việt của một trong hai nhóm được sử dụng bằng cách sử dụng ranh giới dừng liên tục của nhóm đối xứng, không dừng lại quy tắc cho sự vô ích.[40]
Chúng tôi đã so sánh điểm kết thúc chính giữa các nhóm với việc sử dụng thử nghiệm Wald cho sự khác biệt của hai tỷ lệ. Chúng tôi đã thực hiện các phân tích được chỉ định trước theo mức độ nghiêm trọng của ARDS (PaO2:FiO2 <120 mm Hg hoặc ≥120 mm Hg) và thời gian ARDS (thời lượng ít hơn hoặc lớn hơn thời gian trung bình từ khi đáp ứng tiêu chí đưa vào ngẫu nhiên) cũng như về hiệu quả của việc loại trừ các bệnh nhân bị dùng thuốc phong bế thần kinh cơ trước đó (các bệnh viện được chia thành các tercile trên cơ sở tỷ lệ loại trừ các bệnh nhân trước đó đã bị thuốc phong bế thần kinh cơ). Chúng tôi cũng kiểm tra sự tương tác giữa nhóm điều trị và giới tính, chủng tộc và dân tộc. Tất cả các tương tác giữa các nhóm điều trị được phân tích theo thang chênh lệch rủi ro với việc sử dụng mô hình tuyến tính tổng quát với hàm phân phối nhị thức và hàm liên kết nhận dạng. Điểm cuối thứ cấp được báo cáo với sự khác biệt quan sát và khoảng tin cậy 95%. Các sự kiện bất lợi được so sánh giữa các nhóm, với sự kiện là đơn vị phân tích và với việc sử dụng hồi quy Poisson có trọng số; các sự kiện không có trọng số được tính bằng 1 và các sự kiện nghiêm trọng có trọng số là 2. Tỷ lệ tử vong sau 90 ngày và 1 năm được so sánh giữa các nhóm với việc sử dụng phép thử z, dựa trên ước tính điểm và sai số chuẩn của bên trong- nhóm chức năng sinh tồn không kiểm duyệt khoảng tham số. Tất cả các phân tích được thực hiện theo nguyên tắc cố ý điều trị, mà không cần điều chỉnh cho nhiều so sánh. Giá trị P hai mặt nhỏ hơn 0,05 được xem xét để biểu thị ý nghĩa thống kê. Các phân tích được thực hiện với phần mềm SAS, phiên bản 9.4 (Viện SAS).
Kết quả
Bệnh nhân
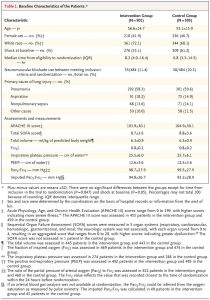
Từ tháng 1 năm 2016 đến tháng 4 năm 2018, chúng tôi đã sàng lọc 4848 bệnh nhân tại 48 bệnh viện trên khắp Hoa Kỳ và 1006 bệnh nhân được đưa vào phân tích chính (Hình 1). Sau khi phân tích tạm thời thứ hai, quyết định dừng thử nghiệm vì vô ích đã được ban giám sát dữ liệu và an toàn đưa ra một cách độc lập; quyết định đã được NHLBI đưa ra và được ban chỉ đạo của PETAL chấp nhận. Lý do phổ biến nhất để loại trừ là cải thiện PaO2:FiO2 trước khi đăng ký (658 bệnh nhân). Lý do phổ biến nhất để loại trừ sau khi sàng lọc là việc nhận được thuốc phong bế thần kinh cơ trước đó (655 bệnh nhân). Trong số những bệnh nhân được ghi danh, 501 được phân ngẫu nhiên vào nhóm can thiệp và 505 cho nhóm đối chứng. Các đặc điểm cơ bản là tương tự nhau trong hai nhóm (Bảng 1 và Bảng S1 trong Phụ lục bổ sung). Bệnh nhân được ghi danh trung bình là 7.6 giờ (phạm vi liên vùng, 3,7 đến 15,6) sau khi chẩn đoán ARDS từ trung bình đến nặng; 9,3% bệnh nhân (94 bệnh nhân) được ghi danh với SpO2:FiO2 đủ điều kiện (Bảng S2 trong Phụ lục bổ sung).
Ức chế thần kinh cơ, an thần và các quy trình chăm sóc khác
Trong nhóm can thiệp, 488 bệnh nhân (97,4%) được truyền dịch cisatracurium, bắt đầu trung bình (± SD) là 1,9 ± 1,4 giờ sau khi ngẫu nhiên. Thời gian trung bình của điều trị bằng cisatracurium trong thời gian can thiệp 48 giờ là 47,8 giờ (phạm vi liên vùng, 43,8 đến 48,0) và liều tích lũy trung bình là 1807 mg (phạm vi liên vùng, 1706 đến 1815). Nhìn chung, truyền thuốc cisatracurium đã dừng lại sớm ở 74 bệnh nhân (14,8%) vì cải thiện lâm sàng. Trong nhóm đối chứng, 86 bệnh nhân (17,0%) đã nhận được một chất ức chế thần kinh cơ trong 48 giờ đầu tiên với liều cisatracurium trung bình (hoặc tương đương) là 38 mg (phạm vi liên vùng, 14 đến 200). Chi tiết bổ sung về việc sử dụng các thuốc phong bế thần kinh cơ cơ được cung cấp trong Bảng S3 trong Phụ lục bổ sung.
Bệnh nhân trong nhóm can thiệp được dùng thuốc an thần sâu hơn so với bệnh nhân trong nhóm đối chứng cả trong thời gian can thiệp 48 giờ và vào ngày thử nghiệm thứ ba (Hình 2).
Trong 24 giờ đầu tiên, các bệnh nhân trong nhóm can thiệp có yêu cầu PEEP thấp hơn so với bệnh nhân trong nhóm đối chứng (chênh lệch giữa các nhóm, -0,9 cm nước; khoảng tin cậy 95% [CI], -1,5 đến -0,4). Trong khoảng thời gian 24 giờ đầu tiên và thứ hai, bệnh nhân trong nhóm can thiệp cũng có thông khí phút thấp hơn (chênh lệch giữa các nhóm vào ngày 1 là -0,7 lít mỗi phút [95% CI, -1,1 đến -0,2], và vào ngày 2, – 0,8 lít mỗi phút [95% CI, -1,2 đến -0,4]), yêu cầu FiO2 thấp hơn (chênh lệch giữa các nhóm ở cả ngày 1 và ngày 2 là -0,04 [95% CI, −0,06 đến – 0,02]) và áp lực đẩy cao hơn (chênh lệch giữa các nhóm vào ngày 1 là 0,7 cm nước [95% CI, 0,0 đến 1,3] và vào ngày 2, 0,8 cm nước [95% CI, 0,1 đến -1,5]). Tuy nhiên, không có sự khác biệt giữa các nhóm trong PaO2:FiO2 từ ngày 1 đến ngày 7. Cải thiện oxy là tương tự ở những bệnh nhân được ghi danh sớm và những người đăng ký muộn sau khi bắt đầu ARDS. Từ ngày 1 đến ngày 7, đã tuân thủ tốt giao thức liên quan đến các khuyến nghị của PEEP và FiO2, và việc tuân thủ các hướng dẫn thông khí được khuyến nghị nằm trong khoảng từ 80,1 đến 87,5% đối với thông khí khí lưu thông thấp (≤6,5 ml mỗi kg trọng lượng cơ thể dự đoán) và 85,6 đến 90,8% đối với áp lực cao nguyên thấp (≤30 cm nước). Cân bằng dịch truyền trung bình hàng ngày là 327 ml (phạm vi liên vùng, −951 đến 1456) vào ngày 2 và -242 ml (phạm vi liên vùng, −1432 đến 728) vào ngày 3 và không có sự khác biệt giữa các nhóm thử nghiệm. Các chi tiết bổ sung được cung cấp trong Hình S1 và Bảng S4 đến S8 trong Phụ lục bổ sung.

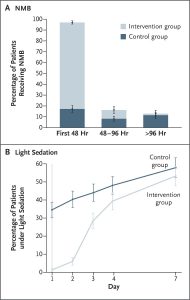
”Bảng A cho thấy tỷ lệ phần trăm trung bình của bệnh nhân bị phong bế thần kinh cơ liên tục và Bảng B cho thấy tỷ lệ trung bình của những bệnh nhân bị an thần nhẹ trong tuần đầu tiên của thử nghiệm. Thuốc an thần nhẹ được xác định bằng điểm số trên Thang điểm Kích thích-An thần của Richmond ở 0 hoặc −1 (điểm số từ 4 [combative] đến -5 [unresponsive], với điểm 0 cho thấy bệnh nhân tỉnh táo và bình tĩnh), điểm số trên thang điểm Kích thích-An thần của Riker, 3 hoặc 4 (điểm số từ 1 [Riker] đến 7 [dangerous agitation], với điểm số 4 cho thấy bệnh nhân bình tĩnh và hợp tác), hoặc điểm trên Thang đo an thần Ramsay từ 2 hoặc 3 (điểm số trong khoảng từ 1 [anxious, restless] đến 6 [unresponsive], với điểm 2 cho thấy bệnh nhân hợp tác và có định hướng).[21-23]”
Điểm cuối chính
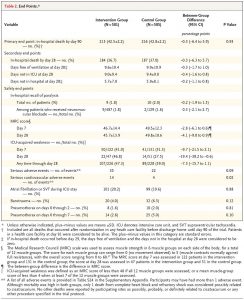
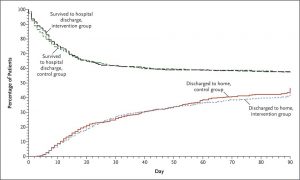
Sau 90 ngày, tử vong tại bệnh viện do bất kỳ nguyên nhân nào gây ra ở 213 bệnh nhân (42,5%) trong nhóm can thiệp và ở 216 bệnh nhân (42,8%) trong nhóm đối chứng (chênh lệch giữa các nhóm, −0,3 điểm phần trăm; 95% CI, −6,4 đến 5,9; P = 0,93) (Hình 3 và Bảng 2). Các tương tác giữa các nhóm điều trị không có ý nghĩa đối với mức độ nghiêm trọng của ARDS, thời gian điều trị ARDS hoặc thuốc phong bế thần kinh cơ trước đó được phân tầng theo phương pháp điều trị tại bệnh viện. Khác với sự tương tác của chỉ định điều trị với nhóm dân tộc (P = 0,02 cho tương tác), không có tương tác nào khác có ý nghĩa (Hình S2 và Bảng S9 đến S15 trong Phụ lục bổ sung).
Điểm cuối phụ
Sau 28 ngày, không có sự khác biệt giữa các nhóm về tỷ lệ tử vong của bệnh viện, những ngày không có thông khí, những ngày ra khỏi ICU hoặc những ngày ra khỏi bệnh viện (Bảng 2). Điểm số SOFA tim mạch ở nhóm can thiệp cao hơn so với nhóm đối chứng vào ngày 1 (khác biệt giữa các nhóm, 0,2; 95% CI, 0,1 đến 0,4) và ngày 2 (chênh lệch nhóm, 0,3; KTC 95%, 0,1 đến 0,5). Tuy nhiên, không có sự khác biệt nào sau đó, cũng như không có sự khác biệt về tổng điểm SOFA hoặc điểm số SOFA dành riêng cho cơ quan khác.
Việc sử dụng các liệu pháp bổ trợ dường như tương tự nhau ở hai nhóm trong thời gian can thiệp 48 giờ (chênh lệch giữa các nhóm, 0,7 điểm phần trăm; 95% CI, −4.0 đến 5.5) và qua ngày 28 (chênh lệch giữa các nhóm, 1.2 điểm phần trăm; KTC 95%, -4,2 đến 6,6). Nhìn chung, tư thế nằm sấp sử dụng ở 15,8% bệnh nhân (159 bệnh nhân), với cách sử dụng tương tự ở hai nhóm (chênh lệch giữa các nhóm, 1,9 điểm phần trăm; 95% CI, −2,6 đến 6,4). Hầu hết (56% [42 bệnh nhân]) trong số 75 bệnh nhân trải qua giai đoạn nằm sấp trong nhóm đối chứng không được điều trị thuốc phong bế thần kinh cơ đồng thời. Sử dụng Glucocorticoid cũng tương tự ở hai nhóm. Tỷ lệ tử vong trung bình (± SE) trong 1 năm cũng không khác nhau giữa các nhóm (51,1 ± 2,2% ở nhóm điều trị và 51,1 ± 2,2% ở nhóm đối chứng). Các kết quả được báo cáo của bệnh nhân là tương tự giữa các nhóm lúc 3, 6 và 12 tháng, bao gồm các điểm liên quan đến sức khỏe và các hạn chế liên quan đến sức khỏe liên quan đến khuyết tật, chức năng nhận thức, các triệu chứng giống như căng thẳng sau chấn thương và đau. Thông tin bổ sung về các điểm cuối phụ được cung cấp trong Bảng S16 đến S23 trong Phụ lục bổ sung.
Sự kiện an toàn và bất lợi
Các sự kiện an toàn và bất lợi được tóm tắt trong Bảng 2 và Bảng S24 đến S28 trong Phụ lục bổ sung. Mặc dù tỷ lệ tử vong cao ở cả hai nhóm, nhưng chỉ có một trường hợp tử vong được coi là có thể liên quan đến cisatracurium, không có trường hợp tử vong nào được coi là có thể hoặc chắc chắn liên quan đến cisatracurium, và không có sự khác biệt giữa các nhóm bệnh nhân tử vong trong 48 giờ – thời gian can thiệp thử nghiệm, hoặc lên đến 96 giờ. Nhớ lại sự tê liệt là không phổ biến và không khác nhau giữa các nhóm. Các bệnh nhân trong nhóm đối chứng có mức độ hoạt động thể chất trung bình cao hơn cho đến ngày 6. Tỷ lệ điểm yếu cơ mắc phải do ICU được đánh giá không khác nhau giữa các nhóm, nhưng nhiều bệnh nhân (trong khoảng từ 51,2 đến 67,5%) không thể hoàn thành hàng tuần trong đánh giá sức khỏe cơ bắp. Các biến cố tim mạch nghiêm trọng hơn đã được báo cáo ở nhóm can thiệp so với nhóm đối chứng (14 so với 4 biến cố; P = 0,02), mặc dù tỷ lệ rung tâm nhĩ khởi phát mới và nhịp nhanh trên thất không khác nhau giữa các nhóm. Tỷ lệ tràn khí màng phổi và barotrauma tổng thể cũng không khác nhau giữa các nhóm.
Bàn luận
Trong một nhóm các bệnh nhân bị bệnh nghiêm trọng được xác định ngay sau khi chẩn đoán ARDS từ trung bình đến nặng, việc bổ sung thuốc phong bế thần kinh cơ liên tục sớm với thuốc an thần sâu đồng thời không dẫn đến tử vong thấp hơn so với phương pháp chăm sóc thông thường đối với thở máy trong đó bao gồm các mục tiêu an thần nhẹ hơn. Thử nghiệm này có sự tuân thủ cao đối với giao thức, bao gồm sử dụng chéo tối thiểu các thuốc phong bế thần kinh cơ và độ tuân thủ cao với chiến lược thông khí và chiến lược được khuyến nghị. Kết quả phân tích phân nhóm được chỉ định trước phù hợp với phân tích chính trong toàn bộ thời gian và thời gian điều trị ARDS và trên các địa điểm thử nghiệm với các tỷ lệ loại trừ khác nhau đối với việc sử dụng thuốc phong bế thần kinh trước đó.
Một số yếu tố có thể giải thích tại sao những phát hiện của chúng tôi khác với ACURASYS, thử nghiệm đa trung tâm trước đây cho thấy lợi ích với thuốc phong bế thần kinh cơ liên tục sớm. Đầu tiên, chúng tôi đã sử dụng chiến lược PEEP cao hơn ở cả hai nhóm để kiểm tra sự can thiệp của chúng tôi trong bối cảnh chăm sóc tốt nhất và để giảm khả năng sử dụng PEEP khác biệt giữa các nhóm. PEEP cao hơn có thể làm giảm tỷ lệ tử vong ở những bệnh nhân mắc ARDS từ trung bình đến nặng, do đó làm giảm hiệu quả điều trị tiềm tàng của phong bế thần kinh liên tục sớm.[16] Thứ hai, trên cơ sở các khuyến nghị hướng dẫn hiện tại và nghiên cứu lâm sàng,[10-12,15] chúng tôi đã thiết kế thử nghiệm này sao cho các mục tiêu được sử dụng trong nhóm kiểm soát nhẹ hơn các mục tiêu được sử dụng trong thử nghiệm ACURASYS; an thần sâu đã được sử dụng trong cả nhóm can thiệp và nhóm đối chứng trong thử nghiệm ACURASYS. Trong thử nghiệm của chúng tôi, số lượng tác dụng phụ tim mạch cao hơn ở nhóm can thiệp so với nhóm đối chứng có thể là kết quả của thuốc an thần sâu trong nhóm can thiệp, có thể gây hạ huyết áp, nhịp tim chậm và các tác dụng tim mạch khác. Do đó, việc sử dụng chiến lược an thần nhẹ hơn trong nhóm kiểm soát của chúng tôi có thể đã làm giảm tỷ lệ tử vong trong nhóm đó. Thứ ba, tư thế nằm sấp giảm nguy cơ tử vong ở bệnh nhân mắc ARDS khi được bắt đầu trong 12 đến 24 giờ đầu sau khi bắt đầu điều trị ARDS từ trung bình đến nặng và được quản lý ít nhất 16 giờ mỗi ngày. Tỷ lệ bệnh nhân trải qua giai đoạn nằm sấp trong thử nghiệm của chúng tôi tương tự như đã thấy trong một nghiên cứu dịch tễ học quốc tế gần đây, nhưng nó thấp hơn so với thử nghiệm ACURASYS.[5,7]
Cho dù thuốc phong bế thần kinh cơ liên tục sớm có hiệu quả hơn với việc xác định tư thế nằm sấp không biết, nhưng đó là một lời giải thích có thể cho các kết quả khác nhau của thử nghiệm của chúng tôi và thử nghiệm ACURASYS.
Bệnh nhân trong thử nghiệm của chúng tôi đã được ghi danh sớm hơn sau khi bắt đầu ARDS so với những bệnh nhân trong thử nghiệm ACURASYS.[42] Do đó, chúng tôi có thể bao gồm những bệnh nhân có thể không sống sót đủ lâu để được đưa vào thử nghiệm trước đó. Mặc dù chúng tôi loại trừ những bệnh nhân có PaO2:FiO2 cải thiện đến hơn 200 mm Hg trước khi ngẫu nhiên hóa, chúng tôi cũng có thể đã tuyển dụng một số bệnh nhân bị tổn thương phổi đã được cải thiện nhanh chóng hoặc ít được thành lập hơn so với quan sát trong thử nghiệm trước đó. Tuy nhiên, các phân tích được phân tầng theo thời gian từ khi bắt đầu ARDS đến khi đăng ký không cho thấy bất kỳ sự khác biệt nào giữa các nhóm về tốc độ cải thiện oxy hoặc hiệu quả điều trị. Sự tương tác bất ngờ giữa nhóm dân tộc gốc Tây Ban Nha và điều trị có thể là kết quả của cơ hội ngẫu nhiên.
Thử nghiệm của chúng tôi có những hạn chế. Lý do phổ biến nhất khiến bệnh nhân đủ điều kiện bị loại là vì trước đó họ đã nhận được thuốc phong bế thần kinh cơ. Có thể là các bác sĩ điều trị đã xác định và điều trị một tập hợp con của những bệnh nhân có nhiều khả năng được hưởng lợi từ việc sử dụng thuốc phong bế thần kinh cơ. Tuy nhiên, không có bằng chứng về lợi ích ngay cả khi các phân tích bị giới hạn ở các địa điểm thử nghiệm hiếm khi loại trừ những bệnh nhân đó. Chúng tôi đã không đo lường một cách có hệ thống ảnh hưởng của phong bế thần kinh cơ đối với sự không đồng bộ của máy thở. Tuy nhiên, ở những bệnh nhân mắc ARDS hoặc có nguy cơ mắc ARDS, ức chế thần kinh cơ về cơ bản sẽ loại bỏ chứng rối loạn đồng bộ máy thở.[43] Cuối cùng, các y tá, vật lý trị liệu và các chuyên gia chăm sóc sức khỏe khác đã nhận thức được các chỉ định điều trị. Việc thiếu mù này có thể ảnh hưởng đến các đánh giá ngắn hạn về chức năng thần kinh cơ sớm, mức độ hoạt động thể chất và báo cáo về các tác dụng phụ. Tóm lại, trong số những bệnh nhân mắc ARDS từ trung bình đến nặng được điều trị bằng chiến lược PEEP cao hơn, việc quản lý truyền cisatracurium sớm và liên tục không dẫn đến tỷ lệ tử vong thấp hơn đáng kể ở 90 ngày so với chăm sóc thông thường với các mục tiêu an thần nhẹ hơn.





