Bài viết Khí máu: Các khía cạnh kỹ thuật và diễn giải được BS. Đặng Thanh Tuấn dịch từ bài viết gốc: ASSISTED VENTILATION OF THE NEONATE: AN EVIDENCE-BASED APPROACH TO NEWBORN RESPIRATORY CARE, SIXTH EDITION
Đo khí máu động mạch là tiêu chuẩn vàng dùng để đánh giá sự oxy hóa và thông khí đầy đủ ở trẻ sơ sinh bị bệnh. Trong chăm sóc đặc biệt hiện đại, đo khí máu được sử dụng đồng thời với các thiết bị giám sát không xâm lấn liên tục, đặc biệt là các máy đo pulse oximeter và máy theo dõi carbon dioxide xuyên qua da, cung cấp các giá trị ước lượng theo thời gian thực về khí trong máu.
Việc đo khí trong máu là rất quan trọng đối với việc điều trị bệnh nhân bệnh lý hô hấp, do đó không chỉ cho phép chẩn đoán suy hô hấp bằng cách ước tính mức độ nghiêm trọng của bệnh đường hô hấp, mà còn cung cấp thông tin quan trọng theo yêu cầu của bác sĩ để điều chỉnh máy thở hoặc các hình thức hỗ trợ hô hấp khác. Trong chương này, đầu tiên chúng ta thảo luận về sinh lý vận chuyển khí trong máu, theo sau là một mô tả về các kỹ thuật đo khí máu thường được sử dụng trong đơn vị chăm sóc tích cực sơ sinh (NICU). Tiếp theo, chúng tôi sẽ mô tả các khía cạnh kỹ thuật của ước lượng khí máu bằng các thiết bị có sẵn trên thị trường. Cuối cùng, chúng tôi sẽ thảo luận về việc giải thích các khí máu, cũng như một số nguy hiểm và cạm bẫy của đo lường khí máu trong thực hành lâm sàng.
1.Sinh lý khí máu
Trao đổi khí xảy ra chủ yếu ở các túi khí nhỏ (saccules) của phổi ở trẻ cực kỳ non tháng và trong phế nang ở trẻ non tháng trưởng thành hơn và trẻ đủ tháng, mặc dù một số trao đổi khí xảy ra qua da trẻ non tháng ngay sau khi sinh. [1–3] Trong giai đoạn ngắn sau sinh, máu tĩnh mạch hệ thống đi vào tâm nhĩ phải và tới tâm thất phải, bơm máu khử oxy vào hệ thống động mạch phổi. Máu này đi qua mạch máu phổi cho đến khi tiếp cận các mao mạch, tiếp giáp với phế nang, do đó tạo thuận lợi cho trao đổi khí. Trao đổi khí xảy ra trong phế nang thông khí, với sự hấp thu oxy từ phế nang vào các
mao mạch phế nang và loại bỏ điôxít cacbon từ tuần hoàn vào phế nang. Nói chung, nồng độ oxy của máu động mạch thoát khỏi tâm thất trái phản ánh sự phù hợp của thông khí và tưới máu. Sự suy giảm hàm lượng oxy sẽ xảy ra nếu tưới máu (máu) không phù hợp với thông khí (phế nang thông khí), hoặc do máu đi từ bên phải của tim sang bên trái tim mà không đi qua tuần hoàn phổi (ví dụ, shunt ngoài phổi) hoặc vì máu đi qua các bộ phận của phổi bị xẹp phổi và/hoặc thông khí kém (shunt trong phổi).
Loại bỏ carbon dioxide (CO2) chủ yếu phụ thuộc vào mức độ của thông khí phế nang. Khi tăng thông khí phế nang, áp suất riêng phần của khí carbon dioxide trong khí phế nang (PACO2) giảm, và nhiều khí CO2 bị thải ra khỏi máu đi qua phổi hơn và áp suất riêng phần của carbon dioxide trong máu (PaCO2) qua tim trái giảm đi. Ngược lại, sự giảm thông khí phế nang sẽ làm tăng PaCO2 trong máu động mạch hệ thống. Một khái niệm quan trọng là trong khi PaO2 và PaCO2 động mạch cung cấp thông tin quan trọng về sự phù hợp thông khí – tưới máu và sự đầy đủ của thông khí phế nang, chúng không cung cấp thông tin trực tiếp về tính đầy đủ của sự cung cấp oxy đến hệ mạch máu và mô ngoại biên.
Chuyển hóa hiếu khí của glucose để sản xuất adenosine triphosphate (ATP) chịu trách nhiệm cho việc tiêu thụ oxy và sản xuất CO2. Chuyển hóa hiếu khí tạo ra khoảng 38 phân tử ATP cho mỗi phân tử glucose tiêu thụ, mặc dù có một số ATP được tiêu thụ trong quá trình này, do đó sinh ra trọn 30 ATP. [4]
Trong điều kiện thiếu oxy cung cấp cho tế bào, tình trạng thiếu oxy mô xảy ra, đặc trưng bởi sự trao đổi chất kỵ khí của glucose thành pyruvate để sản xuất ATP. Quá trình này ít hiệu quả hơn so với trao đổi chất hiếu khí và tạo ra hai phân tử ATP cho mỗi phân tử glucose tiêu thụ. Pyruvate được chuyển hóa thành axit lactic, làm tăng base thiếu – base deficit (hoặc giảm base excess) của máu động mạch. Kiềm dư (Base excess) được định nghĩa là sự khác biệt giữa dung lượng đệm thực tế và dung lượng đệm lý tưởng (actual buffer capacity vs ideal buffer capacity).
Để ước tính chính xác hơn lượng oxy cung cấp cho các mô có đầy đủ hay không, cần đánh giá lượng oxy của máu quay trở lại từ tuần hoàn hệ thống đến tim (máu tĩnh mạch hỗn hợp). Lấy mẫu máu từ tâm nhĩ phải, có thể được thực hiện bằng cách sử dụng catheter tĩnh mạch rốn có đầu ở phần thấp tâm nhĩ phải, gần đúng với máu tĩnh mạch hỗn hợp. Giám sát oxy hóa tĩnh mạch hỗn hợp là cực kỳ hữu ích trong việc đánh giá tính đầy đủ của việc cung cấp oxy mô và được sử dụng rộng rãi trong ICU người lớn và trong quá trình oxy hóa màng ngoài cơ thể ở sơ sinh (ECMO).
2.Vận chuyển oxy
Việc cung cấp oxy cho các mô phụ thuộc vào hàm lượng oxy trong máu cũng như cung lượng tim và sự phân bố của nó đến các mô. Trong hầu hết trẻ sơ sinh, cung lượng tim dao động từ 120 đến 150 mL/kg/phút, mặc dù đánh giá khách quan về cung lượng tim không dễ dàng hoặc chính xác, thường tùy thuộc vào siêu âm tim Doppler hoặc phương pháp thay thế như phân tích sóng huyết áp động mạch (pulse contour analysis), đo trở kháng sinh học (bioimpedance) hoặc kỹ thuật pha loãng chất chỉ thị (thường ở trẻ lớn hơn).
[5a] Hàm lượng oxy của máu động mạch (CaO 2, oxygen content of arterial blood) bao gồm oxy gắn với hemoglobin và oxy hòa tan tự do. Vì thế, CaO2 = (HbO2) + (O2 hòa tan),
trong đó CaO2 là hàm lượng oxy máu động mạch, HbO2 là oxy liên kết với hemoglobin, và O2 hòa tan là oxy hòa tan trong máu.
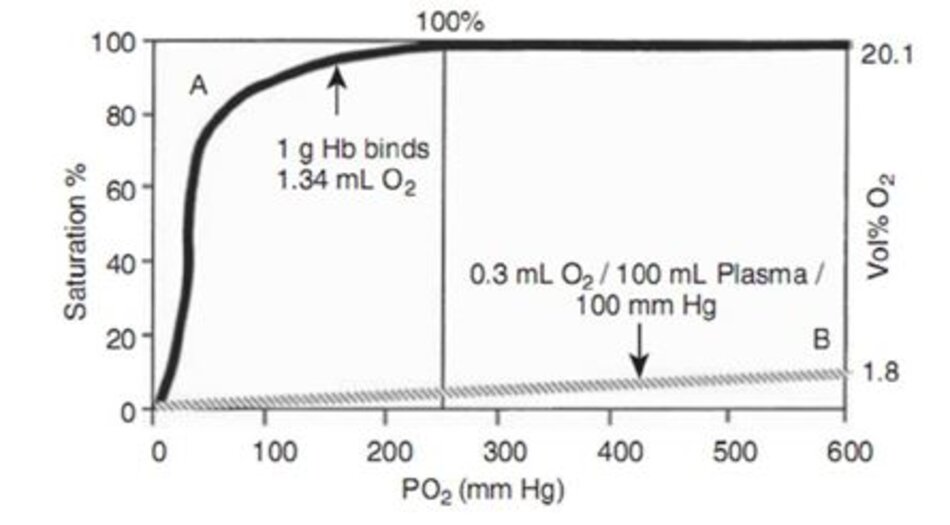
Mối quan hệ giữa PaO2 và độ bão hòa hemoglobin là dạng đường cong xích ma trên phạm vi sinh lý. Hemoglobin gần như hoàn toàn bão hòa ở một PaO 2 từ 80 đến 100 mm Hg (Hình 10-1, đường cong A). Đường cong phân ly oxyhemoglobin (ODC, oxyhemoglobin dissociation curve) mô tả phần trăm hemoglobin bão hòa với oxy tại một PaO2 đã cho.
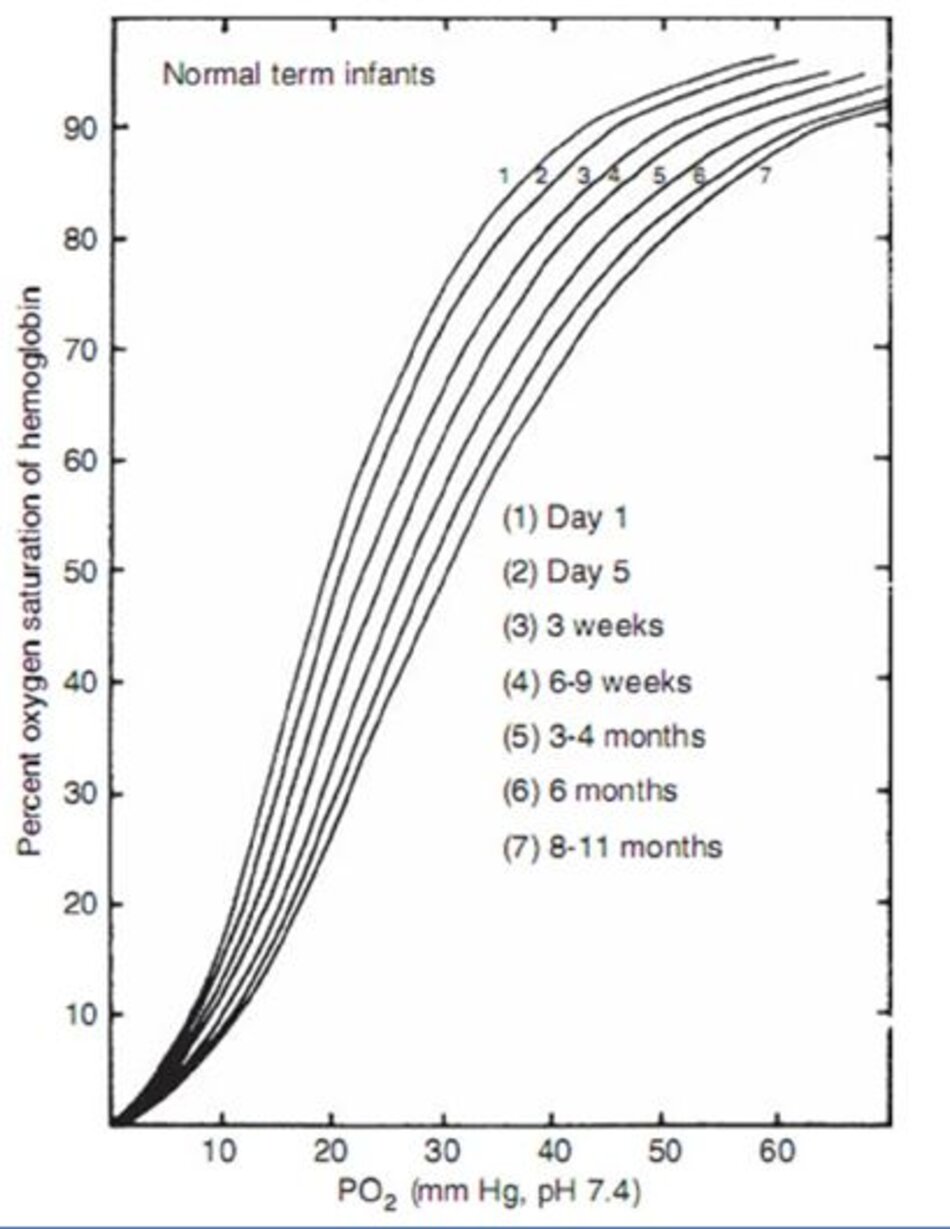
Nồng độ của diphosphoglycerate (DPG) của tế bào hồng cầu và tỷ lệ hemoglobin người lớn (A) đối với hemoglobin bào thai (F) có thể thay đổi vị trí của đường cong phân ly này. Với tuổi tăng sau khi sinh, nồng độ DPG và tỷ lệ hemoglobin A tăng, dịch chuyển đường cong sang phải (Hình 10-2). DPG có ảnh hưởng lớn hơn đến sự gắn kết oxy đối với hemoglobin người lớn, so với hemoglobin của thai nhi.
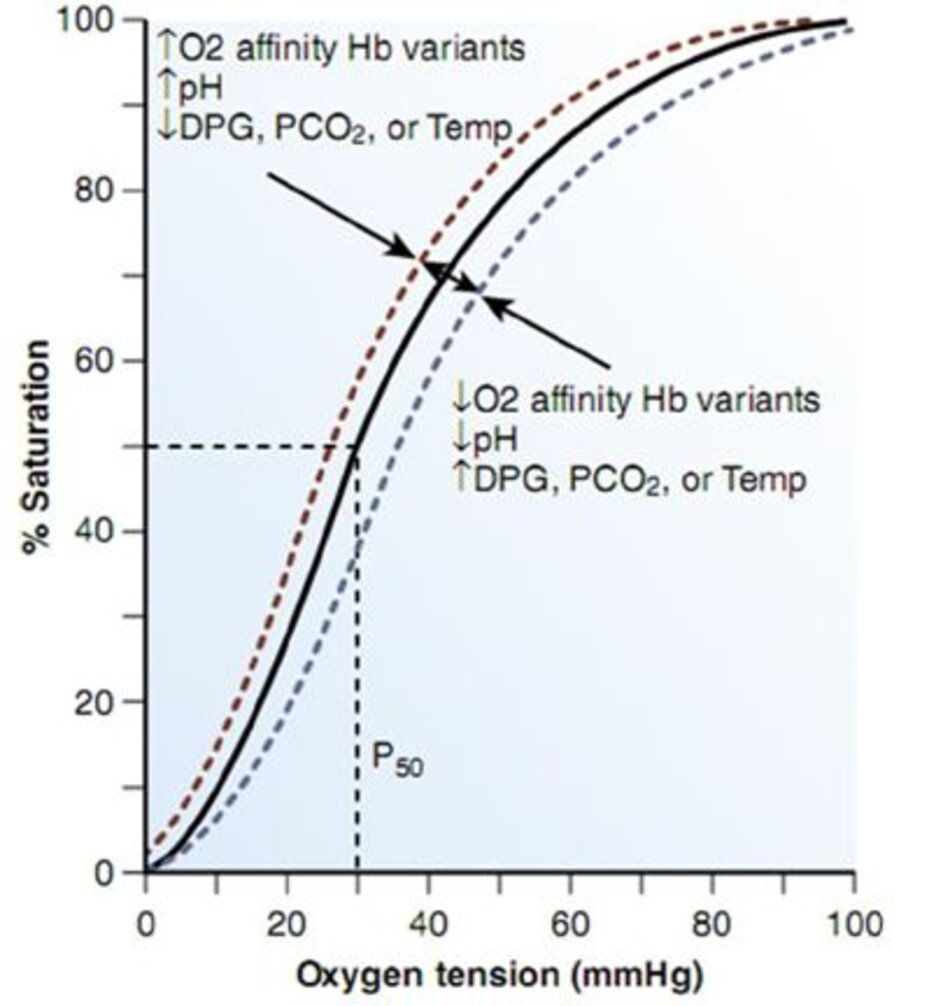
[5b, 5c] Tăng nhiệt độ, PaCO2, và nồng độ ion hydro (toan máu) cũng làm thay đổi đường cong sang bên phải. Khi đường cong dịch chuyển sang phải, hemoglobin có thể kết hợp ít oxy hơn với một PaO2 đã cho và do đó giải phóng oxy dễ dàng hơn cho các mô (Hình 10-3). Thai nhi có nồng độ DPG hồng cầu thấp và nhiều hemoglobin F hơn, và đường cong phân ly do đó được dịch chuyển sang bên trái, giúp duy trì độ bão hòa oxy cao hơn ở PaO2 thấp hơn.
Các điều kiện như kiềm hô hấp hoặc hạ thân nhiệt điều trị (therapeutic hypothermia) cũng sẽ thay đổi đường cong phân ly sang bên trái, dẫn đến độ bão hòa oxy hemoglobin cao hơn cho một PaO2 đã cho.
Tất cả các khí hòa tan trong máu có áp lực riêng phần tỷ lệ thuận với lượng khí. Áp lực gây ra bởi oxy hòa tan trong máu được biểu diễn bằng PaO2. Thông thường, chỉ một lượng nhỏ oxy hòa tan trong huyết tương, trừ khi PaO2 là cực kỳ cao (ví dụ, tiếp xúc với nồng độ cao trong điều trị oxy áp lực cao – hyperbaric oxygen therapy).
Ở 38°C, 0,3 mL oxy được hòa tan trong 100 mL huyết tương (0,003 mL/dL/mm Hg của PaO2, tại một PaO2 giả định là 100 mm Hg). Mối quan hệ này là tuyến tính trên toàn bộ phạm vi của PaO2 (xem hình 10-1, đường cong B). Bởi vì lượng oxy hòa tan trong máu ít hơn nhiều so với lượng hemoglobin liên kết, hàm lượng oxy trong máu xấp xỉ bằng lượng oxy liên kết với hemoglobin, như được biểu thị bằng phương trình:
CaO2 ≈ (HbO2).
Lượng oxy liên kết với hemoglobin phụ thuộc vào nồng độ hemoglobin, độ bão hòa phần trăm của hemoglobin và khả năng mang oxy của hemoglobin, có thể được biểu diễn bằng toán học như sau:
CaO2 ≈ (HbO2) = (gam Hb) × (dung tích O2) × (% bão hòa).
Dung tích O2 đại diện cho lượng oxy tối đa có thể mang trên 1 gam hemoglobin bão hòa hoàn toàn. Giá trị này là 1,34 mL O2 mỗi gam 100% hemoglobin bão hòa. [6]
Giả sử nồng độ hemoglobin là 15 g/100 mL máu và 100% độ bão hòa của máu động mạch, và bỏ qua lượng oxy hòa tan trong máu, hàm lượng oxy của máu động mạch bình thường là khoảng:
CaO2 = 15 × 1,34 × 1,0 = 20 mL O2
trên 100 mL máu động mạch hoặc 0,2 mL trên mililít máu.
Sử dụng các giả định tương tự, và với giả định bổ sung rằng cung lượng tim bình thường ở trẻ sơ sinh là khoảng 120 mL/kg/phút, lượng O2 có thể được cung cấp bởi tuần hoàn hệ thống có thể được tính như sau:
O2 cung cấp = (Cung lượng tim) × (CaO2)
= (120 mL máu/kg/phút) × (0,2 mL O2/mL máu)
= 24 mL O2/kg/phút.
Tiêu thụ oxy cho trẻ sơ sinh là khoảng 6 ml/kg/phút trong các trường hợp bình thường. [7,8] Vì vậy, cơ thể ly trích 6 mL/kg/phút oxy từ khoảng 24 mL/kg/phút được cung cấp thông qua tuần hoàn hệ thống. Lượng oxy cung cấp thường cao hơn nhiều so với số lượng oxy mà mô yêu cầu, cung cấp một phương pháp dự trữ tự nhiên.
Các mô trở nên thiếu oxy và chuyển sang chuyển hóa kỵ khí chỉ khi sự cung cấp oxy giảm xuống dưới ngưỡng mà lượng oxy cung cấp thấp hơn số lượng nhu cầu của các mô. Bởi vì chỉ có khoảng 25% lượng oxy đã được ly trích khỏi máu để cung cấp cho mô nên khi nó quay trở lại tim, máu tĩnh mạch hỗn hợp là khoảng 75% bão hòa.
Nói chung, độ bão hòa tĩnh mạch hỗn hợp từ 70% đến 75% đại diện cho việc cung cấp oxy mô đầy đủ. Do đó, bão hòa tĩnh mạch hỗn hợp thường được duy trì trong phạm vi sinh lý bình thường từ 70% đến 75% ở bệnh nhân có thể theo dõi trực tiếp bão hòa tĩnh mạch hỗn hợp (ví dụ: bệnh nhân dùng ECMO).
3. Đường cong phân ly Oxyhemoglobin
Một trong những vai trò chính của hemoglobin là gắn kết oxy trong phổi để cho phép vận chuyển oxy đến các mô của cơ thể. Oxy sau đó được giải phóng từ hemoglobin và đi vào giai đoạn hòa tan trong huyết tương, được biểu thị bằng áp suất riêng phần của oxy (PaO2).
Nếu không có hemoglobin, cung lượng tim sẽ phải tăng lên rất nhiều để đáp ứng nhu cầu trao đổi chất của cơ thể vì lượng oxy hòa tan trong máu là tối thiểu. Mối quan hệ giữa độ bão hòa oxy và PaO2 được mô tả bằng ODC dạng xích ma. Phần dốc của đường cong chứng minh rằng bão hòa oxy thay đổi nhanh chóng trong quá trình chuyên chở và cung cấp oxy của hemoglobin.
Điều này phản ánh sự thư giãn của cấu trúc hemoglobin xảy ra khi gắn kết oxy. Khi oxy liên kết với heme, phân tử hemoglobin giãn ra, do đó phơi bày thêm các phân tử heme, tạo điều kiện cho sự gắn kết oxy tiếp theo. Quá trình thư giãn này được gọi là sửa đổi dị lập thể (allosteric modification) và được điều chỉnh bởi hiệu ứng Haldane. Quá trình ngược lại xảy ra với việc lấy oxy từ phân tử hemoglobin.
Khi các vị trí gắn kết oxy trên phân tử hemoglobin tiếp cận bão hòa đầy đủ với oxy, ODC bắt đầu dẹt. Do đó, ở mức bão hòa oxy cao hơn, nó trở nên ngày càng khó dự đoán PaO2 từ độ bão hòa oxy. Độ bão hòa oxy 100% có thể tương ứng với một PaO2 khác nhau, từ 80 đến hơn 300 mm Hg.
Trong khi PaO2 đóng góp rất ít vào hàm lượng oxy tổng thể của máu, tầm quan trọng sinh lý của nó không thể bị phóng đại vì nó là oxy hòa tan trong huyết tương có sẵn để xâm nhập vào tế bào.
Oxy được gắn với hemoglobin không sẵn có cho các mô cho đến khi nó được giải phóng khỏi heme và có thể hòa tan trong huyết tương. Trong những trường hợp bình thường (ví dụ, nhiệt độ cơ thể bình thường – euthermia, hàm lượng oxy trong máu động mạch bình thường – normoxemia), 100 mL máu chứa khoảng 20 mL oxy. Phần lớn oxy này liên kết với hemoglobin, với chỉ khoảng 0,31 mL oxy là ở dạng hòa tan trong huyết tương.
Vị trí của ODC được mô tả bởi P50, thể hiện PaO2 ở độ bão hòa oxy là 50%. Vị trí của ODC, và do đó P50, phụ thuộc vào nhiều yếu tố. Sự gia tăng nhiệt độ cơ thể, nồng độ ion hydro (giảm pH), PaCO2, 2,3-DPG, hoặc nồng độ hemoglobin người lớn sẽ độc lập dịch chuyển ODC sang phải, trong khi giảm bất kỳ yếu tố nào trong số này sẽ chuyển đường cong sang trái.
Do đó, PaO2 cho bất kỳ độ bão hòa oxy nhất định nào sẽ thay đổi trong một cá nhân theo thời gian khi các yếu tố này thay đổi. Ví dụ, trong sự hiện diện của một cơn sốt, sự dịch chuyển sang bên phải của đường cong dẫn đến một PaO2 cao hơn cho giá trị P50. Cả nồng độ hemoglobin dành cho người lớn và nồng độ 2,3-DPG tăng lên trong năm đầu tiên, gây ra sự dịch chuyển ở vị trí ODC sang bên phải. [9]
4. Xem xét về Hemoglobin thai (Fetal Hemoglobin)
Ở tất cả trẻ sơ sinh hầu hết có hemoglobin thai, giá trị của nó rất quan trọng. Trẻ sinh ra ở thai kỳ < 30 tuần tuổi có gần 100% hemoglobin thai. Tỷ lệ hemoglobin thai/ hemoglobin người lớn dần dần giảm đi từ tuổi thai 40 tuần, hemoglobin thai (HbF) chiếm khoảng 70% tất cả các loại hemoglobin, còn hemoglobin người trưởng thành (HbA) chiếm 30% còn lại. [10] Sự thay đổi này để tạo ra hemoglobin trưởng thành và ngưng quá trình sản xuất hemoglobin bào thai có liên quan đến tuổi sau thụ thai và không theo tuổi sinh. [11] Do đó, sinh non không ảnh hưởng đến tốcđộ chuyển từsản xuất hemoglobin bào thai sang hemoglobin trưởng thành.
Một em bé sinh ra ở 24 tuần với gần 100% hemoglobin bào thai được dự kiến sẽ có khoảng 70% hemoglobin bào thai lúc 16 tuần tuổi (tuổi thai được điều chỉnh 40 tuần), tương tự như em bé sinh ra ở tuổi thai 40 tuần, mặc dù tỷ lệ sẽ thay đổi nhanh hơn sau khi truyền máu với máu người lớn.
Quan sát đầu tiên rằng hemoglobin bào thai có các đặc tính gắn kết oxy khác với hemoglobin trưởng thành được báo cáo vào năm 1930. [12] Hemoglobin bào thai bao gồm hai chuỗi α và hai chuỗi , trái ngược với hemoglobin dành cho người lớn, chứa hai chuỗi α và 2 chuỗi . Sự khác biệt này dẫn đến hemoglobin bào thai có ái lực oxy cao hơn so với hemoglobin người lớn. Điều này thúc đẩy sự chuyển động của oxy từ phía mẹ của tuần hoàn nhau sang bên thai nhi vì hemoglobin thai nhi sẽ giữ oxy “chặt chẽ hơn” so với hemoglobin người lớn, và điều này được phản ánh ở vị trí của ODC. P50 quan sát thấy ở trẻ sơ sinh đủ tháng khoảng 21 mm Hg so với P50 là 27 mm Hg được quan sát thấy ở người lớn (xem Hình 10-2). [13,14] Ở trẻ non tháng, P50 có thể thấp tới 18 mm Hg do sự hiện diện của hemoglobin thai cao hơn và nồng độ 2,3-DPG thấp hơn. [15]
Điều quan trọng là xem xét cách các liệu pháp điều trị có thể làm thay đổi vị trí của đường cong ODC. Có lẽ quan trọng nhất trong vấn đề này là ảnh hưởng của truyền máu hồng cầu lắng. Bởi vì các tế bào hồng cầu được cung cấp cho bệnh nhân được hiến tặng bởi người lớn, máu truyền máu về cơ bản chứa 100% hemoglobin người lớn. Kết quả là sự dịch chuyển của ODC sang phải sau khi truyền máu. Vì trẻ sinh non có nồng độ hemoglobin của thai nhi cao hơn, truyền máu trong dân số này sẽ có tác dụng lớn hơn trong việc dịch chuyển ODC so với trẻ sơ sinh đủ tháng.
Trẻ sinh non có nhiều khả năng được truyền máu hơn, điều này làm nổi bật thêm tầm quan trọng của thực hành này ở quần thể dễ bị tổn thương này. [16] Có những yếu tố quan trọng khác cần xem xét về ảnh hưởng của truyền máu lên ODC, chẳng hạn như nồng độ 2,3-DPG, nhiệt độ và loại chất bảo quản được sử dụng trong các tế bào hồng cầu lắng. Tuy nhiên, một cuộc thảo luận chi tiết về những yếu tố này nằm ngoài phạm vi của văn bản này.
Điều này có quan trọng về lâm sàng không ? Wimberley và các đồng nghiệp nói rằng dựa trên vị trí của ODC, giới hạn độ bão hòa oxy cho tình trạng thiếu oxy và tăng oxy máu có thể thay đổi từ 85% đến 94% và từ 96% đến 98%, tương ứng. [17] Điều này chứng minh tầm quan trọng của việc xem xét các mục tiêu bão hòa oxy có liên quan đến PaO2 như được mô tả bởi ODC như thế nào. Trong thực tế, các bác sĩ lâm sàng nhắm mục tiêu các dải bão hòa oxy cụ thể để giúp hướng dẫn chuẩn độ oxy và tránh những nguy hiểm của cả tăng oxy máu và thiếu oxy máu.
Tuy nhiên, mục tiêu bão hòa oxy không thường xuyên thay đổi khi vị trí của ODC thay đổi, chẳng hạn như sau khi truyền máu, có thể dẫn đến một PaO2 cao hơn cho bất kỳ độ bão hòa oxy nhất định so với trước truyền máu. Có thể cho rằng, điều này là thích hợp, bởi vì nó là độ bão hòa oxyhemoglobin hơn là PaO2 ảnh hưởng trực tiếp đến hàm lượng oxy trong máu và sự cung cấp oxy của mô.
Máy phân tích khí máu hiện đại có hai cài đặt trước cho hemoglobin bào thai: 0% và 80%. Mặc dù không chính xác, việc sử dụng giá trị đặt trước cho 80% hemoglobin bào thai là thích hợp hơn cho xét nghiệm khí máu sơ sinh.
Ví dụ, hãy xem xét một mẫu khí máu được điều chỉnh đến 80% hemoglobin bào thai với P50 là 15 mm Hg và độ bão hòa oxy là 92% đến 97%. Cùng một mẫu khí máu chạy trên một máy phân tích khí máu không được điều chỉnh cho hemoglobin thai nhi sẽ cung cấp cho một P50 20 mm Hg, tương ứng với độ bão hòa oxy từ 86% đến 95%. [15]
Thỉnh thoảng, các lỗi trong báo cáo giá trị khí máu không được hiệu chỉnh không rõ ràng cho các bác sĩ. Một kết quả khí máu tạo ra độ bão hòa oxy 100% đã được hiệu chỉnh cho hemoglobin bào thai tương ứng với độ bão hòa oxy chưa được hiệu chỉnh là 105%. [18] Tuy nhiên, do máy đo khí máu không báo cáo bão hòa oxy > 100%, điều này sẽ không rõ ràng đối với bác sĩ.
5. Giảm oxy máu và thiếu oxy mô (Hypoxemia and Hypoxia)
Mặc dù giảm oxy máu và thiếu oxy mô thường xảy ra cùng nhau, nhưng chúng không đồng nghĩa. Giảm oxy máu thường được xác định là hàm lượng oxy trong máu động mạch thấp, trong khi tình trạng thiếu oxy mô đề cập đến việc cung cấp oxy không đầy đủ cho mô. Giảm oxy máu xảy ra trong bất kỳ tình huống nào trong đó máu đi vào
tuần hoàn hệ thống mà không đi qua và trao đổi khí với phế nang đầy đủ thông khí (giảm sự tương xứng thông khí – tưới máu). Máu có thể bỏ qua phế nang thông khí đầy đủ do bị các shunts ngoài phổi (extrapulmonary shunts), bởi các shunts trong phổi (intrapulmonary shunts), hoặc kết hợp của cả hai.
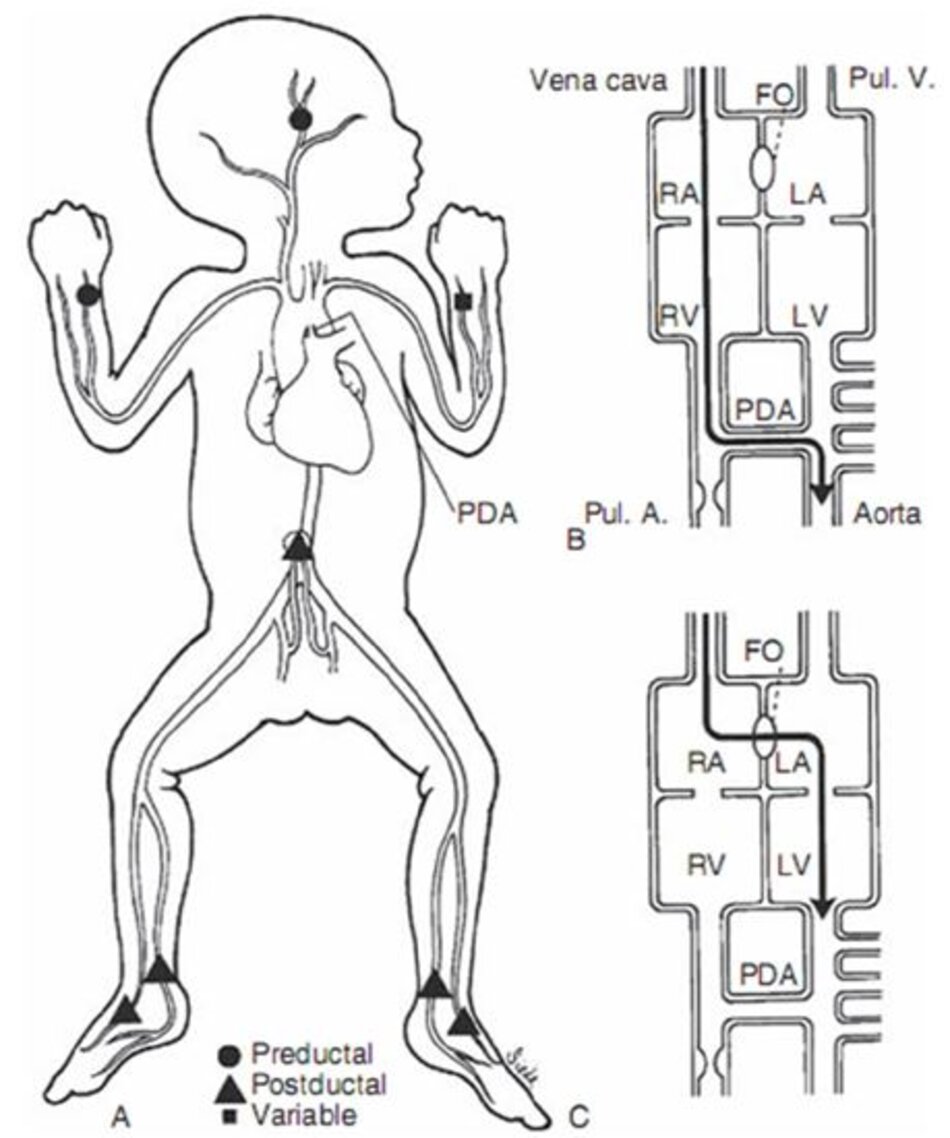
Với bệnh tim bẩm sinh tím, một trái tim bất thường cấu trúc dẫn đến một số máu đi vào động mạch chủ mà không đi qua tuần hoàn phổi (shunt ngoài phổi). Tương tự như vậy, trẻ sơ sinh bị tăng áp phổi tồn tại (persistent pulmonary hypertension) của trẻ sơ sinh cũng có thể có shunt ngoài phổi thông qua lỗ bầu dục (foramen ovale) và/hoặc ống động mạch (ductus arteriosus).
Một shunt từ phải sang trái qua ống động mạch thường có thể được phát hiện bằng cách so sánh PaO2 hoặc độ bão hòa oxy của máu trước ống và sau ống động mạch (preductal and postductal blood) (Hình 10-4). Nếu độ bão hòa của máu trước ống cao hơn đáng kể (≥ 5% đến 10% sự khác biệt) so với độ bão hòa của máu sau ống, thì tồn tại một shunt từ phải sang trái có ý nghĩa lâm sàng.
Tuy nhiên, khi độ bão hòa trước và sau ống bằng nhau không loại trừ khả năng tăng áp động mạch phổi với một shunt qua lỗ bầu dục. Giảm oxy máu kết hợp với các bệnh phổi được đặc trưng bởi atelectasis (ví dụ, hội chứng suy hô hấp, viêm phổi) được gây ra chủ yếu do shunting trong phổi. Bất cứ khi nào phế nang được thông khí không đầy đủ, máu chảy vào những phế nang đó có thể không trở nên bão hòa hoàn toàn. Như vậy, với mức độ của xẹp phổi nhiều hơn, càng nhiều shunt trong phổi, và thiếu oxy máu càng nhiều hơn.
Thiếu oxy mô khi lượng oxy cung cấp cho các mô giảm xuống dưới mức ngưỡng tiêu thụ oxy tới hạn (critical threshold of oxygen consumption). Tình trạng thiếu oxy có thể xảy ra bất chấp đủ PaO2. Nó là hữu ích để khái niệm hóa tình trạng thiếu oxy trong sự mất cân bằng giữa cung cấp, giao hàng và nhu cầu oxy. Việc giảm cung cấp ôxy được quan sát ở độ cao (trên núi cao) do áp suất oxy riêng phần trong khí quyển thấp hơn. Việc “cung cấp” oxy bị suy giảm trong các bệnh cảnh tưới máu mô không đầy đủ (ví dụ, giảm cung lượng tim), thiếu máu và các loại hemoglobin bất thường (ví dụ methemoglobin), lúc mà việc cung ứng oxy đến các mô bị ảnh hưởng tiêu cực. “Nhu cầu” đối với oxy sẽ tăng lên khi nhu cầu oxy của mô tăng lên để đáp ứng với bệnh tật như sốt hoặc nhiễm trùng huyết.
6. Vận chuyển Carbon Dioxide
Vận chuyển carbon dioxide ít phức tạp hơn so với vận chuyển oxy. Carbon dioxide được sản xuất trong các mô trong quá trình chuyển hóa hiếu khí của glucose và được vận chuyển trong máu đến phổi, nơi nó được thải ra.
Đến 85% lượng carbon dioxide trong máu được vận chuyển dưới dạng axit cacbonic, 10% được thực hiện bởi hemoglobin như carbamate, và 5% được vận chuyển dưới dạng khí hòa tan hoặc axit cacbonic. [19,20] Do sự cân bằng giữa cacbon dioxit hòa tan và ion bicarbonate, mối quan hệ giữa áp suất riêng phần của carbon dioxide trong máu (PaCO2) và hàm lượng CO2 tổng của máu về cơ bản là tuyến tính trong phạm vi sinh lý (Hình 10-5).
Bởi vì carbon dioxide khuếch tán nhanh chóng từ máu vào khí phế nang, áp suất riêng phần của CO2 trong máu (PaCO2) rời khỏi phổi về cơ bản giống như áp suất riêng phần của CO2 trong khí phế nang (PACO2). Do đó việc tăng thông khí phút phế nang càng giảm PACO2 và do đó làm giảm PaCO2. Đây là lý do PaCO2 phụ thuộc vào mức độ của thông khí phế nang.
7. Nhiễm toan chuyển hóa
Chuyển hóa kỵ khí của glucose dẫn đến sự tích lũy axit lactic, dẫn đến nhiễm toan chuyển hóa. Axit lactic phản ứng với bicarbonate (một bazơ), làm cho bicarbonat huyết thanh giảm, dẫn đến thâm hụt kiềm (base deficit). Điều này thường xảy ra do cung cấp oxy mô không đầy đủ do một số kết hợp của thiếu oxy máu, thiếu máu và cung lượng tim không đầy đủ. Các nguyên nhân khác của nhiễm toan chuyển hóa ở trẻ sơ sinh bao gồm nhiễm trùng huyết, bất thường chuyển hóa bẩm sinh và thải bicarbonate qua thận. Các nguyên nhân do thầy thuốc, chẳng hạn như lượng lớn protein dưới dạng acid amine trong dinh dưỡng qua đường tĩnh mạch, đặc biệt là khi thêm cysteine, cũng là nguyên nhân thường gặp gây toan chuyển hóa ở trẻ rất non tháng.
Ở hầu hết trẻ sơ sinh khỏe mạnh, base deficit thường là từ +3 đến −1. Mặc dù nó là hợp lý để cung cấp chất kiềm (base) cho trẻ sơ sinh bị toan chuyển hóa từ mất bicarbonate, về cơ bản không có bằng chứng cho thấy liệu pháp bicarbonate có lợi cho bệnh nhân nhiễm toan chuyển hóa do thiếu oxy mô. Ngược lại, có nhiều bằng chứng cho thấy rằng việc sử dụng bicarbonate có thể có hại cho bệnh nhân bị thiếu oxy máu và nhiễm toan chuyển hóa, và nó không nên được sử dụng thường xuyên. [21–23] Ở những trẻ bị nhiễm toan chuyển hóa, khôi phục sự cung cấp oxy mô bằng cách điều chỉnh vấn đề bệnh nền là quan trọng hơn nhiều so với việc dùng dung dịch kiềm ngoại sinh. Sodium bicarbonate không còn được khuyến cáo trong hồi sức tim phổi. [21]
Nếu nhiễm toan chuyển hóa được điều trị bằng kiềm ngoại sinh, loại thường được sử dụng nhất là sodium bicarbonate. Số lượng milliequivalents của bicarbonate cần thiết để xác định một nửa base deficit có thể xấp xỉ từ phương trình sau:
Bicarbonate (mEq) được dùng = (base deficit) × (cân nặng tính bằng kg) × 0,3.
Do áp lực thẩm thấu của nó rất cao, sodium bicarbonate (1 mEq/mL) nên được pha loãng 1:1 bằng nước cất vô trùng và được sử dụng từ từ, tốt hơn là từ 30 đến 60 phút. [24] Nên sử dụng bicarbonate cẩn thận, nếu có, ở trẻ sơ sinh có kết hợp nhiễm toan hô hấp và chuyển hóa, bởi vì khi bicarbonate được chuyển hóa, PaCO 2 sẽ tăng thêm, trừ khi cũng có sự gia tăng trong thông khí phút.
Do đó, việc sử dụng sodium bicarbonate nên được giới hạn trong vài trường hợp tăng thải bicarbonate qua ống thận nặng hoặc một số nguyên nhân hiếm gặp gây ra nhiễm toan lactic bẩm sinh.
8. Kiềm chuyển hóa
Cho đến nay nguyên nhân phổ biến nhất của kiềm chuyển hóa tương đối ở trẻ sơ sinh là bù trừ mãn tính cho nhiễm toan hô hấp. Nếu một nhiễm toan hô hấp đã bù được điều chỉnh bằng cách giảm nhanh PaCO2, một alkalosis chuyển hóa tuyệt đối sẽ là kết quả.
Các nguyên nhân khác của nhiễm kiềm chuyển hóa ở trẻ sơ sinh bao gồm giảm chlor máu từ điều trị lợi tiểu mãn tính, hoặc dẫn lưu dịch dạ dày mãn tính (hoặc nôn thường xuyên), và dùng acetate dư thừa trong chế độ dinh dưỡng qua đường tĩnh mạch.
Nhiễm kiềm chuyển hóa nhẹ cũng có thể xảy ra sau khi truyền máu, khi citrate là chất chống đông máu được chuyển hóa. Hiếm khi cần điều chỉnh kiềm chuyển hóa với các hợp chất có tính axit như amoni clorua hoặc arginine hydrochloride hoặc với thuốc lợi tiểu thải bicarbonate như acetazolamide. Trong hầu hết các trường hợp, điều trị nhiễm kiềm chuyển hóa tương đối với các tác nhân này chỉ dẫn đến nhiễm toan hô hấp không bù. [25]
Tham khảo thêm một số bài viết cùng chủ đề: