Bài viết Thai ngoài tử cung: mô kẽ, cổ tử cung và trong buồng trứng được biên dịch bởi Bs Quản Anh Dũng từ Sách “Chửa ngoài tử cung: Tiếp cận dựa trên ca lâm sàng” của tác giả Margaret Dziadosz, Ana Monteagudo và Ilan E.Timor-Tritsch, Abdulrahman Alserri và Togas Tulandi, Warren J. Huber và Gary N. Frishman.
1. Thai ngoài tử cung ở mô kẽ
1.1. Trường hợp lâm sàng
Một phụ nữ 28 tuổi, G2P0010 (0010 là PARA), đến phòng khám trong tình trạng vô kinh và đau bụng. Kỳ kinh cuối của cô ấy là 10 tuần trước. Khai thác tiền sử ghi nhận bệnh nhân đã từng phá thai nội khoa một lần và nhiễm chlamydia đã được điều trị 1 năm trước đó. Khám lâm sàng cho thấy tử cung to, không cân đối, kích thước tương đương 1 thai 7 tuần tuổi. Nồng độ B-hCG huyết thanh là 40.138 mIU / mL. Siêu âm qua ngả âm đạo thấy ảnh như Hình 11.1.
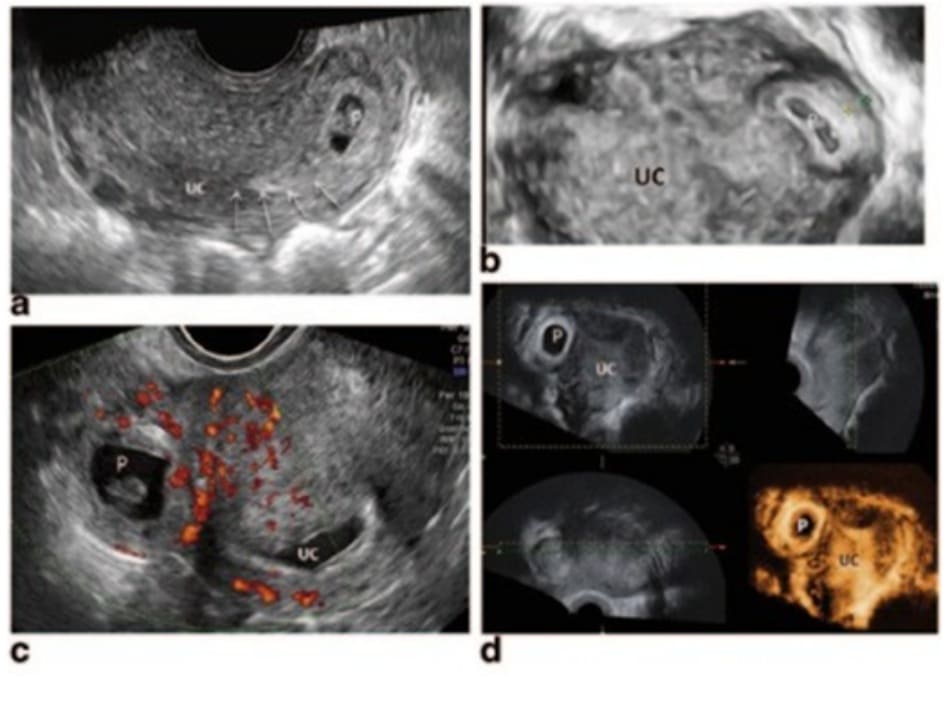
1.2. Hướng xử trí?
- Chờ đợi
- Chỉ định dùng MTX
- Nội soi can thiệp cắt bỏ khối thai
1.3. Chẩn đoán và đánh giá
Bệnh nhân của chúng ta có biểu hiện khá điển hình của EP trong mô kẽ. Thai nghén mô kẽ vòi Fallope là tình trạng thai làm tổ ở đoạn eo vòi đi ngang qua thành cơ tử cung. Tỷ lệ mắc của nó được ước tính là 2-4% trong các ca EP tương đương 1 trong 2500-5000 ca. Nó còn được gọi là “thai ở sừng tử cung”, được tìm thấy ở phần ngoài cùng của sừng tử cung, thường chỉ dùng cho những người có tử cung đôi. Do phần ngoài cùng của sừng tử cung khá dày nên thai có khả năng phát triển thành một khối lớn mà không bị vỡ. Mặc dù vỡ khối EP thường xảy ra trước 12 tuần ở 22% bệnh nhân, nhưng lý do trên khiến bệnh nhân có thể không biểu hiện triệu chứng gì cho tới tuần thứ 16. Tỷ lệ tử vong do không được chẩn đoán kịp thời là 2,5%, cao hơn gấp bảy lần so với các vị trí ngoài tử cung khác. Điều này thường gặp nhất là do xuất huyết lượng lớn sau vỡ khối EP.
Bước quan trọng nhất là đánh giá hình ảnh siêu âm qua ngả âm đạo; một phương thức cận lâm sàng hữu hiệu sẵn có với chi phí thấp
Hình ảnh siêu âm thấy buồng tử cung rỗng, xuất hiện một lớp mỏng cơ tử cung xung quanh phần trên ngoài túi thai (GS), vói khoảng cách ít nhất 1 cm từ thành tử cung đến GS và một đường kẽ là chìa khóa chính cho chẩn đoán. Theo mô tả của Ackerman, đường kẽ là đường tăng âm chạy từ nội mạc tử cung đến sừng tử cung, tiếp giáp với khối mô kẽ hoặc túi thai. Xuất hiện các dấu hiệu này thì chẩn đoán EP mô kẽ có độ đặc hiệu lên đến 88-98% (Hình 11.2).
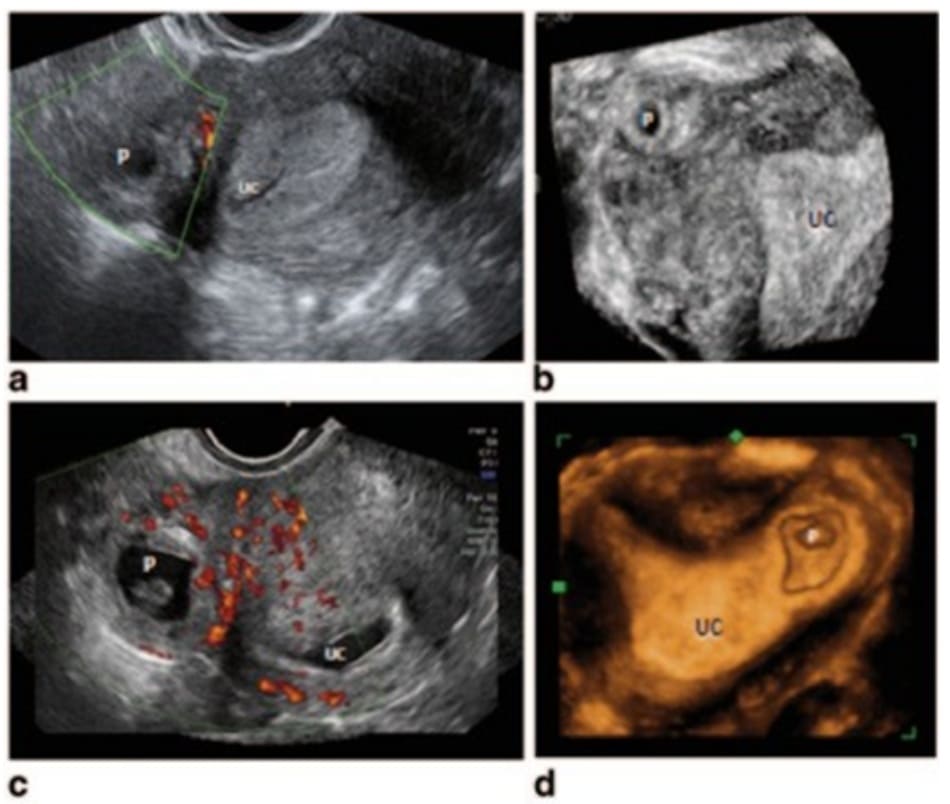
Bước quan trọng nhất là đánh giá hình ảnh siêu âm qua ngả âm đạo; một phương thức cận lâm sàng hữu hiệu sẵn có với chi phí thấp. Hình ảnh siêu âm thấy buồng tử cung rỗng, xuất hiện một lớp mỏng cơ tử cung xung quanh phần trên ngoài túi thai (GS), vói khoảng cách ít nhất 1 cm từ thành tử cung đến GS và một đường kẽ là chìa khóa chính cho chẩn đoán. Theo mô tả của Ackerman, đường kẽ là đường tăng âm chạy từ nội mạc tử cung đến sừng tử cung, tiếp giáp với khối mô kẽ hoặc túi thai. Xuất hiện các dấu hiệu này thì chẩn đoán EP mô kẽ có độ đặc hiệu lên đến 88-98% (Hình 11.2).
Siêu âm ba chiều (3D) đặc biệt hữu ích trong chẩn đoán thai kẽ (Hình 11.2 và 11.3). Sử dụng chế độ chụp cắt lớp ở các góc chụp khác nhau sẽ giúp bác sĩ lâm sàng nhìn nhận một cách toàn diện. Bằng cách sử dụng công nghệ ảnh tương phản khối (VCI) với lát cắt dày, siêu âm 3D giúp bác sĩ phân biệt được lớp màng rụng (tăng âm) với lớp cơ tử cung phía dưới và vị trí bất thường của túi thai. Vì thế, TVUS nên được ưu tiên lựa chọn để xác định chẩn đoán.
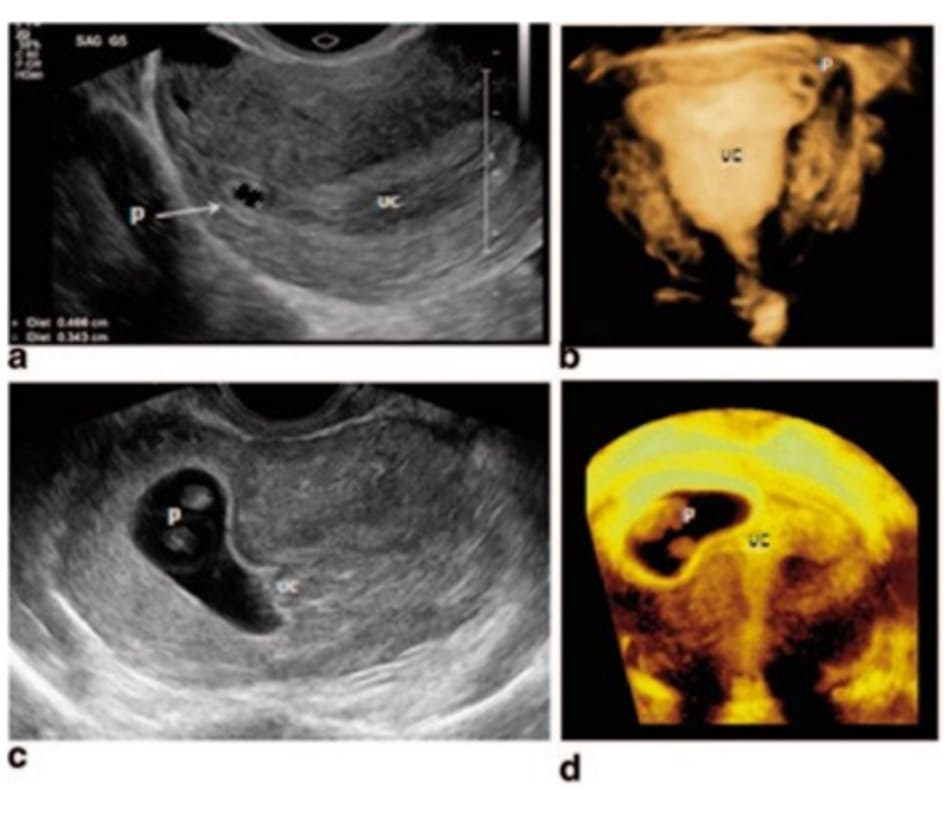
Khi sử dụng TVUS, nên thiết lập bản đồ màu của dòng chảy để xác định nguồn máu nuôi GS. Ngoài ra, việc sử dụng siêu âm 3D, như trong Hình 11.2 b, d và 11.3 b, d, và chụp cắt lớp sẽ giúp bổ sung thêm các chi tiết quan trọng để đánh giá vị trí khối thai trong tử cung.
Nếu trường hợp hiếm hoi mà TVUS 2D và 3D không kết luận được, thì MRI có thể được chỉ định để chẩn đoán xác định. Các tiêu chí chẩn đoán tương tự nhau, bao gồm GS lệch tâm, mô cơ tử cung xung quanh GS, và đường kẽ.
1.4. Điều trị
Nếu xác định có thai kẽ hoặc thai sừng tử cung mà không có hoạt động tim thai, nên chờ đợi theo dõi tiếp. Tuy nhiên, một khi đã có tim thai, nguy cơ vỡ khối EP tăng lên kéo theo các biến chứng khó lường cho sản phụ, khiến chúng ta cần can thiệp ngay.
MTX là phương pháp điều trị không phẫu thuật được sử dụng rộng rãi nhất để điều trị thai kẽ. Liệu pháp đơn liều thường không có hiệu quả ở sản phụ với giá trị B-hCG> 5000 mIU / mL. Vì thế họ nên được áp dụng liệu pháp MTX đa liều, cụ thể như sau: ngày 0: đo nồng độ BhCG, công thức máu (CBC), amino transferase (AST), creatinine, định nhóm máu (ABO và Rh), Rhogam nếu cần, sau đó tiêm bắp MTX 50 mg / m2 diện tích bề mặt cơ thể (BSA); ngày 4: đo B-hCG; và ngày 7: BhCG và tiêm MTX liều thứ hai nếu BhCG giảm <15% từ ngày 4-7. Lựa chọn điều trị này có tỷ lệ thành công là 83%, nhưng có nguy cơ bị vỡ khối EP sau điều trị lên tới 10–20% bệnh nhân.
Liệu pháp tiêm MTX tại chỗ tại túi thai cũng có thể được áp dụng. Các chế độ liều khác nhau của MTX để tiêm bao gồm (a) 1 mg / kg, (b) liều duy nhất 100 mg, hoặc (c) 50 mg / m2 BSA. Tỷ lệ điều trị thành công đạt 91%. Điều trị MTX tại chỗ giúp giảm tác dụng phụ, tỷ lệ thông tắc vòi tử cung là 92% và tránh được can thiệp phẫu thuật.
Tuy nhiên, phương pháp điều trị kinh điển của thai kẽ là phẫu thuật. Về cơ bản, bệnh nhân sẽ được mở ổ bụng cắt bỏ sừng tử cung hoặc cắt bỏ toàn bộ tử cung. Tuy nhiên, với sự phát triển của các kỹ thuật xâm lấn tối thiểu, chúng ta nên sử dụng phẫu thuật nội soi thay vì mổ mở để giảm thiểu các biến chứng cho mẹ. Cách tiếp cận phổ biến nhất vẫn là cắt bỏ sừng tử cung bằng cách rạch một đường xung quanh chu vi của sừng tử cung để lấy khối thai và khâu đóng lại sau khi đã loại bỏ chúng.
1.5. Kết quả
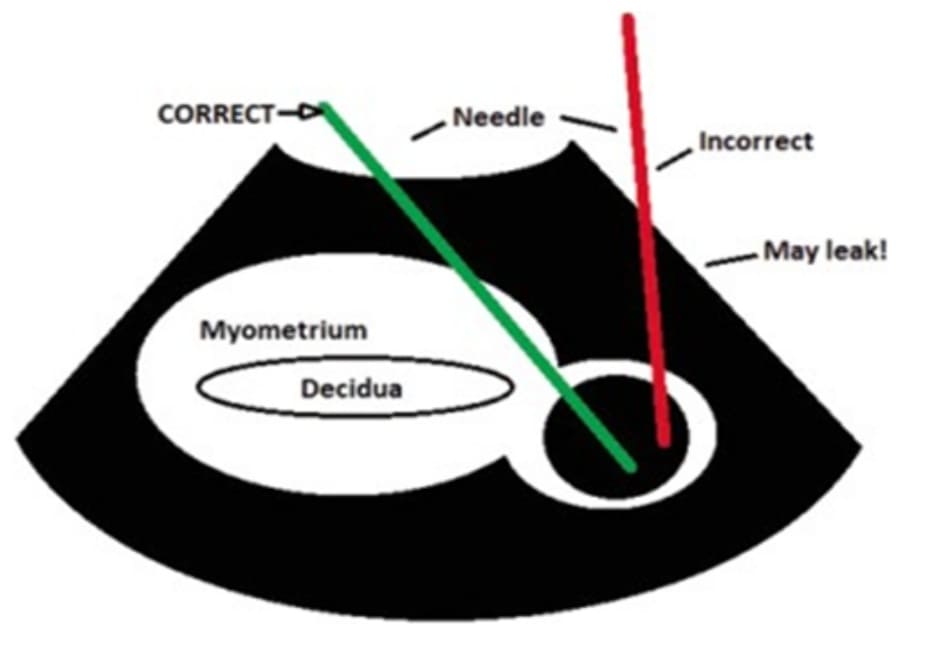
Thai kẽ được chẩn đoán phổ biến nhất ở tuổi thai từ 6,9 đến 8,2 tuần. Các yếu tố nguy cơ bao gồm tổn thương vòi tử cung, cắt bỏ vòi tử cung trước đó, thụ thai bằng phương pháp thụ tinh trong ống nghiệm và tiền sử mắc các bệnh lây truyền qua đường tình dục. Một nửa số bệnh nhân xuất hiện triệu chứng đau bụng, 30% bị ra máu trong ba tháng đầu và 30% không có triệu chứng. Bệnh nhân trong trường hợp này được tiêm MTX tại chỗ theo Hình 11.4. Theo quy trình, một kim 21-G được đưa vào khối thai dưới hướng dẫn của siêu âm và với sự hỗ trợ của thiết bị chọc dò tự động. Tiêm 50 mg MTX đã chuẩn bị trước (pha 100mg trong 2 ml dung môi) và siêu âm lại thấy không còn tim thai. Giữ bông ở vị trí đặt kim trong 5 phút để theo dõi xem có chảy máu sau thủ thuật hay không. Điều quan trọng là phải đưa kim đi qua lớp cơ tử cung sao cho vị tri kim đi vào túi thai phải thông thương với buồng tử cung để tránh chảy máu vào ổ bụng (rò rỉ qua đường kim). Sau can thiệp kiểm tra khoang Morison đánh giá tình trạng rò rỉ máu vào ổ bụng. Bệnh nhân này sau can thiệp có chảy máu âm đạo, với lượng giảm dần và hết hẳn sau 2 tuần, nồng độ B-hCG giảm dần về bình thường và không ghi nhận biến chứng nào.
1.6. Đúc kết lâm sàng
- 3D TVUS là công cụ chính để chẩn đoán
- Nếu có sự xuất hiện của đường kẽ, gần như có thể chẩn đoán xác định.
- Lớp cơ tử cung xung quanh GS dưới 5 mm, khoang tử cung rỗng, và túi thai cách buồng tử cung dưới 1 cm là tiêu chuẩn để chẩn đoán.
1.7. TÀI LIỆU THAM KHẢO
- Damario MA, Rock JA. Ectopic pregnancy. Te Linde’s operative gyne- Philadelphia: Lippincott, Williams & Wilkins; 2003:507–36.
- Tulandi T, Al-Jaroudi Interstitial pregnancy: results generated from the society of reproductive surgeons registry. Obstet Gynecol. 2004;103:47– 50.
- Soriano D, Vicus D, Mashiach R, Schiff E, Seidman D, Goldenberg M. Laparoscopic treatment of cornual pregnancy: a series of 20 consecutive cases. Fertil Steril. 2008;90:839–43.
- Lau S, Tulandi Conservative medical and surgical management of interstitial ectopic pregnancy. Fertil Steril. 1999;72:207–15.
- Jafri SZ, Loginsky SJ, Bouffard JA, Selis Sonographic detection of interstitial pregnancy. J Clin Ultrasound. 1987;15:253–7.
- Timor-Tritsch IE, Moneagudo A, Matera C, Veit Sonographic evo- lution of cornual pregnancies treated without surgery. Obstet Gynecol. 1992;79:1044–9.
- Ackerman TE, Levi CS, Dashefsky SM, Holt SC, Lindsay DJ. Insterstitial line: sonographic finding in instersitital (cornual) ectopic pregnancy. 1993;189:83–87.
- Moawad NS, Mahajan ST, Moniz MH, Taylor SE, Hurd WW. Current diagnosis and treatment of interstitial Am J Obstet Gynecol. 2010;202:15–29.
- Bourdel N, Roman H, Gallot D, et al. Interstitial pregnancy. Ultrasono- graphic diagnosis and contribution of MRI: a case Gynecol Obstet Fertil. 2007;35:121–4.
- Jermy K, Thomas J, Doo A, Bourne T. The conservative management of interstitial BJOG. 2004;111:1283–8.
- Timor-Tritsch IE, Monteagudo A, Lerner A ‘potentially safer’ route for puncture and injection of cornual ectopic pregnancies. Ultrasound Obstet Gynecol. 1996;7:353–5.
- Monteagudo A, Minior VK, Stephenson C, Monda S, Timor-Tritsch
- Non-surgical management of live ectopic pregnancy with ultra- sound-guided local injection: a case series. Ultrasound Obstet Gynecol. 2005;25:282–8.
- Lim JE, Kim T, Lee NW, et Ultrasonographic endometrial features in tubal pregnancy: are they predictive factors in successful medical treat- ment? Ultrasound Med Biol. 2007;33:714–19.
- Tulandi T, Vilos G, Gomel V. Laparoscopic treatment of interstitial Obstet Gynecol. 1995;85:465–7.
- Coric M, Barisic D, Strelec Laparoscopic approach to interstitial pregnancy. Arch Gynecol Obstet. 2004;270:287–9.
- MaCrae R, Olowu O, Rizzuto MI, Odejinmi F. Diagnosis and laparo- scopic management of 11 consecutive cases of cornual ectopic pregnan- Arch Gynecol Obstet. 2009;280:59–64.
2. Thai ngoài tử cung ở cổ tử cung
2.1. Trường hợp lâm sàng
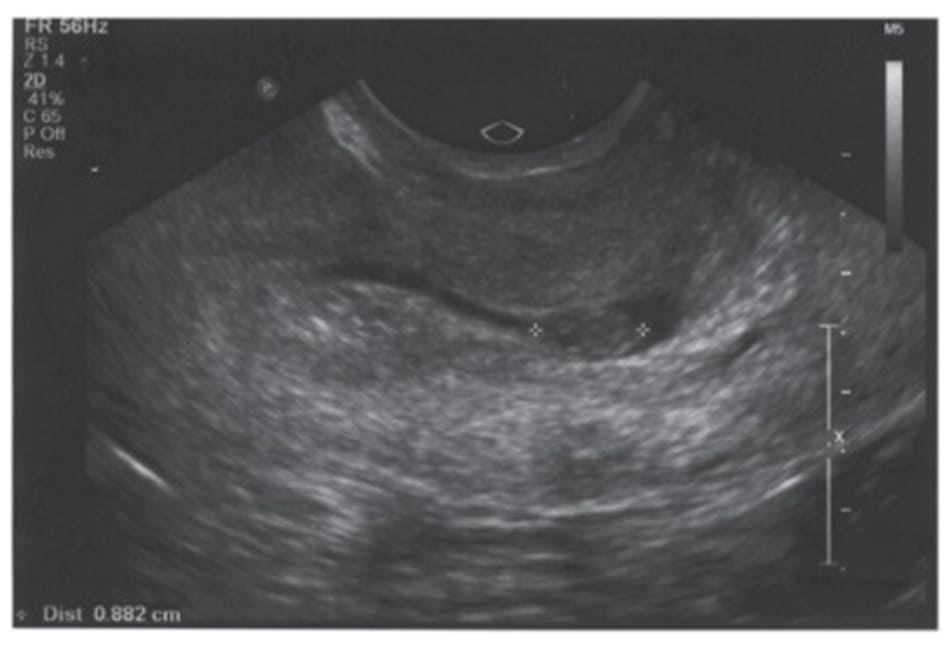
Bệnh nhân 35 tuổi G3P1A1 (A là số lần phá thai/sảy thai) bị chảy máu âm đạo tại tuần thứ 5 sau điều trị bằng phương pháp thụ tinh trong ống nghiệm (IVF), chuyển 1 phôi. Tiền sử cho thấy đã nạo hút thai 1 lần khi thai được 6 tuần và mổ lấy thai. Đặt mỏ vịt thấy cổ tử cung mở rộng bất thường, còn đọng lại 1 lượng máu nhỏ ở cổ tử cung. Nồng độ hCG trong huyết thanh là 9112 IU / L và siêu âm qua ngả âm đạo cho thấy một túi thai trong thân cổ tử cung với một túi noãn hoàng và một cực thai có tim thai (Hình 12.1). Bệnh nhân được chẩn đoán là EP ở cổ tử cung (CEP). Xét nghiệm chức năng gan thận trong giới hạn bình thường.
2.2. Hướng xử trí?
- Thực hiện nạo hút thai ngay lập tức
- Gây tắc động mạch tử cung (UAE) hai bên và sau đó thực hiện nạo hút thai
- Chỉ định MTX đơn liều
- Chỉ định MTX đa liều
2.3. Chẩn đoán và đánh giá
CEP được định nghĩa là tình trạng thai làm tổ trong bề mặt nội mạc cổ tử cung. Tỷ lệ mắc là khoảng 1 trên 9000 ca mang thai và chiếm 0,15% tổng số ca mang thai ngoài tử cung. Bệnh nhân của chúng tôi có một số yếu tố nguy cơ đối với CEP bao gồm tiền sử nạo, hút thai, xuất hiện ở 50–70% bệnh nhân CEP và tiền sử mổ lấy thai, xuất hiện ở 16,7–37,5% bệnh nhân CEP, và thụ thai sau làm IVF. Mang thai cổ tử cung chiếm 0,1% tổng số trường hợp mang thai IVF và 3,7% tổng số trường hợp mang thai ngoài tử cung sau làm IVF. Các yếu tố nguy cơ khác đặc trưng CEP bao gồm đã từng đặt dụng cụ tử cung trước đó hoặc chấn thương ở cổ tử cung và hội chứng Asherman.
Theo y văn, CEP biểu hiện trên lâm sàng bởi tình trạng chảy máu âm đạo (không kèm đau hạ vị) sau một thời gian vô kinh trong 90,1% trường hợp. Khi đặt mỏ vịt, thấy cổ tử cung mềm và to ra không cân xứng. Chẩn đoán phân biệt bệnh lý này bao gồm sảy thai không hoàn toàn, nhau tiền đạo, ung thư biểu mô cổ tử cung, và u cơ trơn thoái hóa.
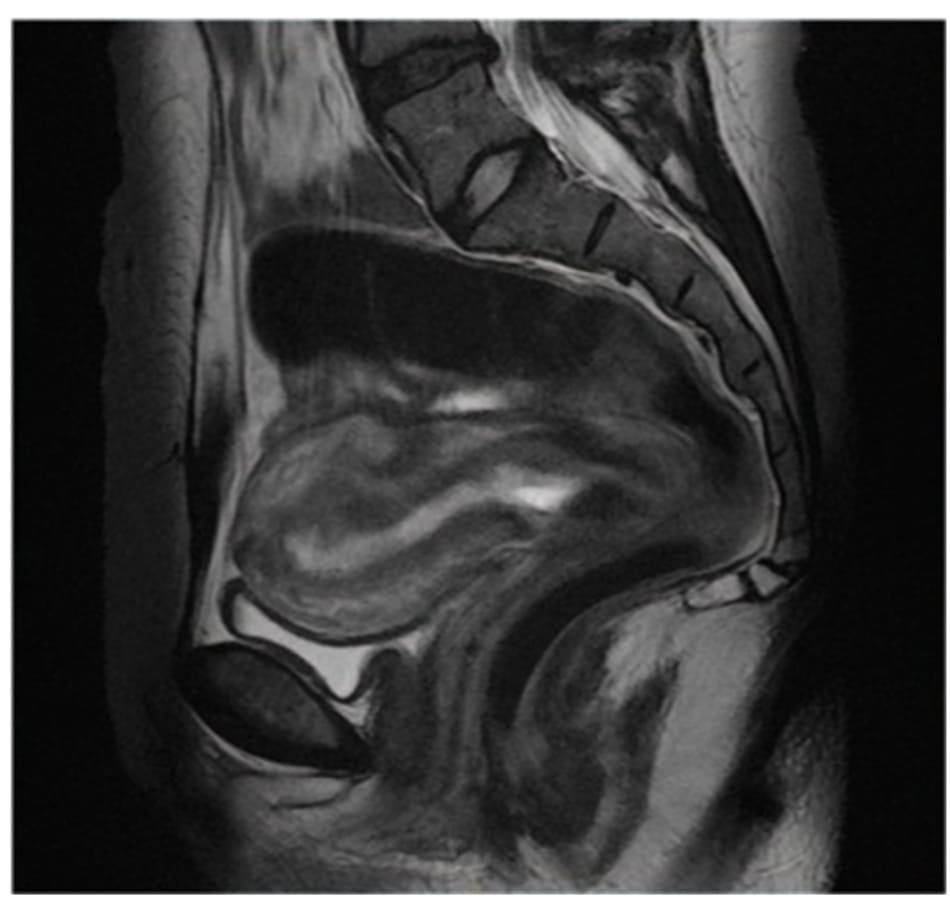
Lần siêu âm thấy CEP đầu tiên được Raskin báo cáo vào năm 1978. Gần một thập kỷ sau, Ushakov mô tả các tiêu chuẩn siêu âm của CEP. Đó là: túi thai trong cổ tử cung, ống cổ tử cung nguyên vẹn phía trên túi thai, cổ tử cung đóng ở phía bên trong, phát hiện sự xâm nhập của các tế bào nuôi vào cổ tử cung trên siêu âm Doppler, sự hiện diện của phôi thai / bào thai/ hoạt động của tim thai, khoang tử cung rỗng, nội mạc tử cung chuyển thành màng rụng và tử cung hình đồng hồ cát. CEP nên phân biệt với sảy thai trong buồng tử cung nhưng bị kẹt trong cổ tử cung bởi “dấu hiệu túi trượt”. Khi ấn đầu dò xuống tạo một áp lực lên khu vực cổ tử cung, nếu thai bám ở cổ tử cung thì sẽ không bị ‘trượt’ đi còn khối thai sảy bị kẹt thì sẽ trượt trên cổ tử cung. Nếu có MRI thì cũng có thể sử dụng để xác định chẩn đoán (Hình 12.2).
Trước đây, CEP được chẩn đoán muộn và nhiều phụ nữ đã phải cắt tử cung do hậu quả của việc chảy máu ồ ạt. Nâng cao nhận thức của sản phụ và siêu âm định kỳ sẽ giúp chẩn đoán sớm và làm giảm tỷ lệ mắc bệnh và tử vong.
2.4. Điều trị
Sau khi chẩn đoán CEP, nên bắt đầu điều trị ngay lập tức.
Điều trị nội khoa
Ở bệnh nhân có huyết động ổn định, điều trị nội khoa bằng meth- otrexate là lựa chọn hàng đầu. Hầu hết các dữ liệu về CEP được lấy từ các loạt ca lâm sàng, và hầu hết các chuyên gia đều ủng hộ điều trị bằng phác đồ đa liều methotrexate. Do nguy cơ chảy máu ồ ạt cao, thường phải cắt tử cung, chúng tôi khuyên bạn không nên dùng phác đồ methotrexate đơn và tiêm methotrexate tại chỗ để điều trị CEP. Chúng tôi khuyên bạn nên tiêm bắp methotrexate 1 mg / kg thể trọng vào các ngày 1, 3, 5 và 7 xen kẽ với leucovorin 0,1 mg / kg thể trọng tiêm bắp vào các ngày 2, 4, 6 và 8. Nói chung, hiệu quả điều trị methotrexate đơn thuần sẽ giảm khi nồng độ β-hCG huyết thanh> 10.000 IU / L, tuổi thai> 9 tuần, có hoạt động tim thai và chiều dài đầu mông (CRL)> 10 mm.
Methotrexate có thể được sử dụng đơn thuần hoặc kết hợp với các thuốc nội khoa/phẫu thuật khác. Mặc dù có một số báo cáo về việc tiêm KCL tại khối thai khi có hoạt động tim thai, nhưng rủi ro lại cao hơn lợi ích. Hơn nữa, theo kinh nghiệm của chúng tôi, tất cả các hoạt động của tim thai cuối cùng sẽ chấm dứt khi điều trị bằng methotrexate đa liều. Mifepristone (RU 486) là một hoạt chất kháng progesterone có tác dụng chống hình thành màng rụng. Trong một loạt trường hợp gồm bốn bệnh nhân CPE được điều trị bằng methotrexate (MTX) và mifepristone đơn liều, ba bệnh nhân yêu cầu điều trị bổ sung bao gồm UAE, nong và nạo hút thai, và misoprostol. Vì thế, hiệu quả của phác đồ điều trị này còn nhiều nghi vấn.
Điều trị phẫu thuật
Điều trị phẫu thuật chỉ nên được áp dụng cho những bệnh nhân bị chảy máu nặng hoặc khi điều trị nội khoa kết hợp với UAE không thành công. Thay vì phẫu thuật, tốt nhất là thực hiện UAE sau khi điều trị bằng methotrexate nếu thấy cần thiết. Thực hiện UAE trước khi điều trị methotrexate không được khuyến khích; nó có thể làm giảm vận chuyển methotrexate đến mô do giảm tưới máu tổ chức. Mặt khác, điều trị bằng methotrexate đơn thuần cũng có xác suất thành công cao, UAE thì chứng tỏ được tính ưu việt trong điều trị CEP trong nhiều trường hợp bao gồm chảy máu cấp tính / bán cấp tính, UAE trước khi nạo để giảm thiểu chảy máu, và sau khi điều trị nội khoa (MTX) thất bại.
Ở những phụ nữ muốn bảo tồn khả năng sinh sản và cần phải phẫu thuật do chảy máu nhiều, điều trị ngoại khoa bao gồm thắt nhánh xuống của động mạch tử cung, tiếp theo là đưa một sonde Foley qua cổ tử cung và bơm bóng hoặc khâu cố định để giữ sonde bên trong, sau đó đặt gạc vào trong âm đạo cầm máu tương đối mới bắt đầu nạo thai. Nếu thời gian cho phép, nên thực hiện UAE chọn lọc trước khi nạo để giảm thiểu chảy máu, nhưng cần nhớ là chúng làm ảnh hưởng tới khả năng sinh sản sau này. Ngày nay UAE không còn được áp dụng nhiều.
2.5. Kết quả
Sau khi bắt đầu điều trị bằng methotrexate đa liều, nồng độ β-hCG huyết thanh của bệnh nhân tăng lên 11,514 IU / L vào ngày thứ 3 rồi bắt đầu có xu hướng giảm. Β-hCG ngày thứ 7 là 6000 IU / L. Bệnh nhân không có dấu hiệu xuất huyết kể từ khi nhập viện và siêu âm lại cho thấy không còn hoạt động tim thai, túi thai dần thoái triển. Cô ấy được xuất viện vào ngày thứ 7 sau khi tiêm liều methotrexate cuối cùng và được theo dõi ngoại trú hàng tuần. Nồng độ β-hCG huyết thanh tiếp tục giảm, và ở tuần thứ 4, nồng độ hCG đã về mức bình thường, siêu âm không còn thấy khối thai. Bệnh nhân kết thúc theo dõi ngoại trú, được dặn phải chú ý hơn ở những lần mang thai kế tiếp.
2.6. Đúc kết lâm sàng
- Chảy máu âm đạo không đau sau một thời gian vô kinh thì nên nghi ngờ có thai ở cổ tử cung, đặc biệt khi có các yếu tố nguy cơ.
- Chẩn đoán và điều trị sớm có thể là biện pháp cứu cánh và giúp giảm tỷ lệ biến chứng.
- Siêu âm là phương pháp chính để chẩn đoán
- Bệnh nhân có chẩn đoán CEP nên được nhập viện và điều trị nội trú.
- Ở bệnh nhân có huyết động ổn định, điều trị nội khoa với methotrexate đa liều là biện pháp hàng đầu.
- Cần điều trị phẫu thuật ngay lập tức khi CEP diễn biến chảy máu đe dọa tính mạng.
- Mặc dù hiếm gặp, nhưng cần phải giải thích với bệnh nhân rằng có thể phải cắt bỏ toàn bộ tử cung để cứu sống họ trong trường hợp chảy máu ồ ạt.
2.7. TÀI LIỆU THAM KHẢO
- Tulandi T. Cervical pregnancy. UpToDate. http://www.uptodate.com/contents/cervical-pregnancy?source=search_result&search=cervi- cal+ect opic&selectedTitle=1~150#H1. (2014). Accessed 2 Dec
- Ushakov FB, Elchalal U, Aceman PJ, Schenker Cervical pregnancy: past and future. Obstet Gynecol Surv. 1997;52(1):45–59.
- Vela G, Tulandi Cervical pregnancy: the importance of early diagno- sis and treatment. J Minim Invasive Gynecol. 2007;14(4):481–4. doi:10.1016/j.jmig.2006.11.012.
- Zakaria MA, Abdallah ME, Shavell VI, Berman JM, Diamond MP, Kmak Conservative management of cervical ectopic pregnancy: utility of uter- ine artery embolization. Fertil Steril. 2011;95(3):872–6. doi:10.1016/j. fertnstert.2010.12.024.
- Verma U, Goharkhay N. Conservative management of cervical ecto- pic Fertil Steril. 2009;91(3):671–4. doi:10.1016/j.fertn- stert.2007.12.054.
- Lobo Ectopic pregnancy: etiology, pathology, diagnosis, manage- ment, fertility prognosis. In: Lentz GM, Lobo RA, Gershenson DM, Katz VL. Comprehensive gynecology. 6th ed. Philadelphia: Elsevier Mosby; 2013. pp. 361–81.
- Raskin Diagnosis of cervical pregnancy by ultrasound: a case re- port. Am J Obstet Gynecol. 1978;130(2):234–5.
- Hung TH, Shau WY, Hsieh TT, Hsu JJ, Soong YK, Jeng CJ. Prognostic ac- tors for an unsatisfactory primary methotrexate treatment of cervical pregnancy: a quantitative Hum Reprod. 1998;13(9):2636–42.
- Gómez García MT, Aguarón Benitez G, Barberá Belda B, Callejón Rodrí- guez C, González Merlo G. Medical therapy (methotrexate and mifepris- tone) alone or in combination with another type of therapy for the man- agement of cervical or interstitial ectopic Eur J Obstet Gynecol Reprod Biol. 2012;165(1):77–81. doi:10.1016/j. ejogrb.2012.06.024. Epub 2012 Jul 7.
- Martinelli P, Maruotti GM, Oppedisano R, Agangi A, Mazzarelli LL, Vo- tino C, et Is uterine artery embolization for cervical ectopic pregnancy always safe? J Minim Invasive Gynecol. 2007;14(6):758–63.
3. Thai ngoài tử cung trong buồng trứng
3.1. Trường hợp lâm sàng
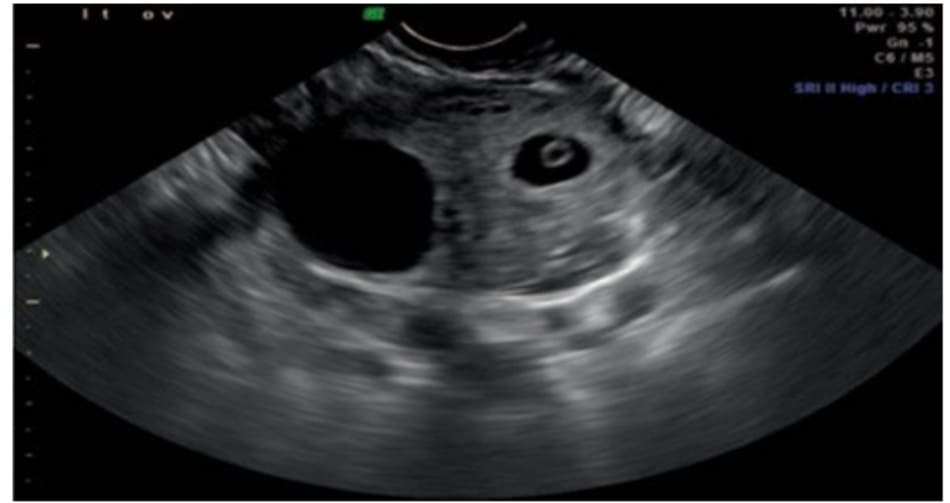
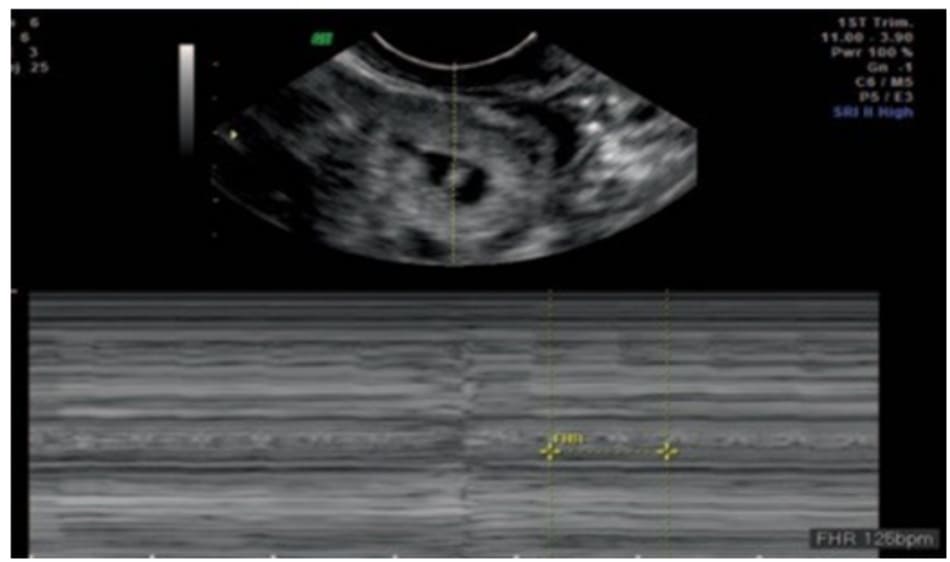
Một phụ nữ 37 tuổi, G3P1, hiện đang mang 1 thai 7 tuần tuổi. Đây là một trường hợp thụ tinh thành công sau điều trị vô sinh yếu tố nam. Nồng độ hCG huyết thanh là 12.074 mIU / ml và có xu hướng tăng phù hợp với 1 thai trong buồng tử cung. Khám lâm sàng, bệnh nhân không có biểu hiện đau bụng, chảy máu âm đạo. Siêu âm qua ngả âm đạo cho thấy tử cung bình thường nhưng không quan sát thấy túi thai trong buồng tử cung. Phần phụ bên phải không có bất thường nhưng ở buồng trứng trái xuất hiện 1 túi thai kích thước 2,1 × 1,9 × 2,4 cm chứa túi noãn hoàng và cực thai (Hình 13.1). Nhịp tim thai là 125 nhịp / phút (Hình 13.2). Tuổi thai được tính là 6 tuần 1 ngày. Ngoài ra còn quan sát được 1 hoàng thể ở buồng trứng trái, nằm ngay cạnh khối thai. Không có dịch bất thường ở túi cùng.
3.2. Hướng xử trí?
- Dùng MTX đơn liều 50mg tiêm bắp. Kiểm tra nồng độ hCG tại ngày thứ 4 và thứ 7 sau tiêm để đánh giá xu hướng. (giảm)
- Thực hiện nội soi ổ bụng cắt buồng trứng (có kèm theo vòi tử cung hoặc không) bên trái và gửi giải phẫu bệnh để khẳng định chẩn đoán.
- Tiêm MTX trực tiếp vào túi thai dưới hướng dẫn siêu âm qua ngả âm đạo.
3.3. Chẩn đoán và đánh giá
Thai phát triển ở bên ngoài lớp nội mạc tử cung, được gọi chung là chửa ngoài tử cung, gây biến chứng cho khoảng 2% các trường hợp mang thai. EP không nằm trong vòi tử cung đặc biệt đáng quan ngại vì chúng có thể biểu hiện triệu chứng muộn, với khả năng được tưới máu nhiều hơn nên sẽ có nguy cơ chảy máu đe dọa tính mạng cao khi khối thai bị vỡ. Thai ngoài tử cung trong buồng trứng (OEP) là một dạng thai ngoài tử cung hiếm gặp, ước tính xảy ra ở 3,6% tổng số trường hợp mang thai ngoài tử cung. Căn nguyên của OEP nguyên phát vẫn chưa được biết và có thể xảy ra khi không có các yếu tố nguy cơ. Như chúng ta đã biết, trứng di chuyển từ buồng trứng đến vòi tử cung, có thể gặp tinh trùng để thụ tinh tại bất cứ vị trí nào, và buồng trứng cũng là 1 trong số đó. Một nghiên cứu của Joseph và Irvine đã cho thấy việc sử dụng các dụng cụ tử cung và công nghệ hỗ trợ sinh sản ‘đóng góp’ khoảng 20% số ca EP mỗi năm.
Do nhiều phụ nữ mang thai ngoài tử cung không có triệu chứng nên việc chẩn đoán sớm EP, đặc biệt là EP ở vị trí ngoài vòi tử cung, là điều hết sức quan trọng (và lúc này chúng ta cũng cần 1 bác sĩ siêu âm có kinh nghiệm nữa!). Đau bụng và chảy máu âm đạo là những biểu hiện thường gặp của thai ngoài tử cung bất kể vị trí nào, khiến việc phân biệt OEP với TEP và NTEP (thai trong vòi tử cung và thai ngoài vòi tử cung nhưng ở vị trí khác buồng trứng) trở nên rất khó khăn. Không chẩn đoán được OEP có thể là 1 thảm họa, do biến chứng vỡ khối EP và xuất huyết ồ ạt có thể làm tăng nguy cơ cắt bỏ buồng trứng thậm chí là tử vong. Thật vậy, khối thai vỡ có thể có biểu hiện bụng cấp tính, lan lên vai, và thậm chí sốc giảm thể tích do ngập máu ổ bụng.
Chẩn đoán OEP được xác nhận bằng phẫu thuật dựa trên bốn tiêu chuẩn của Spiegelberg (1878): (1) vòi Fallope và tua vòi cùng bên (tổn thương) còn nguyên vẹn và tách biệt khỏi buồng trứng chứa khối thai, (2) túi thai ở vị trí bình thường trong buồng trứng , (3) túi thai được nối với tử cung bởi dây chằng tử cung – buồng trứng, và (4) có tổ chức buồng trứng trong thành túi thai. Mặc dù chẩn đoán xác định OEP phụ thuộc vào những phát hiện mô bệnh học thu được sau phẫu thuật, nhưng những tiến bộ trong siêu âm qua ngả âm đạo đã khiến nó trở thành một công cụ chẩn đoán quan trọng trong các trường hợp OEP cũng như EP ở các vị trí khác. OEP thường biểu hiện trên siêu âm là 1 nang giảm âm nằm trên hoặc trong buồng trứng, ranh giới là 1 viền tăng âm. Ít khi thấy túi noãn hoàng hoặc cực thai. Điều thú vị là khoảng 70% trường hợp thai ngoài tử cung không được chẩn đoán, thay vào đó bị nhầm lẫn là vỡ hoàng thể hoặc nang xuất huyết do các đặc điểm lâm sàng khá giống nhau. Trong trường hợp ở trên, OEP được chẩn đoán bằng siêu âm với sự xuất hiện của túi thai, cực thai, và tim thai ở buồng trứng trái.
3.4. Điều trị
Các chiến lược điều trị đối với OEP tương tự như các trường hợp EP trong vòi tử cung. Ổn định huyết động sau đó phẫu thuật ngay trong trường hợp nghi ngờ vỡ khối thai. Phương pháp phẫu thuật phụ thuộc vào cả bệnh nhân và bác sĩ phẫu thuật, bao gồm nội soi và / hoặc phẫu thuật mở ổ bụng với mục tiêu cuối cùng là loại bỏ khối thai, cầm máu và bảo tồn tổ chức buồng trứng không bị tổn thương. Trong y văn, OEP thường được điều trị bằng cách cắt bỏ toàn bộ buồng trứng hoặc bằng phương pháp cắt hình chêm (cắt hình tam giác đỉnh quay về trung tâm buồng trứng) để cố gắng bảo tồn sổ tổ chức buồng trứng khỏe mạnh còn lại. Nên cân nhắc sử dụng MTX sau phẫu thuật ở một số bệnh nhân nghi ngờ còn tồn dư mô nguyên bào nuôi.
Điều trị nội khoa ban đầu có thể được xem xét ở những bệnh nhân ổn định về huyết động. Mặc dù điều trị nội khoa với methotrexate tiêm bắp có tỉ lệ thành công tương đối cao, vẫn tồn tại mối lo ngại về một số trường hợp điều trị thất bại và cần phẫu thuật cấp cứu. Điều này đặc biệt đúng với trường hợp có tim thai, cho thấy một thai kỳ đang tiến triển. Dùng MTX có thể tránh can thiệp phẫu thuật; tuy nhiên, quá trình theo dõi sát thường mất cả tuần hoặc lâu hơn và điều này có thể gây căng thẳng cho cả bác sĩ lẫn bệnh nhân.
Sự phát triển của dịch vụ chăm sóc y tế hiện nay cho phép chẩn đoán sớm hơn, do đó tỷ lệ điều trị bảo tồn cũng cao hơn trước. Tiêm tại chỗ methotrexate, KCL, hoặc Glucose ưu trương dưới hướng dẫn của siêu âm mang lại nhiều ưu điểm, bao gồm hạn chế tác động toàn thân (chủ yếu của MTX), nồng độ dược chất tập trung tại vị trí khối thai và có thể tác động trực tiếp gây hủy khối thai. Điều trị OEP bằng cách hút thai dưới hướng dẫn của siêu âm qua ngả âm đạo, sau đó dùng methotrexate tại chỗ, có thể đặc biệt có giá trị trong trường hợp thai có tim thai (+). Ưu điểm là đạt hiệu quả điều trị sớm (gây ngừng hoạt động tim thai ngay lập tức), tránh phải phẫu thuật, không gặp phải các biến chứng liên quan đến nội soi hoặc phẫu thuật mở ổ bụng.
3.5. Kết quả
Sau khi thảo luận về các lựa chọn điều trị, bệnh nhân vẫn muốn duy trì khả năng sinh sản nên đã chọn can thiệp không phẫu thuật. Bệnh nhân được mê tĩnh mạch, dưới hướng dẫn của siêu âm qua ngã âm đạo, túi thai trong buồng trứng được chọc hút bằng kim IVF 17-G. Sau đó tiêm 50mg MTX vào vị trí khối thai mới hút bỏ, sau đó phá vỡ nang hoàng thể. Siêu âm qua ngã âm đạo theo dõi 1 tuần sau không thấy bất thường gì, nồng độ hCG huyết thanh giảm đều đặn về mức bình thường sau 8 tuần Bệnh nhân sau đó đã thụ thai và sinh ra một đứa trẻ khỏe mạnh.
3.6. Đúc kết lâm sàng
- Bốn tiêu chí lâm sàng ban đầu của Spiegelberg để chẩn đoán OEP đã lỗi thời vì chúng cần can thiệp phẫu thuật để chẩn đoán và các phác đồ điều trị trước đây cũng không còn nhiều giá trị.
- Những tiến bộ trong siêu âm qua ngả âm đạo cho phép chẩn đoán sớm
- Khi nghi ngờ có chửa ngoài tử cung, nên siêu âm đánh giá EP ở vị trí ngoài vòi tử cung trước, bao gồm các vị trí như buồng trứng, mô kẽ, cổ tử cung và sẹo mổ cũ.
- OEP thường bị nhầm với nang hoàng thể.
- Đối với bệnh OEP có huyết động ổn dịnh, nên lựa chọn phương án điều trị bảo tồn, xâm lấn tối thiểu vì tính an toàn và hiệu quả của chúng.
3.7. TÀI LIỆU THAM KHẢO
- Pagidas K, Frishman Nonsurgical management of primary ovarian pregnancy with transvaginal ultrasound-guided local administration of methotrexate. J Minim Invasive Gynecol. 2013;20(2):252–4.
- Cepni I, Guralp O, Ocal P, Salahov R, Gurleyen H, Idil M. An alternative treatment option in tubal ectopic pregnancies with fetal heartbeat: aspi- ration of the embryo followed by single-dose methotrexate administra- Fertil Steril. 2011;96(1):79–83.
- Xie PZ, Feng YZ, Zhao Primary ovarian pregnancy. Report of fifteen cases. Chin Med J (Engl). 1991;104(3):217–20.
- Marcus SF, Brinsden PR. Primary ovarian pregnancy after in vitro fertilization and embryo transfer: report of seven cases. Fertil Steril. 1993;60(1):167–9.
- Joseph RJ, Irvine Ovarian ectopic pregnancy: aetiology, diag- nosis, and challenges in surgical management. J Obstet Gynaecol. 2012;32(5):472–4.
- Hallatt Primary ovarian pregnancy: a report of twenty-five cases. Am J Obstet Gynecol. 1982;143(1):55–60.
- Comstock C, Huston K, Lee W. The ultrasonographic appearance of ovarian ectopic Obstet Gynecol. 2005;105(1):42–5.
- Odejinmi F, Rizzuto MI, Macrae R, Olowu O, Hussain M. Diagnosis and laparoscopic management of 12 consecutive cases of ovarian pregnancy and review of J Minim Invasive Gynecol. 2009;16(3):354–9.
- Kraemer B, Kraemer E, Guengoer E, Juhasz-Boess I, Solomayer EF, Wallwiener D, et al. Ovarian ectopic pregnancy: diagnosis, treatment, correlation to Carnegie stage 16 and review based on a clinical Fer- til Steril. 2009;92(1):392–5.
- Kudo M, Tanaka T, Fujimoto S. A successful treatment of left ovarian pregnancy with Nihon Sanka Fujinka Gakkai Zasshi. 1988;40(6):811–3.
- Su WH, Cheung SM, Chang SP, Chang WH, Cheng Is ovarian preg- nancy a medical illness? Methotrexate treatment failure and rescue by laparoscopic removal. Taiwan J Obstet Gynecol. 2008;47(4):471–3.
- Raughley MJ, Frishman Local treatment of ectopic pregnancy. Se- min Reprod Med. 2007;25(2):99–115.
Tham khảo thêm một số bài viết cùng chủ đề