Bài viết Theo dõi nỗ lực hít vào của bệnh nhân trong quá trình thở máy: Thông khí bảo vệ phổi và cơ hoành được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Monitoring Patient Respiratory Effort During Mechanical Ventilation: Lung and Diaphragm-Protective Ventilation
Giới thiệu
Như một số thời điểm trong khi thở máy, thở tự nhiên phải được bắt đầu. Thở tự nhiên có nguy cơ chấn thương phổi và cơ hoành quan trọng trên lâm sàng. Mặc dù các bác sĩ lâm sàng chủ yếu tập trung vào việc theo dõi chức năng phổi để ngăn ngừa tổn thương phổi do máy thở (VILI, ventilator-induced lung injury) khi thở máy thụ động, nhưng ít chú ý đến nguy cơ VILI khi thở máy hỗ trợ. Nỗ lực hít vào tự phát mạnh mẽ có thể gây ra cả tổn thương phổi (bệnh nhân tự gây tổn thương phổi [P-SILI, patient self-inflicted lung injury]) [1,2] và chấn thương cơ hoành (myotrauma) [3,4]. Những tổn thương này dẫn đến thông khí kéo dài, cai máy khó khăn, tăng tỷ lệ mắc bệnh và tử vong [5,6,7]. Thở tự nhiên an toàn là một thách thức phức tạp vì người ta phải nhằm mục đích giảm thiểu thể tích và áp lực xuyên phổi (PL, transpulmonary pressure) để tránh P-SILI trong khi vẫn duy trì mức độ nỗ lực hít vào phù hợp của bệnh nhân để tránh teo cơ hoành. Để có điều này, theo dõi hô hấp là chìa khóa. Một số phương pháp thực tế có sẵn để theo dõi nỗ lực hít vào của bệnh nhân trong khi thở máy hỗ trợ; đánh giá này mô tả việc sử dụng chúng trong thực hành lâm sàng.
Cơ chế của hơi thở tự phát
Trong quá trình thở máy được hỗ trợ, mỗi hơi thở dẫn đến sự lệch âm trong áp lực màng phổi (Ppl, pleural pressure) (phát sinh từ nỗ lực hít vào của bệnh nhân) kết hợp với áp lực đường thở dương (Paw) do máy thở cung cấp. Paw tăng lên tùy theo mức hỗ trợ được đặt trên máy thở, trong khi Ppl giảm xuống tỷ lệ thuận với nỗ lực của bệnh nhân. PL tương ứng với sự khác biệt giữa Paw và Ppl (PL = Paw – Ppl); áp lực này phản ánh lực căng áp dụng cho phổi bởi tác động kết hợp của máy thở và nỗ lực của bệnh nhân. Mặc dù trong thông khí cơ học thụ động, Paw là một đại diện hợp lý cho PL [8], trong khi thở máy được hỗ trợ, các nỗ lực hít vào mạnh mẽ có thể làm tăng PL trên giới hạn an toàn. Áp lực quá mức như vậy là không thể nhìn thấy được khi dựa vào dạng sóng của máy thở; ở cùng giá trị áp lực đường thở, áp lực xuyên phổi có thể được hỗ trợ cao hơn nhiều so với thở máy có kiểm soát (Hình 1).
Tổn thương phổi trong quá trình thở tự nhiên: Bệnh nhân tự gây tổn thương cho phổi
Trong quá trình thở tự nhiên, những nỗ lực hít vào mạnh mẽ của bệnh nhân có thể gây tổn thương phổi (P-SILI) thông qua các cơ chế khác nhau (Hình 2).
Căng thẳng phổi quá mức tổng thể. Như đã thảo luận, các nỗ lực hít vào của bệnh nhân có thể làm tăng thể tích khí lưu thông và PL trên giới hạn an toàn khi tăng cường hô hấp.
Căng thẳng phổi quá mức khu vực. Trong phổi bị tổn thương, phổi bị xẹp và đông đặc làm cho không đồng nhất cơ học nhu mô phổi [9], làm tăng nguy cơ volutrauma thông qua khuếch đại căng thẳng khu vực (local stress). Stress và strain cơ học không được phân phối đều trong quá trình bơm phồng. Do đó, các nỗ lực hít vào tạo ra sự dao động PL lớn ở các vùng đông đặc phía lưng, dẫn đến sự chuyển động của không khí từ khu vực không phụ thuộc sang các khu vực phụ thuộc (Hiện tượng Pendelluft). Trong khi điều này làm huy động phổi xẹp và cải thiện sự không phù hợp thông khí-tưới máu, hiện tượng này làm tăng kéo căng của khu vực phổi phụ thuộc. Trong trường hợp này, sự gia tăng PL được phát hiện bằng đo áp lực thực quản có thể không phải là thước đo đáng tin cậy của stress cục bộ [10].
Áp lực xuyên mạch máu và phù phổi. Trong quá trình thở tự nhiên, Ppl âm tính được tạo ra bởi nỗ lực hít vào làm tăng áp lực xuyên mạch máu (độ chênh áp lực di chuyển chất lỏng qua các mạch phổi), làm tăng tổng lượng nước phổi và phù phổi [9, 10] và làm suy giảm thêm chức năng hô hấp.

”Trong quá trình thông khí thụ động, sự thay đổi áp lực màng phổi là dương tính và do đó áp lực xuyên phổi thấp hơn áp lực đường thở (Paw). Trong quá trình thông khí hỗ trợ, một nỗ lực hít vào mạnh mẽ tạo ra một sự thay đổi âm tính về áp lực màng phổi dẫn đến sự gia tăng áp lực xuyên phổi; Do đó áp lực xuyên phổi có thể cao hơn nhiều so với áp lực đường thở.”
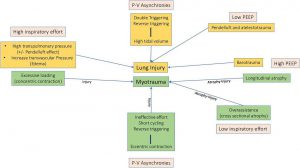
Không đồng bộ. Sự không đồng bộ của máy thở, bao gồm kích hoạt kép (thở cơ học kép từ một nỗ lực hít vào duy nhất) và kích hoạt ngược (co thắt cơ hoành do bơm phồng lồng ngực thụ động ở bệnh nhân thở máy thụ động) [11] có thể làm tăng thể tích khí lưu thông và PL và gây ra chấn thương phổi.
Do đó, việc theo dõi chặt chẽ nỗ lực hít vào của bệnh nhân trong quá trình thở máy hỗ trợ để phát hiện và giảm thiểu các cơ chế chấn thương tiềm tàng này là bắt buộc.
Chấn thương cơ hoành trong khi thở tự nhiên: Myotrauma
Việc sử dụng thông khí cơ học không phù hợp có thể làm tổn thương không chỉ phổi (barotrauma và volutrauma) mà cả cơ hô hấp (myotrauma). Thông khí cơ học gây ra chấn thương cơ do nhiều cơ chế khác nhau, dẫn đến một con đường chung cuối cùng của VIDD [5].
Các cơ chế của myotrauma được tóm tắt trong hình 2:
- Không tải quá mức (Excessive unloading). Hỗ trợ quá mức từ thở máy và ức chế trung khu hô hấp từ thuốc an thần dẫn đến teo cơ cấp tính do không sử dụng và yếu cơ hoành [12]. Không tải cơ hoành gây ra bởi thông khí hỗ trợ quá mức (cả trong chế độ kiểm soát hoặc hỗ trợ) là thường xuyên trong thông khí cơ học, đặc biệt là trong 48 giờ đầu tiên. Lưu ý, mức độ nỗ lực hít vào thấp cần thiết để kích hoạt máy thở là không đủ để tránh teo cơ [3], do đó teo cơ hoành có thể xảy ra dưới thông khí hỗ trợ áp lực.
- Tải đồng tâm quá mức (Excessive concentric loading). Cơ hoành nhạy cảm với tải hô hấp quá mức. Nỗ lực hít vào của bệnh nhân cao hơn, rối loạn đồng bộ và hỗ trợ dưới mức độ không đủ hỗ trợ thường xuyên trong thở máy hỗ trợ. Các cơn co thắt đồng tâm mạnh mẽ gây ra lực căng cơ bắp cao dẫn đến viêm cơ, phân giải protein, tổn thương myofibrillar và xáo trộn sarcolemma [13, 14]. Ở những bệnh nhân nguy kịch, viêm hệ thống làm cho myofibrils cơ dễ bị tổn thương cơ học hơn [10, 15].
- Tải lệch tâm (Eccentric loading). Các cơn co thắt lệch tâm xảy ra khi một cơ tạo ra sức căng co thắt trong khi nó đang kéo dài (thay vì rút ngắn); các cơn co thắt như vậy gây tổn thương nhiều hơn so với các cơn co thắt đồng tâm (rút ngắn) [16]. Khi có áp lực dương cuối thì thở ra (PEEP) thấp và giảm quá mức thể tích phổi cuối thì thở ra, cơ hoành sẽ co lại ngay cả khi nó kéo dài trong giai đoạn thở ra (hiện tượng sau hít vào) để tránh xẹp phổi (hiện tượng phanh thở ra) [17]. Các dạng rối loạn đồng bộ cụ thể (kích hoạt ngược, chu kỳ ngắn, nỗ lực không hiệu quả) có thể tạo ra các cơn co thắt lệch tâm vì cơ hoành được kích hoạt trong giai đoạn thở ra.
- PEEP quá mức. Bằng chứng thực nghiệm sơ bộ cho thấy rằng việc duy trì cơ hoành ở độ dài ngắn hơn với việc sử dụng PEEP quá mức có thể khiến các sarcomeres rơi ra khỏi cơ bắp và rút ngắn chiều dài của nó (teo dọc) [18]. Về mặt lý thuyết điều này có thể gây bất lợi cho các đặc điểm lực căng của cơ bắp khi PEEP bị giảm, làm giảm hiệu suất cơ hoành.
Ba cơ chế chấn thương đầu tiên có thể được phát hiện bằng cách theo dõi nỗ lực hít vào, nhấn mạnh tiềm năng theo dõi như vậy để giúp các bác sĩ lâm sàng đảm bảo thở tự nhiên an toàn trong khi thở máy. Bây giờ chúng tôi tiến hành xem xét một loạt các kỹ thuật giám sát để đạt được mục tiêu này.
Theo dõi hơi thở tự nhiên bằng áp lực thực quản
Việc sử dụng theo dõi áp lực thực quản (Pes) được mô tả tốt ở những bệnh nhân mắc hội chứng suy hô hấp cấp tính (ARDS) khi thở máy thụ động [19]. Kỹ thuật này cũng là tiêu chuẩn vàng để đánh giá nỗ lực hít vào và công hô hấp nhưng việc sử dụng nó vẫn chưa phổ biến, có lẽ vì tiện ích của thông tin có nguồn gốc từ Pes đã bị đánh giá thấp. Khi được sử dụng để theo dõi sự an toàn của hơi thở tự phát, việc theo dõi Pes cho phép ước tính một số lượng các tham số khác nhau có liên quan.
Áp lực xuyên phổi
Pes có thể được sử dụng như một biện pháp thay thế của Ppl, ghi nhớ các biến thiên khu vực [20]. Do đó, nó có thể được sử dụng để đo PL (Paw – Ppl), bằng cách thay thế Ppl bằng Pes. Như được hiển thị trong Hình 1, PL có thể dễ dàng đạt giá trị cực kỳ cao trong quá trình thở máy được hỗ trợ (trong đó cả bệnh nhân và máy thở đều làm căng phổi). Giới hạn trên chấp nhận được đối với PL chưa được xác định; Giá trị hít vào tối đa “cẩn trọng” là 20 cmH2O ở bệnh nhân bị tổn thương phổi là mục tiêu hợp lý để hạn chế nguy cơ chấn thương [2,21].
Đáng lưu ý, với sự hiện diện của sự không đồng nhất thông khí khu vực và pendelluf, giá trị đo được của PL sẽ đánh giá thấp căng thẳng phổi ở các khu vực phổi phụ thuộc. Trong khi PL cao nguyên bán tĩnh (quasi-static plateau PL) thu được trong khi thủ thuật tắc nghẽn cuối thì hít vào phản ánh căng thẳng phổi khi thở máy thụ động, thì thay đổi động của PL (ΔPL) có thể phản ánh nhiều hơn về nguy cơ chấn thương khi thở tự nhiên vì hiện tượng pendelluft [22]. ΔPL có khả năng phản ánh giới hạn trên của căng thẳng cơ học đã trải qua ở các vùng lưng của phổi trong điều kiện động [23]. Hơn nữa, nhiều bằng chứng khác nhau cho thấy rằng căng thẳng phổi động (tăng theo cu kỳ thở) là yếu tố thúc đẩy tổn thương phổi quan trọng hơn so với căng thẳng phổi (đỉnh) tổng thể [24,25,26].
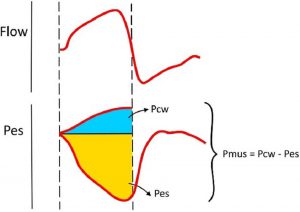
”Pmus xuất phát từ sự khác biệt giữa Pes và áp lực cơ được thêm vào để vượt qua độ đàn hồi thành ngực (Pcw). Pcw đại diện cho độ đàn hồi của thành ngực thư giãn; nó có thể được tính là tích số của thể tích khí lưu thông và độ đàn hồi của thành ngực (Ecw). Vùng Pmus theo thời gian tạo thành tích số áp lực thời gian (PTP, pressure-time product) (khu vực màu vàng và màu xanh với nhau)”
Áp lực cơ hô hấp
Pes cho phép đo lường nỗ lực hít vào. Áp lực cơ hô hấp (Pmus) tương ứng với lực tổng thể được tạo ra bởi các cơ hô hấp. Mặc dù cơ hoành là cơ hô hấp quan trọng nhất, cơ hô hấp phụ (cơ liên sườn, cơ ức đòn chũm và cơ thang) đóng góp đáng kể trong nỗ lực mạnh mẽ, đặc biệt là khi chức năng cơ hoành bị suy yếu. Như được hiển thị trong Hình 3, Pmus được tính toán từ sự khác biệt giữa Pes và áp lực bổ sung cần thiết để vượt qua độ đàn hồi thành ngực (Pcw) (Pmus = Pcw – Pes).
Mức Pmus tối ưu trong khi thở máy được hỗ trợ là không chắc chắn; dữ liệu gần đây cho thấy các giá trị Pmus tương tự như các đối tượng khỏe mạnh thở khi nghỉ ngơi có thể an toàn và có thể ngăn ngừa teo cơ hoành (5-10 cmH2O) [4, 27]. Trong thực hành lâm sàng thông thường, người ta thường có thể bỏ qua việc điều chỉnh Pcw vì độ đàn hồi của thành ngực thường tương đối thấp (ngay cả khi áp lực màng phổi tăng cao). Do đó, một mục tiêu ΔPes khoảng 3-8 cmH2O có thể được coi là có thể so sánh hợp lý với Pmus bình thường là 5-10 cmH2O.
Đo lường tiêu chuẩn vàng về nỗ lực hít vào là tích phân của Pmus trong suốt thời gian hít vào (tích số áp lực thời gian [PTP]) (Hình 3). PTP có liên quan chặt chẽ với chi tiêu năng lượng cơ hô hấp. Giá trị PTP trong khoảng từ 50 đến 100 cmH2O/s/phút có thể phản ánh mức tiêu thụ oxy thích hợp và nỗ lực hít vào chấp nhận được [28].
Trong thực hành lâm sàng thông thường, cường độ và tần số của dao động ΔPes có thể đủ để theo dõi nỗ lực hít vào.
Áp lực xuyên cơ hoành (Transdiaphragmatic Pressure)
Một ống thông bóng đôi (double balloon catheter) có thể được sử dụng để theo dõi sự thay đổi theo thì hít vào của Pes và áp lực dạ dày (Pga) để định lượng cụ thể áp lực do cơ hoành tạo ra (áp lực xuyên cơ hoành [Pdi]). Trong một nỗ lực hít vào (tùy thuộc vào mô hình chuyển động của ngực-bụng), nỗ lực co thắt cơ hoành di chuyển các cơ quan bụng xuống dưới, làm tăng áp lực bụng (làm dương tính Pga) và mở rộng khoang ngực (làm âm tính Pes). Ngay cả khi chuyển động của ngực là cơ hoành di chuyển lên trên trong khi hít vào (tức là, Pga giảm), nỗ lực co thắt của cơ hoành được phản ánh bởi thực tế là Pga giảm ít hơn so với Pes (và do đó Pdi tăng). Kỹ thuật này được sử dụng chủ yếu trong nghiên cứu hơn là thực hành lâm sàng.
Theo dõi hơi thở tự phát bằng thao tác tắc nghẽn
Thủ thuật làm tắc nghẽn thì hít vào và thì thở ra đại diện cho các thao tác dễ dàng, không xâm lấn và đáng tin cậy để đánh giá sự an toàn của hơi thở tự nhiên trong thở máy hỗ trợ.
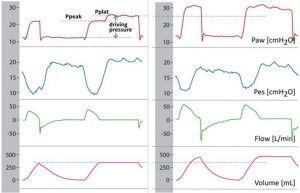
”Việc giữ thì hít vào ngắn cho phép đo Pplat đáng tin cậy trong AMV, miễn là bệnh nhân thư giãn mà không cần nỗ lực hít vào ngay lập tức. Sự khác biệt giữa Pplat và áp lực dương cuối thì thở ra (PEEP) dẫn đến áp lực đẩy ΔPaw. Trong bảng kiểm soát (a), nỗ lực hít vào của bệnh nhân rất mạnh mẽ (dao động áp lực thực quản lớn hơn): trong quá trình giữ hít vào, luồng khí dừng lại và Pplat tăng lên trên Ppeak; các cơ hô hấp được kích hoạt trước đó thư giãn và thở ra, làm cho Paw tăng lên. Trong bảng (b), nỗ lực hít vào của bệnh nhân rất thấp: sự khác biệt giữa Ppeak và Pplat là tối thiểu, cho thấy nỗ lực cơ hô hấp tối thiểu trong hơi thở hiện tại. Kỹ thuật này cho phép đánh giá hoạt động của cơ hô hấp bằng cách đo Pplat. (Được sửa đổi từ [29] với sự cho phép)”
Thao tác tắc nghẽn thì hít vào
Thao tác tắc nghẽn thì hít vào được sử dụng rộng rãi để đo áp lực cao nguyên (Pplat) trong thở máy thụ động. Áp lực đẩy (ΔP), được tính bằng chênh lệch giữa PEEP và Ppl, phản ánh căng thẳng phổi động và nguy cơ tổn thương phổi và liên quan chặt chẽ đến tỷ lệ tử vong ở bệnh nhân mắc ARDS [25]. Bellani và cộng sự [29] đề xuất rằng một thao tác tắc nghẽn thì hít vào ngắn có thể cho phép đo Pplat đáng tin cậy ngay cả trong thở máy hỗ trợ. Khi bị tắc nghẽn thì hít vào trong thở máy hỗ trợ, bệnh nhân thư giãn các cơ hô hấp co thắt ở cuối hít vào, dẫn đến tăng Paw, dễ dàng phát hiện trên dạng sóng của máy thở. Khi bệnh nhân được hỗ trợ quá mức và nỗ lực hít vào thấp, Paw bị giảm trong quá trình tắc (Hình 4). Một Pplat và ΔP cao được đo theo cách này làm tăng mối lo ngại về tình trạng quá căng chướng và tổn thương phổi. Bellani và các đồng nghiệp [29] gần đây đã báo cáo rằng ΔP và độ giãn nở được đo bằng các tắc nghẽn thì hít vào trong khi thở máy được hỗ trợ dự đoán tỷ lệ tử vong, hỗ trợ tính hợp lệ và mức độ phù hợp của các biện pháp này.
Kỹ thuật đo lường có một số hạn chế. Đầu tiên, bởi vì áp lực thu được trong điều kiện bán tĩnh, phép đo này có thể đánh giá thấp nguy cơ tổn thương phổi khu vực do cơ chế pendelluft của P- SILI [23]. Thứ hai, các bác sĩ lâm sàng cần đánh giá cẩn thận tính ổn định và mô hình của đường cong Paw trong quá trình tắc để xác định xem liệu phép đo có bị nhiễu bởi hoạt động của cơ bụng có thể làm tăng nhanh chóng khi bắt đầu thở ra thần kinh trong quá trình tắc.
Thao tác tắc nghẽn thì thở ra
Tắc nghẽn thì thở ra thường được sử dụng để đo PEEP nội tại ở bệnh nhân thở máy thụ động hoặc để đo áp lực hít vào tối đa ở bệnh nhân thở tự nhiên trong những nỗ lực hít vào tối đa. Tuy nhiên, sự thay đổi áp lực đường thở trong một thao tác tắc nghẽn cuối thì thở ra, được áp dụng ngẫu nhiên (thời gian bằng một chu kỳ hô hấp) thực sự có thể được sử dụng để đánh giá nỗ lực hít vào. Trong điều kiện kín, sự dao động trong áp lực đường thở có mối tương quan chính xác với sự dao động trong áp lực màng phổi. Do đó, sự thay đổi áp lực đường thở trong quá trình tắc (ΔPocc) có thể được sử dụng để đánh giá sự hiện diện và cường độ của sự thay đổi áp lực màng phổi do nỗ lực hít vào của bệnh nhân (có tính đến sự khác biệt về sự thay đổi áp lực màng phổi giữa các điều kiện bị tắc và động). Trên cơ sở này, ΔPocc có thể được sử dụng để dự đoán ΔPes, Pmus và ΔPL trong chu kỳ hô hấp miễn là tình trạng hô hấp của bệnh nhân không thay đổi bởi một lần tắc thở cuối, ngắn và bất ngờ [30, 31]. Phương pháp thao tác tắc nghẽn cuối thì thở ra thoáng qua là một phương pháp thực tế và không xâm lấn để phát hiện thường xuyên nỗ lực hít vào không đủ hoặc quá mức và PL trong khi thở máy hỗ trợ [32, 33].
Áp lực tắc nghẽn đường thở
P0.1 (áp lực đường thở được tạo ra trong 100 ms hít vào đầu tiên chống lại tắc nghẽn thì thở ra) cung cấp một trị số đo của trung khu hô hấp bệnh nhân (Hình 5) [34]. Whitelaw và cộng sự. [35] đã chứng minh rằng thao tác tắc nghẽn không làm thay đổi cung lượng hô hấp vỏ não cho đến khi nó bị kéo dài quá 200 ms. Ngoài ra, trong 100 ms đầu tiên, việc tạo áp lực hô hấp độc lập với cơ học phổi hoặc chức năng cơ hoành [35, 36]. Mặc dù độ tin cậy của P0.1 chỉ được xác nhận trong các nghiên cứu nhỏ, nhưng giá trị giữa 1,5 và 3,5 cmH2O [37, 38] dường như là một phương pháp dễ dàng để hướng dẫn bác sĩ lâm sàng điều chỉnh thông khí trong khi thở máy hỗ trợ [34, 39,40, 41]. Các giá trị P0.1 nhỏ hơn 1,5 cmH2O có thể gợi ý rằng nỗ lực hít vào là không đủ [42] và các giá trị lớn hơn 3,5 cmH2O cho thấy tăng hoạt trung khu hô hấp [37].
P0.1 có một số ưu điểm: rất dễ dàng và thiết thực, và hầu hết các máy thở hiện đại đều có chức năng đo nó. Phương pháp thiết lập mức hỗ trợ áp lực dựa trên giá trị P0.1 đã được mô tả [43]. P0.1 có thể có độ biến thiên trong bệnh nhân đáng kể và một số phép đo lặp lại được yêu cầu để ước tính giá trị trung bình ổn định. Hơn nữa, ở những bệnh nhân bị siêu bơm phồng phổi, PEEP nội tại gây ra sự chậm trễ trong việc giảm Paw, điều này có thể làm phát sinh sự đánh giá thấp P0.1. Conti et al. đã chứng minh rằng trong điều kiện này, bắt đầu 100 ms cho phép đo P0.1 khi lưu lượng thở ra bằng 0 khắc phục vấn đề này [44].
Theo dõi hơi thở tự phát bằng hoạt động điện cơ hoành
Việc sử dụng ống thông chuyên dụng có gắn điện cực điện cho phép theo dõi liên tục hoạt động điện của cơ hoành (EAdi) [45]. EAdi đã được chứng minh là có thể so sánh với áp lực xuyên cơ hoành, và thực tế hơn so với điện cơ bề mặt (EMG) [46].
![Hình 5. Áp lực tắc đường thở (P0.1) là áp lực đường thở (Paw) được tạo ra trong 100 ms hít vào đầu tiên chống lại tắc nghẽn thì thở ra. Điều quan trọng, thời gian 100 ms cho tính toán P0.1 nên bắt đầu tại điểm mà đường cong lưu lượng thở ra bằng 0 (đường đứt nét) để điều chỉnh auto-PEEP. (Từ [34] với sự cho phép)](https://www.healcentral.org/wp-content/uploads/2020/09/theo_doi_no_luc_hit_vao_cua_benh_nhan_trong_qua_trinh_tho_may_5-300x188.jpg)

Khi thông khí được kiểm soát bởi EAdi (trong quá trình hỗ trợ thở điều chỉnh theo tín hiệu thần kinh [NAVA, neurally adjusted ventilatory assist], tương tác bệnh nhân – máy thở được cải thiện [47, 48]; EAdi cũng giúp các bác sĩ lâm sàng nhận ra các bất đồng bộ khác nhau [47, 49]. Như được chứng minh bởi Barwing et al. [50], xu hướng EAdi có thể được sử dụng để phát hiện thất bại cai máy ở giai đoạn đầu [51, 52]: nó tăng dần ở những bệnh nhân cuối cùng thất bại trong thử nghiệm thở tự nhiên trong khi hoạt động cơ hoành vẫn ổn định ở những bệnh nhân vượt qua thử nghiệm. Thay đổi EAdi xuất hiện trước khi có dấu hiệu mệt mỏi [50].
Là một tín hiệu điện, EAdi là một biểu hiện của đầu ra vận động hô hấp (kích hoạt hệ thống thần kinh trung ương của cơ hoành) chứ không phải tạo ra lực hoành (nỗ lực). Trong khi nghỉ ngơi ở những đối tượng khỏe mạnh, EAdi thay đổi ở bất cứ đâu trong khoảng từ 5 đến 30 V [53]. Do sự khác biệt lớn này, rất khó để xác định EAdi mục tiêu cần đạt được trong quá trình thông khí cơ học. Ngoài ra, EAdi có thể được sử dụng để ước tính Pmus trong các điều kiện khác nhau của hỗ trợ máy thở [54]. Bằng cách xem xét sự kết hợp giữa hoạt động điện và hằng số tạo áp lực trong suốt thời gian (khớp thần kinh cơ học = Pmus/EAdi thu được trong quá trình tắc nghẽn thở ra), EAdi có thể cho phép đánh giá Pmus bằng hơi thở trong chu kỳ thở bình thường.
Theo dõi hơi thở tự phát bằng siêu âm cơ hoành
Kỹ thuật siêu âm cơ hoành không xâm lấn, dễ thực hiện và có thể lập lại. Sự thay đổi độ dày cơ hoành trong chu kỳ hô hấp (phần dày, TFdi) có liên quan đến việc tạo áp lực hô hấp và EAdi [55] và có thể được sử dụng để phát hiện yếu cơ hoành [55]. Giá trị TFdi dưới 30% trong nỗ lực hít vào tối đa phát hiện yếu cơ hoành với độ nhạy cao [55]. Đo độ dày cơ hoành cuối thì thở ra hàng ngày có thể phát hiện những thay đổi cấu trúc trong cơ hô hấp. Ở những bệnh nhân thở máy, sự gia tăng dần dần về độ dày cơ hoành theo thời gian có liên quan đến nỗ lực quá mức và có thể đại diện cho chấn thương cơ dưới hỗ trợ thông khí [3]. TFdi 15-30% khi thông khí có liên quan đến độ dày cơ hoành ổn định và thời gian thông khí ngắn nhất [4]. Siêu âm được sử dụng tốt nhất để đánh giá bệnh nhân ngắt quãng, vì nó không phù hợp để theo dõi liên tục.
Phần kết luận
Mục tiêu cho thông khí bảo vệ phổi và cơ hoành
Bảng 1 tóm tắt các phương pháp khác nhau có sẵn để theo dõi nỗ lực hít vào và kiểm soát hô hấp trong thở máy hỗ trợ, cùng với các mục tiêu có thể để thở tự nhiên an toàn như được thảo luận trong suốt chương này. Việc giải thích và áp dụng các phép đo phải luôn được hướng dẫn bởi bối cảnh lâm sàng. Các dạng và giai đoạn khác nhau của suy hô hấp cấp đòi hỏi một số ưu tiên khác nhau: trong ARDS sớm, phải chú ý chặt chẽ để tránh nỗ lực hít vào cao để hạn chế VILI và P- SILI. Điều chỉnh thông khí và an thần để đạt được mức độ nỗ lực hít vào thấp nên được thực hiện càng sớm càng tốt để tránh chấn thương cơ.
Vẫn chưa chắc chắn liệu có thể đạt được mức độ nỗ lực hít vào chấp nhận được trong giai đoạn cấp tính của bệnh hay không và đây vẫn là một lĩnh vực quan trọng để điều tra lâm sàng. Hiện tại, các bác sĩ lâm sàng nên cố gắng nhận thức được nỗ lực hít vào của bệnh nhân và đánh giá cao những lợi ích và tác hại tiềm tàng của việc kiểm soát nỗ lực hít vào trong suy hô hấp cấp tính.





