Bài viết Chiến lược thông khí không xâm lấn điều trị sớm RDS ở trẻ sinh non được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Noninvasive ventilation strategies for early treatment of RDS in preterm infants: an RCT
BỐI CẢNH VÀ MỤC TIÊU: Có bằng chứng cho thấy các phương pháp mới của hỗ trợ thông khí không xâm lấn (NIV) đã làm thay đổi đáng kể xử trí hội chứng suy hô hấp (RDS) ở trẻ non tháng. Các quan điểm khác cho các nhà sơ sinh học bao gồm việc đánh giá các chiến lược NIV khác nhau về tính sẵn có, hiệu quả và thất bại. Nghiên cứu này đánh giá hiệu quả của 2 chiến lược NIV khác nhau đối với điều trị RDS ở trẻ sơ sinh rất nhẹ cân (VLBW): thông khí áp lực dương liên tục qua mũi (NSIPPV), là phương thức thông khí thông thường với áp suất thở thì hít vào cao gián đoạn so sánh với thông khí hai mức áp lực dương (BiPAP), không đồng bộ.
PHƯƠNG PHÁP: Chúng tôi tiến hành một nghiên cứu đối chứng ngẫu nhiên 2 trung tâm gồm 124 trẻ VLBW (1500g và 32 tuần tuổi thai) bị RDS đã nhận được sự hỗ trợ NIV (NSIPPV, n = 62, và BiPAP, n = 62) trong vòng 2 giờ sau khi sinh. Chúng tôi đánh giá hiệu quả của các chiến lược NIV theo các kết quả chính (tỷ lệ thất bại và thời gian thông khí) và các kết cục thứ phát.
KẾT QUẢ: Tỷ lệ thất bại và thời gian hỗ trợ thông khí không khác nhau giữa NSIPPV và các chiến lược BiPAP (P0.05 cho cả hai). Hơn nữa, không có sự khác biệt giữa các nhóm đối với các kết cục thứ phát (P <0,05 cho tất cả).
KẾT LUẬN: Dữ liệu hiện tại không có sự khác biệt có ý nghĩa thống kê giữa NSIPPV và BiPAP về thời gian thông khí và thất bại, cho thấy cả hai kỹ thuật NIV đều có hiệu quả trong điều trị sớm RDS ở trẻ non tháng. Cần thêm các nghiên cứu ngẫu nhiên đối với quần thể rộng hơn để đánh giá hiệu quả của các kỹ thuật NIV đối với những kết cục lâu dài.
PHƯƠNG PHÁP
Chúng tôi tiến hành một nghiên cứu ngẫu nhiên ở 124 trẻ VLBW, được nhận vào trong 2 NICU (C. Arrigo, Bệnh viện Nhi, Alessandria, Ý, và V. Buzzi, Bệnh viện Nhi, Milan, Ý) từ tháng 1 năm 2010 đến tháng 12 năm 2012, tuổi thai (wGA) 32 tuần với cân nặng khi sinh, 1500 g (Hình 1). Sự chấp thuận đã thu được từ các ủy ban đạo đức địa phương tương ứng. Có sự đồng ý bằng văn bản và bằng văn bản, trước khi sinh, từ tất cả các bậc cha mẹ của bệnh nhân trước khi đưa vào nghiên cứu. Giao thức xử trí tại phòng sinh, xử lý RDS, các thiết bị và giao diện được sử dụng, và điều chỉnh máy thở cũng như nhau đối với 2 trung tâm. Trẻ sơ sinh có dấu hiệu của RDS lúc sinh đã được xử trí với thủ thuật bơm giữ phổi phồng (SLI, sustained lung inflation) [14] và NCPAP ngoài các khuyến nghị của Học viện Nhi khoa Hoa Kỳ. [15]
Các chiến lược hô hấp để điều trị RDS ở trẻ sơ sinh là như sau. Trong phòng sinh, sau khi hút máu mũi và miệng, SLI (25 cmH2O) được kiểm soát bằng áp lực đã được thực hiện trong 15 giây bằng mặt nạ sơ sinh và máy thở T-piece ventilator (Neopuff Infant T-Piece Resuscitator, Fisher & Paykel, Auckland, New Zealand), tiếp theo là cung cấp 5 cmH2O NCPAP. [16] Phương pháp SLI được lặp lại ở bệnh nhân suy hô hấp và/hoặc suy tim. Sau khi thất bại của SLI thứ hai, trẻ sơ sinh được đặt nội khí quản. Ở cả hai nhóm, chăm sóc sơ sinh được bắt đầu ở nồng độ oxy thấp nhất, FIO2 giữa 0,21 và 0,4, để duy trì độ bão hòa ôxy động mạch (SaO2) từ 85% đến 93%. Tất cả trẻ sơ sinh được chuyển đến NICU với hỗ trợ NCPAP (5 cmH2O). Sự hỗ trợ thêm phụ thuộc vào tuổi thai (GA):
1. Trẻ sơ sinh ≤ 26 wGA đã được thay thế surfactant dự phòng bằng INSURE trong 2 giờ đầu của cuộc sống. Sau khi INSURE, trẻ sơ sinh được chuyển sang dùng BiPAP hoặc NSIPPV.
2. Trẻ sơ sinh > 26 và ≤ 29 wGA nhận được BiPAP hoặc NSIPPV trong 2 giờ đầu tiên của cuộc đời.
3. Trẻ sơ sinh > 29 wGA không đòi hỏi hoặc có phản ứng tích cực với phương pháp hồi sức ban đầu được duy trì trên hỗ trợ NCPAP cho đến khi đến NICU; sau 2 giờ kể từ khi chào đời, nếu họ không có dấu hiệu RDS, NCPAP đã bị dừng lại. BiPAP/NSIPPV đã được thực hiện nếu các mô hình phân tích máu và lâm sàng gợi ý RDS như sau: (a) nhu cầu FIO2 > 0.4 và/hoặc (b) pH < 7.20 và/hoặc PO2 < 50 mm Hg và/hoặc PCO2 > 65 mmHg và (c) các kiểu lâm sàng của RDS đặc trưng bởi co lõm ngực và/hoặc khó thở. Ngưng thở, được định nghĩa là ≥ 4 lần/ giờ hoặc cần thông khí mặt nạ ≥ 2 lần/giờ, là một tiêu chí để bắt đầu hỗ trợ NIV.
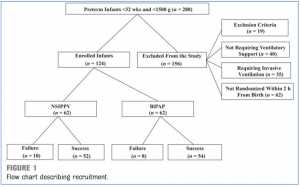
Trẻ sơ sinh biến chứng do RDS yêu cầu hỗ trợ NIV trong vòng 2 giờ kể từ khi sinh nhưng không đặt nội khí quản được phân bổ bằng cách sử dụng các số ngẫu nhiên được máy tính tạo ra để nhận NSIPPV (n = 62) hoặc BiPAP (n = 62). Những trẻ sơ sinh bị ngưng thở hoặc suy hô hấp nặng cần MV trong vòng 2 giờ sau khi sinh đã bị loại trừ khỏi nghiên cứu và bắt đầu ở MV. [17]
BiPAP
Hỗ trợ BiPAP được cung cấp bằng thiết bị Infant Flow-driver (Infant Flow System, Viasys Corp, Yorba Linda, CA). Chúng tôi sử dụng giao diện là cannula 2 ngạnh mũi (CareFusion, Yorba Linda, CA) với các kích cỡ khác nhau theo trọng lượng trẻ. Phương pháp hỗ trợ thông gió không đồng bộ này cung cấp 2 mức áp lực thấp và cao của CPAP; trẻ sơ sinh có thể tự thở ở hai mức này. Các thông số máy thở ban đầu: mức CPAP thấp 4 đến 6 cmH2O và CPAP cao 8 đến 9 cmH2O, thời gian CPAP cao là 1 giây; và tần số luân chuyển áp lực là 20 lần/phút, với điều chỉnh FIO2 mức thấp nhất để duy trì SaO2 88% đến 93%. Các thông số có thể điều chỉnh để đạt tình trạng khí máu bình thường (CPAP thấp 7 cmH2O, CPAP cao 10 cmH2O, tần số luân chuyển áp lực tối đa 30 lần/phút). Việc cai máy bắt đầu với việc giảm dần tần số luân chuyển áp lực (tối thiểu 15 lần/phút), tiếp theo là giảm mức CPAP cao xuống còn 6 cmH2O và mức CPAP thấp tới 4 cmH2O. BiPAP đã được ngừng lại khi trẻ không thấy dấu hiệu của RDS với FIO2 < 0,30.
NSIPPV
Hỗ trợ NSIPPV được cung cấp bằng máy thở (Giulia, Ginevri, Rome, Italy) qua đường mũi. Để phát hiện nỗ lực hít thở của trẻ bằng một máy pneumotachograph được trang bị một lỗ thông cố định (đường kính 2 mm đối với trẻ sơ sinh nhẹ cân). Đây là một chiến lược thông thường của thông khí đồng bộ được cung cấp bởi giao diện mũi, với ngạnh 2 mũi ngắn (bộ NIV, Ginevri, Rome, Italy) có kích cỡ khác nhau theo trọng lượng. Lưu lượng hít vào được phát hiện như một sự thay đổi áp suất trên trở kháng, được đặt gần với giao diện mũi. Các thông số máy thở ban đầu: PEEP từ 4 đến 6 cmH2O; áp lực đỉnh hít vào (PIP) 15 đến 20 cmH2O; thời gian hít vào 0,3 đến 0,4 giây; lưu lượng 6 đến 10 L/phút; Tần số hô hấp (RR) 40 lần/phút với FIO2 điều chỉnh thấp nhất, để duy trì một SaO2 từ 88% đến 93%. Cài đặt hô hấp (PIP tối đa 25 cmH2O, PEEP tối đa 7 cmH2O, RR tối đa 60 lần thở/phút) được điều chỉnh để đảm bảo khí máu trong phạm vi bình thường. Đã chọn độ nhạy cao nhất để kích hoạt tính năng tự động kích hoạt. Việc cai máy từ NSIPPV được thực hiện với việc giảm RR xuống 15 lần/phút với PIP từ 10 đến 15 cmH2O và PEEP là 4 cmH2O và đã ngừng khi trẻ không có dấu hiệu RDS với FIO2 < 0,30.
Tiêu chuẩn Thất bại
NIV thất bại được xác định khi một hoặc nhiều tiêu chuẩn sau tiếp tục tồn tại hoặc tái phát, sau khi dùng surfactant liều tối đa 3 liều hoặc trong vòng 12 giờ kể từ lần dùng trước đó:
(1) thiếu oxy (FIO2 yêu cầu > 0,40),
(2) toan máu (pH < 7.20) và hypercarbia (PCO2 > 65 mm Hg), và
(3) ngưng thở ≥ 4 lần/giờ hoặc cần thông khí qua mặt nạ ≥ 2 lần/giờ. Chúng tôi cũng xem xét viêm ruột hoại tử (NEC), thủng ruột và điều kiện không ổn định huyết động đối với thất bại NIV. [18]
Xử trí Surfactant
Theo quy trình quản lý hô hấp, liều surfactant đầu tiên được dùng là 200 mg/kg (Curosurf, Chiesi, Parma, Ý). Các liều surfactant bổ sung được cho ở liều 100 mg/kg, ít nhất 12 giờ sau khi dùng liều trước đó. Sau khi INSURE, trẻ sơ sinh được nhận cùng thiết bị hỗ trợ NIV như trước đây. Tất cả trẻ sơ sinh được điều trị bằng caffein (caffeine citrate 20 mg/kg, 5 đến 10 mg/kg/ngày).
Thông số giám sát
Trẻ sơ sinh được theo dõi bằng cách sử dụng giám sát SaO2 (Masimo Datascope Radical, Masimo Corporation, Irvine, CA) trước khi điều trị. Đối với mỗi trẻ sơ sinh, các biến sau đây được ghi nhận: GA, BW, giới tính, các bệnh chính của mẹ lúc mang thai, phương thức sinh, và điểm Apgar từ 1 đến 5 phút. Tại thời điểm nhận vào nghiên cứu, FIO2, áp suất đường thở trung bình (MAP), SaO2, pH và PCO2 được ghi lại.
Kết quả chính
Các điểm cuối chính là thời gian hỗ trợ NIV và tỷ lệ thất bại.
Kết quả phụ
Các điểm cuối phụ là thời gian hỗ trợ hô hấp, tần suất tràn khí màng phổi (PNX), xuất hiện BPD trung bình/nặng, tỷ lệ xuất huyết não thất (IVH) nhiều hơn mức độ thứ hai, nhuyễn hóa chất trắng quanh não thất (PVL), cần liều surfactant thứ hai/nhiều lần, cần điều trị bằng glucocorticoid sau sinh, sự tồn tại của ống động mạch (PDA) cần điều trị bằng thuốc, bệnh võng mạc do non tháng (ROP) nhiều hơn mức độ thứ hai, NEC, viêm phổi muộn (LOS), tử vong, và ngày để lấy lại BW. BPD trung bình/nặng được xác định theo phân loại Jobe và Bancalari, [19] IVH được phân loại theo Papile và cộng sự, [20] và ROP được xếp loại theo tiêu chuẩn do Ủy ban Quốc tế về Phân loại ROP. [21]
Phân tích thống kê
Đối với việc tính toán cỡ mẫu, chúng tôi sử dụng thời gian thông khí làm kết quả chính. Vì không có dữ liệu cơ bản cho trẻ có nguy cơ cao nên chúng tôi có thể thu thập được thời lượng thông khí bằng 2 chiến lược NIV khác nhau từ cơ sở dữ liệu của 2 NICUs của chúng tôi. Những dữ liệu này được sử dụng để tính toán power.
Chúng tôi giả định có sự khác biệt 24 giờ giữa 2 nhóm trong thời gian NIV có liên quan đến lâm sàng. Ở mức độ tin cậy a = 0,05 và mức công suất 0,80, chúng tôi cần 62 bệnh nhân cho mỗi nhóm. [22] Kích thước mẫu được tính bằng cách sử dụng nQuery Advisor (Giải pháp Thống kê, Saugus, MA), phiên bản 5.0.
Dữ liệu được báo cáo là trung bình và SD, và trung vị và interquartile ranges cho các biến liên tục, trong khi đó các tần số tuyệt đối và tương đối được sử dụng cho các biến phân loại. Các thông số của 2 nhóm được so sánh bằng cách sử dụng các test Student t hoặc MannWhitney U 2-sided tests cho các biến liên tục và x2 hoặc Fisher kiểm tra chính xác các biến phân loại. P, 0,05 được xem là có ý nghĩa thống kê, và tất cả các giá trị P được dựa trên các bài kiểm tra 2 đuôi. Phân tích thống kê được thực hiện bằng cách sử dụng SPSS cho Windows (SPSS, Chicago, IL).
CÁC KẾT QUẢ
Bảng 1 cho thấy các đặc điểm chu sinh ở các nhóm nghiên cứu. Không có sự khác biệt đáng kể giữa nhóm NSIPPV và nhóm BiPAP đối với WGA, BW, giới tính, tỷ lệ mổ lấy thai, vỡ ối sớm, bằng chứng của bệnh viêm màng ối, tăng huyết áp thai kỳ đòi hỏi phải điều trị thuốc hạ áp, abruptio placentae, tỷ lệ các trường hợp mang nhiều thai, điều trị dự phòng glucocorticoid trước khi sinh, và điểm số Apgar ở phút 1 và 5 phút. Không có sự khác biệt nào được trình bày về phân tích khí máu, FIO2, SaO2, pH, và PCO2 khi thu nhận vào nghiên cứu. Chúng tôi đã quan sát thấy sự khác biệt đáng kể trong MAP ở nhóm NSIPPV cao hơn nhóm BiPAP, tùy thuộc vào cài đặt thông khí ban đầu.

Bảng 2 cho thấy các đặc điểm kết cục chính và phụ. Không có sự khác biệt đáng kể giữa các nhóm về thời gian thông khí hỗ trợ NIV và tỷ lệ thất bại. Hơn nữa, không có sự khác biệt đáng kể về tỷ lệ tử vong sau sinh, BPD trung bình/nặng, PNX, IVH, PVL, dung nạp glucocorticoid sau sinh, liều surfactant nhiều lần, PDA, ROP, NEC, LOS, hoặc thời gian để lấy lại BW. PNX xảy ra trong 6 trường hợp (NSIPPV, n = 2, BiPAP, n = 4) và đại diện cho nguyên nhân thất bại NIV trong 3 trường hợp (NSIPPV, n = 2, BiPAP, n = 1).

Ở 18 trong số 124 trẻ sơ sinh (NSIPPV, n = 10; BiPAP, n = 8), hỗ trợ NIV thất bại. Nguyên nhân là nhiễm khuẩn huyết sớm (NSIPPV, n = 5, BiPAP, n = 3), cao áp phổi (NSIPPV, n = 5, BiPAP, n = 4), thiếu oxy máu và tăng CO2 máu (NSIPPV, n = 2; BiPAP, n = 4), thiếu oxy đơn thuần (NSIPPV, n = 3; BiPAP, n = 3), PDA (NSIPPV, n = 1), NEC (BiPAP, n = 2) và PNX (NSIPPV, n = 2; BiPAP, n = 1). Thời gian thất bại NIV không khác nhau giữa các nhóm nghiên cứu (trung bình 25 đến 75 centile đối với NSIPPV, 36 giờ [17-72], đối với BiPAP, 34 giờ [19 đến 65]) (P > 0,05) (Bảng 3).
Chúng tôi không thấy sự khác biệt có ý nghĩa thống kê về tỷ lệ thất bại giữa 2 nhóm nghiên cứu (P > 0.05 cho tất cả) hoặc giữa các phân nhóm thất bại sau khi phân tầng cho wGA (Bảng 3). Ngoài ra, trẻ sơ sinh thất bại không có sự khác biệt đáng kể về đặc điểm cơ bản từ trẻ sơ sinh không bị thất bại NIV.

THẢO LUẬN
Trong thập kỷ qua, các chiến lược điều trị mới và những tiến bộ kỹ thuật đã thay đổi đáng kể điều trị RDS ở trẻ VLBW. Xử trí tại phòng sinh mới và hỗ trợ NIV sớm góp phần đáng kể vào giảm nhu cầu hỗ trợ thở máy. [23-28] Như vậy, các quan điểm khác của các nhà nghiên cứu sơ sinh liên quan đến việc đánh giá các chiến lược NIV khác nhau về tính sẵn có, hiệu lực và thất bại.
Trong nghiên cứu ngẫu nhiên ở trung tâm 2, chúng tôi thấy không có điểm khác nhau giữa 2 chiến lược NIV khác nhau (NSIPPV và BiPAP) được thực hiện như các phương thức cơ bản để điều trị RDS. Các kết quả phù hợp và cung cấp hỗ trợ bổ sung cho một quan sát không ngẫu nhiên trước đó sử dụng NSIPPV và BiPAP như các phương thức chính trong điều trị RDS. [13] Trong loạt nghiên cứu của chúng tôi, chúng tôi cũng phát hiện thấy tỷ lệ thất bại thấp (18/112 trẻ sơ sinh, 15%) và một thời gian hỗ trợ hô hấp (trung vị cho NSIPPV 89 giờ, đối với BiPAP 87 giờ). Hơn nữa, không có mối tương quan nào giữa tỉ lệ thất bại và các phân nhóm GA.
Sự thất bại trong việc hỗ trợ NIV thấp cũng có thể được giải thích trên cơ sở các phương pháp điều trị chu sinh, như dự phòng bằng glucocorticoid trước sinh (85% đến 90% đối với dân số), được biết là có hiệu quả đối với tình trạng chưa trưởng thành ở phổi và cải tiến trong việc xử trí phòng cấp cứu như SLI và NCPAP sớm. Những quan sát gần đây cho thấy sự cải thiện sau sinh, về phổi và chức năng tim mạch, ở những trẻ sơ sinh và động vật được điều trị bằng SLI. [29,30] Một giải thích khác có thể là sự hỗ trợ NCPAP sớm ở phòng sinh, được biết là có lợi cho kết cục phổi. [2,23-28]
Mặc dù nghiên cứu hiện tại cho thấy cả hai phương pháp NIV (SIPPV và BiPAP) đều có tính khả thi và có thể có hiệu quả tương đương nhưng nó không trả lời câu hỏi liệu NIV có tốt hơn NCPAP như là phương pháp điều trị chính của RDS hay không. Một số tác giả trong nghiên cứu nhỏ (NIPPV hoặc BiPAP so với NCPAP) và một phân tích gộp cho thấy các biện pháp không xâm lấn làm tăng số trẻ không cần thở máy, ít cần đặt nội khí quản trong 72 giờ đầu tiên kể từ khi sinh, và giảm thời gian nằm viện và sự phụ thuộc của O2. [7,10,31-33] Tuy nhiên, Kirpalani et al, trong một thử nghiệm lớn đa trung tâm gần đây, cho thấy không có sự khác biệt đáng kể về tỷ lệ tử vong hoặc sự xuất hiện BPD giữa các chiến lược NCPAP và NIV, sử dụng cả hai như là mục đích đầu tiên hoặc trong giai đoạn cai máy nhưng không có một quy trình cụ thể cho NIV (các thiết bị, đồng bộ hóa) . [11] Cuối cùng, Roberts và cộng sự cho rằng NIPPV (đồng bộ hoặc không đồng bộ) có thể có lợi hơn NCPAP như là sự hỗ trợ chính cho việc giảm đặt nội khí quản, mặc dù không có lợi thế rõ ràng. [12]
Trên cơ sở các phát hiện hiện tại, lưu ý rằng các chiến lược NIV có thể hành động thông qua các phương thức khác nhau, điều tra tiếp theo đánh giá hiệu quả của chúng trong điều trị RDS là hợp lý. [34] Thực sự, NSIPPV sử dụng một phương thức đồng bộ thông thường của thông khí áp lực dương gián đoạn, thông qua mũi, trong khi đó BiPAP sử dụng thông khí không đồng bộ, cung cấp 2 mức CPAP khác nhau thay vì áp suất đường thở không đều, trong đó trẻ sơ sinh có thể hít thở tự nhiên, tạo ra 2 FRC khác nhau. Cả hai phương pháp đều có lợi ích lý thuyết. Đặc biệt,
(1) NSIPPV thông qua tăng áp lực ngắt quãng làm tăng thể tích khí lưu thông (VT), thông khí phút, và MAP, dẫn đến việc huy động phế nang và trao đổi khí tốt hơn [9,12,35];
(2) BiPAP, sử dụng khoảng thời gian áp lực cao dài hơn rất nhiều, cho phép chu kỳ hô hấp hoàn toàn (hít vào và thở ra) ở mức áp lực CPAP cao, tạo ra 2 FRCs khác nhau; tăng MAP; và sự chuyển đổi FRC tạo ra một VT với sự trao đổi khí tốt hơn. [7,36]
Các lợi ích khác của NIV thông thường, do sự thay đổi áp lực, bao gồm kích thích sự thở tự nhiên làm giảm nguy cơ thất bại do ngừng thở. [37]
Một vấn đề khác cần được quan tâm nữa là các cài đặt NIV. Một mặt, một số tác giả nêu bật sự cần thiết của các phác đồ và hướng dẫn nghiêm ngặt [6-38]; Mặt khác, vẫn không có sự nhất trí, vì các kết quả mâu thuẫn đã được báo cáo về cách cài đặt áp lực đường thở không thống nhất, tăng VT và thông khí phút, và giảm công thở. [39-43] Do đó, cần có các nghiên cứu để đánh giá sự truyền áp lực cài đặt vào các đường dẫn khí nhỏ hơn, trong một hệ thống hở với sự rò rỉ lớn và thay đổi, và cải tiến sự đồng bộ NIV với nhịp thở tự nhiên của trẻ sơ sinh. Tuy nhiên, chúng tôi thấy không có sự khác biệt về hiệu quả giữa các chiến lược đồng bộ (NSIPPV) và các chiến lược không đồng bộ (BiPAP).
Dữ liệu về sử dụng surfactant dự phòng/ban đầu có sẵn tại thời điểm thu thập bệnh nhân vẫn còn đang tranh cãi và đang được tranh luận. Vì vậy, ở trẻ sơ sinh ≤ 26 wGA, chúng tôi đã chọn sử dụng surfactant dự phòng (tức là, trong vòng 2 giờ sau khi sinh, sau khi ổn định trên NCPAP) cho nguy cơ cao bị thất bại, [23] trong khi một chiến lược điều trị chọn lọc đã được lên kế hoạch cho những người > 26 wGA. [44] Hiện tại, các phương pháp tiếp cận dự phòng dường như không hợp lý và cần được nghiên cứu thêm để làm rõ tính hiệu quả của NIV sớm với thời gian thích hợp nhất để sử dụng surfactant, đặc biệt ở trẻ sơ sinh có cân nặng rất thấp. [45] Chúng tôi không tìm thấy sự khác biệt giữa các nhóm nhu cầu sử dụng surfactant đơn/nhiều liều.
Trong loạt ca này, chúng tôi không tìm thấy sự khác biệt có ý nghĩa thống kê trong kết cục thứ cấp giữa các thiết bị NIV [2]. Tất nhiên, số trẻ nhỏ đủ điều kiện để phân tích thống kê các kết cục thứ phát không cho phép chúng ta đưa ra kết luận rõ ràng. Về mặt này, chúng tôi quan sát thấy tỷ lệ BPD vừa phải/nặng, tương đương với các nghiên cứu trước đây. [38,46] Tần suất thấp của PNX, NEC, hoặc thủng ruột cho thấy kỹ thuật NIV có thể được xem là an toàn hợp lý cho những trẻ này.
Cuối cùng nhưng không kém phần quan trọng, xử trí NIV thành công đòi hỏi chất lượng chăm sóc sơ sinh cao. Trẻ sơ sinh có nguy cơ cao đòi hỏi các điều dưỡng có kinh nghiệm để làm sạch đường thở trên tốt nhất, vị trí ống thông mũi, và duy trì vị trí thông khí tốt của trẻ sơ sinh. Những biện pháp phòng ngừa này được thực hiện để đảm bảo luồng không khí hiệu quả, duy trì áp lực đầy đủ từ lỗ mũi đến đường thở xa, tăng sự thoải mái của trẻ sơ sinh và ngăn ngừa tổn thương đến lỗ mũi. [47]
KẾT LUẬN
Dữ liệu hiện tại cho thấy cả NSIPPV và BiPAP, được sử dụng như hỗ trợ hô hấp chính trong điều trị RDS của trẻ sơ sinh VLBW, đều khả thi và có hiệu quả tương đương. Những kết quả này nhắc tới các cuộc điều tra RCT tiếp theo để đánh giá hiệu quả của các chiến lược NIV khác nhau đối với các kết cục lâu dài.





