Bài viết Có nên sử dụng máy thở di động trong tất cả các phương tiện vận chuyển trong bệnh viện? được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Should a Portable Ventilator Be Used in All In-Hospital Transports?
Tóm tắt
Vận chuyển của bệnh nhân thở máy có thể do cần làm một thủ thuật thông thường hoặc cấp cứu y tế. Những rủi ro của vận chuyển dường như có thể kiểm soát được, nhưng ký ức về thảm họa liên quan đến hô hấp vẫn khiến nhiều học viên tạm dừng. Tỷ lệ rủi ro/lợi ích của vận chuyển phải được đánh giá trước khi di chuyển. Trong quá trình vận chuyển bệnh nhân thở máy, chúng ta có nên sử dụng máy thở thường xuyên không? Nguy cơ của việc sử dụng thông khí bằng tay là gì? PEEP và FIO2 được thay đổi như thế nào? Có ảnh hưởng đến khả năng kích hoạt trong quá trình thông khí bằng tay không? Tăng thông khí và giảm thông khí có phải là một vấn đề phổ biến? Liệu tăng thông khí hoặc giảm thông khí dẫn đến các biến chứng? Máy thở di động có giá trị chi phí? Còn chức năng của máy thở di động thì sao? Những thiết bị này có thể tái tạo một cách trung thực chức năng của máy thở ICU không? Các cuộc thảo luận thuận và chống sau đây sẽ cố gắng giải quyết nhiều vấn đề này bằng cách xem xét các bằng chứng hiện tại về thông khí vận chuyển.
Giới thiệu
Việc vận chuyển bệnh nhân trong môi trường bệnh viện là một sự kiện phổ biến khiến bệnh nhân gặp rủi ro thường không gặp phải trong điều kiện không di chuyển. Các tác dụng phụ liên quan đến vận chuyển là phổ biến, với tỷ lệ mắc được báo cáo lên tới 68%.[1] Mặc dù hầu hết các tác dụng phụ là nhỏ, các tác dụng phụ nghiêm trọng dẫn đến suy giảm tình trạng sinh lý cần can thiệp điều trị xảy ra, với tỷ lệ mắc được báo cáo là từ 4.2 đến 8,9%.[1, 2] Các khuyến nghị được thiết lập để giảm thiểu khả năng xảy ra các sự kiện bất lợi bao gồm lập kế hoạch cẩn thận trước khi vận chuyển cũng như đảm bảo rằng những điều sau đây có sẵn: một máy theo dõi nhịp tim với chức năng khử rung tim; thiết bị và thuốc hồi sức; cung cấp đủ oxy và pin; một bóng giúp thở bằng tay với mặt nạ; một máy thở vận chuyển; và, quan trọng nhất là nhân viên lành nghề.[3,4]
Ửng hộ: Máy thở di động nên được sử dụng trong tất cả các phương tiện vận chuyển trong bệnh viện
Sử dụng máy thở vận chuyển được coi là thực hành tiêu chuẩn cho bệnh nhân ICU cần hỗ trợ thở máy mức độ cao.[5] Bóng giúp thở bằng tay được sử dụng thường xuyên trong quá trình chuyển từ phòng phẫu thuật hoặc khoa cấp cứu, khi thời gian vận chuyển được dự kiến là ngắn và ở bệnh nhân chỉ cần hỗ trợ thở máy một phần. Điều này chủ yếu dựa trên giả định rằng thông khí bằng tay là an toàn và hiệu quả. Tuy nhiên, do nhận thức của chúng tôi về khả năng bị tổn thương phổi do tiếp xúc với stress và strain quá mức trong quá trình thở tự nhiên và có kiểm soát, 6-9 có mối lo ngại về những nguy cơ tiềm ẩn của thông khí bằng tay. Mặc dù được sử dụng thường xuyên trong môi trường có kiểm soát của ICU trong các thủ thuật như nội soi phế quản và hút, thông khí bằng tay có nhiều rủi ro và ít đặt ra, ngoại trừ trong trường hợp khẩn cấp, trong quá trình vận chuyển bệnh nhân được đặt nội khí quản.
Thông khí bằng tay không an toàn cũng không hiệu quả
Hầu hết các nhân viên hô hấp có thể nói rằng họ cảm thấy tự tin vào khả năng cung cấp thông khí bằng tay an toàn. Rốt cuộc, đó là một yêu cầu kỹ năng cơ bản của đào tạo hồi sức và được thực hiện gần như hàng ngày trong việc chăm sóc bệnh nhân thở máy. Thật không may, người chăm sóc không có khả năng kiểm soát chính xác thể tích khí lưu thông (VT) và áp lực đường thở trong quá trình thông khí bằng tay đã được chứng minh trong một số nghiên cứu, cho thấy kỹ thuật này thực sự không an toàn đến mức tin cậy.
Lee et al[10] đã thực hiện một nghiên cứu đơn giản đánh giá thể tích khí lưu thông được cung cấp bởi 114 cá nhân được đào tạo về hỗ trợ cuộc sống cơ bản bằng cách sử dụng bóng giúp thở bằng tay 1.6 L. Những người tham gia được hướng dẫn cung cấp thì hít vào 1 giây với tần số 10 nhịp thở/phút bằng cách sử dụng bóp bóng bằng một tay, bóp bóng 2 tay và bóp bóng nửa tay. Thể tích được đo bằng máy đo thể tích kết nối với ống nội khí quản người lớn (kích thước không được mô tả). Các đặc tính vật lý của chiều rộng tay, chiều cao và sức mạnh cầm nắm cũng được đo. Kết quả cho thấy thông khí bằng tay dẫn đến sự thay đổi lớn về thể tích khí lưu thông được phân phối (trung bình ± SD): bóp bóng bằng một tay, 592 ± 117 mL; Bóp bóng 2 tay, 644 ± 144 mL; và nửa bóp bóng nửa tay, 458 ± 121 mL. Không có mối tương quan giữa kích thước bàn tay hoặc sức mạnh cầm nắm và thể tích được cung cấp. Các tác giả kết luận rằng những phát hiện của họ hỗ trợ các nghiên cứu trước đây chỉ ra rằng bóng giúp thở bằng tay không phải là thiết bị phù hợp để thông khí chính xác.
Một nghiên cứu gần đây đã được thực hiện bởi Turki et al[11] để xác định áp lực được tạo ra trong quá trình thông khí bằng tay. Một mô hình phổi mô phỏng 4 điều kiện tải khác nhau thể hiện các kịch bản lâm sàng điển hình: sức cản đường thở (15 cm H2O/L/s) và độ giãn nở (0,033 L/cm H2O) bình thường, sức cản đường thở cao (50 cm H2O/L/s) và độ giãn nở bình thường (0,033 L/cm H2O), sức cản đường thở bình thường (15 cm H2O/L/s) và độ độ giãn nở thấp (0,012 L/cm H2O) và sức cản đường thở cao (50 cm H2O/L/s) và độ độ giãn nở thấp (0,012 L/cm H2O). Sử dụng bóng giúp thở bằng tay 1.8 L Hudson dành cho người lớn (Hudson RCI, Temecula, California), 9 nhà trị liệu hô hấp đã mô tả riêng biệt 3 kịch bản lâm sàng và được yêu cầu tự thở máy theo mô hình mà họ không biết về mục đích của nghiên cứu. Mô hình phổi được bao phủ bởi một tấm trải giường, cho phép quan sát vận chuyển, nhưng không thể nhìn thấy áp lực hoặc thể tích của mô hình hoặc thiết bị ghi âm. Kết quả cho thấy sự khác biệt đáng kể giữa các nhà trị liệu hô hấp và giữa các tải trọng khác nhau, với áp lực cao tới 100 cm H2O được tạo ra. Các nhà trị liệu hô hấp nam tạo ra áp lực đỉnh cao hơn (91 ± 20 cm H2O) so với các nhà trị liệu hô hấp nữ (56 ± 18 cm H2O) theo kịch bản độ giãn nở bình thường sức cản đường thở cao. Các tác giả lưu ý rằng mặc dù sức cản đường thở cao có thể hạn chế việc truyền áp lực cao đến phế nang, làm giảm nguy cơ mắc barotrauma trong nhóm này, thể tích khí lưu thông 0,3-0,8 L trong kịch bản độ giãn nở thấp có sức cản đường thở cao sẽ làm cho phế nang chịu áp lực 26-68 cm H2O, cao hơn ngưỡng an toàn hiện tại là 30 cm H2O. Sự khác biệt về tần số và thể tích khí lưu thông không có ý nghĩa giữa các kịch bản, khiến các tác giả kết luận rằng thông khí phút là mục tiêu nhận thức bất kể tải trọng do hậu quả của thông khí bằng tay.
Một nghiên cứu được thực hiện bởi Godoy et al[12] đã kiểm tra ảnh hưởng của tốc độ dòng oxy đến thể tích khí lưu thông và áp lực hít vào. Sử dụng một điều kiện độ giãn nở và sức cản đường thở duy nhất, 7 bóng giúp thở bằng tay đã được thử nghiệm với lưu lượng oxy 1, 5, 10 và 15 L/phút trong khi cùng một người bóp thiết bị bằng 2 tay. Sự khác biệt lớn về thể tích khí lưu thông được giao đã được quan sát giữa các bóng giúp thở. Việc tăng lưu lượng từ 1 đến 15 L/phút dẫn đến thể tích khí lưu thông tăng 99 và 48% và tăng áp lực cực đại 155 và 105% ở 2 thiết bị. Các tác giả cho rằng vị trí của đầu vào oxy, với lưu lượng > 5 L/phút khiến van bệnh nhân bị dính và khí được hướng về phía bệnh nhân trong khi thở ra.
Hai nghiên cứu đã xem xét thể tích và áp lực được tạo ra trong quá trình thông khí sơ sinh. Bassani et al[13] đã kiểm tra ảnh hưởng của kỹ thuật lên thông khí. Một trăm bảy mươi hai nhà cung cấp dịch vụ chăm sóc ICU sơ sinh (bác sĩ y tế, y tá đã đăng ký và vật lý trị liệu) đã được yêu cầu thông khí một bộ phổi thử nghiệm để mô phỏng trẻ sơ sinh nặng 3 kg, độ giãn nở 0,003 L/cm H2O và sức cản 200 cm H2O/L/phút sử dụng 5 kỹ thuật: một tay sử dụng 5, 4, 3 hoặc 2 ngón tay và 2 tay sử dụng 10 ngón theo thứ tự ngẫu nhiên. Một bóng tự phồng (self-inflating bag) 300 ml đã được sử dụng với van giảm áp đặt ở mức 40 cm H2O. Các thông số thông khí có thể chấp nhận là áp lực hít vào tối đa 20-25 cm H2O, thể tích khí lưu thông (VT) là 24-30 mL, và tần số 40-60 lần/phút dựa trên những gì tác giả mô tả là hướng dẫn thông khí sơ sinh tiêu chuẩn. Bất kể chuyên môn hay kỹ thuật, 155 trong số 172 (88%) cung cấp áp lực quá mức (> 25 cm H2O), 127 (74%) cung cấp thể tích quá mức (> 30 mL) và 49% cung cấp tần số không đủ (< 40 nhịp thở/phút). Các tác giả kết luận rằng bất kể kỹ thuật, phạm vi mục tiêu thông khí sử dụng thông khí bằng tay không được thực hiện thường quy.
Một nghiên cứu để xác định liệu can thiệp giáo dục có cải thiện việc cung cấp thể tích khí lưu thông mục tiêu trong điều kiện độ giãn nở thay đổi hay không được thực hiện bởi Bowman et al.[14] Một mô phỏng ASL 5000 (Ingmar Medical, Pittsburgh, Pennsylvania) đã được lập trình để bắt chước một trẻ sơ sinh nặng 3 kg với độ giãn nở ngẫu nhiên khác nhau giữa thấp (0,5 mL/cm H2O), bình thường (1,1 mL/cm H2O) và cao (1,8 mL/cm H2O). Hai mươi bảy chuyên gia sơ sinh được yêu cầu thông khí bằng tay với tần số 40-60 trong khi duy trì VT 12-18 ml (4-6 mL/kg) bằng cách sử dụng bóng với nguồn khí 10 L/phút và một bóng tự phồng 160 ml. Người tham gia được phép thực hành trong khi xem màn hình áp lực và thể tích trên trình giả lập. Các thử nghiệm cơ bản sau đó đã được tiến hành trong đó những người tham gia chỉ được phép xem áp lực hoặc thể tích hiển thị riêng khi có sự thay đổi độ giãn nở. Sau đó, các buổi thực hành giáo dục và hướng dẫn từng bước một đã được tiến hành, sau đó là các thử nghiệm sau can thiệp. Các thử nghiệm đã được thực hiện khoảng 8 tháng sau đó để đánh giá liệu các kỹ năng có được giữ lại hay không. Hiệu suất trên VT mục tiêu được cải thiện so với lúc ban đầu nhưng kém khi sử dụng bóng tự phồng và chỉ hiển thị áp lực, với mức trung bình cơ bản là 6% (95% CI 3-11%) của hơi thở trên mục tiêu đến 21% (95% CI 15−30%) sau can thiệp (P <.01). Sử dụng bóng phồng theo lưu lượng (flow-inflating bag), trên VT mục tiêu đã đạt được 1% (95% CI 1-4%) của nhịp thở lúc ban đầu và được cải thiện thành 7% (95% CI 4-14%) sau can thiệp (P <0,01). Với việc sử dụng máy đo hiển thị thể tích cơ bản, VT trên mục tiêu đã đạt được 84% (95% CI 82-87%) và 81% (95% CI 73- 90%) nhịp thở sau khi được huấn luyện (P = 0,41). Bóng phồng theo lưu lượng vào hơi thở mục tiêu là 68% (95% CI 64-73%) ở mức cơ bản và 73% (95% CI 67-80%) sau can thiệp (P = 0,13). Kiểm tra duy trì cho thấy các kỹ năng đã bị mất không có sự khác biệt giữa các giá trị cơ bản. Các tác giả kết luận rằng đào tạo giáo dục đã làm rất ít để cải thiện khả năng của người hồi sức để phát hiện và điều chỉnh các thay đổi về độ giãn nở phổi và việc bổ sung một máy đo thể tích đã cải thiện hiệu suất.
Bằng chứng tiếp tục tích lũy nhấn mạnh tầm quan trọng của việc giới hạn thể tích khí lưu thông và áp lực đường thở.[15,16] Chiến lược thông khí bảo vệ kết hợp sử dụng thể tích khí lưu thông thấp và hạn chế áp lực đường thở làm giảm nguy cơ tổn thương phổi do thở máy ở tất cả các bệnh nhân được đặt nội khí quản có nguy cơ bị tổn thương và nên được áp dụng như là tiêu chuẩn chăm sóc.[17] Sự cần thiết của vận chuyển bắt buộc phải tuân thủ các chiến lược này, và như đã chứng minh, kiểm soát áp lực và thể tích trong quá trình thông khí bằng tay đơn giản là không thể ngay cả trong các điều kiện được kiểm soát. Quan niệm rằng các nhân viên có kinh nghiệm có thể cung cấp thông khí bằng tay trong quá trình vận chuyển chỉ đơn giản dựa trên huyền thoại nhiều hơn thực tế.
Rủi ro sinh lý liên quan đến thông khí bằng tay
Các hậu quả sinh lý liên quan đến tăng thông khí và giảm thông khí được biết đến.[18] Nhiễm kiềm hô hấp ảnh hưởng đến trương lực mạch máu tim và não. Co thắt tim có thể dẫn đến co thắt động mạch vành, thiếu máu cơ tim, rối loạn nhịp tim và nhịp tim nhanh. Nhiễm kiềm gây ra co thắt mạch máu não, làm giảm lưu lượng máu não xuống 40-50%.[20] Mặc dù được sử dụng trong điều trị bệnh nhân đột quỵ để giảm áp lực nội sọ, nhưng vô tình làm giảm nồng độ CO2 xuống < 25 mm Hg có thể gây ra tetany và dẫn đến tổn thương do thiếu máu cục bộ.[21] Nên tránh nhiễm kiềm ở bệnh nhân có hoặc có nguy cơ bị thiếu máu cục bộ vì nó gây ra sự dịch chuyển trái của đường cong oxyhemoglobin, làm giảm việc cung cấp oxy đến các mô.
Các tác dụng sinh lý của tình trạng thiếu oxy đã được nghiên cứu rộng rãi.[22] Trong quá trình vận chuyển, các tác dụng phụ liên quan đến thiếu oxy có liên quan đến việc dự trữ oxy không đầy đủ, xẹp phổi và kích động bệnh nhân.[4] Không cần phải nói, oxy phải được theo dõi chặt chẽ trong quá trình vận chuyển, và thiết bị phải được theo dõi chặt chẽ được sử dụng có thể cung cấp nồng độ oxy cao và lượng PEEP đầy đủ khi có chỉ định lâm sàng.
Các tác dụng phụ của tăng oxy máu ở trẻ sơ sinh được nhận biết rõ. Tiếp xúc với nồng độ oxy cao cũng đã được chứng minh là bất lợi ở các quần thể bệnh nhân trưởng thành khác nhau.[24,25] Phản ứng tim mạch đối với tăng oxy máu bao gồm: giảm thể tích nhát bóp và cung lượng tim, tăng sức cản mạch máu ngoại biên và co mạch vành động mạch. Độc tính oxy do tiếp xúc với nồng độ oxy cao làm suy yếu chức năng phổi.[24] Giảm vận chuyển của tế bào ông chuyển, viêm, phù phổi và xơ hóa đều được quy cho chứng tăng oxy máu. Có bằng chứng cho thấy stress oxy hóa từ các gốc tự do có thể làm trầm trọng thêm tổn thương phổi ở những bệnh nhân bị suy hô hấp và việc kiểm soát chính xác FIO2 nhắm mục tiêu oxy hóa mô đầy đủ có thể là một chiến lược điều trị tốt hơn so với việc tập trung vào việc đạt được độ bão hòa oxy cao.[27, 28] Tiếp xúc không cần thiết với nồng độ oxy cao là không thể tránh khỏi với các thiết bị hồi sức thủ công, được thiết kế đặc biệt để cung cấp nồng độ oxy gần 100%.
Vận chuyển thực tế của bệnh nhân nghiêm trọng thở máy thường yêu cầu qua một mê cung của hành lang, thang máy và chướng ngại vật. Mặc dù trách nhiệm chính của bác sĩ trị liệu hô hấp đi cùng bệnh nhân là duy trì đường thở và đảm bảo bệnh nhân được thở máy đúng cách, nhưng bác sĩ trị liệu hô hấp cũng hỗ trợ giám sát việc theo dõi các dấu hiệu sinh tồn, nhận biết báo động và khắc phục sự cố thiết bị, đồng thời giúp đỡ để điều khiển một băng ca vận chuyển. Trong môi trường đòi hỏi khắt khe này, việc bóp bóng bóng giúp thở bằng tay một cách hiệu quả trong khi duy trì sự cảnh giác liên tục về thể tích và áp lực được cung cấp là không thực tế, và không có gì đáng ngạc nhiên khi các nghiên cứu về thông khí bằng tay trong quá trình vận chuyển đã cho thấy rằng bệnh nhân trải qua những thay đổi đáng kể về pH và PaCO2, dẫn đến các tác dụng phụ có khả năng đe dọa tính mạng.
Một trong những nghiên cứu sớm nhất về thông khí bằng tay trong quá trình vận chuyển đã được Braman et al[29] thực hiện vào năm 1987. Họ đã đánh giá khí máu ở 20 đối tượng được vận chuyển từ ICU nội khoa bằng cách sử dụng bóp bóng bằng tay. Kết quả cho thấy 14 trong số 20 (70%), bị tăng hoặc giảm thông khí, được định nghĩa là thay đổi PaCO2 > 10 mm Hg và pH > 0,05. PaCO2 dao động từ −18 đến +28 mm Hg và pH dao động từ -0,17 đến +0,18. Sáu đối tượng bị hạ huyết áp và rối loạn nhịp tim. Đánh giá khí máu động mạch (ABGs) trong nhóm 16 đối tượng tiếp theo được vận chuyển bằng máy thở tại nhà được điều chỉnh để vận chuyển, không tìm thấy sự thay đổi đáng kể nào trong PaCO2.
Gervais et al[30] đã so sánh ABG của 30 đối tượng trong quá trình vận chuyển. Các đối tượng được chia thành 3 nhóm và được thông khí bằng tay có hoặc không có máy đo thể tích để theo dõi thể tích thở ra hoặc bằng máy thở vận chuyển được đặt trong cùng một thông khí phút như được sử dụng trong ICU. Khí máu được rút ra trước khi vận chuyển trong khi trên máy thở chăm sóc tích cực và sau khi hoàn thành. Nó đã được tiết lộ rằng thông khí bằng tay mà không theo dõi dẫn đến giảm đáng kể PaCO2, từ 41 ± 2 đến 34 ± 2 mm Hg (P <0,05) và tăng pH tương ứng so với đường cơ sở. Kết luận của họ là các biến số khí máu đầy đủ có thể đạt được trong quá trình vận chuyển, với điều kiện thông khí phút được kiểm soát và việc bổ sung một máy đo thể tích để theo dõi thể tích khí lưu thông được khuyến nghị trong quá trình thông khí bằng tay.
Hurst et al[31] đã chọn ngẫu nhiên 28 đối tượng để nhận thông khí bằng tay được cung cấp bởi một nhà trị liệu hô hấp lành nghề hoặc thông qua máy thở vận chuyển với các thiết lập phù hợp với máy thở được sử dụng trong khoa cấp cứu. Các đối tượng được thông khí bằng một phương pháp đến đích nơi làm thủ thuật cho họ và chuyển qua phương pháp khác khi họ trở về. Nhịp tim cơ bản, huyết áp và giá trị ABG thu được ở khoa cấp cứu được so sánh với các giá trị được thực hiện khi đến đích ban đầu và khi trở về khoa cấp cứu hoặc vị trí cuối cùng. Nhịp tim, huyết áp và oxy hóa ổn định trong suốt quá trình vận chuyển, bất kể phương pháp thông khí. Trong quá trình thông khí bằng tay, sự thông khí làm tăng độ pH đáng kể, từ 7,39 ± 0,03 đến 7,51 ± 0,2 và giảm PaCO2 từ 39 ± 4 đến 30 ± 3 mm Hg (P <0,05). Hai đối tượng trong nhóm này đã trải qua nhịp tim nhanh trên thất, mà các tác giả lưu ý có thể được thúc đẩy bởi nhiễm kiềm hô hấp. Điều thú vị là thời gian vận chuyển trung bình chỉ 9 ± 3 phút, cho thấy thực tế là sự tăng thông khí có thể xảy ra ngay cả trong thời gian vận chuyển tương đối ngắn. Các tác giả kết luận rằng việc sử dụng máy thở vận chuyển được ưu tiên hơn là thông khí bằng tay trong quá trình vận chuyển.
Việc sử dụng capnography đã được khuyến nghị cho bệnh nhân đặt nội khí quản trong quá trình vận chuyển.[32] Việc sử dụng nó trong khi thông khí bằng tay trong quá trình vận chuyển cũng đã được chứng minh là giúp kiểm soát thông khí chặt chẽ hơn [33]; tuy nhiên, nó không bảo vệ chống lại và, trong trường hợp trị số CO2 ở cuối thì thở ra (end-tidal) cao, thực sự có thể khiến nhân viên bóp bóng vượt quá ngưỡng an toàn.[13] Như đã mô tả trước đây, luôn luôn dán mắt vào máy theo dõi trong khi đang vận chuyển một bệnh nhân đơn giản là không thực tế. Máy thở vận chuyển cho phép kiểm soát chặt chẽ các thông số thông khí, và khả năng giám sát và báo động tiên tiến của chúng cung cấp phương tiện duy nhất để thực sự hoàn thành mục tiêu chính là bảo vệ bệnh nhân.
Thở tự nhiên trong quá trình vận chuyển
Như đã mô tả trước đây, không phải tất cả bệnh nhân cần vận chuyển đều cần hỗ trợ thở máy. Việc sử dụng thuốc an thần nặng cho mục đích duy nhất là tạo thuận lợi cho việc vận chuyển có ý nghĩa rất nhỏ và khiến bệnh nhân gặp phải những rủi ro bổ sung liên quan đến ngưng thở. Do kiểu thở của bệnh nhân có thể thay đổi đáng kể, thiết bị được sử dụng phải có khả năng cung cấp sự hỗ trợ và nồng độ oxy phù hợp trong nhiều điều kiện khác nhau. Đặc biệt quan trọng là khả năng của thiết bị cho phép dễ dàng bắt đầu lưu lượng khí và thở ra mà không có sức cản quá mức, bởi vì sự không đồng bộ trong cả hai trường hợp làm tăng công thở.[34,35]
Một nghiên cứu ban đầu của Hess et al[36] đã đánh giá công hít vào và thở ra và cung cấp oxy của 11 bóng giúp thở bằng tay. Một phổi thử nghiệm 2 buồng được điều khiển bởi một máy thở cơ học cung cấp các mẫu thông khí thấp, trung bình và cao. Tín hiệu áp lực, lưu lượng và thể tích được ghi lại và tích hợp điện tử để tính toán công thở theo J/L. Lưu lượng oxy 15 L/phút được kết nối với mỗi bóng giúp thở trong khi máy phân tích oxy đo FIO2 tại kết nối bệnh nhân. Mặc dù chi tiết chính xác nằm ngoài phạm vi của cuộc thảo luận này, các phát hiện cho thấy rằng tất cả các bóng giúp thở gây ra sự gia tăng trong công thở áp đặt trong cả hít vào và thở ra. Khi mức độ thông khí tăng lên, công thở tăng đáng kể (P <0,01) lên tới 0,965 ± 0,097 J/L. Có một sự khác biệt đáng kể giữa công hít vào và thở ra (P <.01), được khuếch đại ở mức độ thông khí cao hơn. Hai trong số các bóng giúp thở được thử nghiệm có van PEEP tích hợp. Việc bổ sung 10 cm H2O PEEP dẫn đến sự gia tăng hơn nữa trong công thở thì hít vào của hơi thở > 1 J/L trong cả hai thiết bị. Điều này là do thực tế là, không giống như máy thở vận chuyển được bù PEEP, lưu lượng hít vào được duy trì thông qua bóng giúp thở bằng tay chỉ bởi bệnh nhân tạo ra độ dốc áp lực âm lớn hơn mức van PEEP. Ngoài ra, chỉ có 7 trong số 11 thiết bị có thể cung cấp FIO2> 0,85 trong các điều kiện thử nghiệm. Các tác giả lưu ý rằng công thở được tạo ra bởi bóng giúp thở bằng tay lớn gấp 10 lần 100 lần so với báo cáo trên máy thở ICU và kết luận bằng cách khuyến cáo không nên sử dụng bóng giúp thở bằng tay trong quá trình thở tự nhiên.
Mặc dù những cải tiến trong các mô hình khác nhau của bóng giúp thở bằng tay đã làm giảm bớt một số thất bại được tìm thấy trong các thiết bị trước đó,[37] nhưng nghiên cứu tiếp tục cho thấy những hạn chế của bóng giúp thở bằng tay.[37,38] Duy trì sự hỗ trợ nhất quán và FIO2 ổn định trong quá trình thở tự nhiên là không thể với bóng giúp thở bằng tay, được thiết kế để cho phép không khí trong phòng không được vào dù bệnh nhân có nhu cầu hô hấp cao và chỉ dựa vào khả năng của người vận hành để đồng bộ hóa việc bóp bóng thủ công với các nỗ lực tự phát của bệnh nhân khi được hỗ trợ một phần. Việc sử dụng chúng trong quá trình thở tự nhiên đã được chứng minh là không hiệu quả và dẫn đến hậu quả sinh lý tiêu cực. [38,39]
Máy thở vận chuyển
Sự phát triển của máy thở vận chuyển ra đời từ việc nhận ra rằng thông khí bằng tay đơn giản là không đủ trong nhiều trường hợp. Các máy thở vận chuyển đầu tiên là máy thở ICU cồng kềnh hoặc máy thở tại nhà không thể thích nghi cho nhiệm vụ và phải bắt vít vào xe vận chuyển. Máy thở sớm được thiết kế đặc biệt để vận chuyển, mặc dù nhỏ hơn so với các đối tác ICU của họ, lại bị thiếu sót nghiêm trọng. Bộ phân trộn khí của thiết bị đã tiêu thụ một lượng oxy đáng kể ngay cả khi không sử dụng. Các thiết bị điện tử bị cản trở bởi trọng lượng và tuổi thọ hạn chế của pin có sẵn tại thời điểm đó. Khi xem xét các sản phẩm về vận chuyển nội viện, Fanara et al4 đã xác định máy thở di động chiếm 22% các tác dụng phụ do các yếu tố thiết bị gây ra. Tuổi thọ pin, hết oxy, ngắt kết nối do vô ý và nhân viên không được đào tạo đúng cách với hoạt động của máy thở được trích dẫn là nguyên nhân gốc rễ. May mắn thay, những cải tiến trong công nghệ đã giảm bớt nhiều vấn đề này. Các máy thở vận chuyển hiện đại ngày nay cung cấp nhiều tính năng tương tự được tìm thấy trên các máy ICU, bao gồm điều khiển FIO2, nhiều chế độ và khả năng giám sát và báo động tiên tiến. Việc lựa chọn máy thở vận chuyển phải dựa trên các yêu cầu thông khí dự kiến phù hợp với khả năng của máy thở.
Có hàng chục thiết bị được bán trên thị trường như máy thở vận chuyển. Chúng bao gồm từ loại bóng giúp thở tự động điều khiển bằng khí đơn giản cung cấp oxy 100% và ít kiểm soát về tần số và thể tích khí lưu thông và van giảm áp, cho đến loại máy thở vận chuyển tinh vi với nhiều chế độ và khả năng giám sát và báo động tiên tiến. Đối với vận chuyển trong bệnh viện, Hướng dẫn thực hành lâm sàng chăm sóc hô hấp của Hiệp hội Hoa Kỳ năm 2002 khuyến cáo rằng máy thở vận chuyển phải có đủ năng lượng trong suốt thời gian vận chuyển, kiểm soát độc lập tần số và thể tích khí lưu thông, khả năng hỗ trợ đầy đủ, cung cấp thể tích không đổi trong bệnh cảnh của thay đổi trở kháng phổi, cung cấp báo động ngắt kết nối và có khả năng cung cấp PEEP và FIO2 là 1.0. Nhiều máy thở vận chuyển thế hệ mới hơn vượt qua các khuyến nghị này và cạnh tranh với hiệu suất của các đối tác ICU của họ.
Hai nghiên cứu đã xem xét hiệu suất của máy thở vận chuyển thế hệ mới. Blakeman và Branson[40] đã tiến hành đánh giá kỹ lưỡng 4 máy thở vận chuyển thế hệ mới nhất. Họ đã đánh giá độ chính xác của VT, các đặc điểm kích hoạt, thời lượng pin, mức tiêu thụ khí và độ ổn định của FIO2 trong các điều kiện khác nhau về sức cản đường thở, độ giãn nở, VT và tần số. Họ phát hiện ra rằng tất cả các máy thở đều nằm trong tiêu chuẩn của Hiệp hội Thử nghiệm và Vật liệu Hoa Kỳ là ± 10% với mục tiêu thể tích khí lưu thông là 400 mL, nhưng 3 trong số 4 máy thở nằm ngoài phạm vi chấp nhận được là 10% ở mức 50 mL với phạm vi 55,7 ± 1,4 đến 58,2 ± 1,2 mL. Áp lực kích hoạt (PImax) thay đổi từ 0,32-1,72 cm H2O với cài đặt độ dốc từ nhanh nhất 0,34-3,29 cm H2O đến chậm nhất. Tiêu thụ khí sử dụng thông khí phút 10 L/phút thay đổi từ 9,2 đến 16 L/phút. Tiêu thụ khí cao hơn được quy cho lưu lượng lệch trong quá trình kích hoạt lưu lượng. Tất cả các máy thở đều cung cấp nồng độ FIO2 ổn định trong các điều kiện khác nhau, mặc dù người ta không thể đạt được ngưỡng ± 5% ở cài đặt FIO2 cao hơn với FIO2 tối đa đạt được là 0,919. Thử nghiệm cho thấy cần phải cải thiện khả năng cung cấp thể tích khí lưu thông nhỏ hơn một cách chính xác; tuy nhiên, tất cả các máy thở đều hoạt động tốt trong các yêu cầu đã được thiết lập cho vận chuyển người lớn.
Boussen et al [41] đã đánh giá 3 máy thở chạy bằng khí và 5 máy thở chạy bằng tua-bin trong điều kiện thở mô phỏng thụ động và tự phát. Máy thở đã được thử nghiệm bằng cách sử dụng các chế độ hỗ trợ áp lực và nhắm mục tiêu theo thể tích. Hỗ trợ áp lực là 5 và 10 cm H2O có và không có PEEP 5 cm H2O đã được thử nghiệm trong điều kiện mức hoạt động trung khu hô hấp cao và thấp. Các mô hình điều khiển bằng tuabin vượt trội hơn các máy thở chạy bằng khí về độ chính xác về thể tích khí lưu thông, đặc điểm kích hoạt và hiệu suất điều áp. So với các nghiên cứu khác, các tác giả đã tìm thấy sự cải thiện đáng kể về độ chính xác VT so với máy thở vận chuyển cũ. Máy thở vận chuyển điều khiển bằng tuabin thể hiện hiệu suất tương đương với máy thở ICU ở chế độ hỗ trợ áp lực.
Chụp cộng hưởng từ (MRI) đặt ra một thách thức duy nhất về thông khí cơ học. Bất kỳ thiết bị nào chứa kim loại đều có thể trở thành một viên đạn bay nếu được đặt quá gần thiết bị chụp MRI. Để duy trì khoảng cách an toàn, bộ dây máy thở nối dài được sử dụng thường xuyên trên máy thở, thêm vào việc làm tăng thêm thể tích nén và làm giảm độ nhạy kích hoạt. Rất ít máy thở vận chuyển là an toàn với MRI, và những cái có sẵn trong quá khứ đã được cung cấp năng lượng bằng khí bóp bóng, với khả năng và báo động hạn chế. Chikata et al[42] gần đây đã so sánh hiệu suất của máy thở di động an toàn MRI cũ với máy thở ICU. Không ai trong số các máy thở MRI được thử nghiệm cung cấp thể tích khí lưu thông trong giới hạn Vật liệu và Thử nghiệm của Hiệp hội Hoa Kỳ là ± 10% trong mọi điều kiện. Ở bối cảnh FIO2 là 1.0, các thay đổi FIO2 được phân phối là tối thiểu, nhưng nó thay đổi đáng kể ở mức FIO2 là 0,60 (hỗn hợp không khí). Van giảm áp lực đỉnh hoạt động phù hợp trong tất cả các mô hình, nhưng PEEP sai lệch đáng kể so với giá trị đặt và giữa các mô hình. Mặc dù máy thở MRI thế hệ cũ được trang bị báo động áp lực âm thanh, cung cấp một số mức độ giám sát an toàn, các dấu hiệu sinh tồn cũng cần được theo dõi liên tục. Các máy thở di động MRI mới nhất xuất hiện trên thị trường đòi hỏi sự cải thiện hiệu suất đáng kể về độ chính xác so với các nghiên cứu của Chikata et al,[42] với các tính năng bổ sung như máy đo tốc độ tích hợp, khả năng giám sát vượt trội và chế độ tiên tiến.
Mặc dù chi phí của máy thở vận chuyển hiện đại lớn hơn đáng kể so với bóng giúp thở bằng tay, nhưng sự khác biệt phải được cân nhắc với các chi phí bổ sung liên quan đến thông khí gây tổn thương và tăng oxy máu có thể xảy ra trong quá trình thông khí bằng tay. Thể tích khí lưu thông không phù hợp đã được xác định là một yếu tố nguy cơ độc lập góp phần làm tăng tỷ lệ tử vong và thời gian nằm viện,[16,43] và tăng oxy máu, trong thời gian ngắn, đã được chứng minh là làm xấu đi kết quả và tăng tỷ lệ tử vong ở các bệnh nhân chọn lọc. Gắn trực tiếp với kết quả của bệnh nhân, giảm thiểu rủi ro trong khi cải thiện sự an toàn của bệnh nhân là một điều cần thiết về tài chính. Chi phí trung bình hàng ngày của một bệnh nhân thở máy được ước tính là 4.000 đô la,[44] và số bệnh nhân cần thở máy kéo dài dự kiến sẽ vượt quá 600.000 vào năm 2020.[45] Rõ ràng, việc tăng thông khí cơ học có nghĩa là nhiều bệnh nhân sẽ phải vận chuyển. Mặc dù thiếu bằng chứng, người ta có thể thấy trước rằng việc loại bỏ tiếp xúc không cần thiết với các tác động gây tổn thương liên quan đến thông khí bằng tay có thể giúp tiết kiệm đủ để bù đắp chi phí cho máy thở vận chuyển.
Tóm tắt về ủng hộ thở máy vận chuyển
Máy thở vận chuyển hiện đại vượt trội hơn so với thông khí bằng tay ở khả năng giảm thiểu nguy cơ tổn thương phổi do máy thở trong khi duy trì mục tiêu thông khí thông qua việc kiểm soát và theo dõi liên tục lượng khí lưu thông và áp lực đường thở. Kiểm soát chính xác nồng độ oxy trong quá trình thở tự nhiên và có kiểm soát làm giảm nguy cơ tăng oxy máu hoặc thiếu oxy. Những cải tiến đáng kể về tuổi thọ pin và khả năng trao đổi pin nóng trong khi hoạt động hầu như loại bỏ các mối lo ngại về năng lượng, và khả năng giám sát và báo động tiên tiến được tìm thấy trong các máy thở vận chuyển ngày nay đã loại bỏ những thiếu sót của các mẫu trước đó. Không có gì ngạc nhiên khi việc sử dụng của họ đã được xác nhận bởi nhiều tổ chức chuyên nghiệp và nên được coi là tiêu chuẩn chăm sóc cho tất cả các vận chuyển trong bệnh viện. Đã đến lúc từ bỏ thói quen thông khí cổ xưa và không an toàn.
Chống: Không nên sử dụng máy thở di động trong tất cả các phương tiện vận chuyển trong bệnh viện
Vận chuyển nội viện của bệnh nhân nguy kịch là một phần khó khăn nhưng cần thiết trong quản lý bệnh nhân. Nó có thể nguy hiểm do sự mất ổn định sinh lý của bệnh nhân cũng như vượt qua các rào cản hậu cần. Về mặt logic, nguy cơ của các sự kiện bất lợi có thể xuất phát từ việc đào tạo không đầy đủ, các bác sĩ lâm sàng không thể làm việc theo nhóm và bảo trì và trục trặc thiết bị. Một khía cạnh cực kỳ quan trọng của vận chuyển bệnh nhân nội viện là thông khí đầy đủ trong quá trình chuyển. Cho đến khoảng 15 năm trước hoặc lâu hơn, điều này đã được thực hiện bằng cách thông khí bằng tay được thực hiện bởi một nhà trị liệu hô hấp, y tá hoặc bác sĩ. Điều này đã được thực hiện thông qua việc sử dụng bóp bóng bằng tay trong đó các thông số thông khí được xác định bởi bác sĩ lâm sàng. Gần đây, máy thở di động đã được giới thiệu với mục đích cung cấp thông khí bệnh nhân phù hợp hơn trong quá trình vận chuyển cũng như giải phóng bác sĩ lâm sàng để giúp đỡ các khía cạnh khác của việc vận chuyển. Ngày nay, máy thở di động được sử dụng cho hầu hết các phương tiện vận chuyển nội viện. Câu hỏi được trả lời là liệu thông khí bệnh nhân trong tất cả các vận chuyển nội viện có nên được thực hiện với máy thở di động hay không. Mặc dù thông khí bằng tay được sử dụng phổ biến trong các nỗ lực hồi sức và đáp ứng nhanh, thông khí bằng tay vẫn có chỗ trong quá trình vận chuyển bệnh nhân.
Máy thở di động
Sự ra đời của máy thở di động là một tiến bộ công nghệ lớn, nhưng để thực sự hiệu quả, chúng phải đủ tin cậy để cung cấp các thông số thông khí phù hợp khi đối mặt với sự thay đổi của cơ học phổi. Sự chấp thuận của Cục quản lý dược phẩm và thực phẩm Hoa Kỳ vào năm 2001 đã dẫn đến phạm vi sử dụng ngày càng tăng trong quá trình vận chuyển, đặc biệt là khi chúng trở nên tinh vi hơn. Theo hướng dẫn của Hiệp hội Chăm sóc Hô hấp Hoa Kỳ, nếu sử dụng máy thở vận chuyển, nó cần có đủ nguồn điện dự trữ trong suốt thời gian vận chuyển, kiểm soát độc lập thể tích khí lưu thông và tần số hô hấp, có thể hỗ trợ thở máy đầy đủ như trong phương thức hỗ trợ-kiểm soát hoặc thông khí bắt buộc ngắt quãng (không nhất thiết là cả hai), cung cấp một thể tích không đổi khi đối mặt với trở kháng phổi, theo dõi áp lực đường thở, cung cấp báo động ngắt kết nối, có khả năng cung cấp PEEP và cung cấp FIO2 là 100%.3 Tầm quan trọng mà mỗi tổ chức thực hiện phân tích máy thở vận chuyển trước khi mua để đảm bảo rằng trên thực tế, nó có thể đáp ứng các hướng dẫn này.
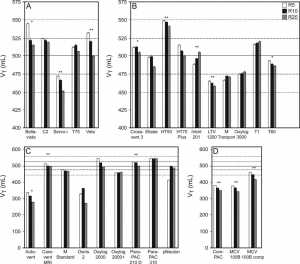
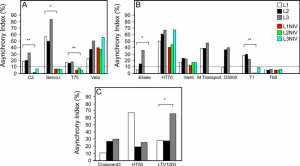
Tuy nhiên, chúng ta cần cẩn thận khi đưa ra giả định rằng tất cả các máy thở vận chuyển đều được tạo ra như nhau. Máy thở vận chuyển được quảng cáo là hiệu quả và phù hợp hơn cho thông khí bệnh nhân trong quá trình vận chuyển. Tuy nhiên, điều quan trọng là chỉ ra rằng sự khác biệt đáng kể vẫn có thể tồn tại giữa các loại máy thở di động khác nhau. Trong một nghiên cứu của Zanetta et al,[46] chức năng của 5 máy thở di động khác nhau và 3 máy thở loại ICU được sử dụng để vận chuyển đã được kiểm tra. Các nhà điều tra đã tạo ra 3 kịch bản cơ học phổi khác nhau với một phổi thử nghiệm: bình thường, ARDS và bệnh tắc nghẽn. Họ phát hiện ra rằng việc cung cấp VT, kháng lực đường thở với thở ra và độ nhạy kích hoạt khác nhau đáng kể giữa các máy thở khác nhau.[46] Điều này đặc biệt đúng với máy thở di động. Có sự khác biệt giữa 3 máy thở loại ICU, nhưng không cùng mức.46 Chipman et al[47] đã đánh giá 15 máy thở vận chuyển (với cơ học phổi khác nhau) và ở cừu nặng khoảng 30 kg với phổi bình thường và sau đó lại bị tổn thương ở phổi. Họ phát hiện ra rằng tất cả các máy thở đều có thể thông khí phổi khỏe mạnh.[47] Tuy nhiên, VT thay đổi đáng kể khi giảm độ giãn nở và/hoặc tăng sức cản đường thở đến mức các tác giả kết luận rằng chỉ có 4 loại có thể thông khí phổi bị tổn thương do rửa nước muối (gây giảm độ giãn nở).[47] Ngoài ra, phần lớn các máy thở không thể thông khí bằng pin một mình, và giống như mức VT, thời lượng pin và mức tiêu thụ oxy thay đổi đáng kể giữa các thiết bị.[47] Các tác giả kết luận rằng chỉ có 2 trong số 15 máy thở vận chuyển sẽ hoạt động phù hợp khi vận chuyển bệnh nhân có yêu cầu thông khí cao.[47] Trong một nghiên cứu gần đây hơn về 8 máy thở vận chuyển, Boussen et al[41] đã đánh giá khả năng cung cấp VT trong điều kiện bình thường, điều kiện ARDS và điều kiện tắc nghẽn. Nhóm cũng đánh giá hiệu suất của hệ thống kích hoạt và chất lượng tăng áp lực. Họ thấy rằng có sự khác biệt đáng kể trong cung cấp VT. Phạm vi lỗi là −5 đến 53%.[41] Họ cũng nhận thấy rằng các máy thở vận chuyển dựa trên tuabin đạt được độ phân phối và độ nhạy kích hoạt khí lưu thông tốt hơn so với máy thở điều hòa khí (pneumatic).[41] Blakeman và Branson[40] đã kiểm tra hiệu suất của 4 máy thở vận chuyển thường được sử dụng và thấy rằng có sự khác biệt đáng kể về hiệu suất trong một phạm vi hoạt động rộng, bao gồm độ nhạy kích hoạt, thời lượng pin, độ ổn định FIO2, mức tiêu thụ khí và độ chính xác VT. Sự gia tăng thời gian áp lực cũng khác nhau rất nhiều. Các thiết bị có thời gian tăng nhanh nhất có áp lực vượt mức lớn nhất.[40] Về mặt lâm sàng, điều này có thể quan trọng vì cài đặt độ dốc nhanh có thể gây ra lưu lượng rối trong mạch, có khả năng quá áp ở bệnh nhân. Đặt độ dốc quá chậm có thể dẫn đến độ trễ trong việc đạt áp lực cài đặt hoặc khả năng áp lực cài đặt có thể không đạt được. Điều này sẽ dẫn đến tình trạng đói khí hoặc không đồng bộ lưu lượng với sự gia tăng quá mức trong công hô hấp. Có lẽ nghiên cứu lớn nhất cho đến nay được thực hiện bởi L’Her et al.[48] Nhóm này đã đánh giá 26 máy thở vận chuyển và cấp cứu khác nhau được nhóm thành 4 loại khác nhau tùy theo độ tinh vi: (1) giống như ICU, (2) tinh vi, (3) ) đơn giản, và (4) cấp cứu thảm họa. Họ đã kiểm tra việc cung cấp VT với các cơ chế hô hấp khác nhau và chỉ số không đồng bộ, trong số những thứ khác. Mặc dù các giá trị VT của ICU và máy thở tinh vi nằm trong phạm vi chính xác 10%, vẫn sẽ có sự khác biệt đáng kể giữa các thiết bị trong mỗi loại.[48] Chúng cũng bị ảnh hưởng ở một mức độ nhất định khi thay đổi cơ chế hô hấp (Hình 1).[48] Nhóm cũng đã kiểm tra sự hiện diện của đồng bộ máy thở của bệnh nhân khi có rò rỉ (không phổ biến trong quá trình vận chuyển) và thấy rằng hầu hết các máy thở đều có chỉ số không đồng bộ > 10%.(Hình 2).[48] Chỉ số không đồng bộ được định nghĩa là số nhịp thở không đồng bộ/tổng số nhịp thở và ngưỡng 10% cho biết bệnh nhân có được coi là đồng bộ với máy thở hay không. Một số máy thở tinh vi thậm chí còn vượt trội hơn máy thở giống ICU trong nghiên cứu này. Lưu ý là sự không đồng bộ máy thở của bệnh nhân có khả năng xảy ra ở 3 giai đoạn khác nhau trong khi thì hít vào: (1) Sự khởi đầu của nhịp thở (kích hoạt tự động hoặc kích hoạt không hiệu quả), (2) không đồng bộ lưu lượng (đói lưu lượng hoặc lưu lượng quá nhanh dẫn đến kích hoạt kép) và 3) không đồng bộ theo chu kỳ (nhịp thở kết thúc quá sớm hoặc quá muộn cho bệnh nhân). Hậu quả của sự không đồng bộ máy thở – bệnh nhân có thể là sự gia tăng công hô hấp do bệnh nhân chống máy thở và thuốc an thần quá mức. Ngay cả trong bối cảnh ICU với máy thở tinh vi nhất, người ta đã ước tính rằng sự không đồng bộ của máy thở bệnh nhân là khoảng 24%.[49]
Chức năng và thời lượng pin cũng là những yếu tố cực kỳ quan trọng để có hiệu suất tối ưu của máy thở di động. Vận chuyển nội viện có thể đưa bệnh nhân vào môi trường không có điện ngay lập tức. Không có hướng dẫn ngành công nghiệp cho thời lượng pin. Hướng dẫn của Hiệp hội Chăm sóc Hô hấp Hoa Kỳ khuyến nghị thời lượng pin tối thiểu của máy thở di động là 4 giờ trên danh nghĩa.[3] Tuy nhiên, có một số yếu tố có thể ảnh hưởng đến thời lượng pin. Chúng bao gồm cài đặt máy thở (cài đặt cao hơn sẽ rút ngắn thời lượng pin), loại và kích cỡ pin, và đặc điểm hoạt động của máy thở và hệ thống truyền động. Như đã chỉ ra trước đó, có sự khác biệt đáng kể về thời lượng pin giữa các máy thở vận chuyển khác nhau.[40,47] Một nghiên cứu trước đó của Blakeman et al[50] cho thấy VT giảm trong một số máy thở di động được nghiên cứu về cuối thời lượng pin.
Trên lâm sàng, điều này có thể góp phần gây tăng CO2 máu và nhiễm toan hô hấp. Tiêu thụ khí là một cân nhắc quan trọng khác với việc sử dụng máy thở di động. Đặc điểm hoạt động của các cài đặt máy thở và vấn đề xác định mức sử dụng oxy và tính toán thời gian một bình khí oxy sẽ kéo dài bao lâu. Ví dụ, thể tích khí lưu thông lớn hơn và tần số thở cao hơn sẽ dẫn đến tiêu thụ khí nhiều hơn, trong khi đó thể tích khí lưu thông nhỏ hơn và tần số thở thấp hơn dẫn đến tiêu thụ khí ít hơn. Các đặc tính hoạt động khác ảnh hưởng đến tiêu thụ khí là lưu lượng lệch. Các nhà sản xuất sử dụng dòng khí liên tục này thông qua hệ thống dây máy thở để tạo điều kiện kích hoạt và ổn định PEEP, nhưng nó dẫn đến việc tăng mức tiêu thụ khí từ bình.
Sự kiện bất lợi với máy thở di động
Mặc dù không nhất thiết phải xảy ra phổ biến, sự cố máy thở có thể và có thể xảy ra. Một nghiên cứu của Beckmann và cộng sự đã kiểm tra tỷ lệ trục trặc thiết bị từ một báo cáo về các sự cố được gửi đến Nghiên cứu theo dõi sự cố của Úc trong Chăm sóc chuyên sâu trong thời gian 6 năm. Họ đã tìm thấy tổng cộng 75 sự cố liên quan đến thiết bị, trong đó có 4 sự cố là sự cố máy thở vận chuyển.[51] Các quan sát khác được thực hiện trong nghiên cứu này liên quan đến các yếu tố rủi ro tiềm ẩn bao gồm đào tạo không đầy đủ, bảo trì kém, không có thiết bị, thiếu kinh nghiệm và vội vàng.[51]
Trong một nghiên cứu khác, Papson et al[1] đã xem xét các sự kiện bất ngờ trong quá trình vận chuyển. Trong số 277 sự kiện bất ngờ liên quan đến thiết bị trong 339 lần vận chuyển, có 11 sự cố máy thở và 18 vụ rò rỉ máy thở.[1] Cũng như bất kỳ thiết bị điện tử nào, các bác sĩ lâm sàng phải biết rằng có thể xảy ra sự cố. Họ cũng phải nhận thức được bất kỳ lịch sử trục trặc nào với loại máy thở vận chuyển đang được sử dụng trong tổ chức của họ.
Chụp cộng hưởng từ
Trong khi chụp MRI, có một số vấn đề với máy thở thông thường do các thành phần sắt từ của chúng. Chúng bao gồm tăng nguy cơ các sự kiện phóng từ, suy giảm chất lượng hình ảnh và hiệu suất của máy thở bị tổn hại. Để tương thích MRI, máy thở phải có các thành phần sắt từ thay thế bằng các thành phần không sắt từ. Do đó, có thể nhận thấy rằng các máy thở tương thích MRI có thể có nhiều thay đổi hơn trong các thông số thông khí. Chikata et al[42] đã đánh giá 4 máy thở tương thích MRI trong điều khiển hỗ trợ thể tích với 3 cài đặt VT khác nhau. Họ đã tìm thấy sự khác biệt có ý nghĩa thống kê về thể tích khí lưu thông và PEEP. Phạm vi lỗi VT là 28,1-25,5% và phạm vi lỗi PEEP là −29,2 đến 42,5%. Do sự khác biệt lớn về chức năng của máy thở, các tác giả kết luận rằng bệnh nhân trải qua MRI khi thở máy cần phải được theo dõi chặt chẽ cả từ quan điểm hô hấp và huyết động.
Sự kiện bất lợi với thông khí bằng tay
Đã có báo cáo rằng thông khí bằng tay trong quá trình vận chuyển có khả năng gây ra một số vấn đề, cụ thể là áp lực đường thở kiểm soát và thể tích khí lưu thông không ổn định [29- 31,39] Tuy nhiên, nếu chúng ta kiểm tra bằng chứng chặt chẽ hơn, một số sự không nhất quán trở nên rõ ràng. Ví dụ, không có định nghĩa cho việc được đào tạo đầy đủ về thông khí bằng tay. Điều này dẫn đến thực tế là các nhóm kiểm soát có thể không phù hợp với nhóm can thiệp.
Trong nghiên cứu của Nakamura và cộng sự,[39] ABG được đánh giá tại các điểm khác nhau trong quá trình vận chuyển. Họ kết luận rằng một máy thở vận chuyển cung cấp hỗ trợ hô hấp phù hợp hơn so với thông khí bằng tay. Lưu ý là các bác sĩ ICU là những người cung cấp thông khí bằng tay. Tuy nhiên, không có đề cập đến mức độ đào tạo về thông khí bằng tay và thực tế rằng đó không phải là cùng một bác sĩ thực hiện thông khí bằng tay trong mọi trường hợp mở ra khả năng các kỹ thuật có thể thay đổi đáng kể. Các tác giả cũng trích dẫn nhiều thay đổi về độ pH trong nhóm thông khí bằng tay. Mặc dù điều này là đúng, nhưng nhìn kỹ hơn về mức độ pH cho thấy rằng trong quá trình thông khí bằng tay, các giá trị pH thực sự gần với mục tiêu 7,40 tại mỗi điểm đo hơn so với nhóm được thông khí bằng máy thở vận chuyển (7,44 so với 7,46, 7,41 so với 7,48 và 7,45 so với 7,46).[39] Các nhà điều tra cũng báo cáo rằng PaO2/FIO2 đã giảm ở 5 đối tượng trong nhóm thông khí bằng tay.[39] Tuy nhiên, không có lời giải thích nào về những gì có thể gây ra điều này. Các đối tượng đã chịu một số suy giảm chức năng hoặc thực sự là kết quả của phương pháp thông khí? Các bác sĩ của ICU “bị mù đôi” khi điều chỉnh các mức PEEP, với kết quả là mức PEEP tổng cao hơn trong nhóm thông khí bằng tay không có theo dõi áp lực đường thở. Một lời giải thích khả dĩ cho sự suy giảm có thể là những điều chỉnh PEEP này được thực hiện mà không có hiển thị trực quan của áp kế có thể dẫn đến quá căng phổi, dẫn đến giá trị PaO2/FIO2 thấp hơn.
Trong nghiên cứu của Gervais et al,[30] ABG đã được thu thập trước và sau trong 30 đối tượng thông khí. Các đối tượng này được tách thành 3 nhóm: thông khí bằng tay, thông khí bằng tay với VT được đo và máy thở vận chuyển cầm tay. Như trường hợp trong nghiên cứu của Nakamura và cộng sự,[39] bác sĩ lâm sàng thực hiện thông khí bằng tay ở 2 nhóm đầu tiên là các bác sĩ đi kèm (không có trình độ chuyên môn) và họ đã sử dụng phán đoán lâm sàng của riêng mình để hướng dẫn thông khí.[30] Một lần nữa, một loạt của các bác sĩ đã tham gia, làm suy yếu tầm quan trọng của nhóm thông khí bằng tay. Điều đáng quan tâm trong nghiên cứu cụ thể này là sự khác biệt về PaCO2 ít hơn ở nhóm thông khí bằng tay có theo dõi VT so với nhóm thông khí bằng tay mà không theo dõi VT, cho thấy rằng theo dõi VT trong quá trình thông khí bằng tay giúp giảm thiểu tăng hoặc giảm CO2 máu.[30]
Hurst et al[31] đã so sánh ABG với thông khí bằng tay do bác sĩ kiểm soát so với việc sử dụng máy thở vận chuyển ở 28 đối tượng được đưa vào khoa cấp cứu. Kết quả chỉ ra rằng PaCO2 và pH thay đổi đáng kể trong nhóm thông khí bằng tay.[31] Họ kết luận, dựa trên kết quả của họ và của Gervais et al,[30] mà dữ liệu của chúng tôi và những người khác đề nghị sử dụng máy thở di động HOẶC một hệ thống cho phép đánh giá trực quan thể tích khí lưu thông được cung cấp là phương pháp hỗ trợ máy thở được ưa thích. Thật vậy, yếu tố quan trọng trên thực tế có thể là bác sĩ lâm sàng có thể nhìn thấy VT và áp lực được cung cấp và phản ứng tức thời. Trong nghiên cứu cụ thể này, các tác giả đã chỉ ra rằng bác sĩ lâm sàng cung cấp thông khí bằng tay đã có kinh nghiệm (bác sĩ trị liệu hô hấp hoặc y tá đã đăng ký).[31] Tuy nhiên, họ không xác định có kinh nghiệm là như thế nào, vì vậy không rõ họ có nghĩa là nhiều năm phục vụ hay có kinh nghiệm cụ thể với thông khí bằng tay.
Weg và Haas[52] đã thực hiện một nghiên cứu tiền cứu mù đơn về 20 đối tượng cần vận chuyển đã được thông khí bằng tay. ABG đã được thực hiện tại các điểm khác nhau: trước khi vận chuyển, trong quá trình vận chuyển và sau khi vận chuyển đã kết thúc. Họ báo cáo rằng ABG không thay đổi ở bất kỳ mức độ quan trọng lâm sàng nào ngoại trừ ở 2 đối tượng.[52] Tuy nhiên, trong một đối tượng, oxy đã vô tình bị ngắt kết nối, và ở ca kia, sự giảm PaCO2 liên quan đến ống dẫn lưu ngực bị kẹp. Họ kết luận rằng thông khí bằng tay trong quá trình vận chuyển thực sự an toàn với điều kiện là bác sĩ lâm sàng được đào tạo để ước chừng các thiết lập trên máy thở ICU.[52]
Bowman et al[14] đã xem xét 27 chuyên gia sơ sinh thực hiện thông khí bằng tay trên phổi thử nghiệm mô phỏng trẻ sơ sinh nặng 3 kg. Các bác sĩ lâm sàng được cung cấp máy theo dõi áp lực và thể tích, và họ đã được đánh giá trong thời gian cơ học phổi thay đổi. Họ phát hiện ra rằng việc có áp lực hiển thị trong quá trình thông khí giúp điều chỉnh một chút để thay đổi độ giãn nở, nhưng kết quả này đã tăng lên đáng kể khi thể tích cũng được hiển thị.
Việc xem xét các bằng chứng dẫn đến kết luận rằng không chỉ đơn thuần là thông khí bằng tay góp phần thay đổi thông khí mà còn đào tạo người vận hành, chuyên môn và tín hiệu thị giác. Một bác sĩ lâm sàng được đào tạo đúng cách sẽ có thể thông khí đầy đủ cho bệnh nhân, với điều kiện là anh ta hoặc cô ta có sự tiếp cận trực quan về thể tích/áp lực. Biến thiên vẫn có thể tồn tại với thông khí bằng tay, nhưng chúng sẽ được giảm thiểu. Những nghiên cứu này cho thấy tầm quan trọng của việc đào tạo phù hợp khi nói đến thông khí bằng tay. Thật không may, không có tiêu chuẩn cứng nhắc nào cho việc này, và trách nhiệm phải được áp dụng cho mỗi cơ sở để đào tạo thông khí bằng tay và duy trì năng lực thích hợp.
Ưu điểm của thông khí bằng tay
Có một số lợi thế để sử dụng thông khí bằng tay trong quá trình vận chuyển. Đầu tiên và rõ ràng nhất là chi phí. Chi phí của máy thở di động và thủ công khác nhau tùy theo từng trường hợp. Tuy nhiên, nếu chúng ta cho rằng vì lý do rằng bóng giúp thở bằng tay có giá khoảng 25 đô la và máy thở di động khoảng 12.000 đô la, thì điều này thể hiện sự tiết kiệm chi phí rất lớn. Chi phí này thậm chí không bao gồm bảo trì, đào tạo nhân viên và năng lực liên tục. Thứ hai, có vấn đề hậu cần của không gian trên và xung quanh giường. Càng nhiều thiết bị tham gia, càng ít không gian mà các bác sĩ lâm sàng phải làm việc. Một số máy thở di động được đặt trên giường, trong khi những thiết bị khác cần phải được kéo theo. Sự tắc nghẽn thêm này trên và xung quanh giường có thể hạn chế sự tiếp cận của bác sĩ lâm sàng với bệnh nhân. Thứ ba, lỗi thiết bị là một khả năng khác. Mặc dù lỗi máy thở di động không phổ biến, nhưng khi nó xảy ra thì đó không phải là cách khắc phục nhanh chóng, dễ dàng. Thất bại của bóng giúp thở, mặt khác, rất có thể có thể được khắc phục nhanh chóng ở đầu giường, đặc biệt là với các nhân viên có kinh nghiệm. Thứ tư, tiêu thụ khí là không đổi với thông khí bằng tay. Tuy nhiên, như đã đề cập trước đây, mức tiêu thụ khí với máy thở di động khác nhau, tùy thuộc vào đặc điểm của máy thở và cài đặt máy thở. Thứ năm, các bác sĩ lâm sàng cũng không cần quan tâm đến thời lượng pin, vì không có thiết bị điện tử nào liên quan đến thông khí bằng tay. Cuối cùng, ngoài chi phí, có lẽ ưu điểm lớn nhất của thông khí bằng tay là thời gian thiết lập. Một máy thở di động yêu cầu thiết lập mạch, kiểm tra máy thở trước sử dụng, và thiết lập các tham số. Một bóng giúp thở bằng tay có thể nhanh chóng được thiết lập và việc vận chuyển có thể bắt đầu trong vòng vài phút.
Thông khí bằng tay vẫn được sử dụng ngày nay
Mặc dù đã có những cải tiến đối với máy thở di động, thông khí bằng tay vẫn được sử dụng trong nhiều tình huống lâm sàng, bao gồm (1) vận chuyển bệnh nhân đến và từ phòng mổ, (2) vận chuyển bệnh nhân từ khoa cấp cứu đến ICU, khu chẩn đoán, phòng mổ và buồng siêu âm, và (3) trong các phản ứng nhanh và vận chuyển tiếp theo. Trong nhiều trường hợp, thông khí bằng tay được sử dụng vì có thể không có thời gian để thiết lập và kiểm tra trước sử dụng máy thở di động một cách thích hợp trước khi bệnh nhân cần phải di chuyển.
Mặc dù các tình huống vẫn tồn tại trong đó thông khí bằng tay là phương pháp ưa thích trong quá trình vận chuyển (vì bất kỳ lý do gì), đào tạo nâng cao và sử dụng áp kế và máy theo dõi VT rất thiếu. Khi nói đến thông khí bằng tay, hầu hết các khóa đào tạo của bác sĩ lâm sàng khá cơ bản: cách gắn bóng giúp thở, cách ổn định ống nội khí quản trong quá trình vận chuyển và cách theo dõi hiệu quả của máy thở. Trong lịch sử, không có nhiều sự chú ý đến các mức VT và/hoặc áp lực thông khí được cung cấp.
Tóm tắt về ý kiến chống
Mặc dù việc sử dụng máy thở di động trong quá trình vận chuyển đang trở nên phổ biến hơn, nhưng lập luận có thể đưa ra rằng vẫn có sự biến động rộng rãi giữa các máy thở vận chuyển khác nhau. Nhiều máy thở vận chuyển gặp khó khăn trong việc thông khí hiệu quả khi đối mặt với cơ học phổi ngày càng tồi tệ.[40,41,46-48] Các bác sĩ lâm sàng phải có nhận thức sâu sắc về khả năng và giới hạn của máy thở vận chuyển của tổ chức để tối ưu hóa an toàn cho bệnh nhân trong quá trình vận chuyển. Mặc dù các lập luận đã được đưa ra rằng thông khí bằng tay dẫn đến biến thiên máy thở nhiều hơn, điều quan trọng cần lưu ý là tất cả các bằng chứng đều sử dụng các điểm cuối thay thế, chẳng hạn như ABG và các thông số huyết động. Không có nghiên cứu mà chúng tôi biết rằng đã kiểm tra kết quả tử vong. Chúng tôi không biết liệu việc sử dụng máy thở di động hay thông khí bằng tay trong quá trình vận chuyển có ảnh hưởng gì đến tỷ lệ tử vong hay không. Tóm lại, vẫn còn một nơi để thông khí bằng tay trong quá trình vận chuyển. Tuy nhiên, để có hiệu quả, cần phải chú trọng hơn nhiều vào đào tạo nâng cao tập trung vào bảo vệ phổi. Ngoài ra, áp kế và máy theo dõi VT là những công cụ có giá trị nên được sử dụng để giúp bác sĩ thông khí trong vùng an toàn.
Kết luận
Sự gia tăng của bệnh nhân thở máy chắc chắn sẽ dẫn đến sự gia tăng số lượng bệnh nhân cần hỗ trợ thở máy trong quá trình vận chuyển. Mặc dù có sẵn rất nhiều thiết bị hỗ trợ thông khí, nhưng phải cân nhắc cẩn thận trước khi vận chuyển để đảm bảo rằng thiết bị được chọn cung cấp thông khí đầy đủ một cách an toàn và hiệu quả. Mặc dù chi phí có thể là một sự cân nhắc, các tính năng và hiệu suất tiên tiến của máy thở vận chuyển tinh vi hiện đại rõ ràng là vượt trội so với thông khí bằng tay. Việc sử dụng chúng nên được coi là tiêu chuẩn chăm sóc cho bệnh nhân cần hỗ trợ thở máy mức độ cao. Mặc dù bóng giúp thở bằng tay phải đi cùng với mọi bệnh nhân trong quá trình vận chuyển để sử dụng trong trường hợp khẩn cấp, nhưng việc sử dụng chúng nên được giới hạn ở những bệnh nhân ít nguy kịch hơn và nên kết hợp hoặc bổ sung một phương tiện để theo dõi áp lực và VT. Cuối cùng, vẫn còn một thực tế không thể chối cãi, đó là hơn bất kỳ thiết bị nào, đảm bảo bệnh nhân được thông khí an toàn trong quá trình vận chuyển cuối cùng phụ thuộc vào kỹ năng và kiến thức của người chăm sóc đi kèm.





