Bài viết Những nhận định khoa học cơ bản về trào ngược hầu – thanh quản được biên dịch bởi BS. CK1 Hồ Thị Hoài Thu và BS. Trần Minh Dũng từ Sách “Ho Mạn Tính: Nguyên nhân, chẩn đoán và điều trị” của tác giả Miles Klimara and Nikki Johnston.
1. GIỚI THIỆU
Trào ngược hầu – thanh quản (LPR) là một trong các nguyên nhân phổ biến gây ho mãn tính. Mặc dù các thành phần có tính axít của trào ngược dạ dày thường được xem là yếu tố chiếm ưu thế trong nguyên nhân của bệnh trào ngược, các thành phần khác có trong trào ngược dạ dày như pepsin ngày càng được xem vừa là dấu ấn sinh học vừa là yếu tố trung gian tiềm ẩn của sinh lý bệnh. Cụ thể, bằng chứng chỉ ra khả năng của pepsin kích thích phản ứng tiền viêm trong biểu mô thực quản và thanh quản, ngay cả khi trào ngược axít yếu hoặc không axít, có lẽ được giải thích là thuốc ức chế bơm proton (PPI) không hiệu quả trong điều trị LPR và ho mãn tính khi không có triệu chứng kinh điển của bệnh trào ngược dạ dày thực quản (GERD). Cuối cùng, ức chế pepsin là một mục tiêu quan trọng cho các chương trình chế tạo thuốc, điều này có thể dẫn đến việc tạo ra các liệu pháp mới có thể giải quyết các thành phần không phải axít của bệnh.
2. CÁC DẤU ẤN SINH HỌC TRONG TRÀO NGƯỢC VÀ HO MÃN TÍNH
LPR được biết đến là một trong các nguyên nhân tiềm ẩn của ho mãn tính. Tuy nhiên, các dữ liệu hỗn hợp và hạn chế để hỗ trợ độ tin cậy và độ đặc hiệu của các công cụ hiện tại được thiết kế để giúp chẩn đoán ho mãn tính và LPR, bao gồm từ đánh giá triệu chứng đến phân loại mức độ nặng của soi thanh quản 1-4. Thực vậy, đã có một cuộc điều tra về sự có ích của các dấu ấn sinh học khác nhau như là yếu tố dự báo của LPR liên quan đến ho mãn tính. Đặc biệt, pepsin được sản xuất duy nhất bởi các tế bào chính của dạ dày, do đó sự hiện diện của nó bên ngoài dạ dày được coi như một dấu ấn sinh học nhạy cảm đối với trào ngược và dịch hút dạ dày 5. Ở bệnh nhân nhi được đặt nội khí quản, độ nhạy và độ đặc hiệu của pepsin trong các mẫu rửa phế quản phế nang (BAL) để tiên lượng hít trên lâm sàng lên tới 80% – 100% 6. Ngoài ra, pepsin được phát hiện tăng đáng kể trong các mẫu BAL và khí quản được lấy từ bệnh nhân trào ngược thực quản và triệu chứng ho mãn tính, điều này cho thấy pepsin/ BAL có thể là một biện pháp hữu ích trong việc phân biệt ho mãn tính thứ phát với trào ngược thực quản khác hẳn với các nguyên nhân khác6,7. Theo y văn trước đây, pepsin trong đàm như là một công cụ tiềm ẩn để xác định sự hiện diện của trào ngược gần (độ nhạy 75%, độ đặc hiệu 91%), pepsin có thể xâm nhập vào hầu – thanh quản và gây ra bệnh tăng nhạy cảm thanh quản và bệnh phổi.
Thu thập BAL biểu hiện tiềm năng hấp dẫn và thực tế, một số nghiên cứu được thảo luận dưới đây đã so sánh sự có lợi của pepsin trong các mẫu đàm và nước bọt trong phát hiện LPR với các phương pháp được xác nhận trước đó như chỉ số triệu chứng trào ngược (RSI, bảng câu hỏi xác định mức độ nghiêm trọng của các triệu chứng hô hấp trên do trào ngược) 4, điểm số trào ngược (RFS, một công cụ để phân loại kết quả soi thanh quản chỉ ra tình trạng viêm do trào ngược)3, và theo dõi kháng trở đa kênh-pH (MII-pH), với kháng trở băng qua thực quản và hạ hầu được coi là lý tưởng để theo dõi trào ngược gần.
Ở những bệnh nhân có triệu chứng hô hấp trên mãn tính biểu hiện tăng phản ứng thanh quản, ví dụ như ho mãn tính, cảm giác nghẹn, khó thở, và nghẹt thở. Spyridoulias và cộng sự xác định độ đặc hiệu 0,78 của pepsin nước bọt như một yếu tố dự báo cho những thay đổi viêm trên nội soi thanh quản, nhưng độ nhạy chỉ 0,53 9. Đáng chú ý, pepsin không tương quan đáng kể với điểm số triệu chứng trào ngược hoặc tình trạng trào ngược khi theo dõi MII-pH và nhiều bệnh nhân có kết quả trái ngược giữa các phương thức xét nghiệm khác nhau.Tuy nhiên, gần một nửa bệnh nhân có triệu chứng phổi nhưng thay đổi viêm ít trên nội soi thanh quản – pepsin nước bọt có thể phát hiện được, điều này gợi ý rằng LPR nhẹ có thể đủ để gây ra các triệu chứng tăng phản ứng thanh quản mà không gây ra bất kỳ thay đổi nào có thể nhìn thấy trong đường thở.
Công dụng của pepsin như một dấu ấn sinh học cho LPR ở những người trưởng thành bị ho mãn tính mà không có tiền sử triệu chứng liên quan đến trào ngược dạ dày thực quản dường như ít được thể hiện. Trong một nhóm bệnh nhân ho mãn tính ngẫu nhiên, pepsin đàm được tìm thấy có liên quan nghịch với tần suất ho, và hơn nữa những bệnh nhân này không bị trào ngược gần đáng kể bởi MII-pH 10. Điều này gợi ý về khái niệm trái ngược ho trong bối cảnh LPR, ho mãn tính thứ phát với các nguyên nhân khác. Trên thực tế ho tạo điều kiện cho sự thanh thải trào ngược và do đó ngăn ngừa vi trùng. Những kết quả này phù hợp với các nghiên cứu trước đây về pepsin trong các mẫu rửa khí quản, pepsin trong dịch rửa khí quản có giá trị tiên đoán kém ở bệnh nhân không được lựa chọn với các triệu chứng hô hấp mãn tính, nhưng nó có độ nhạy và độ đặc hiệu cao hơn khi đánh giá bệnh nhân với các triệu chứng kinh điển đã nói ở trên. Hơn nữa, điều này có thể được giải thích là LPR không phải là yếu tố trung gian chính trong bệnh lý ở bệnh nhân ho mãn tính không có biểu hiện các triệu chứng kinh điển của GERD, và trong trường hợp không có triệu chứng GERD điển hình đánh giá dấu ấn sinh học của LPR có thể bị hạn chế.
Ngược lại, những người khác đã lập luận rằng trên thực tế LPR là nguyên nhân chính của hầu hết các bệnh ho mãn tính thông qua việc gây tăng kích ứng đường hô hấp trên đối với kích thích độc hại 11, nếu đúng thì các phương pháp hiện tại được sử dụng để phát hiện pepsin đơn giản không phản ánh chính xác tình trạng trào ngược. Ngoài ra, các nghiên cứu gầnđây sử dụng MII hạ hầu – thực quản với pH kép (HEMII-pH) để chẩn đoán LPR ở những bệnh nhân bị ho mãn tính đã chứng minh rằng những bệnh nhân được lựa chọn cẩn thận có đáp ứng hoàn toàn hoặc một phần với phương pháp cuộn đáy vị Nissen gây ra mặc dù không có mối tương quan với triệu chứng ho. Điều này tiếp tục ủng hộ lý thuyết rằng LPR không axít có thể là một tình trạng viêm mạn tính tiềm ẩn thứ phát sau lắng đọng pepsin ở thanh quản và / hoặc thực quản (đứng đầu các yếu tố khác gây ra ho) không nhất thiết có sự trào ngược phối hợp.
Chỉ số đại thực bào phế nang – lipid (LLMI), được đề xuất như là một dấu hiệu cho sự hít dịch trào ngược dạ dày vì nó phản ánh sự thực bào lipid trong thức ăn trào ngược bởi các đại thực bào trong mẫu bệnh phẩm phế quản phế nang. Việc nhuộm các tế bào trong dịch BAL với dầu O màu đỏ cho thấy các lipit có thể định lượng bằng LLMI. Trong các nghiên cứu trước đây, đã chứng minh chỉ số này có độ nhạy tới 100% nhưng độ đặc hiệu chỉ 57% đối với chọc hút dịch phổi. Tuy nhiên, biện pháp này ít hiệu quả trong việc nghiên cứu ho mãn tính, vì LLMI không tăng đáng kể ở trẻ em bị GERD hoặc ho mãn tính. Người ta cho rằng LLMI có thể phản ánh sựthực bào không chỉ của lipid thực phẩm, mà cả lipid từ sự thoái hóa phospholipids phế nang 6. Điều này giải thích cho độ đặc hiệu kém của nó. Như vậy, mặc dù LLMI có thể có một số giá trị hạn chế trong đánh giá dịch hít trào ngược liên quan tới bệnh, nhưng lợi ích của LLMI trong sự tạo thành ho mãn tính có thể rất thấp.Nhiều thách thức tồn tại trong việc phát triển một dấu ấn sinh học để sử dụng như một công cụ chẩn đoán trong bệnh phổi liên quan đến trào ngược. Độ nhạy và độ đặc hiệu của pepsin nước bọt không đủ để được coi là xét nghiệm có độ tin cậy cao trong phân lập và thu thập mẫu tại một thời điểm duy nhất, dẫn đến âm tính giả ở những bệnh nhân không có trào ngược 9. Do đó lần này, pepsin trong nước bọt và BAL đại diện cho một công cụ tiềm năng để hỗ trợ chẩn đoán phân biệt các than phiền của bệnh phổi mạn tính với tăng phản ứng thanh quản. Và pepsin nước bọt đặc biệt hấp dẫn, vì nó không cần thiết bị chuyên dụng hoặc gây khó chịu cho bệnh nhân. LLMI cung cấp độ nhạy tương đối lớn hơn nhưng độ đặc hiệu kém hơn và tất nhiên đòi hỏi phải thu được mẫu BAL mà điều này bị cấm trong nhiều bối cảnh lâm sàng.
3. PEPSIN – MỘT CHẤT TRUNG GIAN TRONG QUÁ TRÌNH VIÊM
Các nghiên cứu in vitro chỉ ra rằng thực bào thông qua trung gian thụ thể, pepsin nonacid có thể xâm nhập vào biểu mô của hạ hầu và hầu họng 14,15. Sau khi nhập bào, các thụ thể và ligand được đặt trong các endosome có tính axit yếu và thể Golgi, làm tăng khả năng vận chuyển pepsin qua các con đường này. Những phát hiện trên kính hiển vi điện tử miễn dịch đã hỗ trợ cho khái niệm này, xác định có sự chồng lấp của pepsin ở cuối endosome marker Rab-9 và TRG marker TRG-4616. TRG có độ axit yếu pH khoảng 5, trong khi đó pepsin có khoảng 40% hoạt động tối đa 17,18; như vậy, pepsin không hoạt động có thể có khả năng được đưa lên bởi các tế bào biểu mô thanh quản và được kích hoạt trong các kho- ang nội bào có độ pH thấp, tạo tiền đề cho tổn thương nội tế bào (Hình 5-1). Tiếp theo, sự tiếp xúc của các tế bào vòm họng với pepsin ở pH 7 đã được chứng minh là gây ra sự biểu hiện của một số cytokine tiền viêm và thụ thể, bao gồm IL-1, chất kích thích bạch cầu trung tính IL-8, và yếu tố kích thích bạch cầu ái toan IL-5 19. Ngược lại, sự tiếp xúc của biểu mô thanh quản với pepsin đã được chứng minh là tiêu huỷ các protein bảo vệ như Sep70 và carbonic anhydrase-III, điều này cho thấy có nhiều cách mà tổn thương tế bào qua trung gian pepsin có thể góp phần gây ra viêm nhiễm liên tục và được phát hiện qua nội soi của bệnh LPR. Hơn nữa các cytokine tiền viêm đã đề cập ở trên, gây ra trong các mô hạ hầu (độc lập với trào ngược axít) tương tự như biểu hiện trong viêm thực quản trào ngược và được biết là góp phần gây viêm liên tục trong sinh lý bệnh của GERD 19.
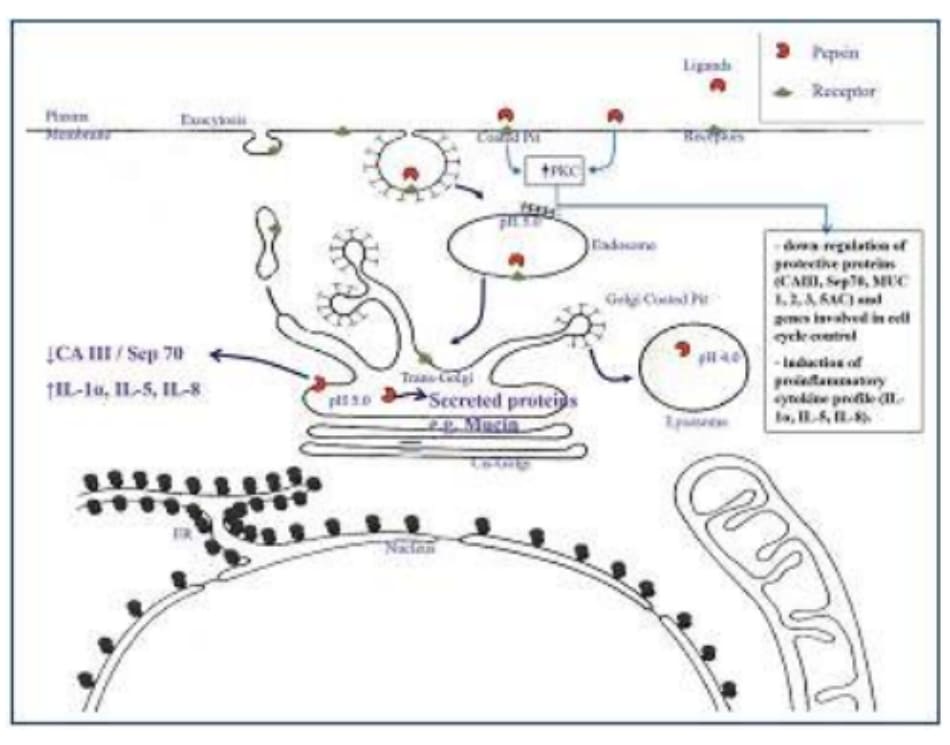
Nghiên cứu trên xác định một cơ chế mới mà pepsin có thể gây tổn thương tế bào và viêm bất kể tính axít của môi trường ngoại bào, có khả năng đưa ra lời giải thích cho sự tồn tại của viêm niêm mạc mãn tính, các triệu chứng và kết quả nội soi ở nhiều bệnh nhân bị bệnh lý thanh quản do trào ngược mặc dù điều trị bằng ức chế axít liều cao. Trong khi pepsin từ lâu đã được biết như là một nguyên nhân trong GERD do hoạt động phân giải protein của nó trong môi trường pH thấp gây ra bởi các cơn trào ngược dạ dày thực quản. Việc phát hiện ra pepsin có khả năng hoạt động nội bào và gây ra phản ứng tiền viêm cho thấy vai trò của pepsin trong bệnh trào ngược qua trung gian của đường thở nơi pH có thể ít liên quan đến lâm sàng. Sự hấp thu qua trung gian thụ thể của pepsin không axít, có thể xảy ra sau LPR, bất kỳ thay đổi viêm hoặc tân sinh nào có thể xảy ra 11,19, 21, không được ngăn chặn bởi PPI, mà chỉ giải quyết việc sản xuất axít trong niêm mạc dạ dày. Vì vai trò của pepsin trong LPR gây tổn thương niêm mạc qua trung gian dường như liên quan đến sự kích hoạt của nó trong các khoang nội bào có tính axit hơn hoặc thông qua các rối loạn hoặc kích hoạt các tầng tín hiệu tế bào. Sự cải thiện môi trường axít của trào ngược dạ dày với PPI hoặc chất đối kháng histamine (thụ thể H2) có thể không giải quyết thỏa đáng những thay đổi viêm qua trung gian pepsin. Mặc dù PPI vẫn là thuốc chính để điều trị GERD, nhưng có bằng chứng kém về hiệu quả của PPI trong điều trị bệnh qua trung gian trào ngược, bao gồm LPR 22. Người ta tin rằng đường hô hấp trên nhạy cảm với trào ngược hơn thực quản, và do đó PPI liều cao hơn là cần thiết để kiểm soát các triệu chứng liên quan đến LPR 23 -25. Tại thời điểm này, các nghiên cứu đối chứng giả dược và lớn chưa cho thấy lợi ích điều trị đáng kể đối với PPI được sử dụng trong LPR 26-31.
Mặc dù một số nghiên cứu đã ghi nhận có sự cải thiện triệu chứng khi điều trị bằng PPI. Khi xem xét lại hai nghiên cứu này, người ta cho rằng những bệnh nhân bị ảnh hưởng chỉ cải thiện đáng kể các triệu chứng trào ngược dạ dày thực quản thay vì cải thiện các triệu chứng đường thở trên 30. Có thể đưa ra lập luận rằng những nghiên cứu này đã được thực hiện trước thời đại xét nghiệm HEMII-pH và chẩn đoán trào ngược không axít là không đầy đủ. Do dữ liệu kém về hiệu quả ức chế axit trong điều trị trào ngược ngoài thực quản, Hiệp hội Tiêu hóa Hoa Kỳ đã khuyến cáo cụ thể chống lại việc sử dụng PPI theo kinh nghiệm đối với nghi ngờ LPR trừ khi có các triệu chứng đồng thời của GERD 34. Tuy nhiên, rất ít các phương pháp điều trị hiệu quả thay thế, PPI tiếp tục được sử dụng trong LPR 35, và thực sự là Viện Hàn lâm Tai mũi họng Hoa Kỳ và Hội Phẫu thuật Đầu – Cổ đã khuyến cáo sử dụng PPI liều cao khi nghi ngờ LPR. Với phương pháp nội soi ổ bụng cuộn đáy vị được đề nghị thay thế như là một phương pháp trong quản lý bệnh. Một cuộc khảo sát gần đây từ Hiệp hội phế quản – thực quản Hoa Kỳ đã báo cáo rằng PPI hai lần mỗi ngày vẫn là một liệu pháp đầu tiên phổ biến trong điều trị LPR 36.
Phương pháp nội soi ổ bụng cuộn đáy vị và quy trình vòng từ tính được thiết lập tốt là lựa chọn đáng tin cậy để phẫu thuật quản lý GERD. Trái ngược với sự cải thiện có thể dự đoán được trong điều trị GERD, ng- hiên cứu về hiệu quả của phẫu thuật chống lại trào ngược trong điều trị LPR còn lộn xộn, với nhiều nghiên cứu khác nhau cho thấy sự hồi phục của bệnh nhân ho mãn tính dao động từ 63% đến 85% 37. Các giả thuyết cho dao động này bao gồm từ sự khác biệt trong kỹ thuật phẫu thuật đến sự khác biệt trong tiêu chí lựa chọn bệnh nhân. Đặc biệt, người ta quan sát thấy rằng những bệnh nhân có triệu chứng GERD nghiêm trọng có nhiều khả năng đạt hiệu quả tốt hơn từ phẫu thuật chống trào ngược và đặc biệt là những bệnh nhân bị ợ nóng trước phẫu thuật và pH < 4 trong hơn 12% của khoảng thời gian 24 giờ thì có 90% bệnh nhân cải thiện triệu chứng 40.
Vai trò của trào ngược không axít trong LPR được hỗ trợ thêm nhờ sử dụng MII-pH theo dõi, đại diện cho một tiến bộ lớn trong chẩn đoán bệnh trào ngược ngoài thực quản do khả năng phát hiện các tình trạng trào ngược không axít. MII-pHđược chứng minh có sự liên quan chặt chẽ với triệu chứng LPR 41, kết hợp với nghiên cứu được mô tả trước đây cho thấy bằng chứng kém về hiệu quả ức chế axit trong LPR và về cải thiện đáng kể triệu chứng sau can thiệp phẫu thuật như cuộn đáy vị chống trào ngược đạt đến thanh quản 12,40,42,43 cho thấy các thành phần không axít của trào ngược phải đóng một vai trò chính trong sinh lý bệnh của trào ngược hầu thanh quản với ho mãn tính. Trong trường hợp không có sự đồng thuận hoặc hướng dẫn phù hợp của phẫu thuật chống trào ngược, đánh giá trước phẫu thuật các biến cố trào ngược thực quản và vận động với MII-pH và hình ảnh thực quản độ phân giải cao đã được đề xuất như một công cụ hữu ích trong việc dự đoán cải thiện triệu chứng sau phẫu thuật 12,43. Các nghiên cứu nhỏ hơn bác bỏ tuyên bố rằng một mình GERD dự đoán đáp ứng với Nissen bằng cách sử dụng công nghệ HEMII-pH mới nhất để lựa chọn các phương pháp cho phẫu thuật chống trào ngược 12,43. Các nghiên cứu in vitro trước đây cũng cho rằng mật có thể gây viêm thanh quản bất kể pH, nhưng những người khác đã phản bác rằng không có bằng chứng nào cho thấy đây là một cơ chế gây tổn thương cho thanh quản của con người 44. Trong in vitro khi tiếp xúc với axít mật gây ra tình trạng chảy máu màng tế bào 45, kiến thức của chúng tôi không có báo cáo về phát hiện mô học này trong niêm mạc thanh quản của bệnh nhân LPR. Đáng chú ý, các nghiên cứu trước đây đã sử dụng nồng độ muối và axít mật độ cao, dao động từ 5 đến 50 mM. Điều này chồng lấp nồng độ sinh lý của muối mật trong tá tràng ở người, dao động từ 10 đến 22 mM. Ngược lại, hàm lượng axit / muối mật sinh lý trong trào ngược dạ dày đạt đến thanh quản được dự kiến sẽnằm trong phạm vi micromol, chúng tôi không biết là điều này gây ra tổn hại cho niêm mạc thanh quản. Hơn nữa, các axít mật không kết hợp, gây tổn thương ở pH cao hơn như thanh quản, hiếm khi được tìm thấy như là thành phần của trào ngược dạ dày.Tuy nhiên, không có bằng chứng mạnh mẽ về nồng độ của mỗi axít mật trong thanh quản và vai trò của axít mật trong sinh lý bệnh của LPR vẫn còn là một vấn đề nan giải. Như vậy, sự hiểu biết phổ biến trước đây về LPR và bệnh trào ngược đường thở – qua trung gian axít đã chuyển sang mô hình trong đó bệnh chủ yếu qua trung gian các thành phần không axít trong dịch trào ngược trong đó điều trị y tế truyền thống với ức chế axit là không đủ.
4. Pepsin là một mục tiêu điều trị
Như đã thảo luận ở trên, PPI tiếp tục được sử dụng phổ biến trong thực hành lâm sàng để điều trịbệnh trào ngược đường thở bao gồm LPR mặc dù có bằng chứng kém về hiệu quả của chúng 26-31, với khoảng 26 tỷ đô la chi tiêu hàng năm cho chỉ định này49 .Trong trường hợp điều trị PPI không hiệu quả cho LPR và các chi phí liên quan và rủi ro tiềm ẩn của nó, tạo nên mối quan tâm đáng kể đến thay đổi phương thức điều trị trong LPR 48,50,51.
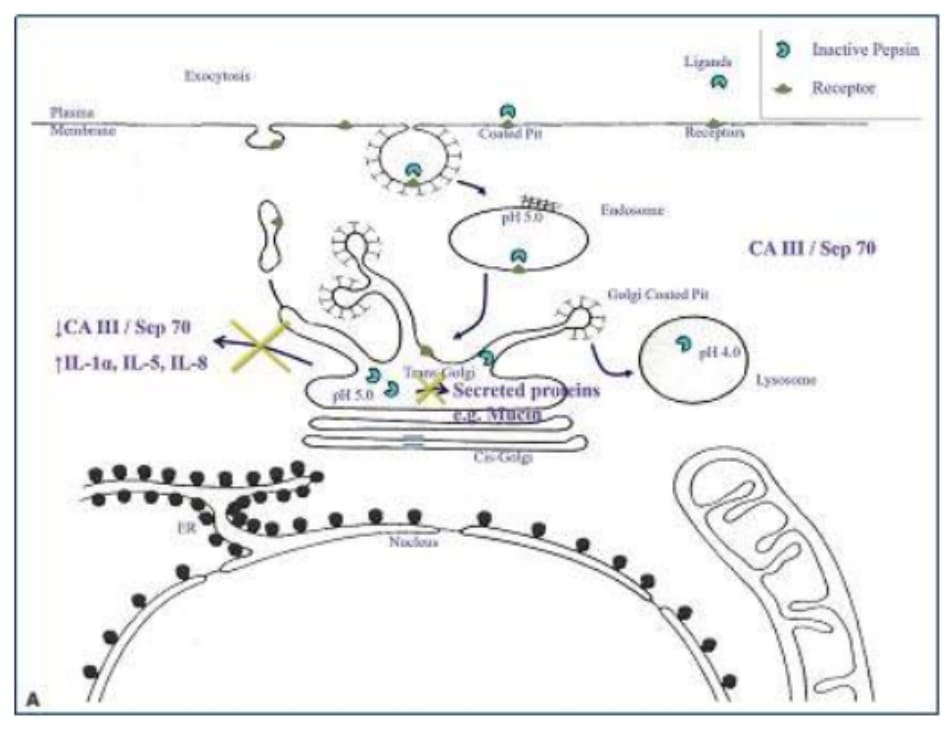
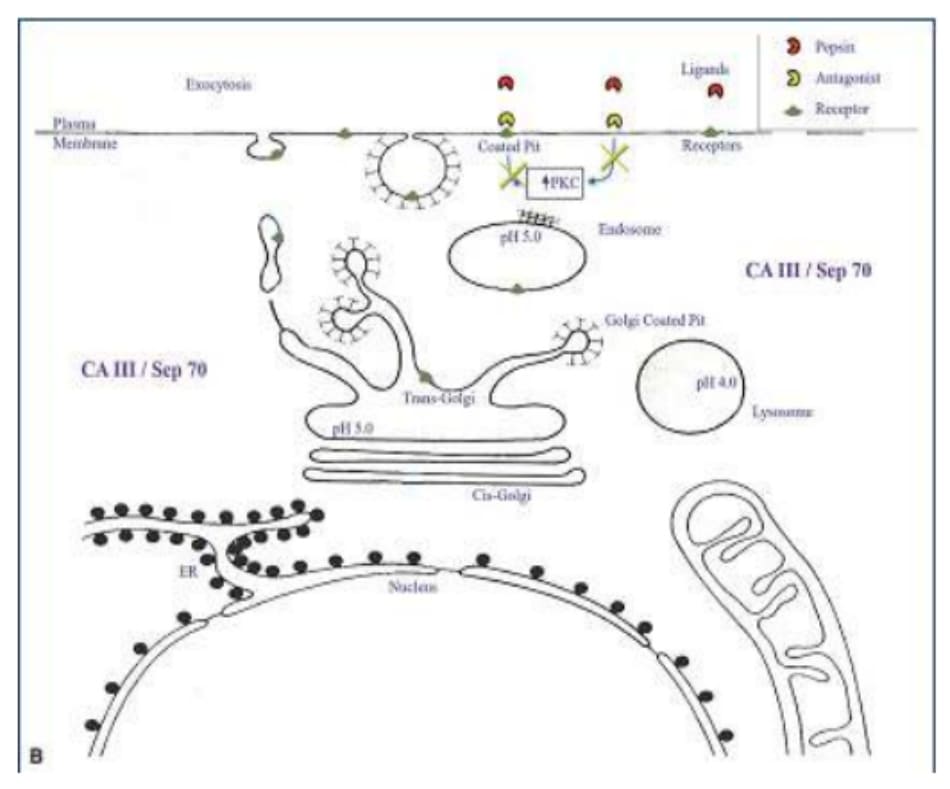
Pepsin đại diện cho một mục tiêu tiềm năng thú vị cho các liệu pháp điều trị trong tương lai, đặc biệt đối với những bệnh nhân gặp phải các triệu chứng khó chữa đối với PPI dựa trên vai trò của nó trong LPR không axít 16,48. Các tài liệu trước đây đã xác định hai cơ chế mà pepsin có thể được nhắm mục tiêu trong điều trị LPR: bằng cách bất hoạt không thể đảo ngược và thông qua sự đối kháng thụ thể 16,48. Đầu tiên sẽ ngăn chặn sự tái hoạt động của pepsin trong môi trường axít của các khoang nội bào (Hình 5 – 2A), thứ hai sẽ ngăn chặn sự nhập bào của nó và có lẽ là sự biểu hiện được mô tả trước đây của cytokine tiền viêm (Hình 5 – 2B). Mặc dù Pepstatin A là một chất ức chế mạnh hoạt động của pepsin và hiện đang có sẵn trên thị trường, dược động học kém và các đặc tính hòa tan trong nước khiến nó trở thành một ứng cử viên tương đối kém cho mục tiêu điều trị LPR. Do đó, các tác nhân mới nhắm vào pepsin hiện đang được phát triển và đại diện cho một con đường tiềm năng thú vị để điều trị bệnh qua trung gian trào ngược bao gồm LPR và ho mãn tính.
5. Suy nghĩ thêm
Mặc dù các tài liệu trên xác định rõ vai trò của pepsin trong sinh lý bệnh của LPR và ho mãn tính, nhưng các nghiên cứu phát hiện công dụng của pepsin nước bọt như là một dấu hiệu của trào ngược ngoài thực quản cho thấy kết quả còn bàn cãi. Điều này có thể cho thấy pep- sin không phải là một dấu ấn sinh học hữu ích cho bệnh đường thở, nhưng điều quan trọng cần nhớ là nồng độ pepsin trong nước bọt chỉ có thểtăng cao thoáng qua do bị trào ngược tự nhiên và ảnh hưởng không liên tục của việc nuốt, cả hai sẽ thay đổi theo lượng thứcănăn vào. Cuối cùng, tối ưu hóa thời gian và phương pháp thu thu nhận các mẫu nước bọt để mang lại sự cân bằng độ nhạy và độ đặc hiệu cao nhất là điều cần thiết nếu pepsin được sử dụng trong lâm sàng như một dấu hiệu của bệnh. Mặc dù các mẫu nước bọt và đàm thường được thu thập ít nhất 1 giờ sau bữa ăn để tránh phát hiện các tình trạng trào ngược sau bữa ăn, chưa có nghiên cứu quy mô lớn nào để xác định thời gian tối ưu hoặc phương pháp lấy mẫu, và do đó thời gian tối ưu cho thu thập mẫu vẫn chưa rõ ràng. Các nghiên cứu lớn hơn với việc thu thập mẫu thường xuyên hơn có thể cho phép xác định thời gian lý tưởng cho việc lấy mẫu, điều này có thể tạo điều kiện thuận lợi cho việc sử dụng pepsin nước bọt như một công cụ có độ nhạy và độ đặc hiệu cao hơn để chẩn đoán bệnh đường thở. Hơn nữa, pepsin nước bọt có thể giúp xác định một nhóm của bệnh nhân ho mãn tính có trào ngược và sự hít dịch trào ngược góp phần vào bệnh, và do đó những bệnh nhân này có thể được hưởng lợi từ việc điều chỉnh lối sống chống trào ngược và phẫu thuật.
Trong khi pepsin nước bọt đại diện cho bằng chứng về tình trạng trào ngược, và pepsin trong khí quản hoặc pepsin BAL là bằng chứng rõ ràng về sự hít dịch do trào ngược, đo lượng pepsin trong dịch tiết có thể không phản ánh đầy đủ sự hấp thu của pepsin qua nhập bào trung gian thụ thể thanh quản và tế bào phổi. Như vậy, pepsin nội bào và pepsin gắn mô có thể là dấu hiệu của bệnh qua trung gian pepsin hơn là pepsin nước bọt hoặc pepsin khí quản / BAL . Các yếu tố khác như các cơ chế bảo vệ niêm mạc của các mô đang được đề cập, có thể dẫn đến tăng nhập bào pepsin, tạo tiền đề cho sự kích hoạt nội bào và phát triển xuống dưới phản ứng viêm. Mặc dù sự xâm lấn của việc lấy mẫu có thể ngăn cản việc sử dụng pepsin trong các mô – một dấu ấn chẩn đoán, thì vai trò chính xác của pepsin trong LPR và ho mãn tính có thể được làm sáng tỏ bởi các nghiên cứu trong tương lai kiểm tra cả hai yếu tố, có thể góp phần làm tăng nhập bào pepsin qua trung gian thụ thể tế bào và mối quan hệ giữa pepsin trong dịch tiết nước bọt và pepsin trong các mô thanh quản.
6. THÔNG ĐIỆP
- Pepsin enzyme dạ dày là một dấu ấn sinh hóa của bệnh trào ngược qua trung gian có thể có ích trong việc hiểu LPR và ho mãn tính.
- Bằng chứng về sự hữu ích của các dấu ấn sinh hóa trong chẩn đoán hoặc quản lý ho mãn tính liên quan đến LPR là không đủ để khuyến nghị sử dụng chúng trong thực hành lâm sàng.
- Tại thời điểm này, bệnh sử kỹ càng và các công cụ bao gồm MII-pH (tốt nhất là với kháng trở băng qua qua thực quản và hạ hầu, HEMII-pH), nội soi thanh quản và nội soi phế quản có nhiều khả năng phát hiện các nguyên nhân của triệu chứng ho mãn tính.
- Trong điều kiện hiệu quả kém của PPI đối với ho mạn tính liên quan đến trào ngược ở những bệnh nhân thiếu các triệu chứng GERD (ví dụ như ợ nóng), các thành phần không axít của trào ngược có khả năng là yếu tố trung gian quan trọng của sinh lý bệnh và là mục tiêu cho nghiên cứu trong tương
- Mặc dù vai trò của phẫu thuật chống trào ngược trong điều trị LPR và ho mãn tính chưa rõ ràng vào thời điểm này, nhưng lợi ích tiềm năng của nó cũng tương tự như vai trò của các thành phần không axít của trào ngược.
- Mặc dù pepsin thường được cho là có khả năng gây viêm chỉ trong môi trường axit, nhưng có bằng chứng thuyết phục rằng pepsin không axít có thể gây tổn thương cho các mô ngay cả ở độ pH trung tính hơn.
- Các chất ức chế Pepsin và chất đối kháng thụ thể đại diện cho các mục tiêu phát triển các liệu pháp điều trị mới cho bệnh liên quan đến trào ngược mà trước đây sử dụng liệu pháp PPI.
7. TÀI LIỆU THAM KHẢO
- Joniau S, Bradshaw A, Esterman A, Carney AS. Reflux and laryngitis: a systematic Otolaryngol Head Neck Surg.2007;136(5):686–692.
- Chang BA, MacNeil SD, Morrison MD, Lee PK. The reliabilty of the reflux finding score among general otolaryngologists. J 2015;29(5):572–577.
- Belafsky PC, Postma GN, Koufman The validity and reliability of the reflux finding score (RFS). Laryngoscope.2001;111(8):1313–1317.
- Belafsky PC, Postma GN, Koufman Validity and reliability of the re- flux symptom index (RSI). J Voice.2002;16(2):274–277.
- Samuels TL, Johnston Pepsin as a marker of extraesophageal reflux. Ann Otol Rhinol Laryngol.2010;119(3):203–208.
- Farrell S, McMaster C, Gibson D, Shields, MD, McCallion Pepsin in bronchoalveolar lavage fluid: a specific and sensitive method of diagnos- ing gastro-oesophageal reflux-related pulmonary aspiration. J Pediatr Surg.2006;41(2): 289–293.
- Rosen R, Johnston N, Hart K, Khatwa U, Nurko The presence of pepsin in the lung and its relationship to pathologic gastro-esophageal reflux. Neurogastroenterol Motil.2012;24(2):129–133, e184-125.
- Spyridoulias A, Lillie S, Vyas A, Fowler SJ. Detecting laryngopharyngeal reflux in patients with upper airways symptoms: symptoms, signs or sal- ivary pepsin? Respir 2015;109(8):963–969.
- Decalmer S, Stovold R, Houghton LA, et al. Chronic cough: relation- ship between microaspiration, gastroesophageal reflux, and cough fre- Chest.2012;142(4):958–964.
- Pearson JP, Parikh S, Orlando RC, et Review article: reflux and its consequences — the laryngeal, pulmonary and oesophageal manifesta- tions. Conference held in conjunction with the 9th International Sympo- sium on Human 5 n basiC sCienCe Considerations for laryngopharyn- geal reflux 93Pepsin (ISHP) Kingston-upon-Hull, UK, 21–23 April 2010. Aliment Pharmacol Ther.2011;33(suppl 1):1–71.
- Suzuki T, Seki Y, Okamoto Y, Hoppo Hypopharyngeal multichan- nel intraluminal impedance leads to the promising outcome of antireflux surgery in Japanese population with laryngopharyngeal reflux symp- toms. Surg Endosc.2017;32(5):2409–2419.
- Corwin RW, Irwin The lipid-laden alveolar macrophage as a marker of aspiration in parenchymal lung disease. Am Rev Respir Dis.1985;132(3):576–581.
- Johnston N, Wells CW, Samuels TL, Blumin Pepsin in nonacidic refluxate can damage hypopharyngeal epithelial cells. Ann Otol Rhinol Laryngol.2009;118(9):677–685.
- Johnston N, Wells CW, Blumin JH, Toohill RJ, Merati Receptor-me- diated uptake of pepsin by laryngeal epithelial cells. Ann Otol Rhinol Lar- yngol.2007;116(12):934–938.
- Johnston N, Wells CW, Samuels TL, Blumin Rationale for target- ing pepsin in the treatment of reflux disease. Ann Otol Rhinol Laryn- gol.2010;119(8):547–558.
- Piper DW, Fenton pH stability and activity curves of pepsin with special reference to their clinical importance. Gut.1965;6(5):506–508.
- Johnston N, Dettmar PW, Bishwokarma B, Lively MO, Koufman JA. Ac- tivity/stability of human pepsin: implications for reflux attributed laryn- geal Laryngoscope. 2007;117(6):1036–1039.
- Samuels TL, Johnston Pepsin as a causal agent of inflammation during nonacidic reflux. Otolaryngol Head Neck Surg.2009;141(5):559–563.
- Johnston N, Yan JC, HoekzemaCR, et Pepsin promotes proliferation of laryngeal and pharyngeal epithelial cells. Laryngo- scope.2012;122(6):1317–1325.
- Kelly EA, Samuels TL, Johnston Chronic pepsin exposure promotes anchorage-independent growth and migration of a hypopharyngeal squamous cell line. Otolaryngol Head Neck Surg.2014;150(4):618–624.
- Martinucci I, de Bortoli N, Savarino E, et al. Optimal treatment of la- ryngopharyngeal reflux disease. Ther Adv Chronic Dis.2013;4(6):287–
- Ford CN. Evaluation and management of laryngopharyngeal reflux. 2005;294(12):1534–1540.
- Koufman JA, Aviv JE, Casiano RR, Shaw Laryngopharyngeal reflux: position statement of the committee on speech, voice, and swallowing disorders of the American Academy of Otolaryngology-Head and Neck Surgery. Otolaryngol Head Neck Surg.2002;127(1):32–35.
- Park W, HicksDM, Khandwala F, et Laryngopharyngeal reflux: prospective cohort study evaluating optimal dose of proton-pump inhibitor therapy and pretherapy predictors of response. Laryngo- scope.2005;115(7):1230–1238.
- Eherer AJ, Habermann W, Hammer HF, Kiesler K, Friedrich G, Krejs Effect of pantoprazole on the course of reflux-associated laryngitis: a placebo-controlled double-blind crossover study. Scand J Gastroenter- ol.2003;38(5):462–467.
- El-Serag HB, Lee P, Buchner A, Inadomi JM, Gavin M, McCarthy Lansoprazole treatment of patients with chronic idiopathic laryngitis: a placebo-controlled trial. Am J Gastroenterol.2001;96(4):979–983.
- Noordzij JP, Khidr A, Evans BA, et Evaluation of omeprazole in the treatment of relux laryngitis: a prospective, placebo-controlled, randomized, double-blind study. Laryngoscope.2001;111(12):2147–2151.
- Steward D Pantoprazole for sleepiness associated with acid relux and obstructive sleep disordered breathing. Laryngoscope.2004;114(9):1525–1528.
- Vaezi MF. Beneit of acid-suppressive therapy in chronic laryngitis: the devil is in the Clin Gastroenterol Hepatol.2010;8(9):741–742.
- Wo JM, Koopman J, Harrell SP, Parker K, Winstead W, Lentsch Double-blind, placebo-controlled trial with single-dose pantoprazole for laryngopharyngeal relux. Am J Gastroenterol.2006;101(9):1972–1978, quiz 2169.
- Lam PK, Ng, ML, Cheung TK, et al. Rabeprazole is efective in treating laryn- gopharyngeal relux in a randomized placebo-controlled trial. Clin Gastroenterol 2010;8(9):770–776.
- Reichel O, Dressel H, Wiederänders K, Issing Double-blind, placebocon- trolled trial with esomeprazole for symptoms and signs associated with laryngopharyngeal relux. Otolaryngol Head Neck Surg.2008;139(3):414–420.
- Kahrilas PJ, Shaheen NJ, Vaezi MF, et al; American Gastroenterological Asso- American Gastroenterological Association Medical position statement on the management of gastroesophageal relux disease. Gastroenterol. 2008;135(4): 1381–1391.
- Barry DW, Vaezi MF. Laryngopharyngeal relux: more questions than an- Cleve Clin J Med.2010;77(5):327–334.
- Gooi Z, Ishman SL, Bock JM, Blumin JH, Akst LM. Changing patterns in relux care: 10-year comparison of ABEA member Ann Otol Rhinol Laryn- gol.2015;124(12):940–946.
- Lugaresi M, Aramini B, Daddi N, Baldi F, Mattioli Efectiveness of anti- relux surgery for the cure of chronic cough associated with gastroesophageal relux disease. World J Surg.2015;39(1):208–215.
- Faruqi S, Sedman P, Jackson W, Molyneux I, Morice AH. Fundoplication in chronic intractable Cough.2012;8(1):3.
- Hoppo T, Komatsu Y, Jobe B Antirelux surgery in patients with chronic cough and abnormal proximal exposure as measured by hypopharyngeal multichannel intraluminal impedance. JAMA Surg.2013;148(7):608–615.
- Francis DO, Goutte M, Slaughter JC, et al. Traditional relux parameters and not impedance monitoring predict outcome ater fundoplication in ex- traesophageal rel Laryngoscope.2011;121(9):1902–1909.
- Tutuian R, Mainie I, Agrawal A, Adams D, Castell Nonac- id relux in patients with chronic cough on acid-suppressive therapy. Chest.2006;130(2):386–391.
- Iqbal M, Batch AJ, Moorthy K, Cooper BT, Spychal Outcome of surgical fundoplication for extra-oesophageal symptoms of relux. Surg Endosc.2009; 23(3):557–561.
- Carroll TL, Nahikian K, Asban A, Wiener D. Nissen fundoplication for la- ryngopharyngeal relux ater patient selection using dual pH, full column im- pedance testing: a pilot Ann Otol Rhinol Laryngol.2016;125(9):722–728.
- Campagnolo AM, Priston J, hoen RH, Medeiros T, Assunção AR. La- ryngopharyngeal relux: diagnosis, treatment, and latest researc Int Arch Otorhinolaryngol.2014;18(2):184–191.
- Hopwood D, Bateson MC, Milne G, Bouchier I Efects of bile acids and hydrogen ion on the ine structure of oesophageal epithelium. Gut. 1981;22(4): 306–311.
- Eto T, Tompkins RK. Further studies on the inhibition of pepsin by bile Ann Surg.1986;203(1):8–12.
- Ali MS, Parikh S, Chater P, Pearson JP. Bile acids in laryngopharyngeal reluxate: will they enhance or attenuate the action of pepsin? Laryngoscope.2013;123(2): 434–439.
- Bardhan KD, Strugala V, Dettmar PW. Relux revisited: advancing the role of pepsin. Int J Otolaryngol.2012;2012:646901.
- Francis DO, Rymer JA, Slaughter JC, et al. High economic burden of car- ing for patients with suspected extraesophageal rel Am J Gastroenter- ol.2013;108(6):905–911.
- Belafsky PC. PRO: Empiric treatment with PPIs is not appropriate without Am J Gastroenterol.2006;101(1):6–8.
- Carroll TL, Werner A, Nahikian K, Dezube A, Roth Rethinking the laryngopharyngeal relux treatment algorithm: evaluating an alternate empir- ic dosing regimen and considering up-front, pH-impedance, and manometry testing to minimize cost in treating suspect laryngopharyngeal relux disease. Laryngoscope.2017;127(suppl 6):S1–S13.
Tham khảo thêm một số bài viết cùng chủ đề





