Bài viết Khó nuốt trong ho mạn tính: chẩn đoán và hướng điều trị được biên dịch bởi BS. CK1 Hồ Thị Hoài Thu và BS. Trần Minh Dũng từ Sách “Ho Mạn Tính: Nguyên nhân, chẩn đoán và điều trị” của tác giả Mark A. Fritz, Debra M. Suiter, and Gregory N. Postma.
1. Sơ lược
Những bệnh nhân có triệu chứng ho mạn tính thường phàn nàn về khó nuốt. ho có thể liên quan tới rối loạn chức năng nuốt của họ từ nguyên nhân căn bản được tìm thấy ở họng thanh quản hoặc thực quản và có thể là triệu chứng duy nhất của họ. Sự hít vào hoặc xâm nhập của chất lỏng hoặc thức ăn vào thanh quản gây nên một phản xạ ho sâu ở những cá thể bình thường như là một cơ chế bảo vệ để ngăn chăn các mảnh nhỏ khỏi xâm nhập vào hệ hô hấp vô trùng. Khi sự hít vào trở thành bệnh lí, gây ra triệu chứng ho hoặc, nghiêm trọng hơn là viêm phổi hít, tầm quan trọng của việ điều trị bệnh nhân chuyển từ vấn đề chất lượng sống sang sống còn.
Có nhiều lí do tại sao một bệnh nhân có cả triệu chứng khó nuốt và nguyên nhân thường gặp nhất ở bệnh nhân cảm thấy ho và khó nuốt là bệnh trào ngược, và điều nào được đề cập kĩ trong chương 4. Bệnh thần kinh phế vị sau nhiễm siêu vi có thể xảy ra sau một đợt nhiễm virus, như là nhiễm trùng hô hấp trên, và có thể biểu hiện với một số các triệu chứng ở vùng hô hấp – tiêu hóa bao gồm ho; điều này được thảo luận trong chương 5. Cả nhánh thần kinh vận động và cảm giác đều bị ảnh hưởng, và bệnh nhân thường kể lại vấn đề cảm giác vướng họng, ngứa họng, khó nói, hắng giọng và nghẹn họng. thêm vào đó, bệnh nhân có thể có triệu chứng ho và than phiền về khó nuốt sau đặt nội khí quản hoặc sau tai biến mạch máu não, cả hai đều có khả năng cao mắc bệnh hơn so với những điều đã nói ở trên. Khám sàng lọc được thực hiện, thường gặp nhất bởi chuyên gia âm ngữ trị liệu, để xác định liệu phản xạ ho và nuốt của bệnh nhân có nguyên vẹn để ngăn chặn bị tàn phá do các đợt hít phải trước khi cho ăn bằng miệng được tiếp tục lại.
Đánh giá chính xác các cá nhân bị hít phải do khó nuốt ở họng miệng là vấn đề rất quan trọng. khó nuốt không nhận biết có thể dẫn đến hậu quả nghiêm trọng về sức khỏe cho bệnh nhân, bao gồm mất nước, suy dinh dưỡng, viêm phổi hít, và thậm chí chết. khi một bệnh nhân than phiền về triệu chứng khó nuốt trong hoàn cảnh ho mạn tính, điều quan trọng là cần xác đinh liệu những than phiền này có phù hợp với chứng khó nuốt ở thực quản hay họng miệng và không được xem là do bệnh lí trào ngược. trong chương này, chúng tôi sẽ xem xét đánh giá về việc sự nuốt ở thực quản và hạ họng ở bệnh nhân ho mạn tính.
2. Tầm soát khó nuốt
Bệnh nhân mắc vấn đề về nuốt và ho mạn tính sẽ thường được điều trị tối thiểu bởi một bác sĩ tai mũi họng và một chuyên gia âm ngữ trị liệu (SLP). Bệnh nhân ở bệnh viện với chứng khó nuốt mới khởi phát sẽ được tầm soát ban đầu để đánh giá tình trạng nuốt (xem danh sách bên dưới). Ngược lại , với bệnh nhân ngoại trú, bệnh nhân tìm đến cả SLP lẫn bác sĩ tai mũi họng tùy vào giấy giới thiệu. Đội ngũ tiếp cận với những bệnh nhân mắc bệnh phức tạp này rất quan trọng cho cả chẩn đoán và can thiệp. Các chuyên khoa bổ trợ thường liên quan tới điều trị khó nuốt đi kèm với ho mạn tính bao gồm bác sĩ khoa hô hấp, tiêu hóa và thần kinh.
Khi một bệnh nhân có triệu chứng ho mạn tính, các triệu chứng khó nuốt nên được phát hiện và theo dõi thêm nếu cần thiết. Các câu hỏi gặt hái được nhiều lợi ích gồm:
- Bạn có vấn đề về nuốt thức ăn lỏng không?
- Bạn có bị nghẹt thở hoặc hít phải chất lỏng không?
- Bạn có sụt cân không?
- Bạn có phải tránh thức ăn cụ thể nào không?
- Bạn đã từng xạ trị vùng đầu và/hoặc cổ chưa
- Bạn có tiền sử nhiễm trùng hô hấp, bao gồm viêm phổi chưa?
- Bạn có tiền sử phẫu thuật đầu cổ không?
- Bạn có từng trào ngược thức ăn chưa?
Một phản hồi tích cực cho 1 trong những câu này đều gợi ý chứng khó nuốt, đảm bảo việc khám toàn diện để xác định có liên quan của chứng khó nuốt tới bệnh nhân ho mạn tính. Bác sĩ tai mũi họng phải luôn thực hiện nội soi thanh quản ống mềm cho bệnh nhân ho mạn tính hoặc khó nuốt, vì nó sẽ chỉ ra những thay đổi về cấu trúc giải phẫu mà có thể giải thích các vấn đề, như khối u thanh quản, khoảng trống thanh môn lớn kèm hoặc không liệt dây thanh âm, hoặc lượng lớn nước bọt pooling đọng ở xoang lê. Nếu trên lâm sàng nghi ngờ nhiều, các xét nghiệm thêm là cần thiết bất kể các dấu hiệu trên nội soi lần đầu.
Bước đầu trong việc đánh giá chính xác chứng khó nuốt của họng miệng là sàng lọc. trong tài liệu “những mô hình thực hành ưa thích cho chuyên gia về âm ngữ trị liệu”, Hội thính học-Âm-Ngữ Hoa Kì đã định nghĩa sáng lọc chứng khó nuốt là “một thủ tục vượt qua/thất bại để xác định các cá nhân cần đánh giá toàn diện về chức năng nuốt hoặc giới thiệu tới các chuyên ngành khác và / hoặc các dịch vụ y khoa. Sàng lọc được thực hiện một cách đặc thù bởi SLP (chuyên gia âm ngữ trị liệu) ở phòng khám hoặc bởi các nhà cung cấp dịch vụ chăm sóc sức khỏe khác như y tá bệnh viện. cá nhân được sàng lọc đều được xem như có hoặc không nguy cơ mắc chứng khó nuốt họng miệng.
Các công cụ sàng lọc là phương tiện nhanh chóng và hiệu quả, và để tiết kiệm thời gian cũng như tiền bạc bằng các xác định những ai mà có nguy cơ khó nuốt và hít sặc, và ai cần đánh giá thêm. Sàng lọc cho phép bác sĩ xác định những người thực sự cần đánh giá đầy đủ, tốn kém hơn và tốn thời gian hơn và ngăn chặn sử dụng những nguồn lực không cần thiết cho những người không cần.
Nhiều phương pháp sàng lọc đã được đề xuất. một số đề nghị sàng lọc nên bao gồm tiếp cận chỉ bằng bảng câu hỏi. mặc dù ban đầu nó được dự định là một công cụ kết quả, có những bằng chứng cho thấy công cụ đánh giá ăn uống EAT-10 có thể được dùng như một công cụ tiên đoán nguy cơ hít sặc. các phương pháp khác để sàng lọc bao gồm triệu chứng khi nuốt một hoặc nhiều “khối tròn” boluses . Những bolus đó là gì và số lượng bolus được bao gồm khác nhau cái gì. Nhiều sàng lọc kết hợp với các test nuốt nước, mặc dù kích cỡ bolus khác nhau giữa các sàng lọc nước khác. Một số sử dụng lên đến 10 khối tròn nhỏ từ 3-5 ml nước, trong khi số khác kết hợp với những thể tích nước lớn hơn từ 90-100ml. một đánh giá hệ thống mới đây và phân tích tổng hợp của phương pháp sàng lọc mà kết hợp thử nghiệm nuốt nước cho thấy độ đặc hiệu cao nhưng độ nhạy thấp với thể tích khối tròn nhỏ, trong khi các test nuốt nước kết hợp từng hớp liên tục với thể tích khối tròn lớn (90-100ml) cho thấy độ nhạy cao nhưng độ đặc hiệu thấp. trong thực hành lâm sàng và do độ nhạy cao hơn, tầm soát bằng khối tròn lớn dường như là một công cụ sàng lọc tốt hơn cho những ai thực sự có hít sặc mà không được phát hiện.
Nếu bệnh nhân vượt qua được sàng lọc nhạy, đáng tin, hợp lí, một đánh giá chức năng nuốt đầy đủ như là phương tiện đánh giá nuốt (nghĩa là nuốt barium đã hiệu chỉnh) không cần thiết và bệnh nhân có thể an toàn để bắt đầu dùng thuốc, chất lỏng và thức ăn mà không cần đánh giá thêm.
Một sàng lọc thất bại cho thấy đánh giá thêm là cần thiết. trong trường hợp khó nuốt, một bệnh nhân mà thất bại với sàng lọc đáng tin cậy và hợp lệ nên được chuyển tới một SLP để đánh giá thêm.
3. Đánh giá khó nuốt trên lâm sàng
Việc đánh giá khó nuốt trên lâm sàng CSE thường là mức đánh giá kế tiếp trong việc đánh giá các cá nhân có nguy cơ mắc chứng khó nuốt họng miệng. theo như ASHA, CSE cho phép SLP:
- Tích hợp thông tin từ bệnh án / phỏng vấn, xem xét hồ sơ y khoa, và quan sát từ khám sức khỏe.
- Quan sát và đánh giá tính toàn vẹn và chức năng của các cấu trúc đường hô hấp trên và ống tiêu hóa.
- Xác định sự hiện diện và đánh giá đặc trưng của chứng khó nuốt dựa trên các dấu hiệu và triệu chứng lâm sàng .
- Xác định các dấu hiệu lâm sàng và triệu chứng của chứng khó nuốt thực quản hoặc bệnh lí trào ngược dạ dày thực quản
- Xác định nhu cầu khám bằng công cụ ( đánh giá chức năng nuốt khách quan hơn).
- Xác dịnh liệu bệnh nhân có là một ứng viên phù hợp để điều trị và / hoặc quản lí không.
- Đề xuất một lộ trình về kiểm soát dinh dưỡng phù hợp.
- Đề nghị can thiệp lâm sàng.
4. Chỉ định đánh giá nuốt lâm sàng
Điều quan trọng với SLP là hiểu điều gì đã thúc đẩy một giấy giới thiệu tới CSE và điều gì mà người giới thiệu lo lắng chủ yếu liên quan đến bệnh nhân. Nếu một sàng lọc được chỉ định, thất bại dẫn đến việc hội chẩn lâm sàng hoặc đánh giá bằng công cụ. trong các trường hợp khác, bác sĩ có thể chuyển trực tiếp tới SLP mà không cần bệnh nhân hoàn tất sàng lọc trước. việc giới thiệu để CSE có thể dựa trên chẩn đoán y khoa của bệnh nhân hoặc tình trạng dinh dưỡng của bệnh nhân.
Thường các than phiền của bệnh nhân thúc đẩy các bác sĩ giới thiệu đến SLP để làm CSE. Các bệnh nhân có thể than phiền về ho thường xuyên hoặc nuốt nghẹn trong bữa ăn, cảm giác như thức ăn hoặc chất lỏng bị kẹt khi họ cố gắng nuốt, hoặc kéo dài thời gian bữa ăn. Họ cũng than phiền về đau liên quan tới nuốt, nuốt đau, hoặc thức ăn hoặc chất lỏng chảy ra từ mũi họ khi họ cố gắng nuốt. Bất kì than phiền nào trong đây có thể chỉ ra vấn đề nuốt tiềm ẩn và dẫn đến việc giới thiệu để CSE.
5. Thành phần của đánh giá nuốt lâm sàng.
5.1. Đánh giá biểu đồ
Bước đầu tiên trong việc đánh giá là xem xét biểu đồ kĩ lưỡng. Đánh giá biểu đồ hỗ trợ các bác sĩ trong việc đề ra giả thuyết liên quan bản chất của bệnh nhân khó nuốt.
Trong trường hợp bệnh nhân ho mạn tính, điều đặc biệt quan trọng là lưu ý bất kì bệnh lí hiện tai hoặc trước đó mà tương ứng với các triệu chứng khó nuốt mới xuất hiện, chẳng hạn như nhiễm trùng hô hấp trên gần đây. Nếu bệnh nhân có tiền sử bệnh hô hấp trên thường xuyên, hít sặc mạn tính nên được cân nhắc như là một nguyên nhân có thể. Sự hiện diện của viêm phổi hoặc tiền sử viêm phổi có khả năng dự báo cao nguy cơ hít sặc. tiền sử nhiễm trùng hô hấp trên hoặc suy hô hấp cần đặt nội khí quản hoặc mở khí quản cần được chú ý. Đặt nội khí quản nhiều lần hoặc rút ống nội khí quản, hoặc chấn thương khi đặt nội khí quản, rút khí quản có thể dẫn đến kích thích thanh quản hoặc giảm di động dây thanh, với ho mạn tính xảy ra do hít phải hoặc xâm nhập khi đối mặt với thanh môn bất toàn. Ngoài ra, các bác sĩ cần chú ý liệu bệnh nhân có tiền sử trào ngược dạ dày thực quản không và liệu bệnh nhân đang điều trị thuốc để kiểm soát triệu chứng trào ngược không. LPR có thể dẫn đến kích thích thanh quản và hạ họng và, quan trọng hơn, được xem như gây ra chứng tăng chức năng cơ vòng thực quản trên dẫn đến cảm giác khó nuốt. LPR đã được bàn luận chi tiết ở chương 4.
Tiền sử phẫu thuật nên được đánh giá. Cụ thể, tiền căn phẫu thuật đầu cổ, bao gồm mở khí quản hoặc phẫu thuật cắt bỏ khối u đầu cổ, nên được chú ý. Phẫu thuật có thể dẫn đến thay đổi cấu trúc giải phẫu mà đưa đến sự thay đổi sinh lý nuốt. tiền sử cho ăn bằng ống thông có thể cho thấy tiền sử khó nuốt hoặc suy dinh dưỡng.
Đánh giá biểu đồ cũng nên bao gồm đánh giá các thuốc hiện tại. một số thuốc nhất định có thể ảnh hưởng xấy tới chức năng nuốt, như là cả tác dụng phụ thông thường cũng như biến chứng điều trị của thuốc.
Các thuốc ảnh hưởng tới chức năng cơ trơn hoặc cơ vân thực quản có thể gây ra chứng khó nuốt. khó nuốt do biến chứng điều trị nội bao gồm viêm thực quản do virus hoặc nấm ở bệnh nhân được điều trị với thuốc ức chế miễn dịch hoặc thuốc điều trị ung thư, hoặc thuốc làm suy yếu hệ thần kinh trung ương như benzodiazepines. Ngoài ra, một số thuốc như Kháng viêm nonsteroid NSAIDS có thể gây ra viêm thực quản, chít hẹp thực quản, hoặc loét thực quản khi sử dụng thường xuyên, dẫn đến các triệu chứng khó nuốt. Các thuốc khác có thể gây ra chứng khô miệng (xe- rostomia) và dẫn cản trở quá trình di chuyển qua đường miệng của “cục thức ăn”, dẫn đến kích thích thanh quản, tạo mô hạt particulate retention, và dẫn đến ho mạn tính. Các bác sĩ nên chú ý liệu bệnh nhân có được kê đơn ức chế men chuyển angiotensin (ACEI) không, vì ho mạn tính có thể xảy ra như là tác dụng phụ ở 10% người dùng thuốc này, và xảy ra thường xuyên ở phụ nữ hơn là đàn ông.
5.2. Bệnh án Case history
Bước tiếp theo trong đánh giá lâm sàng là tiền sử kĩ lưỡng. Mục đích của bệnh án là hỗ trợ bác sĩ trong việc đề ra giải thiết liên quan tới sinh lí bệnh tiềm ẩn gây ra các triệu chứng của bệnh nhân. Thông tin được tập trung trong bệnh án có thể là vô giá trong việc xác định phương pháp đánh giá chức năng nuốt phù hợp, ví dụ nội soi huỳnh quang hoặc nội soi thông thường, và trong việc xác định liệu có cần được tư vấn với chuyên khoa khác như tiêu hóa hay thần kinh không.
5.3. Lí do nhập viện
Lí do thường gặp của bệnh nhân bao gồm ho, nghẹt thở hoặc nghẹn thức ăn hay chất lỏng, thức ăn hoặc chất lỏng bị dính trong họng, khó nhai và thời gian ăn kéo dài. Ở bệnh nhân có tiền sử ho mạn tính, điều đặc biệt quan trọng là hỏi liệu ho tăng lên trong hoặc sau khi ăn uống không. Ho tăng trong khi ăn có thể chỉ ra sự xâm nhập hoặc hít sặc thức ăn hay chất lỏng. ho tăng sau bữa ăn có thể chỉ ra trào ngược, rối loạn vận động thực quản, hoặc túi thừa Zenker. Ngoài ra, bệnh nhân than phiền về cảm giác như là thức ăn bị vướng, khó nuốt thức ăn đặc (thường là bánh mì hoặc bít tết), hoặc khó nuốt chất lỏng ở nhiệt độ quá cao lẫn quá lạnh, có thể chỉ ra một vấn đề về mặt thực quản hơn là khó nuốt họng miệng.
5.4. Triệu chứng cơ năng
Các bác sĩ cũng nên hỏi bệnh nhân về mốc thời gian của chứng khó nuốt. các câu hỏi nên bao gồm khoảng thời gian của các triệu chứng khó nuốt, liệu bệnh nhân có trải qua bất kì bệnh lí nào ở thời điểm các triệu chứng khó nuốt bắt đầu, và liệu các triệu chứng thay đổi tùy theo thời gian trong ngày. Bệnh nhân kể lại các triệu chứng mà tệ hơn khi thức dậy và / hoặc ngay sau đó có thể liên quan tới trào ngược dạ dày thực quản, trong khi những bệnh nhân kể về tiến triển của các triệu chứng của họ suốt cả ngày hoặc suốt bữa ăn có thể bị yếu cơ hoặc mệt mỏi liên quan tới một tình trạng thần kinh tiềm tàng. Những thay đổi về chất lượng âm thanh mà đi cùng với chứng khó nuốt mới khởi phát của bệnh nhân có thể chỉ ra bệnh lí dây thanh âm và chắc chắn cần xem kĩ hơn với nội soi hoạt nghiệm thanh quản. Ví dụ vấn đề cảm giác họng miệng mà dẫn tới ứ đọng thức ăn hạ họng và tràn vào thanh quản khiến giọng nói có vẻ “ướt át” .
5.5. Thăm khám cơ chế miệng
Một thành phần quan trọng khác của CSE là thăm khám cơ chế miệng. tính toàn vẹn của môi, lưỡi, mặt, khẩu cái cứng và mềm, răng, sức khỏe miệng và hàm cần được đánh giá khi ngỉ ngơi và trong khi vận động chức năng. Thăm khám cơ chế miệng có thể giúp các bác sĩ hình thành giả thuyết liên quan bản chất rối loạn nuốt của bệnh nhân. Thăm khám cơ chế miệng cung cấp một phương tiện đánh giá tính toàn vẹn của các dây thần kinh sọ liên quan trong quá trình nuốt và có thể chỉ ra khía cạnh của chức năng nuốt bị suy giảm. Các thần kinh sọ tham gia vào quá trình nuốt là: thần kinh tam thoa V, mặt VII, thiệt hầu IX, lang thang X, và hạ thiệt XII. ở bệnh nhân ho mạn tính, đánh giá chức năng thần kinh lang thang là đặc biệt quan trọng. thần kinh thiệt hầu và thần kinh lang thang thường tổn thương cùng nhau. Vì vậy, tính toàn vẹn của những thần kinh này có thể được đánh giá đồng thời. các bác sĩ nên quan sát vòm miệng mềm (khẩu cái mềm) khi nghỉ ngơi và trong khi nâng lên (nghĩa là khi nói “Ah”). Chất lượng giọng nói có thể chỉ ra chức năng của những thần kinh này. Chất lượng giọng hơi có thể chỉ ra rối loạn chức năng dây thanh cùng bên hoặc đối bên mà đặt bệnh nhân vào tăng nguy cơ hít sặc do giảm bảo vệ đường thở trong khi nuốt. Có một số nghiên cứu cho thấy sự hiện diện của rối loạn giọng, bao gồm giọng thều thào, giọng thô, hoặc khàn giọng, được xem như dự báo của hít sặc. Các nghiên cứu khác cho rằng giảm cao độ lại là dự báo của rối loạn giọng do cùng tồn tại các vấn đề cảm giác liên quan tới bệnh thần kinh thanh quản trên. Các bác sĩ cũng có thể muốn gợi một phản ứng nôn từ bệnh nhân của họ để đánh giá tính toàn vẹn của dây thần kinh sọ IX và X. tính toàn vẹn của ho chủ động của bệnh nhân có thể được dùng để đánh giá chức năng thần kinh thiệt hầu và lang thang.
Các phép đo khách quan về ho chủ động, bằng cách dùng các công cụ như phế đồ ký (Pneumotachograph), có độ nhạy và độ đặc hiệu cao để xác định nguy cơ hít sặc. Smith-Hammond đã phát hiện sự giảm đáng kể lưu lượng thở ra đỉnh (Peak expiratory Airflow) ở các bệnh nhân rối loạn nuốt sau đột quỵ. Những người bị hít sặc nghiêm trọng đã biểu hiện lưu lượng thở ra đỉnh thấp nhất trong ho chủ động (ho tự ý). Ngoài ra, tỉ lệ lưu lượng thở ra đỉnh ở các bệnh nhân Parkinson mà hít sặc so sánh với những bệnh nhân hít sặc. Cuối cùng, lưu lượng ho đỉnh có thể được dùng để dự đoán những biến chứng hô hấp do hít sặc ở những bệnh nhân rối loạn nuốt.
Một phương pháp đánh giá tính toàn vẹn của phản xạ ho là test phản xạ ho, trong đó bệnh nhân được yêu cầu chủ động hoặc thụ động hít thở một dung dịch chứa acid tartaric, acid citric hoặc capsaicin. Tính toàn vẹn của cả phản ứng ho tự nhiên lẫn phản ứng ho bị ức chế được đánh giá. Phản ứng ho bất thường hoặc giảm sau khi hít các dung dịch này được phát hiện là có thể dự đoán nguy cơ viêm phổi ở bệnh nhân đột quỵ trong một vài nghiên cứu nhưng không phỉa trong những nghiên cứu khác.
5.6. Áp dụng bolus
Khi thực hiện CSE, một giao thức chuẩn hóa về việc áp dụng bolus cần được khuyến khích. Tiêu chuẩn hóa các loại bolus, số lượng các bolus, và lượng bolus cho phép để so sánh hành vi của các bệnh nhân qua thử nghiệm. ngoài ra, nó đảm bảo tính nhất quán qua các bác sĩ lâm sàng và qua các phương tiện. Điển hình, một CSE sẽ bao gồm việc đưa vào một dung dịch loãng (thường là nước), một bolus bột hoặc pudding, và một chất rắn đặc. Từng loại bolus có thể được đưa vào với lượng khác nhau, thường tiến triển từ lượng rất nhỏ và tiến triển tới lượng lớn mà được cân nhắc để phản chiếu hành vi bệnh nhân điển hình (nghĩa là, nhấp một ly chất lỏng loãng hoặc tự ăn pudding hoặc bo- lus rắn). các bệnh nhân được quan sát cho bất kỳ dấu hiệu / triệu chứng nào về chứng khó nuốt họng miệng.
Vấn đề giai đoạn miệng có thể được quan sát bao gồm giảm dấu hiệu môi dẫn đến rò rỉ bolus khỏi ổ miệng, việc nhai các kết cấu rắn mất thời gian và không hiệu quả, và đọng lại trong ổ miệng. một ít thông tin về tính toàn vẹn của giai đoạn họng trong việc nuốt có thể được lượm lặt từ CSE. Cấu trúc trong họng, như đáy lưỡi, thành họng sau, rãnh lưỡi thanh thiệt (thung lũng), và xoang lê, không thể nhìn thấy mà không có sự trợ giúp của các dụng cụ như nội soi hay xquang. Mặt khác, các dấu hiệu và triệu chứng của hít sặc có thể được xác định trong CSE. Ho là một trong những dấu hiệu hít sặc đáng tin cậy nhất. chất lượng giọng ướt lập tức sau khi nuốt cũng được đề xuất có giá trị dự đoán để xác định hít sặc. Tuy nhiên, các bác sĩ không chắc chắn nhận biết được chất lượng giọng ướt khi có chất đọng lại trong thanh quản trong quá trình phát âm, và đánh giá chất lượng âm thanh thiếu nhạy và đặc hiệu để phát hiện hít sặc. vì vậy, các bác sĩ nên cân nhắc việc giới thiệu đến hoặc thực hiện nội soi hoạt nghiệm nếu giọng nói bất thường nhưng nên thận trọng khi đưa ra những phán đoán về nguy cơ hít sặc mà chỉ dựa trên sự thay đổi về chất lượng âm thanh. Khả năng là bệnh nhân sẽ xuất hiện các dấu hiệu/ triệu chứng hít sặc quá mức tùy vào thể tích bolus. Đưa thể tích bolus nhỏ từ 1-5 ml thiếu độ nhạy đủ để xác định hít sặc và bệnh nhân mà hít sặc im lặng có thể không được xác định nếu chỉ với thể tích bolus nhỏ.
Thể tích bolus lớn từ 90-100ml có độ nhạy cao để xác định hít sặc, và các bệnh nhân mà hít sặc im lặng khi được đưa vào lượng bolus nhỏ thì ít biểu hiện hơn là khi dùng bolus lớn. mặc dù dễ sử dụng và hữu ích lâm sàng của CSE, môt bài báo đánh giá mới đây đã cho thấy độ nhạy và đặc hiệu của test nuốt nước so với tiêu chuẩn hình ảnh Xquang hoặc nội soi là 71% và 90% lần lượt, đối với những lượng ngụm đơn lẻ, 91% và 53% cho những thử nghiệm liên tiếp 90-100ml, và 86% với 65% cho tăng dần lượng nước.
6. Dụng cụ đo đạc
6.1. Các bước kế tiếp
Nếu bệnh nhân không biểu hiện dấu hiệu hoặc triệu chứng quá mức của hít sặc hoặc khó nuốt, và nếu bệnh nhân ổn định về mặt y tế, các bác sĩ có thể khuyến cáo chế độ ăn uống. nếu các dấu hiệu hoặc triệu chứng hít sặc hoặc khó nuốt quá mức được quan sát trong khi CSE, một công cụ đánh giá như quay video với chất cản quang hoặc nội soi được khuyến khích.
6.2. Chụp X-quang cản quang
Khảo sát nuốt bằng Chụp X-quang cản quang, còn được gọi là nghiệm pháp nuốt barium cải tiến, là một quy trình chụp xquang trong khi nuốt được đánh giá theo thời gian thực. Nó được coi là tiêu chuẩn vàng trong đánh giá các giai đoạn nuốt ở miệng, họng, và miệng thực quản.
Mục đích của VFSS là xác định cơ chế sinh lí bệnh nuốt tiềm ẩn dẫn đến các triệu chứng khó nuốt của bệnh nhân và xác định lựa chọn điều trị thích hợp. Bệnh nhân được cho một liều barium sulfate uống, từ lỏng tới đặc, và cử động nuốt được quan sát từ mặt bên và trước sau. Cũng như với CSE, một giao thức chuẩn hóa được khuyến cáo. Vì VFFS là một quá trình chụp xquang, là một bài kiểm tra giới hạn thời gian. Thời gian chụp X-quang thường giới hạn trong 5 phút hoặc ít hơn.
Trong khi VFSS, các cấu trúc chuyển động bao gồm vận động của lưỡi, nâng màn hầu, vận động lên trên ra trước của xương móng, nâng thanh quản, đậy nắp thanh quản, co rút lại của đáy lưỡi, mở đoạn họng thực quản, và sóng nhu động thực quản được quan sát. Ngoài ra, thời gian của các đợt nuốt, gồm thời gian vận chuyển của miệng, khởi động quá trình nuốt ở họng, thời gian vận chuyển của họng, và khoảng thời gian mở cơ nhẫn hầu được đánh giá. Các bác sĩ nên chú ý sự hiện diện của chất lắng đọng ở vị trí khác nhau gồm khoảng lợi-má 2 bên, nền lưỡi, thành sau họng, nếp giữa rễ lưỡi – nắp thanh môn, và xoang lê cũng như phản ứng của bệnh nhân với chất tồn đọng. trong một số trường hợp, một lượng rất nhỏ chất lắng đọng vẫn còn sót lại trong họng sau khi nuốt sẽ tạo một kích thích đủ để khiến bệnh nhân ho hoặc hắng giọng. Sự xâm nhập, được định nghĩa là chất lỏng hoặc thức ăn đi qua tiền đình thanh quản nhưng không tràn xuống dưới dây thanh âm, và/hoặc hít sặc, được nghĩa là chất lỏng hoặc thức ăn tràn dưới dây thanh âm, nên được chú ý như là vấn đề sinh lí bệnh tiềm ẩn mà dẫn đến dấu hiệu. một lần nữa, phản ứng của bệnh nhân hoặc thiếu phản ứng tới xâm nhập hoắc hít sặc cần được báo cáo. Điều đặc biệt quan trọng là liệu bênh nhân có đáp ứng với ho hoặc hắng giọng với hít sặc, một đợt được biết là “hít sặc thầm lặng” khi không có đáp ứng.
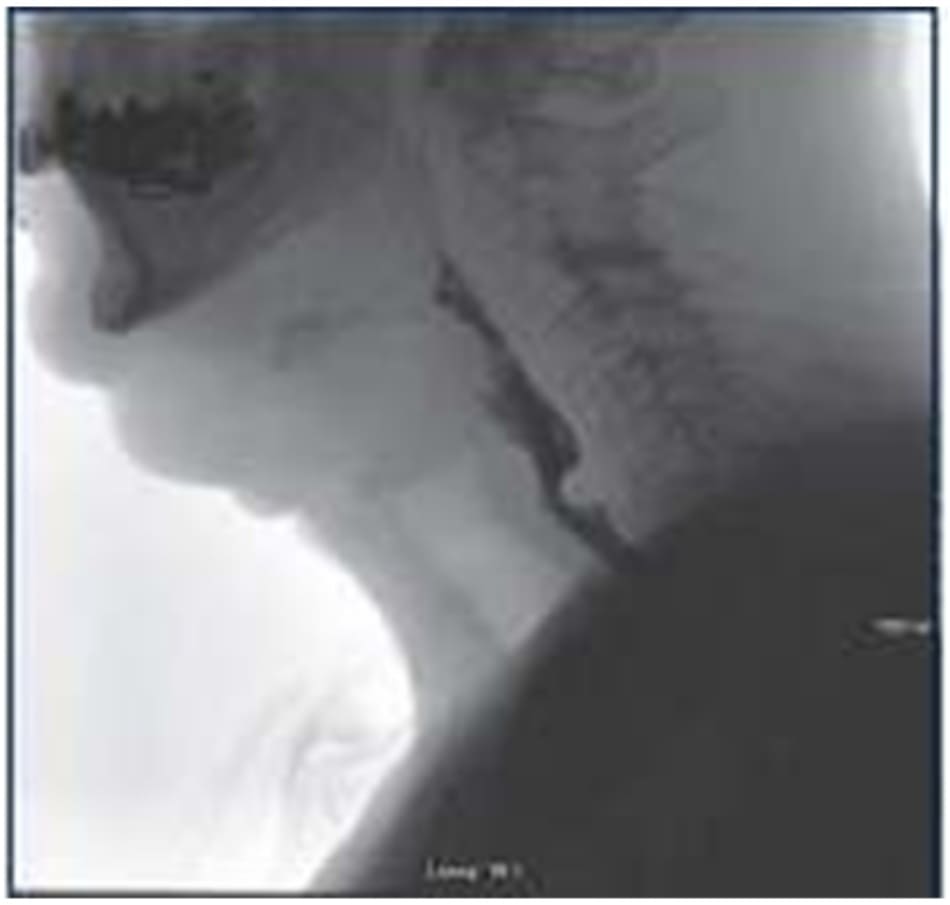
Một dấu hiệu thông thường ở VFSS là hiện diện của thanh chắn nhẫn hầu ở đoạn họng thực quản. một thanh chắn nhẫn hầu được định nghĩa là một gờ liên tục của vùng cơ nhẫn hầu trong quá trình nuốt khi nó không giãn ra được nhìn thấy ở mặt bên trên phim xquang (Hình 7-1). Thanh chắn nhẫn hầu được cho là có ý nghĩa khi nó chiếm hơn 50% khoảng không gian trong lòng thực quản khi chứa đầy chất tương phản và liên quan đến việc giảm kích thước tối đa của cơ thắt thực quản trên UES, được cho là nguyên nhân làm tăng áp lực khối thức ăn ngược dòng lên cơ UES.
6.3. Nội soi ống mềm đánh giá nuốt FEES
Nội soi ống mềm đánh giá nuốt FEES được giới thiệu vào những năm 1980 như một công cụ bổ trợ cho VFSS. Nó liên quan tới việc đưa ống nội soi mềm hoặc chip nội soi đầu xa qua đường mũi vào họng miệng cho phép quan sát tốt hơn những cấu trúc của họng và thanh quản. Các cấu trúc hạ họng và trong thanh quản được đánh giá trước và sau thì nuốt của họng. vì nội soi được đặt qua khoang mũi, thì miệng không được quan sát. Trong khi bắt đầu quá trình nuốt của họng, đầu của ống nội soi bị làm chệch hướng khi nền lưỡi tiếp xúc với thành sau họng. khoảng thời gian này, được biết với cái tên “White-out”, đặc trưng là kéo dài ít hơn 0.5 giây. Các cấu trúc có thể được đánh giá tiếp sau khi hoàn tất thì họng.
Trước khi đặt ống nội soi, các bác sĩ nên sử dụng thuốc gây tê tại chỗ như lidocaine (loại sệt), và / hoặc một thuốc co mạch như oxymetazo- line (Afrin) để tạo sự thoải mái cho bệnh nhân trong khi khám. Các bác sĩ nên cẩn thận để đảm bảo rằng thuốc gây tê được sử dụng ở đầu cuốn mũi chứ không phải say đó vì có khả năng thuốc gây tê đi vào vùng họng. Chức năng nuốt có thể bị ảnh hưởng bất lợi nếu điều này xảy ra. Gây mê có thể tác động tiêu cực tới chức năng nuốt bằng cách thay đổi thời gian thông thường của luồng bolus và giảm độ nhạy cảm với chất xâm nhập hay hít sặc. Ở bệnh nhân ho mạn tính, đặc biệt không cần gây tê họng thanh quản vì bác sĩ muốn quan sát bất kì phản ứng nào của bệnh nhân với vị trí ống soi, chất cặn, hoặc sự xâm nhập / hít sặc. nhiều bệnh nhân có thể chịu đựng việc đặt ống nội soi mà không cần thuốc gây tê tại chỗ hoặc co mạch.
Một FEES điển hình với việc quan sát chức năng hầu-màn hầu. các bệnh nhân lặp lại một loạt các âm tiết chứa âm vị mũi (/n/, /m/, /ng/) và không chứa âm vị mũi ( bất kì nguyên âm hoặc phụ âm nào khác). Sự đầy đủ và kiểu hình của đóng hầu – màn hầu được chú ý. Nhà nội soi sau đó đưa đầu ống nội soi vào khẩu hầu. Ở đây, nội soi quan sát cấu trúc của thanh quản và hạ họng bao gồm đáy lưỡi, thành sau họng, thanh môn, thung lũng thanh thiệt – nắp thanh môn, xoang lê, nếp phễu – thanh thiệt, tiền đình thanh quản, dây thanh giả, dây thanh thật, hạ thanh môn, và vùng trên khí quản. điều quan trọng là cần lưu ý sự hiện diện và vị trí của bất kì dịch tiết nào. Trước khi phân loại thức ăn hoặc chất lỏng hiện diện ở bệnh nhân, sự hiện diện của dịch tiết trong lòng thanh quản cho thấy rất có thể có sự tăng hít sặc chất lỏng loãng và giảm nhạy cảm thanh quản. các bác sĩ cũng cần quan sát chất tiết do hít sặc của bệnh nhân.
Điều này là không thể quan sát được trong VFSS. Nếu đánh giá sự hít sặc của chất tiết, các bác sĩ có thể chọn không sử dụng bất kì boluses nào cho bệnh nhân trong khi khám.
Việc đánh giá độ nhay cảm của họng và thượng thanh môn của thanh quản và do đó, tình toàn vẹn của thần kinh thanh quản trên và sự bảo vệ đường thở, được đề xuất như là một biện pháp hỗ trợ cho nội soi truyền thống đành giá nuốt. Nội soi ống mềm đánh giá nuốt với test cảm giác được giới thiệu vào những năm 1990. Việc sử dụng ống nội soi mềm 2 kênh đặc biệt, một miếng bông xốp được đưa tới nếp phễu thanh thiệt, kích thích phản ứng khép thanh quản (LAR). Sự vắng mặt của LAR được xem như một dấu hiệu của tăng nguy cơ hít sặc thầm lặng trong việc khám chức năng nuốt sau đó. Các giá trị quy chuẩn cho ngưỡng phản ứng với bông xốp đang thiếu và những trang thiết bị chuyên dụng cần thiết để thực hiện FEEST không còn có sẵn trên thị trường. Thay vì dùng FEESST các bác sĩ có thể dùng áp lực nhẹ lên niêm mạc qua sụn phễu 2 bên để đánh giá tính toàn vẹn của độ nhạy thanh quản. Một đáp ứng nguyên vẹn được chỉ ra bởi một phản ứng White-out trên nội soi. Mặc dù phương pháp này không được coi là nhạy cảm với sự thiếu hụt cảm giác nhỏ, nó được dùng để xác định chính xác những vấn đề cảm giác nghiêm trọng hơn. Trong thực tế, việc thiếu hụt bất kì phản ứng nào khi chạm nhẹ với đầu ống nội soi là bằng chứng của việc giảm cảm giác.
Sau khi kiểm tra cấu trúc thanh quản và hầu, chức năng nuốt được đánh giá. Chức năng nuốt được đánh giá trước khi bắt đầu và sau khi hoàn tất thì họng của quá trình nuốt. Điển hình, bệnh nhân tự ăn hoặc được cho một lượng thức ăn từ kẹo Ice chips đến những kết cấu rắn. Trong một số trường hợp, như là khi có sự lo lắng đáng kể, bệnh nhân hít sặc thức ăn hoặc chất lỏng trong khi khám, bác sĩ có thể không chọn sử dụng bất kì khối thức ăn nào. FEES test đem lại một lợi thế khác biệt với VFSS vì, nếu bác sĩ muốn, không cần sử dụng bất kì boluses nào.
Nếu bác sĩ lựa chọn sử dụng chất lỏng hoặc thức ăn trong khi đánh giá, boluses thường là thức ăn được nhuộm với màu xanh dương hoặc xanh lá để tăng cường hìnhảnh trong khi khám. Tuy nhiên, sử dụng các chất mờ đục như sữa hoặc vanilla pudding thường cho phép cái nhìn toàn diện. Một giao thức chuẩn hóa về sử dụng bolus thường được khu- yên dùng, vì nó cho phép so sánh chức năng qua các lần khám. Thường thì, chất lỏng loãng được đưa vào đầu tiên nếu không có nghi ngờ mạnh mẽ với nguy cơ hít sặc. Các loại bolus khác có thể được đưa vòa trong quá trình khám bao gồm bánh pudding hoặc kết cấu xay nhuyễn cũng như lỏng như là một bánh quy bơ giòn hoặc bánh quy Graham.
6.4. Soi thực quản qua đường mũi
Đôi khi VFSS hoặc FEES không giải thích được triệu chứng ho mặc dù tiền sử bệnh nhân về rối loạn nuốt và thông tin thêm đều đầy đủ. Lí do gây ho có thểphát sinh từ phần dưới thực quản do cơ chế phản xạ TK X hoặc bệnh lí thực quản khác. Soi thực quản qua đường mũi (TNE) là một công cụ cho phép bác sĩ dễ dàng quan sát thực quản, cơ thắt thực quản dưới và dạ dày trong tình trạng tỉnh táo, bệnh nhân không dùng thuốc an thần để đánh giá trào ngược, globus, rối loạn nuốt, và ung thư đầu cổ. TNE được báo có là cho thấy những phát hiện quan trọng trong 50% các thủ thuật đã thực hiện. Những dấu hiệu này bao gồm viêm thực quản, thoát vị hoành, thực quản Barrett, bệnh nhiễm nấm Candida, chít hẹp thực quản, carcinoma, rối loạn vận động, màng thực quản, và túi thừa thực quản. Bác sĩ tai mũi họng có thể là người thích hợp lí tưởng để tầm soát sự thay đổi niêm mạc ở thực quản vì các nhà nghiên cứu đã phát hiện rằng những bệnh nhân với thực quản Barrett có 1 tỉ lệ cao mắc các triệu chứng LPR, đặc biệt là ho mạn tính, hơn là các triệu chứng GERD điển hình. Hơn nữa trong một nghiên cứu mới đây, Howell cho thấy rằng 51% bệnh nhân trải qua TNE có một phát hiện mà dẫn đến thay đổi điều trị như là chít hẹp thực quản, đường Z bất thường, Viêm thực quản trào ngược, hoặc viêm thực quản nhiễm trùng. Tỷ lệ mới mắc của những dấu hiệu thực quản này thậm chí còn cao hơn ở những bệnh nhân có tăng thang điểm EAT-10 hoặc tiền sử ung thư đầu cổ (81% nếu ung thư đầu cổ lẫn tiền sử rối loạn nuốt).
TNE được thực hiện ở phòng khám mà không cần dùng an thần. Đầu tiên, hỗn hợp gồm oxymetazoline tại chỗ và lidocaine 4% được phun vào mũi và sau đó gạc được ngâm trong cùng dung dịch được đặt vào hai lỗ mũi ngoài từ 5-10 phút. Cần lưu ý rằng nếu bệnh nhân không thể chịu đựng được ống soi thanh quản mềm thường xuyên, ho sẽ khó có thể chịu đựng được đường kính lớn hơn một chút của ống TNE (nó chứa một kênh vận hành, vì vậy rộng hơn). Không cần gây tê thêm ở họng thanh quản vì nó được chứng minh trước đây là làm bệnh nhân nôn ọe, hít sặc, và thường không thoải mái hơn là chỉ có ống soi bên trong. Ống soi được đưa qua lỗ mũi nào rộng hơn, tốt nhất là qua đường dưới giữa cuốn mũi dưới, vách ngăn mũi và sàn mũi, và đưa vào hạ họng và đưa vào trên khe nằm giữa vùng sau sụn nhẫn và thành họng miệng sau. Bệnh nhân được hướng dẫn nuốt vào thời điểmn ày và sau đó người bác si tiến hành soi nhẹ nhàng đến khi tới dạ dày. Không nên di chuyển thô bạo và nên giữ tầm nhìn ở khoang, nhưng việc quan sát dễ dàng hơn khi kéo ống soi ra khỏi nếu nó ở trung tâm ống soi. Dạ dày được quan sát và sau đó ống soi được quay ngược lại (180 độ) để quan sát ống soi khi nó đi qua cơ thắt thực quản dưới LES, mà cho phép nhìn thấy sức cơ của cơ thắt thực quản dưới quanh ống soi cũng như đường đi của nước bọt khi bệnh nhân nuốt. Không khí sau đó được hút khỏi dạ dày và đường Z sẽ được xác định, điểm nối nơi niêm mạc squamous của thực quản và niêm mạc columnar của thực quản gặp nhau
Hình 7-2 cho thấy một tầm nhìn điển hình của đường Z dạ dày thực quản. Về mặt giải phẫu, chỗ nối dạ dày thực quản (GEJ) là một vùng mà nối giữa đầu xa thực quản và đầu gần dạ dày hoặc tim và mặt gần nhất của nếp dạ dày. Ở vùng LES (cơ thắt thực quản dưới), co thắt cơ hoành xảy ra ở nơi cơ hoành ôm lấy thực quản khi nó đi qua và ra khỏi lồng ngực. Giải phẫu bệnh thêm như thoát vị hoành có thể được xác định ở đây, nơi nếp dạ dày đẩy lên qua cơ hoành vào lồng ngực, làm biến dạng tương quan thông thường giữa LES và cơ hoành. Bất kì biến dạng nào khác với đường Z thông thường đều cần được sinh thiết, vì đây có thể là tình trạng thực quản Barrett (nơi lớp mô bình thường của thực quản được thay thế bởi lớp lót giống ruột) mà chỉ được chứng minh bởi bệnh lí học. thực quản barrett được xem như một biến chứng của GERD mạn tính và là tổn thương tiền ung trong hầu hết các trường hợp ung thư biểu mô tuyến thực quản adenocarcinoma. So sánh với dân số Đan Mâchj nói chung, nguy cơ mắc ung thư biểu mô tuyến ở bệnh nhân Barrett thực quản là 11.3%. Việc phát hiện loạn sản biệt hóa thấp trên sinh thiết thậm chí còn là một yếu tố nguy cơ lớn hơn. Sinh thiết thêm có thể được thực hiện ở vùng dưới và / hoặc giữa thực quản để loại trừ viêm thực quản ưa bạch cầu ái toan nếu điều này cần xem xét cho bệnh nhân. Sinh thiết thường không gây đau hoặc thậm chí được đánh giá cao ở bệnh nhân sinh thiết thực quản giữa đến dưới, nhưng thường trở nên khó chịu khi sinh thiết gần hơn ở đoạn họng. đặt một miếng bông xốp nhỏ để giữ thực quản giãn ra để xem tất cả bề mặt niêm mạc hoặc xịt nước để loại bỏ bất kì cặn thức ăn trên ống soi hoặc trên thành thực quản là hữu ích để quan sát ở khoảng cách tốt hơn. Khi đánh giá thực quản, thỉnh thoảng cần yêu cầu bệnh nhân nuốt cũng có thể cải thiện tầm nhìn mà không cần bơm quá nhiều, điều này có thể dẫn đến cảm giác đầy hơi ở một số bệnh nhân. Toàn bộ bài đánh giá cần được ghi hình lại để cho phép bác sĩ và bệnh nhân xem lại.
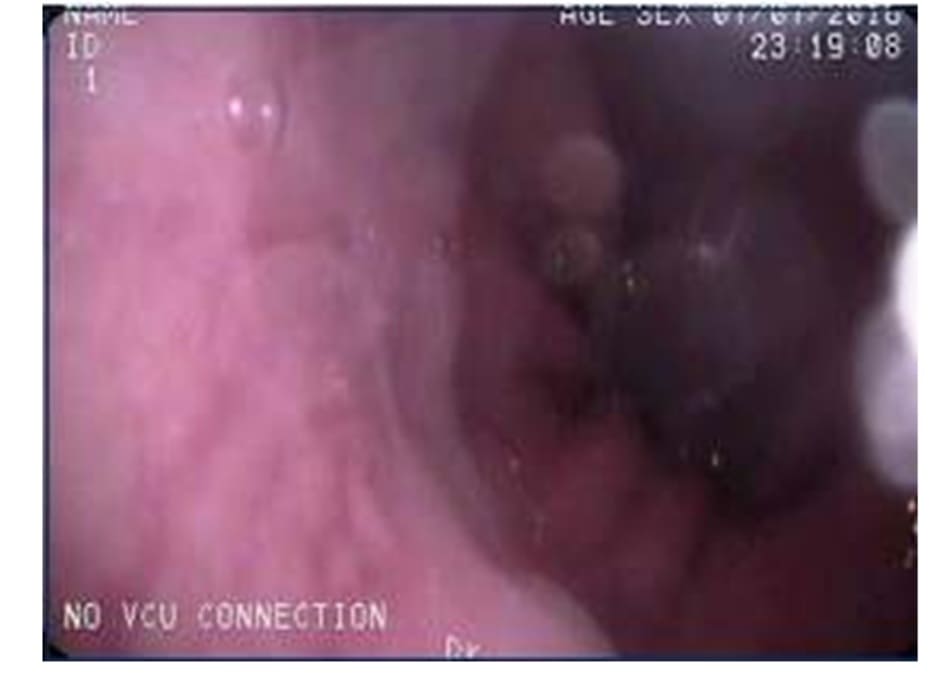
to rule out barrett’s esophagus and other pathologies.
7. Bệnh học rối loạn nuốt và ho
Chương này được tập trung vào chẩn đoán và các công cụ lâm sàng để bác sĩ có thể dùng chẩn đoán vấn đềA nuốt mà có thể dẫn đến hít sặc hoặc bất thường chức năng nuốt mà dẫn đến ho. Trong phần này, các bất thường nuốt cụ thể và cách chúng liên quan với ho sẽ được mô tả.
8. Túi thừa Zenker
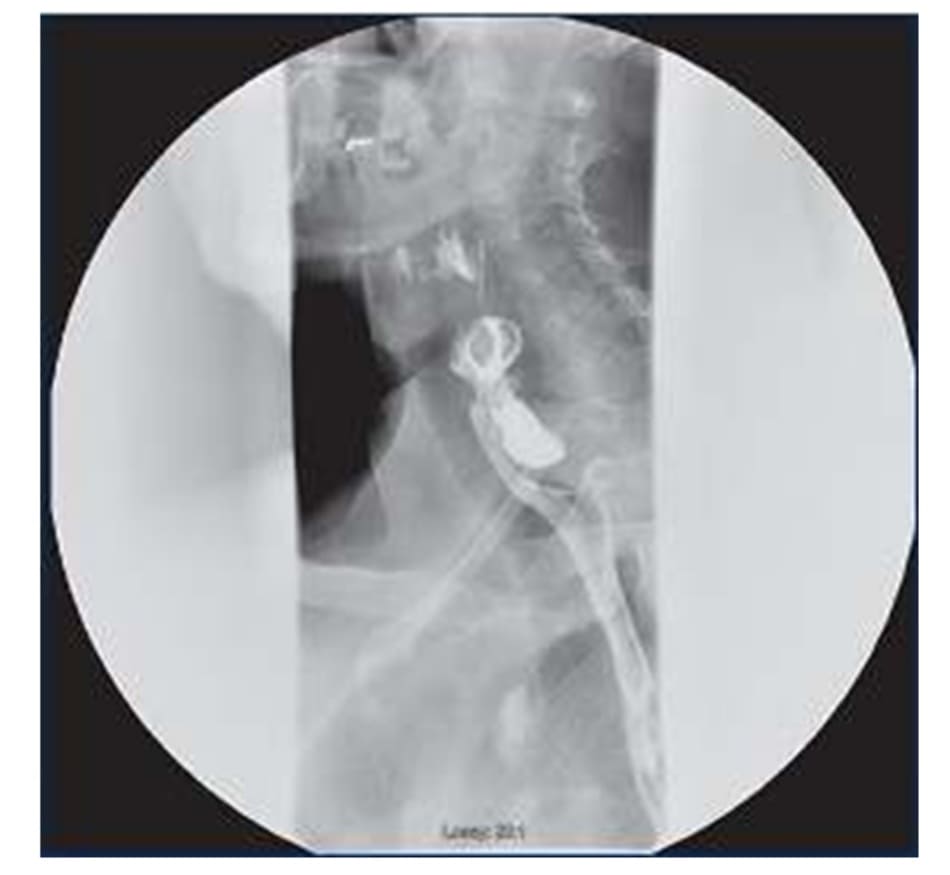
Ho có thể là một trong những triệu chứng phổ biến nhất của một túi thừa zenker hoặc túi thừa vùng cổ khác. Trong trường hợp túi thừa Zenker, tình trạng lộn niêm mạc thực quản ra ngoài ở góc Killian, nằm giữa cơ khít hầu dưới và cơ nhẫn hầu, làm bể chứa chất lỏng hoặc thức ăn mà đôi khi được làm rỗng và quay lại họng gây ra ho chậm sau khi nuốt. sự chậm trễ này rất quan trọng, vì ho với chất lỏng loãng lập tức sau khi nuốt là một dấu hiệu cảnh báo cho tình trạng nuốt không an toàn, như minh họa trước đó. Túi thừa thực quản nên được quan sát dễ dàng với VFSS. Hình 7-3 thể hiện túi thừa Zenker ở mặt bên với chất cản quang bên trong. Wirth và đồng nghiệp đã chứng minh rằng các bệnh nhân có những triệu chứng về rối loạn nuốt (96%), ợ chua (60%) và ho (19%), sau đó là viêm phổi ở bệnh nhân có túi thừa Zenker. Hầu hết các bệnh nhân được giảm ho sau khi túi thừa được điều trị bằng Phương pháp phẫu thuật phá vỡ cơ CP, cho phép túi thừa rỗng và tránh tình trạng ợ chua sau đó vài thanh quản gây kích thích. Trong cùng nghiên cứu, không có trường hợp viêm phổi hít nào được tìm thấy sau phẫu thuật bất kể phương pháp phẫu thuật ( Phẫu thuật nội soi mở cơ CP hoặc qua một Phẫu thuật hở và mở cơ CP).
9. Dị vật
Rối loạn nuốt có thể là một yếu tố nguy cơ đối với dị vật vùng khí quản – tiêu hóa trên. Một sự tắc nghẽn thức ăn hoàn toàn ở thực quản có thể cung cấp rất nhiều hỗn hợp đáng kể trong họng mà dẫn đến hít sặc và ho như một biện pháp bảo vệ. ngoài ra, chứng khó nuốt và mất phối hợp chức nuốt ở họng có thể dễ dàng dẫn tới dị vật đường thở. Dị vật đương thở thường rất rõ rệt khi chúng xảy ra do ho dữ dội và thở rít, khó thở. Ít gặp hơn, một người hoặc đứa trẻ sẽ không nhận ra đợt hít phải dị vật, và cuối cùng tình trạng nhiễm trùng sẽ tiến triển ở xa với dị vật trọng đường thở và ho tiếp đó sẽ tiến triển.
10. Viêm thực quản ưa bạch cầu ái toan
Viêm thực quản ưa bạch cầu ái toan (EoE) được đặc trưng bởi dấu hiệu lâm sàng về tắc nghẽn thức ăn và khó nuốt ở người lớn, nhưng ở trẻ em các triệu chứng thường ít nghiêm trọng hơn, như là biếng ăn, và các triệu chứng phù hợp với GERD. Điều quan trọng, bệnh nhân thường có các triệu chứng như ho hoặc rối loạn phát âm khi bắt đầu triệu chứng. Phát hiện mô học quan trọng ở EoE là thâm nhiễm bạch cầu ái toan của niêm mạc thực quản với hơn 15 bạch cầu ái toan biểu mô trên trường khuếch đại lớn (kính hiển vi) trong một hoặc nhiều mẫu sinh thiết. Một bạch cầu ái toan thực quản dày đặc thường được mô tả liên quan đến sự tăng sản biểu mô vảy nghiêm trọng. có một mối tương quan mạnh mẽ giữa EoE, cơ địa dị ứng, dị nguyên khí đa nhạy cảm, và dị nguyên thức ăn. Ngoài ra, Kelly và cộng sự, cho thấy một chế độ ăn uống giàu vi lượng đã cải thiện kết quả lâm sàng và mô học mô học ở 10 trẻ em mắc EoE. Điều quan trọng, và không phải lúc nào cũng phân biệt được rõ ràng, GERD được cho là không liên quan trước khi EoE được chẩn đoán chính xác.
Điều quan trọng đối với bác sĩ là phải nhận biết EoE vì đây là nguyên nhân chủ yếu của khó nuốt và tắc nghẽn thực quản ở trẻ em và người trẻ tuổi, và là nguyên nhân phổ biến thứ hai của viêm thực quản sau GERD, và có các triệu chứng tương tự như GERD và LPR, đặc biệt ở những bệnh nhân mà không đáp ứng với PPI. TEN với sinh thiết thực quản có hiệu quả trong việc lấy mẫu mô để chẩn đoán xác định hoặc loại trừ EoE.
11. Trào ngược
Dù GERD được đề cập nhiều hơn ở chương 4 của cuốn sách này, chúng tôi vẫn sẽ đề cập tóm tắt về nó ở đây, vì nó được coi là một trong những nguyên nhân phổ biến nhất của ho mạn tính và rối loạn nuốt. Các cơ chế đã được đưa ra bao gồm kích thích trực tiếp trong niêm mạc thực quản các đầu dây thần kinh chịu trách nhiệm gây ho cũng như ở thanh quản hoặc phế quản thông qua kích thích gián tiếp đường dẫn triueefn thần kinh nối thực quản với đường thở (phản xạ phế – thực quản) . Hiếm có bằng chứng hiện tại hỗ trợ cho việc kích thích ho trực tiếp bởi trào ngược họng thanh quản và thông thường hơn là bệnh nhân bị ho do trào ngược không nhất thiết tương quan với một đợt trào ngược cụ thể trên xét nghiệm trở kháng. Chỉ 20%-48% các bệnh nhân có triệu chứng dương tính có liên quan tới các đợt trào ngược trước khi ho, giả sử có liên kết nếu các đợt này xảy ra trong 5 phút. Như đã lưu ý trong Chương 5, bởi vì vai trò nổi bật của enzyme tiêu hóa pepsin đóng vai trò trong sinh lý bệnh của các triệu chứng LPR như ho, các chiến lược trong tương lai để điều trị ho do trào ngược sẽ bao gồm các biên pháp điều trị làm giảm số đợt trào ngược, không chỉ giảm độ acid hoặc điều trị pepsin tiềm ẩn.
Ngược lại, bản thân việc ho dường như không phải là nguyên nhân gây trào ngược vào họng thanh quản. HRM đã chứng minh rằng ho gây ra tăng áp lực UES, tăng cao hơn đáng kể so với thực quản, cơ thắt thực quản dưới và dạ dày. Điều này cho thấy một cơn ho làm tăng trào ngược từ dạ dày vào thực quản và, trong những người dễ bị ho, có thể đặt xếp họ vào đợt LPR tiếp theo sau khi cơn ho hoặc kích hoạt phản xạ ho phế – thực quản đã nói ở trên.
12. Co thắt tâm vị
Co thắt tâm vị là một rối loạn vận động thực quản nguyên phát vẫn chưa rõ nguyên nhân, xảy ra ở mọi lứa tuổi và mọi giới tính. Nó ảnh hưởng đến khoảng 0.5 – 1 / 100,000 người ở Hoa Kỳ. Nó được xác định bởi mất nhu động bình thường và không thể dãn LES như đã được chứng minh trên đo áp lực thực quản. Sinan và đồng nghiệp đã xem xét một nghiên cứu đoàn hệ đơn trung tâm của 110 bệnh nhân mắc rối loạn vận động thực quản. Không có gì đáng ngạc nhiên, 86% những bệnh nhân này than phiền về rối loạn nuốt ít nhất mỗi ngày. Tuy nhiên, 37% kể rằng có ho và 31% có triệu chứng hít sặc. Tất cả đã nói, 40% bệnh nhân có ít nhất một triệu chứng hô hấp. sau đó, họ đã xem xét một nhóm nhỏ với 22 bệnh nhân mà được đo áp lực thực quản trước đó và và sau khi Phẫu thuật cắt cơ Heller (cắt cơ thắt thực quản dưới) để điều trị rối loạn vận động thực quản. họ đã phát hiện rằng ho đã cải thiện ở 8/10 bệnh nhân sau phẫu thuật, và hít sặc đã cải thiện ở 10/11 bệnh nhân. Một trường hợp báo cáo về một bệnh nhân mắc ho mạn tính mà trước đó đã thất bại với can thiệp điều trị GERD, đã thành công giải quyết ho sau khi làm nong thực quản bằng bóng để điều trị co thắt tâm vị của cô ta. Gupta và cộng sự đã xem xét chức năng phổi trước và sau khi nong thực quản bằng bóng.
Hô hấp ký cho thấy bất thường ở 45% bệnh nhân trước khi điều tị. họ đã phát hiện những cải thiện đáng kể trong Thể tích thở ra gắng sức trong 1s (FEV1), dung tích sống gắng sức (FVC), lưu lượng thở ra đỉnh (PEFR), và lưu lượng trung bình thở ra (MEF25-75) trong đo hô hấp ký sau phẫu thuật được thực hiện một tháng sau nong. Bóng họ sử dụng để nong có đường kính 30mm ở nữ và 35mm ở nam. Sự thật rằng các bệnh nhân đã trải qua một cải thiện trong việc ho sau khi nong LES cho thấy mối quan hệ nhân quả giữa co thắt tâm vị và ho.
13. Lão hóa
Phần lớn bệnh nhân ho mạn tính đến khám ở các phòng khám chuyên khoa thường là người trung niên hoặc cao tuổi, và ho cũng được báo cáo là một trong những vấn đề thường gặp nhất đối với những người được chăm sóc y tế. các bệnh nhân già hơn (>65 hoặc >70, tùy theo ng- hiên cứu) có tỷ lệ rối loạn nuốt và các vấn đề ăn uống khác. Cụ thể hơn, các bệnh nhân lớn tuổi đã được tìm thấy có sự giảm đáp ứng nhu động với nuốt ướt khi so sánh với bệnh nhân trẻ tuổi. Giảm biên độ co thắt, co thắt thực quản nhiều pha, giãn thực quản và giảm giãn cơ thắt cũng được báo cáo ở những người lớn tuổi.
Việc góp phần trực tiếp từ lão hóa rất khó xác định vì các bệnh đồng mắc khác tăng theo tuổi và do đó gây ra nhầm lẫn. tuy nhiên, một nghiên cứu gần đây đã xem xét chức năng vận động thực quản ở người lớn tuổi và trẻ tuổi không có triệu chứng khỏe mạnh. Họ phát hiện những thay đổi tinh vi của LES với xu hướng giảm áp lực LES nền xuống thấp hơn và sự giảm giãn LES hoàn toàn. Nó cũng cho thấy sự giảm chức năng UES sau khi bảo vệ họng thanh quản từ trào ngược cả đời, cơ vùng họng trở nên kém hiệu quả theo thời gian với việc kháng lại lực của cơ CP. Điều này có khả năng khôi phục với việc phẫu thuật cắt cơ CP.
14. Các bệnh lí khác
Có vài bệnh lí khác mà liên quan đến cả ho và rối loạn nuốt. Xơ cứng bì hệ thống tiến triển hay Scleroderma, là một bệnh lí tự miễn mạn tính đặc trưng bởi các tổn thương tăng sinh với xơ hóa da và nhiều cơ quan, bao gồm đường tiêu hóa và phổi. Liên quan đến đường tiêu hóa trên và dưới đã được báo cáo đến 90% bệnh nhân với Scleroderma. Liên quan đến đường tiêu hóa thường xảy ra như một chuỗi các vấn đề với cử động và thời gian vận chuyển từ không triệu chứng đến yếu liệt nghiêm trọng ở bất cứ nơi nào dọc theo đường tiêu hóa, bao gồm cả rối loạn vận động thực quản. Ho cũng được tìm thấy ở vài bệnh nhân mắc bệnh phổi mô kẽ do xơ cứng bì. Có bằng chứng chi tiết rằng viêm thần kinh có thể liên quan đến xơ phổi và ho. Những bệnh nhân này có một số nguyên nhân thúc đẩy hoặc tiềm ẩn khác nhau gây ra ho, do các vấn đề đi kèm như rối loạn chức năng vận động thực quản và trào ngược dạ dày thực quản. Cũng có mối liên quan của ho với thực quản Jackhammer. Thực quản Jackhammer là một bất thường vận động chính đặc trưng trên HRM khi ít nhất 20% chất lỏng nuốt vào có co rút phần xa toàn bộ lớn hơn 8000 mmHg/s/cm. trong một nghiên cứu mà bao gồm 17 bệnh nhân đáp ứng các tiêu chí nghiêm ngặt, 29% có đau ngực không do tim, 47% có rối loạn nuốt và 24$ có các triệu chứng khác như ho, ợ nóng và ợ chua.
15. Tư duy sáng tạo
Mỗi bệnh nhân bị ho thường phàn nàn khác nhau. Rối loạn nuốt nên được tầm soát với tối thiểu hai câu hỏi chính sau: “Bạn có phải tránh bất kì thực phẩm nào không? Hay “Bạn có ho hay nghẹn chất lỏng khi nuốt không?” Các xét nghiệm thêm cần được bảo đảm nếu bệnh nhân trả lời có cho bất kì cây hỏi nào hoặc nghi ngờ lâm sàng cao. Ngoài ra, nếu tất cả các xét nghiệm khác và các biện pháp điều trị đã được thử và bệnh nhân vẫn cần phải chăm sóc y tế cho vấn đề ho mạn tính cả ho, điều đó sẽ khiến nhà chăm sóc sức khỏe phải xem xét kĩ lưỡng với đánh giá rối loạn nuốt để loại trừ nguyên nhân bị bỏ qua này. Thú vị nhất trong việc đánh giá và điều trị bệnh nhân với rối loạn nuốt vùng họng thực quản và họng miệng là sự ra đời của một Phép đo áp lực họng độ phân giải cao HRPM. Gần đây, O’Rourke và Humphries đã công bố về việc sử dụng HRPM ở một bệnh nhân để cung cấp phản hồi sinh học. bệnh nhân của họ có VFSS cho thấy khả năng bảo vệ đường thở và thanh thải họng kém cùng với chất cặn ở vùng sau sụn nhẫn phù hợp với rối loạn chức năng cơ nhẫn hầu. HRPM có thể cho thấy sự giãn bình thường của cơ thắt thực quản trên, bao gồm cả áp lực mở và giãn, do đó các điều trị trực tiếp là phẫu thuật cơ nhẫn hầu. trong trường hợp này, HRPM đã có thể cho thấy sự mất khả năng co bóp cơ thắt dưới, mà có thể giải quyết không cần phẫu thuật qua các phản hồi sinh học hàng tuần với HRPM và bài tập nuốt. điều này cho phép cải thiện các triệu chứng hiệu quả và chứng minh tiềm năng cho sự tiến bộ mới này trong việc dùng HRM như một công cụ hỗ trợ chẩn đoán và điều tị RỐi loạn nuốt.
16. Những điểm cần nhớ
- Rối loạn nuốt và hít sặc nên luôn luôn được xem xét khi bệnh nhân bị ho mạn tính.
- Có nhiều lí do tại sao chất lỏng, chất rắn và nước bọt kích thích phản xạ ho trong họng và thực quản. một số là bản chất bảo vệ, trong khi số khác là bệnh lí và không cần thiết từ quanđiểm bảo vệ đường thở.
- Rõ ràng có một sự liên tục của các phản xạ ho phù hợp mà phù hợp với việc bảo vệ đường thở, nhưng bảo vệ đường thở không đầy đủ hoặc ho không cần thiết khiến bệnh nhân phải đi khám.
- Hiểu biết cơ bản về các công cụ có thể đánh giá khoang miệng, họng, thanh quản, và thực quản trong quá trình nuốt là cần thiết để đánh giá đầy đủ và điều trị bệnh nhân
17. TÀI LIỆU THAM KHẢO
- Amin MR, Koufman Vagal neuropathy after upper respiratory infec- tion: a viral etiology? Am J Otolaryngol. 2001;22(4):251–256.
- Rees CJ, Henderson AH, Belafsky Postviral vagal neuropathy. Ann Otol Rhinol Laryngol.2009;118(4):247–252.
- Achilleos Evidence-based evaluation and management of chronic cough. Med Clin North Am.2016;100(5):1033–1045.
- American Speech-Language-Hearing Preferred practice patterns for the profession of speech-language pathology. 2004.
- Belafsky PC, Mouadeb DA, Rees CJ, et Validity and reliability of the Eating Assessment Tool (EAT-10). Ann Otol Rhinol Laryn- gol.2008;117(12):919–924.
- Arslan SS, Demir N, Kilinc HE, Karaduman The ability of the Eatin- gAssessment Tool-10 to detect aspiration in patients with neurological disorders. J Neurogastroenterol Motil.2017;23(4):550–554.
- Cheney DM, Siddiqui MT, Litts JK, Kuhn MA, Belafsky The ability of the 10-Item Eating Assessment Tool (EAT-10) to predict aspiration risk in persons with dysphagia. Ann Otol Rhinol Laryngol.2015;124(5):351–354.
- Plowman EK, Tabor LC, RobisonR, et Discriminant ability of the Eat- ing Assessment Tool-10 to detect aspiration in individuals with amyo- trophic lateral sclerosis. Neurogastroenterol Motil. 2016;28(1):85–90.
- Martino R, Silver F, Teasell R, et The Toronto Bedside Swallowing Screening Test (TOR-BSST): development and validation of a dysphagia screening tool for patients with stroke. Stroke.2009;40(2):555–561.
- Suiter DM, Sloggy J, Leder Validation of the Yale Swallow Pro- tocol: a prospective double-blinded videofluoroscopic study. Dyspha- gia.2014;29:199–203.
- DePippo KL, Holas MA, Reding MJ. Validation of the 3-oz water swal- low test for aspiration following stroke. ArchNeurol. 1992;49(12):1259–
- Daniels SK, Pathak S, Rosenbek JC, Morgan RO, Anderson Rapid aspiration screening for suspected stroke: part 1: development and vali- dation. Arch Phys Med Rehabil.2016;97(9):1440–1448.
- EdmiastonJ, Connor LT, Steger-May K, Ford A simple bedside stroke dysphagia screen, validated against videofluoroscopy, detects dysphagia and aspiration with high sensitivity. J Stroke Cerebrovasc Dis. 2014;23(4):712–716.
- Wakasugi Y, Tohara H, Hattori F, et Screening test for silent aspira- tion at the bedside. Dysphagia.2008;23(4):364–370.
- Momosaki R, Abo M, Kakuda W, Kobayashi Applicability of the two-step thickened water test in patients with poststroke dysphagia:a novel assessment tool for paste food aspiration. J Stroke Cerebrovasc Dis.2013;22(6):817–821.
- Brodsky MB, Suiter DM, González-Fernández M, et Screening ac- curacy for aspiration using bedside water swallow tests: a systematic re- view and metaanalysis. Chest.2016;150(1):148–163.
- American Speech-Language-Hearing Clinical indicators for instrumental assessment of dysphagia. 2000.
- Stoschus B, Allescher Drug-induced dysphagia. Dysphagia. 1993;8(2): 154–159.
- Al-Shehri Drug-induced dysphagia. Ann Saudi Med.2003;23(5):249–253.
- Russell Non-steroidal anti-inflammatory drugs and gastrointesti- nal damage— problems and solutions. Postgrad Med J.2001;77(904):82– 88.
- Sebastian JL, McKinney WP, Kaufman J, Young Angiotensin-con- verting enzyme inhibitors and cough: prevalence in an outpatient medical clinic population. Chest.1991;99(1);36–39.
- Madhavan A, Carnaby GD, Crary, “Food Sticking in My Throat”: videofluoroscopic evaluation of a common symptom. Dyspha- gia.2015;30(3):343–348.
- Daniels SK, Brailey K, Priestly DH, Herrington LR, Weisberg LA, Foun- das Aspiration in patients with acute stroke. Arch Phys Med Reha- bil.1998;79(1):14–19.
- Horner J, Massey EW, Riski JE, Lathrop DL, Chase KN. Aspira- tion following stroke: clinical correlates and outcome. Neurolo- 1988;38(9):1359–1362.
- Malandraki GA, Hind JA, Gangnon R, Logemann JA, Robbins The utility of pitch elevation in the evaluation of oropharyngeal dysphagia: preliminary findings. Am J Speech Lang Pathol. 2011;20(4):262–268.
- Smith Hammond CA, GoldsteinLB, Horner RD, et Predicting aspi- ration in patients with ischemic stroke: comparison of clinical signs and aerodynamic measures of voluntary cough. Chest.2009;135(3):769–777.
- Hammond CS, Goldstein L, Zajac D, Gray L, Davenport P, Bolser Assessment of aspiration risk in stroke patients with quantification of voluntary cough. Neurology.2001;56(4):502–506.
- Pitts T, Bolser D, Rosenbek J, Troche M, Sapienza Voluntary cough production and swallow dysfunction in Parkinson’s disease. Dyspha- gia.2008;23(3):297–301.
- Hegland KW, Okun MS, Troche MS. Sequential voluntary cough and as- piration or aspiration risk in Parkinson’s disease. Lung.2014;192(4):601–608.
- Bianchi C, Baiardi P, Khirani S, Cantarella Cough peak flow as a predictor of pulmonary morbidity in patients with dysphagia. Am J Phys Med Rehabil.2012;91(9):783–788.
- Addington WR, Stephens RE, Gilliland K, Miller Tartaric acid-in- duced cough and the superior laryngeal nerve evoked potential. Am J Phys Med Rehabil.1998;77(6):523–526.
- Addington WR, Stephens RE, Gilliland K, Rodriguez Assessing the laryngeal cough reflex and the risk of developing pneumonia after stroke. Arch Phys Med Rehabil.1999;80(2):150–154.
- Addington WR, Stephens RE, Gilliland Assessing the laryngeal coughreflex and the risk of developing pneumonia after stroke: an inter- hospital comparison. Stroke.1999;30(6):1203–1207.
- Nieto L, de Diego A, Perpiñá M, et Cough reflex testing with inhaled capsaicin in the study of chronic cough. Resp Med. 2003;97(4):393–400.
- Miles A, Zeng IS, McLauchlan H, Huckabee M-L. Cough reflex testing in dysphagia following stroke: a randomized controlled trial. J Clin Med 2013; 5(3): 222.
- McCullough GH, Rosenbek JC, Wertz RT, McCoy S, Mann G, McCullough
- Utility of clinical swallowing examination measures for detecting aspi- ration post-stroke. J Speech Lang Hear Res.2005;48(6):1280–1293.
- McCullough GH, Wertz RT, Rosenbek JC. Sensitivity and specificity of clinical/bedside examination signs for detecting aspiration in adults subsequent to J Commun Disord.2001;34(1-2):55–72.
- Groves-Wright KJ, Boyce S, Kelchner Perception of wet vocal qual- ity in identifying penetration/aspiration during swallowing. J Speech Lang Hear Res.2010;53(3):620–632.
- Waito A, Bailey GL, Molfenter SM, Zoratto DC, Steele CM. Voice-quality abnormalities as a sign of dysphagia: validation against acoustic and vid- eofluoroscopic Dysphagia.2011;26(2):125–134.
- Leder SB, Suiter DM, Green Silent aspiration risk is volume-de- pendent. Dysphagia.2011;26(3):304–309.
- Brodsky MB, Gonzalez-Fernandez M, Michtalki H, Frymark T, Vene- diktov R, Schooling Screening accuracy for aspiration using bed- side water swallow tests: a systematic review and meta-analysis. Chest.2016;150(1):148–163.
- Dantas RO, Cook IJ, Dodds WJ, Kern MK, Lang IM, Brasseur Biomechan- ics of cricopharyngeal bars. Gastroenterology.1990;99(5):1269–1274.
- Lester S, Langmore SE, Lintzenich CR, et The effects of top- ical anesthetic on swallowing during nasoendoscopy. Laryngo- scope.2013;123(7):1704–1708.
- O’Dea MB, Langmore SE, Krisciunas GP, et Effect of lidocaine on swallowing during FEES in patients with dysphagia. Ann Otol Rhinol Lar- yngol.2015;124(7):537–544.
- Leder SB, Ross DA, Briskin KB, Sasaki CT. A prospective, double-blind, randomized study on the use of a topical anesthetic, vasoconstrictor, and placebo during transnasal lexible iberoptic endoscopy. J Speech Lang Hear 1997;40(6):1352–1357.
- Murray J, Langmore SE, Ginsberg S, Dostie he signiicance of accu- mulated oropharyngeal secretions and swallowing frequency in predicting aspiration. Dysphagia.1996;11(2):99–103.
- Donzelli J, Brady S, Wesling M, Craney Predictive value of accumulated oropharyngeal secretions for aspiration during video nasal endo- scopic evaluation of the swallow. Ann Otol Rhinol Laryn gol.2003;112(5):469–475.
- Aviv JE, Martin JH, Debell M, Keen MS, Blitzer Air pulse quantifica- tion of supraglottic and pharyngeal sensation: a new technique. Ann Otol Rhinol Laryngol.1993;102(10):777–780.
- Aviv JE, Kim T, Thomson JE, Sunshine S, Kaplan S, Close Fiberoptic endoscopic evaluation of swallowing with sensory testing (FEESST) in healthy controls. Dysphagia.1998;13(2):87–92.
- Aviv JE, Kaplan ST, Thomson JE, Spitzer J, Diamond B, Close The safety of flexible endoscopic evaluation ofswallowing with sensory testing (FEESST): an analysis of 500 consecutive evaluations. Dyspha- gia.2000;15(1):39–44.
- Kaneoka A, Krisciunas GP, Walsh K, Raade AS, Langmore A com- parison of 2 methods of endoscopic laryngeal sensory testing: a prelimi- nary study. Ann Otol Rhinol Laryngol.2015;124(3):187–193.
- Langmore, Endoscopic Evaluation and Treatment of Swallowing Disorders. New York, NY: Thieme; 2001.
- Leder SB, Acton LM, Lisitano HL, Murray Fiberoptic endoscopic evaluation of swallowing (FEES) with and without blue-dyed food. Dys- phagia.2005;20(2):157–162.
- Belafsky PC, Postma GN, Daniel E, Koufman Transnasal esophago- scopy. Otolaryngol Head Neck Surg. 2001;125(6):588–589.
- Postma GN, Cohen JT, Belafsky PC, et Transnasal esophagoscopy: revis- ited (over 700 consecutive cases). Laryngoscope.2005;115(2):321–323.
- Reavis KM, Morris CD, Gopal DV, Hunter JG, Jobe Laryngopha- ryngealreflux symptoms better predict the presence of esophageal ade- nocarcinoma than typical gastroesophageal reflux symptoms. Ann Surg. 2004;239(6):849–858.ChroniCCough 140
- Howell RJ, Pate MB, Ishman SL, et Prospective multi-institutional transnasal esophagoscopy: predictors of a change in management. La- ryngoscope.2016;126(12):2667–2671.
- Odze Pathology of the gastroesophageal junction. Semin Diagn Pathol.2005;22(4), 256–265.
- Cameron AJ, Souto EO, Smyrk Small adenocarcinomas of the esophagogastric junction: association with intestinal metaplasia and dysplasia. Am J Gastroenterol.2002;97(6):1375–1380.
- Hvid-Jensen F, Pedersen L, Drewes AM, Sørensen HT, Funch-Jensen Incidence of adenocarcinoma among patients with Barrett’s esophagus. N Engl J Med.2011;365(15):1375–1383.
- Fox MR, Bredenoord Oesophageal high-resolution manometry:moving from research into clinical practice. Gut.2008;57(3):405–423.
- Kessing BF, Smout AJPM, Bredenoord Clinical applications of esophageal impedance monitoring and high-resolution manometry. Curr Gastroenterol Rep.2012;14(3):197–205.
- Bredenoord AJ, Smout High-resolution manometry. Dig Liver Dis.2008;40(3):174–181.
- Wirth D, Kern B, Guenin MO, et Outcome and quality of life after open surgery versus endoscopic stapler-assisted esophagodiverticulos- tomy for Zenker’s diverticulum. Dis Esophagus.2006;19(4):294–298.
- Lin L, Lv L, Wang Y, Zha X, Tang F, Liu The clinical features of foreign body aspiration into the lower airway in geriatric patients. Clin Interv Aging. 2014;9:1613–1618.
- Dabu J, Lindner M, Azzam M, et A case of chronic cough and pneu- monia secondary to a foreign body. Case Rep Med.2017;3092623.
- Orizio P, Cinquini M, Minetti S, et Chronic cough and eosino- philic esophagitis: an uncommon association. Case Rep Gastroenter- ol.2011;5(2):497–501.
- Roy-Ghanta S, Larosa DF, Katzka Atopic characteristics of adult patients with eosinophilic esophagitis. Clin Gastroenterol Hepatol. 2008;6(5):531–535.
- Kelly KJ, Lazenby AJ, Rowe PC, Yardley JH, Perman JA, Samp- son Eosinophilic esophagitis attributed to gastroesophageal reflux: improvement with an amino acid–based formula. Gastroenter- ol.1995;109(5):1503–1512.
- Gorriz-Gil C, Villarreal IM, Alvarez-Montero O, Rodriguez-Valiente A, Magaz M, Garcia-Berrocal Eosinophilic esophagitis: a relevant enti- ty for the otolaryngologist. Acta Otorrinolaringol Esp. 2016;67(3):167– 178.
- Smith JA, Houghton The oesophagus and cough: laryngo-pharyn- geal reflux, microaspiration and vagal reflexes. Cough.2013;9(1):12.
- Amaris M, Dua KS, Naini SR, Samuel E, Shaker Characteriza- tion of the upper esophageal sphincter response during cough. Chest, 2012;142(5):1229–1236.
- Pohl D, Tutuian Achalasia: an overview of diagnosis and treatment. Gastrointestin Liver Dis.2007;16(3):297–303.
- Sinan H, Tatum RP, Soares RV, Martin AV, Pellegrini, CA, Oelschlager Prevalence of respiratory symptoms in patients with achalasia. Dis Esophagus.2011;24(4):224–228.
- Kwon HY, Lim JH, Shin YW, Kim C-W. A case of chronic cough caused by achalasia misconceived as gastroesophageal reflux disease. Allergy Asthma Immunol Res.2014;6(6):573–576.
- Gupta M, Ghoshal UC, Jindal S, Misra A, Nath A, Saraswat VA. Respi- ratory dysfunction is common in patients with achalasia and improves after pneumatic Dig Dis Sci.2014;59(4):744–752.
- Won HK, Yoon SJ, Song WJ. The double-sidedness of cough in the el- Respir Physiol Neurobiol.2018;257:65–69
- Morice AH, Jakes AD, Faruqi S, et A worldwide survey of chronic cough: a manifestation of enhanced somatosensory response. Eur Respir J.2014;44(5):1149–1155.
- Dicpinigaitis Clinical perspective — cough: an unmet need. Curr Opin Pharmacol.2015;22:24–28.
- Cook Oropharyngeal dysphagia. Gastroenterol Clin North Am.2009;38(3):411–431.
- Humbert IA, Robbins Dysphagia in the elderly. Phys Med Rehabil Clin North Am., 2008;19(4):853–866.
- Andrews JM, Heddle R, Hebbard GS, Checklin H, Besanko L, Fraser Age and gender affect likely manometric diagnosis: audit of a tertiary referral hospital clinical esophageal manometry service. J Gastroenterol Hepatol.2009;24(1):125–128.
- Gutschow CA, Leers JM, Schröder W, et Effect of aging on esophageal motility in patients with and without GERD. Ger Med Sci.2011;9:Doc22.
- Grande L, Lacima G, RosE, et Deterioration of esophageal motility with age: a manometric study of 79 healthy subjects. Am J Gastroenterol. 1999; 94(7):1795–1801.
- Gregersen H, Pedersen J, Drewes Deterioration of muscle func- tion in the human esophagus with age. Dig Dis Sci.2008;53(12):3065– 3070.
- Ren J, Shaker R, Kusano M, et Effect of aging on the secondary esophageal peristalsis: presbyesophagus revisited. Am J Physiol Gastro- intest Liver Physiol.1995; 268(5):G772–G779.
- Besanko LK, Burgstad CM, Cock C, Heddle R, Fraser A, Fraser RJL. Changes in esophageal and lower esophageal sphincter motility with healthy J Gastrointestin Liver Dis.2014;23(3):243–248.
- Allen J, White CJ, Leonard R, Belafsky PC. Effect of cricopharyngeus muscle surgery on the Laryngoscope. 2010;120(8):1498–1503.
- Sallam H, McNearney TA, Chen JD. Systematic review: pathophysiolo- gy and management of gastrointestinal dysmotility in systemic sclerosis (scleroderma). Aliment Pharmacol 2006:23(6);691–712.
- Lim Scleroderma lung-associated coug Chest.2012;142 (3):556–557.
- Sloan JA, Mulki R, Sandhu N, Samuel S, Katz Jackhammer esoph- agus: symptom presentation, associated distal contractile integral, and assessment of bolus transit. J Clin Gastroenterol. Published online March 7, 2018.
- O’Rourke A, Humphries The use of high-resolution pharynge- al manometry as biofeedback in dysphagia therapy. Ear Nose Throat J.2017;96(2):56–58.
Tham khảo thêm một số bài viết cùng chủ đề





