Hội chứng Marfan là gì? Nguyên nhân gây bệnh
Hội chứng Marfan (Marfan Syndrome – MFS) là một rối loạn di truyền hiếm gặp của mô liên kết, đặc trưng bởi một loạt các biểu hiện khác nhau trên tim mạch, cơ xương khớp, mắt và phổi.
Trong nhiều năm, một số nhà điều tra đã nghiên cứu nhiều phân tử khác nhau được tìm thấy trong chất nền ngoại bào để nỗ lực làm sáng tỏ nguyên nhân của MFS. Những phân tử này bao gồm collagen, elastin, acid hyaluronic và fibrillin. Sakai và các cộng sự đã xác định được fibrillin, một protein có khối lượng 350 kDa, bằng cách sử dụng các kháng thể đơn dòng chống lại các tơ cơ. Sau đó, các nghiên cứu miễn dịch huỳnh quang đã được sử dụng để so sánh khả năng phản ứng ở cả những người khỏe mạnh và những người mắc MFS. Trong giai đoạn này, công nghệ tương tự đã được sử dụng để xây dựng bản đồ loại trừ gen dẫn đến định vị được khiếm khuyết trên nhiễm sắc thể 15 (dải q15 – q23).
Một số đột biến điểm đã được xác định trên gen fibrillin, hầu hết trong số đó ảnh hưởng đến phần cystein dư thừa trong vi sợi. Do đó, những đột biến này được cho là gây ra khiếm khuyết của fibrillin. Cấu trúc và chức năng của fibrillin bị thay đổi bởi sự gấp nếp protein bất thường do sự thay đổi liên kết giữa các phần cystein dư thừa đó, từ đó gây ra lỗi trong sản xuất vi sợi.
Đột biến trên locus FBN1 của gen fibrillin trên nhiễm sắc thể 15 đã cho thấy có liên quan đến MFS.
Dịch tễ học hội chứng Marfan
Tỷ lệ mắc MFS ước tính dao động từ 1/5000 đến 2-3/10000 người. Đột biến trong gen fibrillin gây ra hiệu ứng đa hiệu, do đó xuất hiện một loạt các đặc điểm kiểu hình có nguồn gốc từ một đột biến gen duy nhất. Một số bệnh khác có các biểu hiện tương tự như MFS, khiến việc xác định tỉ lệ mắc bệnh chính xác cực kỳ khó khăn.
Chẩn đoán hội chứng Marfan
Với biểu hiện rất thay đổi của MFS, không có dấu hiệu đơn lẻ nào là bệnh lý. Chẩn đoán được thực hiện trên cơ sở lâm sàng của các bất thường điển hình (xem hình dưới).
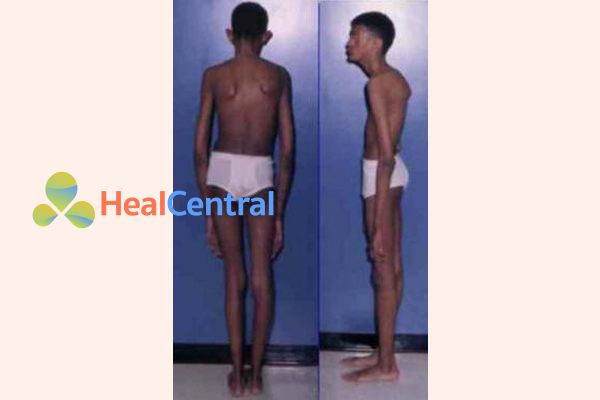
Danh sách sau đây mô tả các phát hiện lâm sàng phổ biến nhất và các tiêu chí Berlin sửa đổi (1986) để chẩn đoán MFS. Năm 1996, tiêu chí Ghent đã cập nhật các hướng dẫn trước đây, nhấn mạnh hơn vào các phát hiện trên xương, cũng như các tiêu chí về tiền sử gia đình và di truyền. Các tiêu chí Ghent sau đó đã được cập nhật vào năm 2010.
Hệ thống xương
Phải có ít nhất 2 tiêu chí chính hoặc 1 tiêu chí chính và 2 tiêu chí phụ.
Các tiêu chí chính là:
- Ngực ức gà.
- Chứng ngực lõm cần phẫu thuật.
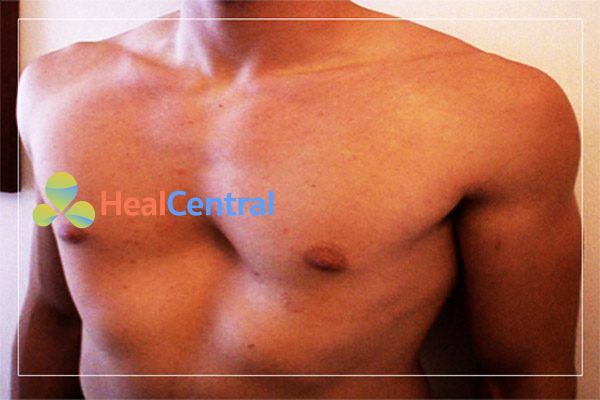
- Tỉ lệ phân đoạn từ trên xuống dưới giảm (nghĩa là khoảng cách từ đầu đến khớp mu chia cho khoảng cách từ khớp mu đến lòng bàn chân) nhỏ hơn 0.85.
- Tỉ lệ chiều dài sải tay so với chiều cao lớn hơn 1.05.
- Dấu hiệu cổ tay dương tính (Walker-Murdoch) (nghĩa là ngón cái và ngón út gối lên nhau khi bao quanh cổ tay đối diện).
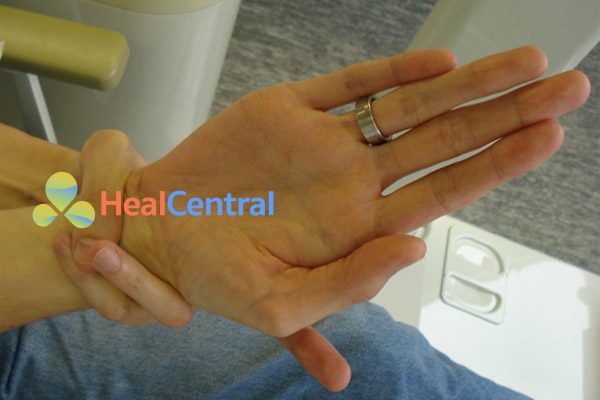
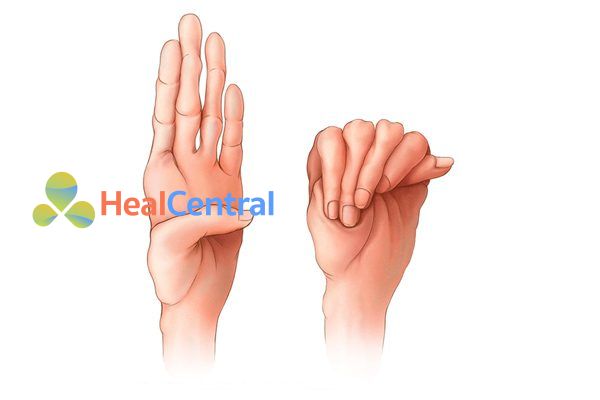
- Dấu hiệu ngón tay cái dương tính (Steinberg) (nghĩa là ngón tay cái vượt ra ngoài đường viền của bàn tay khi nó được giữ uốn cong trong lòng bàn tay)
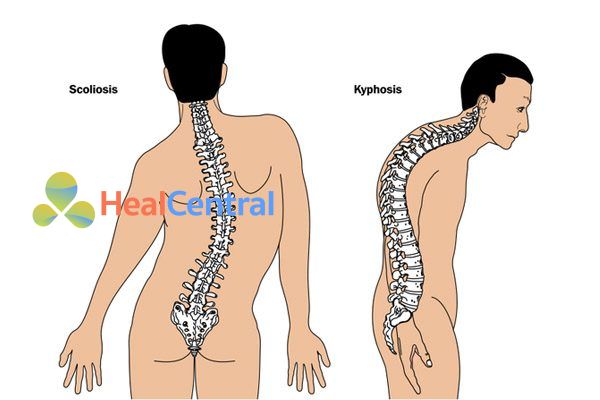
- Vẹo cột sống ngực – thắt lưng hơn 20○ hoặc trượt đốt sống ra trước.
- Xẹp dần chân sau, dẫn đến biến dạng bẹt.
- Sự nhô ra ổ cối ở bất kì mức độ nào (nhìn thấy trên X-quang phía trước và sau xương chậu).
Các tiêu chí phụ là:
- Lõm ngực mức độ nghiêm trọng vừa phải.
- Khớp dẻo khác thường.
- Vòm miệng cao.
- Các sự xuất hiện khác trên khuôn mặt (giảm sản xương gò má, sọ dài, lõm mắt, thụt hàm, khe mi mắt nghiêng xuống).
Hệ thống mắt
Phải có tiêu chí chính hoặc ít nhất 2 tiêu chí phụ.
Tiêu chí chính là lạc vị thể thủy tinh (thể thủy tinh di chuyển).
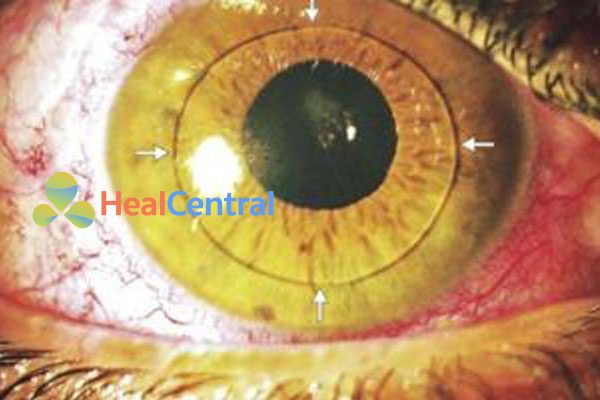
Các tiêu chí phụ là:
- Giác mạc phẳng bất thường.
- Chiều dài trục cầu mắt tăng lên, được chẩn đoán bằng siêu âm.
- Giảm sản mống mắt hoặc cơ mi, gây ra cận thị.
Hệ tim mạch
Phải có 1 trong những tiêu chí chính hoặc phụ được trình bày dưới đây.
Các tiêu chí chính là:
- Sự giãn nở của động mạch chủ tăng, có hoặc không có hở và ít nhất có liên quan đến xoang Valsalva.
- Bóc tách động mạch chủ tăng.
Các tiêu chí phụ là:
- Sa van hai lá, có hoặc không có hở.
- Sự giãn nở của động mạch phổi chính trong trường hợp không bị hẹp van động mạch phổi hoặc ngoại biên hoặc bất kì nguyên nhân rõ ràng nào khác ở bệnh nhân dưới 40 tuổi.
- Vôi hóa van hai lá ở bệnh nhân dưới 40 tuổi.
- Sự giãn nở hoặc bóc tách động mạch chủ ngực hoặc bụng giảm ở những bệnh nhân dưới 50 tuổi.
Hệ thống phổi
Không có tiêu chí chính cho hệ thống phổi.
Phải có 1 trong những tiêu chí phụ dưới đây:
- Tràn khí màng phổi tự phát.
- Các bọt đỉnh.
Da và tích hợp
Phải có tiêu chí chính hoặc 1 trong những tiêu chí phụ.
Tiêu chí chính là giãn màng cứng thắt lưng – xương cùng, được mô tả bằng chụp cắt lớp vi tính (CT) hoặc cộng hưởng từ (MRI).
Các tiêu chí phụ là:
- Rạn da không liên quan đến mang thai hoặc stress lặp lại nhiều lần.
- Thoát vị vết mổ hoặc tái phát.
Tiền sử gia đình
Phải có 1 trong các tiêu chí chính sau:
- Sự hiện diện của đột biến FBN1 được biết đến gây ra MFS.
- Sự hiện diện của một kiểu gen đơn bội quanh FBN1, được thừa kế từ thế hệ được biết là có liên quan đến MFS được chẩn đoán chắc chắn trong gia đình.
Yêu cầu chẩn đoán MFS
- Trường hợp chỉ số – Tiêu chí chính trong ít nhất 2 hệ thống cơ quan khác nhau và có sự tham gia vào hệ thống cơ quan thứ ba.
- Thành viên gia đình – Sự hiện diện của 1 tiêu chí chính trong tiền sử gia đình, 1 tiêu chí chính trong hệ thống cơ quan và sự tham gia của hệ thống cơ quan thứ hai.
Tiêu chí Ghent sửa đổi (2010)
Trong tiêu chí Ghent sửa đổi năm 2010, chẩn đoán MFS dựa trên 7 quy tắc. Trong trường hợp không có tiền sử gia đình, có 4 tiêu chí sau đây được chẩn đoán mắc MFS:
- Giãn gốc động mạch chủ có Z score từ 2 trở lên và lạc vị thể thủy tinh.
- Giãn gốc động mạch chủ có Z score từ 2 trở lên và xác định được đột biến FBN1.
- Giãn gốc động mạch chủ có Z score từ 2 trở lên và điểm toàn thân từ 7 trở lên.
- Lạc vị thể thủy tinh và đột biến FBN1 với sự giãn nở của động mạch chủ đã biết.
Khi có sự hiện diện của tiền sử gia đình, có 3 tiêu chí sau đây dẫn đến chẩn đoán MFS:
- Lạc vị thể thủy tinh và tiền sử gia đình có MFS.
- Điểm toàn thân từ 7 trở lên và tiền sử gia đình có MFS.
- Điểm giãn nở động mạch chủ từ 2 trở lên (ở độ tuổi ≥ 20) hoặc từ 3 trở lên (ở những người < 20 tuổi) và tiền sử gia đình mắc MFS.
Không có xét nghiệm cận lâm sàng cụ thể để chẩn đoán MFS.
Xét nghiệm di truyền phân tử có thể được sử dụng để hỗ trợ chẩn đoán MFS.
Chụp X-quang cũng được sử dụng để hỗ trợ chẩn đoán: X-quang cột sống, X-quang lồng ngực, X-quang phía trước và sau xương chậu, X-quang xương sọ, X-quang bàn tay và bàn chân.
Chụp CT, MRI, siêu âm cũng có thể hữu ích.
Điện tâm đồ (ECG), siêu âm tim qua thực quản, chụp MRI là các biện pháp thường dùng để xác định các bất thường tim mạch.
Chẩn đoán phân biệt
Chẩn đoán phân biệt với hội chứng MASS, hội chứng Shprintzen-Goldberg, hội chứng Ehlers-Danlos, hở van hai lá và các bệnh khác có biểu hiện phình động mạch chủ khác như hội chứng Loeys-Dietz.
Điều trị hội chứng Marfan
Điều trị nội khoa
Phần lớn các điều trị nội khoa liên quan đến MFS nhằm mục tiêu ngăn ngừa tổn thương tim mạch, đây là nguyên nhân chính dẫn đến tử vong ở hội chứng này. Thuốc chẹn β và các thuốc làm giảm hậu gánh được sử dụng để giảm áp lực cho van động mạch chủ, van hai lá và gốc động mạch chủ.
Tất cả bệnh nhân cần phải được điều trị dự phòng bằng kháng sinh thông thường trước khi trải qua các thủ tục có thể gây nhiễm khuẩn huyết. Các nhà nghiên cứu đã chứng minh rằng toàn bộ động mạch chủ, đặc biệt là phần gốc, cứng hơn bình thường ở bệnh nhân mắc MFS.
Thuốc chẹn β đã được sử dụng trong các nỗ lực nhằm làm giảm khởi phát và tốc độ giãn và bóc tách gốc động mạch chủ. Các nghiên cứu đã chứng minh tác dụng hiệp đồng liên quan đến giảm độ cứng động mạch chủ, giảm sức cản mạch máu và cải thiện tuân thủ điều trị khi sử dụng đồng thời nitroprusside và thuốc chẹn β.
Thuốc chẹn β được sử dụng vì nó làm giảm cả sức co bóp và nhịp tim, do đó làm giảm áp lực trên gốc động mạch chủ. Nitroprusside làm giảm sức cản mạch máu toàn thân, giúp giảm cả tiền gánh và hậu gánh và giảm áp lực cho tim. Vấn đề các tác dụng này liệu có giúp giảm tỉ lệ mắc bệnh và tử vong tại thời điểm này hay không vẫn chưa rõ ràng, chưa có nghiên cứu dài hạn nào được thực hiện. Thuốc chẹn kênh calci (ví dụ: verapamil) đang được nghiên cứu để đánh giá tác dụng của chúng với sinh lý tim mạch ở bệnh nhân mắc MFS.
Vẹo cột sống là biến dạng xương lớn phổ biến nhất gặp phải ở bệnh nhân mắc MFS cần can thiệp. Không có can thiệp bằng thuốc cụ thể để điều trị vẹo cột sống. Các phương pháp điều trị không phẫu thuật (ví dụ: nẹp cột sống) có thể được thử nhưng thường không thành công. Vẹo cột sống xảy ra ở khoảng 50-70% bệnh nhân mắc MFS và khác với vẹo cột sống vô căn ở thanh thiếu niên.
Không may, những bệnh nhân này thường bị vẹo cột sống sớm hơn với các đường cong cứng nhắc, đau đớn và biến dạng nghiêm trọng, cũng như tỉ lệ tiến triển cao. Sự tiến triển của đường cong có thể trung bình 7-10° mỗi năm từ khi bắt đầu vẹo cột sống và thường tiến triển nhanh chóng trong giai đoạn thanh thiếu niên sớm, đây là quá trình tăng trưởng đốt sống nhanh nhất. Điều này cũng trái ngược với loại vô căn, thường không đau và không biến dạng dần như vẹo cột sống ở bệnh nhân mắc MFS. Vẹo cột sống kết hợp với biến dạng ngực và cơ bắp kém, có thể gây tổn thương hô hấp đáng kể, chúng bắt buộc phải được phát hiện và phòng ngừa sớm nếu có thể trong quần thể bệnh nhân này.
Can thiệp không phẫu thuật cho vẹo cột sống thường sử dụng dụng cụ chỉnh hình TLSO nếu đường cong nhẹ và cho thấy dấu hiệu tiến triển. Nẹp cột sống đang gây tranh cãi. Nhiều bác sĩ phẫu thuật tin rằng phần lớn các đường cong ở bệnh nhân MFS tiến triển dù có dụng cụ này và do đó cần phải can thiệp phẫu thuật để ngăn ngừa biến dạng xấu đi.
Với những bệnh nhân có đường cong dưới 25°, quan sát và chụp X-quang nối tiếp sau mỗi 3-4 tháng là cách xử trí được khuyến nghị. Khi đường cong nằm trong phạm vi 25-40°, nẹp lưng Milwaukee hoặc TLSO nách được sử dụng. Đây có thể là cầu nối cho sự can thiệp phẫu thuật trong tương lai. Nẹp lưng chỉ được sử dụng ở những bệnh nhân có đường cong nhẹ (ví dụ: 25-40°) và không có biến dạng mặt phẳng đứng dọc (ưỡn đốt sống ngực hoặc gù cột sống thắt lưng). Nẹp lưng không được chỉ định cho các đường cong cứng, lớn hoặc có biến dạng mặt phẳng đứng dọc liên quan.
Điều trị ngoại khoa

Hẹp van hai lá có thể trở nên nghiêm trọng đến mức phải thay thế điều trị nội khoa bằng can thiệp phẫu thuật. Sửa chữa van hai lá được thực hiện nếu có thể để trì hoãn thay van do những bệnh này thường xuất hiện ở độ tuổi trẻ và có thể cần phẫu thuật tái tạo lại sau này. Sửa chữa phẫu thuật cũng bảo tồn chức năng cơ nhú và ngăn ngừa khả năng chống đông mạn tính, không giống như thay van nhân tạo.
Van động mạch chủ có thể cần sửa chữa nếu nó không thực hiện tốt chức năng của mình. Kĩ thuật ghép mô hoặc valve-sparing có thể được thực hiện. Kĩ thuật valve-sparing thường được thực hiện ở những bệnh nhân có động mạch chủ giãn ra khoảng 50 mm. Bệnh nhân có gốc động mạch chủ bị giãn rộng hoặc đỉnh động mạch chủ mỏng đáng kể thường cần sửa chữa bằng cách ghép mô. Đây cũng là thủ tục được lựa chọn trong trường hợp bóc tách động mạch chủ cấp tính. Một số bác sĩ phẫu thuật ủng hộ ghép mô dự phòng ở những bệnh nhân có tiền sử giãn động mạch chủ và tiền sử gia đình đột tử do tim mạch.
Khía cạnh quan trọng nhất trong đánh giá trước phẫu thuật của bệnh nhân mắc MFS là loại trừ bất kì tổn thương tim nào. Công việc hoàn chỉnh bao gồm điện tâm đồ (ECG) và siêu âm tim là bắt buộc. Giãn và vỡ động mạch chủ có thể phát triển trong suốt thời thơ ấu và cuộc sống trưởng thành của những bệnh nhân này. Do đó, người ta phải loại trừ các yếu tố này trước khi thực hiện phẫu thuật. Bất kì bằng chứng nào của giãn động mạch chủ phải được điều trị nội khoa hoặc phẫu thuật trước khi tái tạo cột sống.
Chỉ định chính cho phẫu thuật hệ thống cơ xương là vẹo cột sống tiến triển từ trung bình đến nặng. Biến dạng thành ngực cũng có thể nghiêm trọng đến mức ảnh hưởng đến hoạt động cơ học của tim phổi, chúng cần được phẫu thuật sửa chữa. Trước đây, bệnh nhân mắc MFS không được chẩn đoán các biến dạng thành ngực này và hầu hết đã tử vong khi còn nhỏ do bệnh tim mạch nội tại. Sự ra đời của phẫu thuật gốc động mạch chủ thành công cũng như thay van động mạch chủ và van hai lá đã thay đổi quan điểm dài hạn tổng thể cho bệnh nhân mắc bệnh.
Cần điều trị đầy đủ cho những bệnh nhân bị vẹo cột sống để giảm đau, cải thiện thẩm mỹ và quan trọng nhất là cải thiện hoạt động cơ học của phổi thông qua giảm các biến dạng cột sống và thành ngực.
Cần lưu ý phẫu thuật cho MFS khác với phẫu thuật cho chứng vẹo cột sống tự phát ở tuổi vị thành niên. Những khác biệt này phải được tính đến trong kế hoạch phẫu thuật.
Như đã mô tả ở phần trước, nẹp lưng có thể được xem xét ở những bệnh nhân bị cong cột sống nhẹ. Tuy nhiên, hầu hết bệnh nhân mắc MFS sẽ có tiến triển đường cong đáng kể mà cuối cùng phải can thiệp phẫu thuật. Bệnh nhân có cột sống cong lớn hơn 40-50º hoặc biến dạng đường cong đứng dọc bất thường liên quan cần phải phẫu thuật.
Hợp nhất cột sống sau và dụng cụ cột sống phân đoạn, cùng với ghép xương tự sinh là cơ sở chính của điều trị. Hầu hết các tác giả đồng ý rằng vẹo cột sống có thể được sửa chữa bằng phương pháp này. Tuy nhiên, tỉ lệ biến chứng tổng thể thay đổi theo từng loại khác nhau. Khớp giả và mất hiệu chỉnh có thể xảy ra, các tỉ lệ nằm trong khoảng từ 12% đến 40%.
Hầu hết các tác giả đề nghị ghép xương tích cực, cố định phần bên trong cứng nhắc và giám sát bệnh nhân đầy đủ sau phẫu thuật để chẩn đoán các biến chứng sớm trên lâm sàng. Định hướng sai mặt phẳng đứng dọc (biến dạng gù) có thể cần hợp nhất phía trước (cắt bỏ đĩa đệm), sau đó hợp nhất cột sống sau và dụng cụ cột sống phân đoạn để mặt phẳng đứng dọc được căn chỉnh thẳng.
Biến chứng của phẫu thuật vẹo cột sống cho MFS được Levy và các cộng sự đánh giá tốt.
Tiên lượng hội chứng Marfan
Những tiến bộ trong quản lí các biểu hiện tim mạch của MFS đã làm giảm đáng kể tỉ lệ mắc bệnh và tử vong có liên quan đến tình trạng này. Trước khi liệu pháp dược lý và phẫu thuật đối với bệnh van và gốc động mạch chủ ra đời, tuổi thọ trung bình của bệnh nhân mắc MFS bằng khoảng 2/3 so với dân số khỏe mạnh. Bóc tách động mạch chủ và suy tim sung huyết do dị tật van động mạch chủ và van hai lá chiếm hơn 90% các nguyên nhân gây tử vong đã biết.
Tuổi thọ của bệnh nhân MFS hiện đã tiệm cận với những người không mắc MFS, mặc dù tổn thương tim mạch vẫn là nguyên nhân phổ biến nhất gây tử vong cho họ, hầu như là do đột tử ở bệnh nhân chưa được chẩn đoán trước đó hoặc chẩn đoán mới ở những người có diễn biến bệnh đã tiến triển vượt quá phạm vi điều trị nội khoa hoặc khả năng phẫu thuật để chữa bệnh.