Tác giả: Thạc sĩ – Bác sĩ Hồ Hoàng Kim – ICU Bệnh viện NGUYỄN TRI PHƯƠNG.
Giới thiệu
Viêm tụy cấp là tình trạng viêm tụy mà nguyên nhân phổ biến nhất là do sỏi mật hoặc sử dụng quá nhiều rượu. Ở hầu hết các bệnh nhân, bệnh diễn ra nhẹ, trong đó hồi sức dịch vừa phải, kiểm soát đau và buồn nôn, và cho ăn bằng miệng sớm giúp cải thiện lâm sàng nhanh chóng.
Dạng nặng bao gồm khoảng 20 – 30% bệnh nhân là một tình trạng đe dọa đến tính mạng với tỷ lệ tử vong trong bệnh viện khoảng 15% [1]. Hệ thống phân loại được sử dụng phổ biến nhất cho viêm tụy cấp là phiên bản 2012 của phân loại và định nghĩa Atlanta dựa trên sự đồng thuận quốc tế [2]. Phân loại này xác định hai giai đoạn (sớm và muộn). Mức độ nghiêm trọng được phân loại là nhẹ, trung bình hoặc nghiêm trọng. Dạng nhẹ (viêm tụy phù nề mô kẽ) không có suy nội tạng, biến chứng tại chỗ hoặc hệ thống, và thường hết trong tuần đầu tiên. Nếu có suy nội tạng thoáng qua (dưới 48 giờ), biến chứng cục bộ hoặc làm trầm trọng thêm bệnh đồng mắc, thì được phân loại là vừa. Bệnh nhân bị suy nội tạng kéo dài (hơn 48 giờ) là thể bệnh nặng.
Nhiễm trùng mô tụy hoại tử và xung quanh tụy xảy ra ở khoảng 20 – 40% bệnh nhân bị viêm tụy cấp tính nặng, và có liên quan đến rối loạn chức năng nội tạng. Trong một tổng quan hệ thống và phân tích tổng hợp 6970 bệnh nhân, tỷ lệ tử vong ở bệnh nhân bị hoại tử nhiễm trùng và suy nội tạng là 35,2% trong khi hoại tử vô trùng đồng thời và suy nội tạng có liên quan đến tỷ lệ tử vong là 19,8%. Nếu bệnh nhân bị nhiễm trùng hoại tử mà không bị suy nội tạng, tỷ lệ tử vong là 1,4% [3].
| Bảng 1 Phân loại đánh giá khuyến nghị, phát triển và đánh giá (GRADE) hệ thống phân cấp bằng chứng từ Guyatt et al.[5] | |||
| Grade of recommendation | Clarity of risk/benefit | Quality of supporting evidence | Implications |
| 1A | |||
| Khuyến cáo mạnh mẽ, bằng chứng chất lượng cao | Lợi ích rõ ràng lớn hơn rủi ro và gánh nặng, hoặc ngược lại | RCT không có giới hạn quan trọng hoặc bằng chứng áp đảo từ các nghiên cứu quan sát | Khuyến cáo mạnh mẽ, áp dụng cho hầu hết bệnh nhân trong hầu hết các trường hợp mà không cần do dự |
| 1B | |||
| Khuyến cáo mạnh mẽ, bằng chứng chất lượng vừa phải | Lợi ích rõ ràng lớn hơn rủi ro và gánh nặng, hoặc ngược lại | RCT với những hạn chế quan trọng (kết quả không nhất quán, sai sót về phương pháp, phân tích gián tiếp hoặc kết luận không chính xác) hoặc bằng chứng đặc biệt mạnh mẽ từ các nghiên cứu quan sát | Khuyến cáo mạnh mẽ, áp dụng cho hầu hết bệnh nhân trong hầu hết các trường hợp mà không cần do dự |
| 1C | |||
| Khuyến cáo mạnh mẽ, bằng chứng chất lượng thấp hoặc chất lượng rất thấp | Lợi ích rõ ràng lớn hơn rủi ro và gánh nặng, hoặc ngược lại | Nghiên cứu quan sát hoặc loạt trường hợp | Khuyến cáo mạnh mẽ nhưng có thể thay đổi khi có bằng chứng chất lượng cao hơn |
| 2A | |||
| Khuyến cáo yếu, bằng chứng chất lượng cao. | Lợi ích cân bằng chặt chẽ với rủi ro và gánh nặng. | RCT không có giới hạn quan trọng hoặc bằng chứng áp đảo từ các nghiên cứu quan sát. | Khuyến cáo yếu, hành động tốt nhất có thể khác nhau tùy thuộc vào bệnh nhân, hoàn cảnh điều trị hoặc xã hội |
| 2B | |||
| Khuyến cáo yếu, bằng chứng chất lượng vừa phải. | Lợi ích cân bằng chặt chẽ với rủi ro và gánh nặng. | RCT với những hạn chế quan trọng (kết quả không nhất quán, sai sót về phương pháp, phân tích gián tiếp hoặc kết luận không chính xác) hoặc bằng chứng đặc biệt mạnh mẽ từ các nghiên cứu quan sát. | Khuyến cáo yếu, hành động tốt nhất có thể khác nhau tùy thuộc vào bệnh nhân, hoàn cảnh điều trị hoặc xã hội. |
| 2C | |||
| Khuyến cáo yếu, bằng chứng chất lượng thấp hoặc chất lượng rất thấp. | Sự không chắc chắn trong ước tính lợi ích, rủi ro và gánh nặng; lợi ích, rủi ro và gánh nặng có thể được cân bằng chặt chẽ. | Nghiên cứu quan sát hoặc loạt trường hợp. | Khuyến cáo rất yếu; phương pháp điều trị thay thế có thể là hợp lý như nhau và xem xét. |
Theo phân loại Atlanta 2012 được cập nhật, tụ dịch xung quang tụy liên quan đến hoại tử gọi là tụ dịch hoại tử cấp tính (ANC- acute necrotic collection) và hoại tử có vách hóa (WON- walled- off necrosis) [2]. ANC là tình trạng tụ dịch xuất hiện trong 4 tuần đầu tiên và chứa một lượng dịch và mô hoại tử bao gồm mô tụy và / hoặc các mô xung quanh tụy. WON là một dạng tiến triển sau đó, mô hoại tử tụy và / hoặc xung quang tụy hình thành vách viêm được xác định rõ, tăng cường. Sự hình thành rõ nhất thường mất 4 tuần hoặc lâu hơn sau khi bắt đầu viêm tụy cấp.
Hiện nay, một số xu hướng trong việc kiểm soát viêm tụy cấp mức độ nặng đã thay đổi thực hành lâm sàng của chúng ta; cho ăn đường ruột sớm, vai trò chọn lọc của kháng sinh dự phòng, tránh phẫu thuật ở bệnh nhân hoại tử vô trùng, phương pháp bảo tồn hơn đối với hoại tử nhiễm trùng với can thiệp trì hoãn, dù là nội soi hay phẫu thuật, xử trí viêm tụy đường mật. Mục đích của các hướng dẫn này là để trình bày các tuyên bố đồng thuận quốc tế dựa trên bằng chứng về việc quản lý viêm tụy cấp tính nặng từ sự hợp tác của một hội đồng chuyên gia trong Hội nghị Phẫu thuật Cấp cứu Thế giới vào ngày 27 tháng 6 năm 2018 tại Bertinoro, Ý.
Phương pháp quản lý viêm tụy cấp mức độ nặng
Những hướng dẫn này đã được tạo ra bởi sự hợp tác và thảo luận quốc tế giữa một hội đồng chuyên gia gồm các bác sĩ lâm sàng, thực hành trong lĩnh vực phẫu thuật khẩn cấp và quản lý bệnh nhân bị viêm tụy cấp nặng. Những hướng dẫn đồng thuận này đã được Hiệp hội Phẫu thuật Cấp cứu Thế giới tạo điều kiện thuận lợi và là bản cập nhật tài liệu của Hiệp hội Phẫu thuật Cấp cứu Thế giới 2014 (WSES) về chủ đề này [4].
Các báo cáo được xây dựng và phân loại theo hệ thống phân loại đánh giá, phát triển và đánh giá đề xuất (GRADE) của Guyatt và các đồng nghiệp [5], được tóm tắt trong Bảng 1. Để rõ ràng, các tuyên bố và thảo luận đã được chia thành năm chủ đề: Chẩn đoán, điều trị bằng kháng sinh, Quản lý trong Đơn vị Chăm sóc Chuyên sâu (ICU), Quản lý phẫu thuật và phẫu thuật và Mở bụng.
Kết quả điều trị theo WSES
Câu hỏi chẩn đoán:
- Những tiêu chuẩn để thiết lập chẩn đoán viêm tụy cấp nặng?
- Chẩn đoán hình ảnh phù hợp trong trường hợp nghi ngờ viêm tụy cấp nặng là gì? Vai trò của hình ảnh cộng hưởng từ (MRI), chụp cắt lớp vi tính (CT), siêu âm (US), siêu âm nội soi (EUS) và các xét nghiệm phụ trợ khác là gì?
- Những thông số cận lâm sàng nào nên được xem xét trong quá trình chẩn đoán?
- Làm thế nào để chấn đoán các nguyên nhân khác nhau?
- Điểm số nào được chỉ định để đánh giá nguy cơ?
- Thời gian và xét nghiệm phù hợp cho các thăm dò hình ảnh để theo dõi trong giai đoạn sớm là gì?
Tuyên bố đồng thuận (phân độ nghiêm trọng)
- Viêm tụy cấp mức độ nặng có liên quan đến suy cơ quan dai dẳng (tim mạch, hô hấp và / hoặc thận) và tỷ lệ tử vong cao. Cả hai hệ thống phân loại mới, Phân loại Atlanta sửa đổi và Phân loại viêm tụy cấp tính dựa trên yếu tố xác định, đều tương tự nhau trong việc xác định chẩn đoán và mức độ nghiêm trọng của viêm tụy cấp (1C).
- Bệnh nhân bị suy nội tạng dai dẳng khi bị hoại tử nhiễm trùng có nguy cơ tử vong cao nhất (1C).
- Bệnh nhân bị suy nội tạng nên được đưa vào phòng chăm sóc đặc biệt bất cứ khi nào có thể (1C).
Thảo luận: Viêm tụy cấp (AP) đại diện cho một bệnh đặc trưng bởi viêm cấp mô tụy và phá hủy tế bào vẩy mô học [6]. Chẩn đoán AP đòi hỏi ít nhất sự hiện diện của hai trong ba tiêu chuẩn sau: (i) đau bụng phù hợp với bệnh, (ii) bằng chứng sinh hóa của viêm tụy (amylase huyết thanh và / hoặc lipase lớn hơn ba lần giới hạn bình thường trên) và (iii) những phát hiện đặc trưng từ hình ảnh học ổ bụng [2].
Hầu hết bệnh nhân (80 – 85%) sẽ phát triển một đợt bệnh nhẹ (tự giới hạn, tỷ lệ tử vong <1 – 3%), nhưng khoảng 20% sẽ có một đợt AP vừa hoặc nặng, với tỷ lệ tử vong từ 13 – 35% [7, 8]. Do đó, điều quan trọng là chẩn đoán (hoặc tiên lượng tốt hơn) một đợt viêm tụy cấp tính nặng (SAP) và nhận diện các bệnh nhân có nguy cơ cao bị biến chứng.
Trong gần 20 năm, Phân loại Atlanta năm 1992 đã được sử dụng, nhưng một số định nghĩa và phân loại đã gây nhầm lẫn [9]. Trong một bản nhìn lại của 447 bài báo, Bollen et al. thấy rằng các định nghĩa thay đổi của Phân loại Atlanta năm 1992 đã được sử dụng trong hơn một nửa các nghiên cứu và các định nghĩa thường được sử dụng sai [9].
Những hiểu biết quan trọng về quản lý AP, hiểu rõ hơn về sinh lý bệnh của suy nội tạng và viêm tụy hoại tử, chẩn đoán hình ảnh được cải thiện, các kỹ thuật xâm lấn tối thiểu và các nghiên cứu cho thấy các bệnh nhân thuộc nhóm nghiêm trọng của Phân loại Atlanta năm 1992 bao gồm các phân nhóm rất khác nhau, chỉ ra rằng một phân loại chính xác hơn cần được đưa ra. Trong một đánh giá năm 2004, Johnson et al. báo cáo rằng suy nội tạng kéo dài (POF- persistant organ failure) trong hơn 48 giờ trong tuần đầu tiên có liên quan mạnh mẽ đến nguy cơ tử vong hoặc biến chứng cục bộ [10]. Họ đã sử dụng một cơ sở dữ liệu trước đó gồm 290 bệnh nhân với tiên lượng SAP được tuyển dụng từ 78 bệnh viện thông qua 18 trung tâm ở Anh và cũng trích dẫn rằng giải quyết suy nội tạng trong vòng 48 giờ cho thấy tiên lượng tốt.
Một nghiên cứu hồi cứu trên 759 bệnh nhân mắc AP do Đại học Edinburgh thực hiện cho thấy 25,4% bệnh nhân mắc hội chứng đáp ứng viêm toàn thân kéo dài (SIRS) đã chết, so với 8% với SIRS thoáng qua và 0,7% không có SIRS [11].Những nghiên cứu này và các nghiên cứu khác cho thấy rằng suy nội tạng là trọng tâm của định nghĩa về SAP. Nếu suy nội tạng kéo dài hơn 48 giờ, bệnh nhân có nguy cơ tử vong cao (một trong ba) và có thể thành lập một phân loại thể nghiêm trọng. Ngoài ra, điều quan trọng cần nhắc là thời gian bị bệnh có phản ứng viêm rõ rệt (SIRS) xảy ra trước suy nội tạng và nếu có SIRS, bệnh nhân có nguy cơ tiến triển thành suy nội tạng, và phải thực hiện mọi nỗ lực để phục hồi tình trạng bình thường càng sớm càng tốt [12].
Gần như đồng thời vào năm 2012, hai hệ thống phân loại mới của AP đã được xuất bản: Phân loại dựa trên quyết định mức độ nghiêm trọng của viêm tụy cấp tính (DBC) và Phân loại Atlanta sửa đổi 2012 (RAC) [2, 13]. Phân loại mới DBC dựa trên một cuộc khảo sát dựa trên web toàn cầu và một hội thảo quốc tế dành riêng với những người đóng góp từ các chuyên ngành khác nhau: thư mời e-mail đã được gửi tới 528 bác sĩ chuyên khoa tụy từ 55 quốc gia và có 240 bác sĩ từ 49 quốc gia tham gia khảo sát. Trong Đại hội Thế giới của Hiệp hội Tụy Quốc tế 2011 (Kochi, Ấn Độ), khoảng 100 người tham gia đã thảo luận về phân loại được đề xuất và cố gắng đồng ý về các định nghĩa [13]. RAC được tạo ra bởi một quá trình tham vấn dựa trên web lặp đi lặp lại kết hợp các phản hồi từ các thành viên của 11 hiệp hội tuyến tụy quốc gia và quốc tế. Các sửa đổi đã được thực hiện để phản hồi các bình luận và tham vấn dựa trên web được lặp lại ba lần. Sự đồng thuận cuối cùng đã được xem xét và chỉ những tuyên bố dựa trên bằng chứng được công bố mới được giữ lại [2]. RAC là một tổng quan rộng hơn DBC: ngoài phân loại mức độ nghiêm trọng, nó cung cấp một định nghĩa rõ ràng về chẩn đoán AP, nêu bật sự khởi đầu của cơn đau như một điểm tham chiếu quan trọng, và xác định các biến chứng cục bộ riêng lẻ cũng như viêm tụy mô kẽ và hoại tử [2, 14]. RAC có ba loại: nhẹ, nặng vừa và nặng, theo suy nội tạng và biến chứng tại chỗ hoặc toàn thân. DBC đã thêm một loại thứ tư: thể rất nghiêm trọng, dựa trên hai yếu tố chính quyết định tỷ lệ tử vong: hoại tử mô tụy có nhiễm trùng (xung quanh) và suy nội tạng (Bảng 2).
| Bảng 2 Định nghĩa về mức độ nghiêm trọng trong viêm tụy cấp. | |
| Phân loại của Atlanta (RAC) | Phân loại dựa theo yếu tố xác định(DBC) |
Viêm tụy cấp nhẹ (AP):
AP mức độ trung bình:
AP nặng:
|
AP nhẹ:
AP trung bình:
AP nặng:
AP rất nặng:
|
Sau đó, Bansal et al. trong một đoàn hệ gồm 248 bệnh nhân thấy rằng RAC và DBC tương tự nhau về các biến cố nhập ICU, cần dẫn lưu qua da, cần phẫu thuật và tử vong nội viện. Phân loại rất nghiêm trọng theo DBC đã xác định bệnh nặng nhất [15]. Nawaz et al. đã thu thập được 256 bệnh nhân trong một nghiên cứu tiến cứu và phân độ một mức độ nghiêm trọng theo cả ba phân loại: RAC, DBC và Atlanta 1992. Họ thấy rằng các loại nghiêm trọng của RAC và DBC phản ánh chính xác kết cuộc lâm sàng và vượt trội so với Atlanta 1992 (đánh giá tỷ lệ tử vong, nhập viện ICU, thời gian nằm ICU) [16].
Hai năm sau, một nghiên cứu hồi cứu trên 395 bệnh nhân ở Trung Quốc, với tỷ lệ tử vong tại bệnh viện là 8,9%, cho kết quả tương tự. Các tác giả nhận thấy rằng cả ba hệ thống phân loại (RAC, BDC và Atlanta 1992) đều phân loại chính xác mức độ nghiêm trọng của AP. Tuy nhiên, RAC và DBC hoạt động tốt hơn Atlanta 1992 và họ có thể so sánh với nhau trong việc dự đoán tiên lượng lâm sàng dài hạn, các biến chứng chính và các can thiệp lâm sàng [17].
Choi và cộng sự. nghiên cứu 553 bệnh nhân mắc AP được nhận vào một trung tâm duy nhất trong thời gian 7 năm, xác nhận RAC tương quan tốt với kết quả lâm sàng, mặc dù không xem xét hoại tử nhiễm trùng. Tuy nhiên, những bệnh nhân trong nhóm nặng và bị hoại tử nhiễm trùng (được phân loại là nguy kịch trong DBC) nên được xem xét tách biệt với những người không mắc bệnh (tỷ lệ tử vong tăng gấp bốn lần: lên tới 32%) [18]. Một nghiên cứu khác đã phân tích 543 đợt AP từ 459 bệnh nhân trong một đoàn hệ tiến cứu. Họ phát hiện ra rằng các loại mức độ nghiêm trọng khác nhau cho mỗi hệ thống phân loại có liên quan đến sự khác biệt có ý nghĩa thống kê và lâm sàng về thời gian nằm viện, cần nhập viện tại khoa chăm sóc đặc biệt, hỗ trợ dinh dưỡng, điều trị xâm lấn và tử vong tại bệnh viện. Ngoài ra, so sánh trực tiếp giữa các loại của cả hai phân loại (sau khi đồng nhất loại nghiêm trọng và rất nghiêm trọng của DBC) không mang lại sự khác biệt đáng kể nào [19].
Nói chung, bệnh nhân bị suy cơ quan (được xác định chính xác bằng cách sử dụng một trong các tiêu chuẩn đã được thiết lập hoặc hệ thống tính điểm) cần được chuyển khẩn cấp đến ICU. Theo đó, có thể không cần thiết phải chuyển bệnh nhân bị suy cơ quan tạm thời sang trung tâm y tế cấp ba hoặc ICU. Tuy nhiên, để xác nhận suy cơ quan dai dẳng, nó cần phải được ghi nhận trong hơn 48 giờ.
Tuyên bố đồng thuận (hình ảnh)
1. Khi nhập viện, siêu âm (US) nên được thực hiện để xác định nguyên nhân của viêm tụy cấp (đường mật) (1C).
2. Khi nghi ngờ, chụp cắt lớp vi tính (CT) cung cấp bằng chứng tốt về sự hiện diện hoặc vắng mặt của viêm tụy (1C).
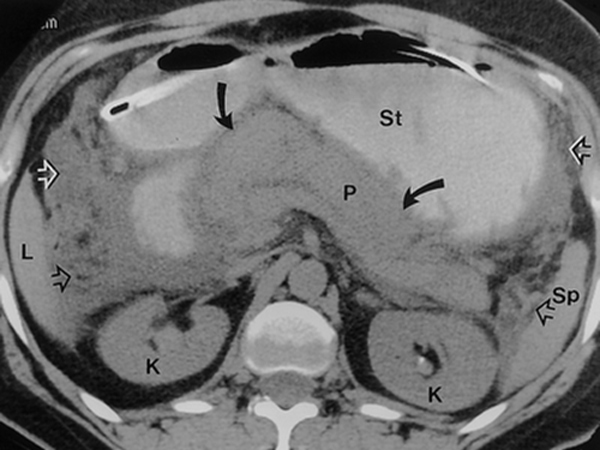
3. Tất cả các bệnh nhân bị viêm tụy cấp tính nặng cần được đánh giá bằng chụp cắt lớp vi tính cản quang (CE-CT) hoặc chụp cộng hưởng từ (MRI). Thời gian tối ưu cho lần đánh giá CE-CT đầu tiên là 72 – 96 h sau khi xuất hiện triệu chứng (1C).
4. Chụp đường mật cộng hưởng từ (MRCP) hoặc siêu âm nội soi nên được xem xét để sàng lọc sỏi ống mật chủ ở bệnh nhân không rõ nguyên nhân (1C).
Thảo luận: Khi nhập viện, cần xác định nguyên nhân của AP, để dự đoán nhu cầu điều trị xác định (ví dụ, bệnh sỏi mật) và để tránh tái phát (ví dụ, uống rượu, tăng triglyceride máu) [20]. Việc điều trị và theo dõi phụ thuộc vào nguyên nhân của AP. Một siêu âm qua thành bụng nên được thực hiện khi nhập viện (để thực hiện cắt túi mật trong viêm tụy đường mật khi thích hợp). Hầu như tất cả các hướng dẫn của AP trên toàn thế giới (dựa trên các sửa đổi và phân tích tổng hợp) đều khuyên bạn nên thực siêu âm khi nhập viện hoặc trong 48 giờ đầu [7, 8, 20 – 23].
Ở phần lớn bệnh nhân mắc AP, CT không bắt buộc [24]. Sự mở rộng của mô tụy hoại tử (hay xung quanh) có thể được phát hiện bằng CT cản quang (CECT) sau 72 giờ kể từ khi bắt đầu AP [20]. Mối lo ngại đã được đặt ra đối với tổn thương thận cấp tính sau tiêm cản quang (AKI). Một phân tích tổng hợp gần đây với 28 nghiên cứu quan sát và hơn 100.000 người tham gia không tìm thấy bằng chứng nào cho thấy mối liên quan của thuốc cản quang với AKI, liệu pháp thay thế thận hoặc tử vong [25]. Tuy nhiên, không có nghiên cứu so sánh ở những bệnh nhân bị viêm tụy cấp hoặc nhiễm trùng huyết nặng, và do đó, nên thận trọng khi áp dụng. Chụp CT sớm sẽ không cho thấy các vùng hoại tử / thiếu máu cục bộ và sẽ không làm thay đổi cách thức quản lý lâm sàng trong tuần đầu tiên của bệnh. Tuy nhiên, khi chẩn đoán không chắc chắn, CT nên được xem xét, đặc biệt để loại trừ viêm phúc mạc thứ phát do thủng hoặc thiếu máu cục bộ mạc treo. Nó cũng cho thấy tình trạng xuất huyết hoạt động và huyết khối liên quan đến viêm tụy [21, 22].
CECT đã được chứng minh là mang lại tỷ lệ phát hiện sớm gần 90% với độ nhạy gần 100% sau 4 ngày đối với hoại tử mô tụy [26]. Balthazar et al. đã thiết lập một chỉ số mức độ nghiêm trọng của CT (Bảng 3) phân loại viêm tụy dựa trên mức độ viêm, sự hiện diện của tụ dịch và mức độ hoại tử: điểm càng cao càng có liên quan đến tăng tỷ lệ mắc bệnh và tử vong [26-28].
CECT là phương thức chẩn đoán hình ảnh được lựa chọn để chẩn đoán, phân loại và phát hiện các biến chứng của viêm tụy cấp và có vai trò chính trong việc đánh giá bệnh nhân mắc AP đã biết hoặc nghi ngờ: (i) chẩn đoán, (ii) phân loại mức độ nghiêm trọng và ( iii) phát hiện các biến chứng, đặc biệt là xác định và định lượng hoại tử mô tụy (xung quanh) [20, 24, 26]. Tuy nhiên, quét CT lặp lại thường xuyên làm tăng tổng liều phóng xạ và có tác dụng hạn chế trong quá trình ra quyết định tiếp theo [29].
MRI thích hợp hơn với CECT ở bệnh nhân dị ứng với cản quang i-ốt, ở bệnh nhân suy thận/suy thận (MRI không điều hòa), ở bệnh nhân trẻ hoặc mang thai để giảm thiểu phơi nhiễm phóng xạ để xác định mô bệnh lý (ví dụ, mảnh vụn hoặc mô hoại tử), nhưng ít nhạy hơn CT để phát hiện khí trong các khối tụ dịch [24, 26]. CT không có độ tương phản là một lựa chọn thay thế cho hai nhóm bệnh nhân đầu tiên, nếu MRI không có sẵn.
| Bảng 3 Chỉ số mức độ nghiêm trọng trên CT (Được sửa đổi từ: Balthazar EJ, Robinson DL, Megibow AJ, Ranson JH. Viêm tụy cấp: giá trị của CT trong việc thiết lập tiên lượng. X quang. 1990; 174: 331 Thay6 [27]). | ||
| CT | Điểm | Định nghĩa |
| A | 0 | Tụy bình thường |
| B | 1 | Tụy to |
| C | 2 | Tụy viêm hay/hoặc thâm nhiễm mỡ quanh tụy |
| D | 3 | 1 ổ tụ dịnh quanh tụy |
| E | 4 | 1 ổ tụ dịnh quanh tụy |
| % hoại tử | Điểm | Định nghĩa |
| Không | 0 | Bắt thuốc đồng nhất |
| <30% | 2 | Không bắt thuốc vùng (s) của tuyến tương đương kích thước của đầu tụy |
| 30-50% | 4 | Không bắt thuốc 30–50% tuyến |
| >50% | 6 | Không bắt thuốc > 50% tuyến |
| CTSI | Bệnh xuất | Tử xuất |
| 0-1 | 0 | 0 |
| 2-3 | 8% | 3% |
| 4-6 | 35% | 6% |
| 7-10 | 92% | 17% |
CTSI = điểm phân độ (0–4) + điểm hoại tử (0–6).
Khi US không cho thấy sỏi mật, bùn, hoặc tắc nghẽn đường mật và trong trường hợp không có viêm đường mật và / hoặc xét nghiệm chức năng gan bất thường cho thấy tắc nghẽn đường mật, chụp đường mật cộng hưởng từ (MRCP) hoặc siêu âm nội soi (EUS) thay vì chẩn đoán nội soi mật tụy ngược dòng (ERCP) nên được sử dụng để sàng lọc bệnh sỏi đường mật, nếu không có nguyên nhân nào khác có thể được chẩn đoán [20, 24]. Trong một đoàn hệ hồi cứu nghiên cứu 221 bệnh nhân, MRCP có độ nhạy 97,98% và độ đặc hiệu 84,4% đối với sỏi túi mật tránh phải thực hiện chẩn đoán hình ảnh xâm lấn ở hầu hết các bệnh nhân nghi ngờ mắc sỏi đường mật [30].
1. Giá trị giới hạn của huyết thanh amylase và lipase thường được xác định là gấp ba lần giới hạn trên.
2. Mức protein phản ứng C ≥ 150 mg/l vào ngày thứ ba có thể được sử dụng như một yếu tố tiên lượng cho viêm tụy cấp tính nặng (2A).
3. Hematocrit > 44% đại diện cho một yếu tố nguy cơ độc lập của hoại tử mô tụy (1B).
4. Urê > 20 mg/dl là một yếu tố dự báo độc lập về tỷ lệ tử vong (2B).
5. Procalcitonin là xét nghiệm nhạy nhất để phát hiện nhiễm trùng mô tụy và giá trị huyết thanh thấp dường như là yếu tố dự báo âm tính mạnh của hoại tử nhiễm trùng (2A).
6. Trong trường hợp không có sỏi mật hoặc tiền sử sử dụng rượu đáng kể, nên đo nồng độ triglyceride và canxi huyết thanh. Nồng độ triglyceride huyết thanh trên 11,3 mmol/l (1000 mg/dl) cho thấy nó là nguyên nhân (2C).
Thảo luận: Đo lường enzyme tụy trong huyết thanh là “tiêu chuẩn vàng” để chẩn đoán AP [31]. Trong một đợt của AP, amylase, lipase, elastase và trypsin được giải phóng vào máu cùng một lúc nhưng độ thanh thải thay đổi tùy thuộc vào thời điểm lấy mẫu máu. Amylase là một loại enzyme do tuyến tụy tiết ra, và cả tuyến nước bọt, ruột non, buồng trứng, mô mỡ và cơ xương. Có hai đồng phân chính của amylase: tụy và nước bọt, và chức năng hàng đầu là tiêu hóa tinh bột, glycogen, và poly- và oligosacarit liên quan, bằng cách thủy phân [32]. Trong AP, nồng độ amylase trong huyết thanh thường tăng trong vòng 6 đến 24 giờ, đạt cực đại ở 48 giờ và giảm xuống mức bình thường hoặc gần mức bình thường trong 3 đến 7 ngày tiếp theo [23, 32, 33].
Lipase là một enzyme khác do tuyến tụy tiết ra. AP là lý do chính làm tăng lipase, và nhiều tác giả nhấn mạnh rằng lipase đặc hiệu hơn, nhưng cũng có thể được tìm thấy tăng trong các bệnh không do tụy như bệnh thận, viêm ruột thừa, viêm túi mật cấp, viêm tụy mãn tính, tắc ruột, v.v. [23]. Trong AP, lipase huyết thanh vẫn tăng trong thời gian dài hơn amylase huyết thanh. Nó tăng trong vòng 4 đến 8 giờ, cực đại ở mức 24 giờ và giảm xuống mức bình thường hoặc gần mức bình thường trong 8 đến 14 ngày tiếp theo [32, 33].
Trypsinogen là zymogen của enzyme trypsin tuyến tụy. Trong AP, nồng độ trypsinogen trong huyết thanh và nước tiểu thường tăng lên mức cao trong vòng vài giờ và giảm trong 3 ngày [32, 33]. Nói chung, lipase huyết thanh được coi là một dấu hiệu chẩn đoán đáng tin cậy hơn của AP so với amylase huyết thanh. Không có xét nghiệm đơn lẻ nào cho thấy độ chính xác cho chẩn đoán là tối ưu, nhưng hầu hết các hướng dẫn và khuyến cáo hiện tại chỉ ra rằng lipase nên được ưu tiên hơn so với amylase toàn phần và p-amylase [32]. Những lý do chính ủng hộ lipase trên cả hai loại amylase để chẩn đoán viêm tụy cấp bao gồm độ nhạy cao hơn và cửa sổ chẩn đoán lớn hơn [32]. Một tổng quan của Cochrane với mục đích so sánh độ chính xác chẩn đoán của các enzyme tuyến tụy khác nhau trong chẩn đoán AP cho thấy độ nhạy và độ đặc hiệu của 72% và 93% đối với amylase huyết thanh, và 79% và 89% đối với lipase huyết thanh, tương ứng [33].
Chang et al. được tìm thấy trong một phân tích tổng hợp bao gồm 13 nghiên cứu cho thấy xét nghiệm que thử trypsinogen-2 là một thử nghiệm trên giường nhanh chóng và không xâm lấn với độ nhạy 82% và độ đặc hiệu 94% cho AP [34].
Nhiều dấu ấn sinh học đã được nghiên cứu như là yếu tố dự báo sớm về mức độ nghiêm trọng của AP để điều trị có thể được điều chỉnh tối ưu để ngăn ngừa các biến chứng [34, 35]. Tại thời điểm này, không có xét nghiệm trong phòng thí nghiệm thực tế có sẵn nào hoặc luôn chính xác để dự đoán mức độ nghiêm trọng ở bệnh nhân mắc AP [23].
Trong trường hợp không có sỏi mật hoặc tiền sử sử dụng rượu đáng kể, nên đo và coi triglyceride huyết thanh là nguyên nhân nếu giá trị > 11,3 mmol/l (> 1000 mg/dl) [23].
Nhiều sách giáo khoa coi protein phản ứng C (CRP) là tiêu chuẩn vàng để đánh giá mức độ nghiêm trọng của bệnh [36]. Sử dụng giá trị giới hạn từ 110 đến 150 mg/l, độ nhạy và độ đặc hiệu dao động từ 38 đến 61% và 89 đến 90%, tại thời điểm nhập viện [36]. Hạn chế lớn của CRP là mức cực đại chỉ đạt được sau 48 đến 72 giờ. Trong một nghiên cứu tiền cứu trên 175 bệnh nhân được chia thành viêm tụy cấp nhẹ và không nhẹ theo phân loại Atlanta, CRP và IL-6 kết hợp đã chứng minh khả năng phân biệt tốt với diện tích dưới đường cong 0,804 [37].
Resistin là một hormone peptide mới được xác định, được tiết ra đặc biệt bởi các tế bào mỡ có thể gây béo phì và tăng triglyceride máu, do sự liên quan của nó với kháng insulin. Các nghiên cứu đã cho thấy rằng resistin cũng là một cytokine quan trọng trong các phản ứng viêm và trong sự điều hòa của các cytokine khác [38]. Trong một nghiên cứu quan sát tiến cứu, nồng độ resistin tốt hơn để dự đoán SAP so với mức CRP hoặc WBC vào ngày thứ 3 và tốt hơn mức CRP để dự đoán sự phát triển của hoại tử [38]. Một nghiên cứu đoàn hệ hồi cứu từ dữ liệu của 90 bệnh nhân cho thấy resistin có độ chính xác tương tự với điểm số Sinh lý học cấp tính và Đánh giá sức khỏe mãn tính II (APACHE II) khi dự đoán POF và leptin có tương quan yếu với POF [39].
Các phát hiện trong phòng thí nghiệm khác được sử dụng để mô tả một đợt của SAP là BUN > 20 mg/dl (> 7,14 mmol/l) hoặc BUN tăng, hematocrit (HCT) > 44% hoặc tăng HCT, dehydrogenase (LDH) và procalcitonin để dự đoán hoại tử ở bệnh nhân bị hoại tử tụy đã được xác nhận [36, 40 – 43].
Giá trị procalcitonin là 3,8 ng / ml hoặc cao hơn trong vòng 96 giờ sau khi xuất hiện triệu chứng cho thấy hoại tử tụy với độ nhạy và độ đặc hiệu là 93% và 79% [36, 42]. Mức độ lactate huyết thanh khi nhập viện dự đoán AP nặng, tử vong và nhập viện ICU, nhưng nên được coi là dưới mức tối ưu nếu như được đánh giá một cách đơn lẻ [44].
Tuyên bố đồng thuận (chẩn đoán trong viêm tụy chưa rõ căn nguyên)
1. Trong viêm tụy chưa rõ căn nguyên, cần loại trừ nguyên nhân đường mật bằng hai lần siêu âm và nếu cần MRCP và / hoặc siêu âm (EUS) qua nội soi, để ngăn ngừa viêm tụy tái phát (2B).
Thảo luận: AP chưa rõ căn nguyên được định nghĩa là viêm tụy không có nguyên nhân được chẩn đoán sau các xét nghiệm hình ảnh và xét nghiệm ban đầu. Ở những bệnh nhân mắc AP chưa rõ căn nguyên, nên thực hiện ít nhất hai lần kiểm tra US để loại trừ nguyên nhân đường mật [31]. Tiếp theo đó, CE-CT và EUS, sau khi giai đoạn cấp tính kết thúc, là các bước tiếp theo để đánh giá bệnh vi sỏi mật, tân sinh hoặc viêm tụy mãn tính. Nếu EUS âm tính, MRI nên được thực hiện để xác định các bất thường về hình thái [31]. Cắt túi mật nội soi dường như để ngăn ngừa viêm tụy cấp chưa rõ căn nguyên tái phát; tuy nhiên, hiện tại không đủ bằng chứng để hỗ trợ phương pháp này thường xuyên [45].
Tuyên bố đồng thuận (điểm nguy cơ)
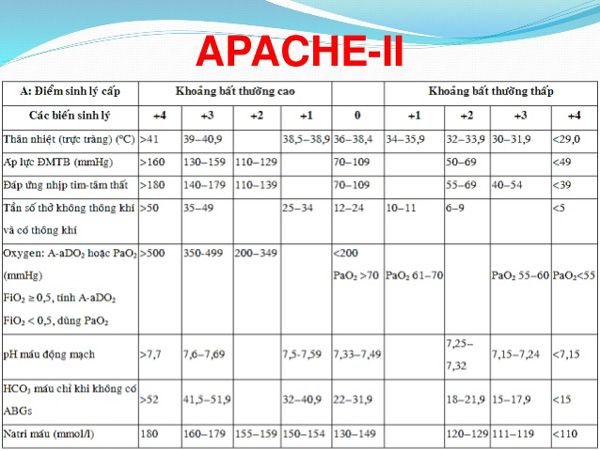
1. Không có điểm số tiên lượng chuẩn vàng nào để dự đoán viêm tụy cấp nặng. Có lẽ chỉ số đầu giường về mức độ nghiêm trọng của viêm tụy cấp (BISAP) là một trong những chỉ số chính xác và có thể áp dụng trong thực hành lâm sàng hàng ngày vì tính đơn giản và khả năng dự đoán mức độ nghiêm trọng, tử vong và suy nội tạng cũng như APACHE-II (rất phức tạp) và các điểm số khác (1B).
Thảo luận: Một số hệ thống tính điểm đã được phát triển để dự đoán SAP, nhưng bằng chứng về hiệu suất dự đoán của chúng là khác nhau [46, 47]. Hiện tại, không có tổng quan hệ thống nào bao gồm các nghiên cứu đánh giá tính chính xác của các hệ thống tính điểm lâm sàng khác nhau được sử dụng để dự đoán mức độ nghiêm trọng và tử vong ở những người bị viêm tụy cấp. Cơ sở dữ liệu tổng quan hệ thống của Cochrane đang phát triển một giao thức để tổng hợp các nghiên cứu đánh giá độ chính xác dự đoán của các hệ thống tính điểm lâm sàng (được đo khi nhập viện và tối đa 48 giờ sau khi nhập viện) [46].Hầu hết các điểm dự đoán trong AP tập trung vào kết cuộc tử vong. Với tỷ lệ tử vong chung giảm dần trong những thập kỷ qua, cần xem xét liệu tử vong có còn là kết quả chính để tiên lượng viêm tụy [48] hay không.
Một khía cạnh khác là ít nhiều tất cả các điểm số nghiêm trọng đều mất hơn 24 giờ để phân tầng bệnh nhân và có lẽ điều đó thể hiện sự mất thời gian ở một số bệnh nhân bị bệnh nặng [48]. Một nghiên cứu đoàn hệ hồi cứu từ Vương quốc Anh thực hiện ở 159 ICU đánh giá 2.462 bệnh nhân nhập viện ICU với SAP cho thấy 75% bệnh nhân cần được chăm sóc đặc biệt đã được chuyển đến ICU trong 72 giờ đầu nhập viện, trong thời gian trung bình -transfer 24 h sau khi nhập học [49]. Theo thời gian, hầu hết các điểm số được dựa trên nhân khẩu học của bệnh nhân, đặc điểm lâm sàng, thông số trong phòng thí nghiệm hoặc phương thức chẩn đoán hình ảnh và được đánh giá khi nhập viện hoặc trong vòng 48 giờ: tiêu chuẩn Ranson (1974), điểm số của Glasgow-Imrie (1978), đánh giá Sinh lý học cấp tính và Sức khỏe mãn tính II (APACHE II), Điểm sinh lý cấp tính đơn giản (SAPS II) (1984), Đánh giá suy cơ quan (SOFA), chỉsố mức độ nghiêm trọng trên CT (CTSI), Chỉsố mức độ nghiêm trọng tại giường của bệnh viêm tụy cấp tính (BISAP) (2008), chỉ số nghiêm trọng của Nhật [46].
Các yếu tố dự đoán (hoặc dự đoán khả năng) có trong hầu hết các hệ thống tính điểm được đề cập ở trên bao gồm tuổi, suy cơ quan hoặc suy giảm miễn dịch, tiền sử bệnh mãn tính, nhiệt độ, huyết áp, nhịp tim, nhịp hô hấp, chỉ số khối cơ thể, mức độ ý thức, sự hiện diện viêm phúc mạc, sự hiện diện của suy thận cấp, số lượng bạch cầu trong máu, hematocrit máu, số lượng tiểu cầu trong máu, đường huyết, BUN, creatinine huyết thanh, transaminase huyết thanh, dehydrogenase huyết thanh, canxi huyết thanh, điện giải đồ huyết thanh, bilirunin huyết thanh , độ bão hòa oxy, pH và dữ trữ kiềm dư, và nhiều phương thức hình ảnh mà chủ yếu là CT.
Điểm số Apache II đánh giá điểm sức khỏe mãn tính và 12 phép đo sinh lý, nhưng không đặc hiệu cho AP và không được thiết kế để đánh giá hàng ngày ở bất kỳ bệnh nhân nào. Ưu điểm của điểm số này là nó là một công cụ được xác nhận rộng rãi và có thể được thực hiện bất cứ lúc nào, nhưng nó có nhược điểm; tức là, cồng kềnh và không phải tất cả các tham số đều được thu thập thường xuyên [48]. Trong một nghiên cứu trên 81 bệnh nhân liên tiếp bị AP, Thandassery et al. phát hiện ra rằng các yếu tố dự đoán độc lập về sự xuất hiện của hoại tử bị nhiễm trùng là hạ huyết áp và điểm APACHE II sau 24 giờ nhập viện [50].
Một nghiên cứu trên 161 bệnh nhân đã đánh giá việc lượng giá và so sánh khả năng dự đoán sớm của các thông số khác nhau được sử dụng rộng rãi nhất trong AP. Họ đã tìm thấy các giá trị ngưỡng đáng kể để dự đoán AP nặng là Ranson ≥ 3, BISAP ≥ 2, APACHE-II ≥ 8, CTSI ≥ 3 và CRP ở mức 24 h ≥ 21 mg/dl (> 210 mg/l). Họ kết luận rằng các hệ thống tính điểm khác nhau cho thấy độ chính xác dự đoán tương tự về mức độ nghiêm trọng của AP, nhưng APACHE-II đã chứng minh độ chính xác cao nhất cho dự đoán của SAP [51].
Chỉ số PPV cho điểm số Ranson dao động từ 28,6 đến 49% (độ nhạy 75, 87%, độ đặc hiệu 68 – 77,5%), đối với điểm số của Glasgow từ 59 đến 66% (độ nhạy 61, 71%, độ đặc hiệu 88, 89%), cho điểm số APACHE II, 55,6% sau 48 giờ (độ nhạy 83,3%, độ đặc hiệu 91%) và đối với điểm số APACHE- O 54-80% (độ nhạy 69-74%, độ đặc hiệu 86-90%). Tất cả các điểm số này chỉ có thể được đánh giá sau 48 giờ, và do đó không cho phép phân tầng rủi ro khi nhập viện. Mặc dù có những điểm yếu, những điểm số này vẫn hữu ích để chứng minh hoặc loại trừ bệnh nặng [31]. BISAP, một hệ thống chấm điểm tiên lượng được phát triển gần đây, đã được đề xuất như một phương pháp đơn giản để dự đoán AP nghiêm trọng so với các hệ thống tính điểm truyền thống. BISAP đại diện cho một từ viết tắt của các tham số được đánh giá trong điểm số (Bảng 3) [48].
| Bảng 4 Chỉ số đầu giường về mức độ nghiêm trọng của viêm tụy cấp (BISAP) |
| BISAP: ghi một điểm cho mỗi tiêu chí sau |
| BUN > 8,9 mmol / L.
Tình trạng tinh thần bị suy giảm. Hội chứng đáp ứng viêm toàn thân. Tuổi> 60 tuổi Tràn dịch màng phổi trên X quang. |
Điểm số BISAP được lấy từ dữ liệu từ dân số 17.992 bệnh nhân và được xác nhận trên dân số 18.256 bệnh nhân tại Hoa Kỳ [52]. Nó có độ chính xác tương tự với điểm số APACHE-II để dự đoán tử vong và là một hệ thống tính điểm rất đơn giản có thể dễ dàng áp dụng trong các giai đoạn sớm nhất. Một trong những điểm chính của nghiên cứu này là nó có thể xác định bệnh nhân có nguy cơ tử vong cao hơn trước khi bắt đầu suy tạng [52]. Một phân tích hồi cứu của 303 bệnh nhân cho thấy BISAP dự đoán mức độ nghiêm trọng, tử vong và đặc biệt là suy tạng (OF) ở AP tương tự APACHE-II, và tốt hơn các tiêu chuẩn của Ranson, chỉ số độ nghiêm trọng trên CT, CRP, hematocrit và BMI. Điểm BISAP của hai là giá trị cắt có ý nghĩa thống kê trong chẩn đoán viêm tụy cấp nặng, suy tạng và tử vong [53] (Bảng 4).
Nhiều nghiên cứu trích dẫn rằng BMI, béo phì và thừa cân là những yếu tố nguy cơ độc lập để phát triển AP nặng, biến chứng cục bộ hoặc tử vong [54, 55]. Một nghiên cứu được thực hiện ở hai bệnh viện từ Nam Kinh, Trung Quốc, đoàn hệ một nhóm 1073 bệnh nhân để phát triển một số điểm mới và 326 bệnh nhân để xác nhận nó, xác nhận rằng những thay đổi về áp lực trong ổ bụng (IAP) và BMI có liên quan đáng kể đến mức độ nghiêm trọng của AP [46 ]. Ngoài ra, họ thấy rằng mô hình mới sử dụng BMI và thay đổi IAP có độ nhạy và độ đặc hiệu tốt hơn (77,6% và 82,6%) so với APACHE-II (73,1% và 81,7%), BISAP (68,7% và 76,2%), CTSI ( 70,6% và 78,5%) và điểm của Ranson (68,5% và 75,9%) [55].
Tuyên bố đồng thuận (hình ảnh theo dõi)
1. Trong viêm tụy cấp mức độ nặng (chỉ số mức độ nghiêm trọng chụp cắt lớp vi tính ≥ 3), chụp CECT được chỉ định 7-10 ngày sau đó kể từ lần chụp CT ban đầu (1C).
2. Chỉ nên chụp CE-CT bổ sung nếu tình trạng lâm sàng xấu đi hoặc không cho thấy sự cải thiện liên tục hoặc khi xem xét can thiệp xâm lấn được cân nhắc (1C).
Thảo luận: Bệnh nhân bị AP nhẹ không cần chụp CT trong phần lớn các trường hợp. Những bệnh nhân này sẽ yêu cầu thêm CT chỉ khi có sự thay đổi về tình trạng lâm sàng của bệnh nhân, mà điều này cho thấy một biến chứng mới [20].
CT theo dõi định kỳ (ví dụ: hàng tuần hoặc cứ sau 10 ngày) được ủng hộ trong một số hướng dẫn, nhưng thiếu bằng chứng để chứng minh cho thực hành này. Phần lớn các biến chứng ở bệnh nhân AP / SAP có thể bị nghi ngờ khi đánh giá lâm sàng hoặc xét nghiệm [20]. Do đó, trong SAP, chỉ nên chụp theo dõi bổ sung nếu tình trạng lâm sàng của bệnh nhân xấu đi hoặc không cho thấy sự cải thiện liên tục [21, 31].
Độ phân giải của các biểu hiện CT của quá trình viêm tụy (xung quanh) hầu như luôn luôn chậm so với tình trạng lâm sàng của bệnh nhân được cải thiện. Do đó, nếu bệnh nhân cho thấy tình trạng lâm sàng được cải thiện, chỉ nên chụp theo dõi thêm trong khi nhập viện nếu bệnh nhân lâm sàng bệnh nhân xấu đi hoặc không thấy cải thiện liên tục.
Điều trị kháng sinh
Câu hỏi:
- Những chỉ định cho một liệu pháp kháng khuẩn trong trường hợp viêm tụy cấp nặng?
- Dự phòng bằng kháng sinh có hiệu quả trong viêm tụy cấp nặng vô trùng?
- Thời điểm chính xác để bắt đầu một liệu pháp kháng khuẩn là gì?
- Nên dùng kháng sinh kháng khuẩn nào?
- Thời gian chính xác của liệu pháp kháng khuẩn là gì?
Tuyên bố đồng thuận (kháng sinh dự phòng)
1. Bằng chứng gần đây đã chỉ ra rằng kháng sinh dự phòng ở bệnh nhân viêm tụy cấp không liên quan đến việc giảm đáng kể tỷ lệ tử vong hoặc bệnh tật. Vì vậy, kháng sinh dự phòng thường qui không còn được khuyến cáo cho tất cả các bệnh nhân bị viêm tụy cấp (1A).
Thảo luận: Việc sử dụng và hiệu quả của liệu pháp kháng sinh dự phòng trong viêm tụy cấp từ lâu đã là một điểm gây tranh cãi. Dự phòng đề cập đến việc sử dụng kháng sinh ở bệnh nhân khi không có nhiễm trùng lâm sàng với mục đích ngăn ngừa nhiễm trùng mô tụy. Mặc dù các thử nghiệm ban đầu cho thấy việc sử dụng kháng sinh có thể ngăn ngừa các biến chứng nhiễm trùng ở bệnh nhân bị hoại tử vô trùng [56], nhưng các thử nghiệm được thiết kế tốt hơn đã liên tục thất bại trong việc xác nhận lợi ích. Bằng chứng gần đây đã chỉ ra rằng kháng sinh dự phòng ở bệnh nhân viêm tụy cấp không liên quan đến việc giảm đáng kể tỷ lệ tử vong hoặc bệnh tật [57, 61]. Vì vậy, kháng sinh dự phòng thường quy cho tất cả bệnh nhân viêm tụy cấp không còn được khuyến cáo.
Tuyên bố đồng thuận (hoại tử nhiễm trùng và kháng sinh)
1. Kháng sinh luôn được khuyến cáo để điều trị viêm tụy cấp nặng nhiễm trùng. Tuy nhiên, chẩn đoán là khó khăn do hình ảnh lâm sàng không thể phân biệt với các biến chứng nhiễm trùng hoặc tình trạng viêm do viêm tụy cấp (2A).
2. Procalcitonin (PCT) huyết thanh có thể có giá trị trong việc dự đoán nguy cơ mô tụy hoại tử bị nhiễm trùng (1B).
3. Chọc hút bằng kim mịn (FNA) được hướng dẫn bằng CT để nhuộm Gram và nuôi cấy có thể xác nhận viêm tụy cấp nặng nhiễm trùng và điều trị bằng kháng sinh nhưng không còn được sử dụng thường quy (1B).
Thảo luận: Kháng sinh luôn được khuyến cáo để điều trị viêm tụy cấp bị nhiễm trùng. Tuy nhiên, chẩn đoán viêm tụy bị nhiễm trùng là một thách thức do hình ảnh lâm sàng không thể phân biệt với các biến chứng nhiễm trùng khác hoặc tình trạng viêm do viêm tụy cấp. Thời điểm nhiễm trùng trong hoại tử tụy là khác nhau và không thể đoán trước và đạt đỉnh trong tuần thứ hai đến thứ tư sau khi bắt đầu viêm tụy. Dấu hiệu lâm sàng có thể rất nhạy cảm nhưng không đủ đặc hiệu [62, 63].
Một số lượng hạn chế các nghiên cứu nhỏ hơn đã đánh giá protein phản ứng (CRP). Ngược lại, PCT đã được nghiên cứu như một yếu tố dự báo hiệu quả cho mức độ nghiêm trọng của viêm tụy cấp và nguy cơ phát triển viêm tụy bị nhiễm trùng. PCT là tiền peptide có 116 axit amin của hormone calcitonin hoạt tính sinh học, lần đầu tiên được mô tả là có nồng độ tăng đáng kể ở bệnh nhân bị nhiễm vi khuẩn và nấm[64]. Một số nghiên cứu đã chứng minh rằng đo PCT trong huyết thanh có thể có giá trị trong việc dự đoán nguy cơ phát triển mô tụy hoại tử bị nhiễm trùng [65-68].
Công cụ chẩn đoán được lựa chọn vẫn là FNA mô tụy hoại tử dưới hướng dẫn CT. Một mẫu bệnh phẩm FNA dưới hướng dẫn CT cho nhuộm Gram và nuôi cấy có thể hướng dẫn các bác sĩ lâm sàng trong việc lựa chọn kháng sinh phù hợp [69, 70]. Tuy nhiên, do tỷ lệ phát hiện âm tính giả cao, một số trung tâm đã từ bỏ việc sử dụng FNA thường qui.
Sự hiện diện của khí trong khu vực sau phúc mạc được coi là dấu hiệu của viêm tụy bị nhiễm trùng trong bối cảnh viêm tụy cấp nặng, nhưng nó chỉ xuất hiện hạn chế ở một số bệnh nhân [62].
Tuyên bố đồng thuận (loại kháng sinh)
1. Ở những bệnh nhân bị hoại tử bị nhiễm trùng, nên sử dụng kháng sinh có thể xâm nhập vào hoại tử tụy (1B).
2. Ở những bệnh nhân bị hoại tử nhiễm trùng, phổ của chế độ kháng sinh theo kinh nghiệm nên bao gồm cả vi khuẩn Gram âm và Gram dương và vi khuẩn kỵ khí. Sử dụng thuốc kháng nấm thường qui không được khuyến cáo ở những bệnh nhân bị viêm tụy cấp nhiễm trùng, mặc dù Candida spp. thường gặp ở bệnh nhân bị hoại tử tụy bị nhiễm trùng và cho thấy bệnh nhân có nguy cơ tử vong cao hơn (1B).
Thảo luận: Kháng sinh Aminoglycoside (ví dụ, gentamicin và tobramycin) ở liều tiêm tĩnh mạch chuẩn không xâm nhập vào tuyến tụy ở nồng độ trong mô đủ để đạt được nồng độ ức chế tối thiểu (MIC) của vi khuẩn thường thấy trong nhiễm trùng tụy thứ phát [71].
Acylureidopenicillins và cephalosporin thế hệ thứ ba có sự xâm nhập vừa phải vào mô tụy và có hiệu quả chống lại các vi sinh vật gram âm và có thể bao phủ MIC cho hầu hết các sinh vật gram âm được tìm thấy trong nhiễm trùng tụy [72]. Trong số các loại kháng sinh này, chỉ có piperacillin / tazobactam có hiệu quả chống lại vi khuẩn gram dương và vi khuẩn kỵ khí.
Quinolones (ciprofloxacin và moxifloxacin) và carbapenems đều cho thấy sự thâm nhập tốt vào mô tuyến tụy, lợi ích bổ sung là phủ kỵ khí tuyệt vời [73 – 76]. Tuy nhiên, do quinolone có tỷ lệ đề kháng cao trên toàn thế giới, quinolone nên được khuyến khích và chỉ được sử dụng ở những bệnh nhân bị dị ứng với các thuốc betalactam. Carbapenem do sự lây lan của Klebsiella pneumoniae kháng carbapenem nên luôn luôn được tối ưu hóa và chỉ nên được sử dụng ở những bệnh nhân rất nguy kịch.
Metronidazole, với phổ diệt khuẩn tập trung hầu hết vào vi khuẩn kỵ khí, cũng cho thấy sự xâm nhập tốt vào mô tuyến tụy.
Sinh bệnh học của nhiễm trùng tụy thứ phát vẫn còn đang được tranh luận. Các mầm bệnh có thể đến tuyến tụy thông qua con đường máu, thông qua hệ thống mật, xâm nhập lên từ tá tràng thông qua ống tụy chính hoặc di chuyển xuyên thành đại tràng thông qua hiện tượng dịch chuyển của vi khuẩn đại tràng [77].
Hầu hết các mầm bệnh trong nhiễm trùng tụy là vi khuẩn gram âm đường tiêu hóa (Escherichia coli, Proteus, Klebsiella pneumonia), xảy ra thông qua sự phá vỡ hệ vi khuẩn đường ruột và tổn thương niêm mạc ruột. Phòng thủ cơ thể suy yếu có xu hướng dịch chuyển các sinh vật đường tiêu hóa và độc tố gây nhiễm trùng tụy thứ phát sau đó. Tuy nhiên, vi khuẩn Gram dương (Staphylococcus aureus, Streptococcus faecalis, Enterococcus), kỵ khí, và, đôi khi, nấm cũng đã được tìm thấy [78].
Nhiễm nấm là một biến chứng nghiêm trọng của viêm tụy cấp với sự gia tăng tỷ lệ mắc bệnh và tử vong [79]. Candida albicans là sinh vật thường gặp nhất, tiếp theo là Candida tropicalis và Candida krusei. Mặc dù nhiễm nấm gây biến chứng viêm tụy cấp thường phát sinh tương ứng với mức độ hoại tử tụy, nhưng không có đủ dữ liệu để hỗ trợ phòng ngừa nhiễm nấm và do đó không được khuyến cáo.
Hồi sức
Câu hỏi:
- Những chỉ dẫn nào cho việc nhập khoa chăm sóc đặc biệt (ICU)?
- Khi nào cần hồi sức truyền dịch và nên sử dụng dịch nào? Tốc độ truyền dịch tối ưu và đo lường đáp ứng cho hồi sức ban đầu là gì? Phương pháp dược lý ưa thích để sốc dai dẵng là gì?
- Cách tiếp cận đúng để kiểm soát đau là gì?
- Những chỉ dẫn cho thở máy?
- Cách tiếp cận y tế đối với hội chứng chèn ép khoang bụng là gì? Vai trò của các loại thuốc như Gabexate Mesilate và somatostatin đồng phân là gì?
- Dinh dưỡng qua đường ruột: chỉ định, loại dinh dưỡng nào nên được sử dụng và cách nào là tốt nhất để quản lý dinh dưỡng đường ruột?
Tuyên bố đồng thuận (theo dõi)
1. Cần theo dõi các dấu hiệu sinh tồn liên tục trong đơn vị chăm sóc phụ thuộc cao nếu rối loạn chức năng nội tạng. Rối loạn chức năng cơ quan dai dẳng hoặc xảy ra suy tạng mặc dù hồi sức đầy đủ là một chỉ định cho nhập ICU (1C).
Thảo luận: Sự không đồng nhất trên toàn thế giới trong các thiết lập đơn vị chăm sóc chuyên sâu và trung gian gây khó khăn cho việc xác định các con đường chung nhất. Không có dấu hiệu duy nhất nào có thể xác định mức độ nghiêm trọng của bệnh. Một số hệ thống tính điểm nên được sử dụng để đánh giá mức độ nghiêm trọng trong một giai đoạn, địa điểm và trên từng bệnh nhân khác nhau.
Quản lý dịch truyền lượng lớn, quản lý đau đầy đủ nhưng với các chiến lược có hại và đánh giá chức năng cơ quan trong quá trình điều trị ban đầu là lý do tại sao việc theo dõi các dấu hiệu quan trọng liên tục là rất quan trọng, bất kể điều trị là gì. Rối loạn chức năng cơ quan dai dẳng mặc dù hồi sức đầy đủ cần hỗ trợ cơ quan chuyên biệt thường chỉ được hỗ trợ trong ICU [11, 80].
Tuyên bố đồng thuận (hồi sức truyền dịch)
1. Hồi sức truyền dịch sớm được chỉ định để tối ưu hóa các mục tiêu tưới máu mô, mà không phải chờ đợi tình trạng huyết động xấu đi. Quản lý dịch truyền nên được hướng dẫn bằng cách đánh giá lại thường xuyên tình trạng huyết động, vì quá tải dịch được biết là có tác dụng bất lợi. Các dịch tinh thể đẳng trương là dịch được ưu tiên (1B).
Thảo luận: Việc giảm tỷ lệ tử vong quan sát được trong thập kỷ qua có thể là do việc ngăn ngừa hoại tử tụy bằng cách duy trì vi tuần hoàn thông qua hồi sức truyền dịch tích cực hơn. Dữ liệu về lượng dịch cần thiết để ngăn ngừa hoại tử hoặc cải thiện kết quả là mâu thuẫn và khối lượng phải được điều chỉnh theo tuổi bệnh nhân, cân nặng, và tình trạng thận và / hoặc tim trước đó [81].
Hematocrit, nitơ urê máu, creatinine và lactate là các dấu hiệu cận lâm sàng về tình trạng thể tích và tưới máu mô đầy đủ, và cần được theo dõi. Ringer’s Lactate có thể liên quan đến tác dụng chống viêm, nhưng bằng chứng về sự vượt trội của Ringer’s Lactate so với nước muối bình thường dựa trên các thử nghiệm ngẫu nhiên là yếu [82 – 84]. Nó có thể tốt hơn trong việc điều chỉnh mức kali. Giá trị của liệu pháp hồi sức đạt mục tiêu sớm ở bệnh nhân viêm tụy cấp vẫn chưa được biết rõ [81, 85].
Tuyên bố đồng thuận (kiểm soát đau)
1. Không có bằng chứng hoặc khuyến cáo về bất kỳ hạn chế trong thuốc giảm đau có sẵn. Thuốc chống viêm không steroid (NSAID) nên tránh ở bệnh nhân tổn thương thận cấp tính (AKI). Giảm đau ngoài màng cứng nên là một biện pháp thay thế hoặc một thuốc giảm đau tiêm tĩnh mạch, trong cách tiếp cận đa phương thức. Thuốc giảm đau do bệnh nhân kiểm soát (PCA) nên được tích hợp với mọi chiến lược được mô tả. (1C) Dilaudid (hydromorphone) được ưu tiên hơn morphin hoặc fentanyl ở bệnh nhân không đặt nội khí quản.
Thảo luận: Đau là triệu chứng cốt yếu của viêm tụy cấp và giảm đau là ưu tiên lâm sàng. Tất cả bệnh nhân bị viêm tụy cấp phải nhận được một số phương thức giảm đau trong 24 giờ đầu nhập viện để không ảnh hưởng đến chất lượng cuộc sống của bệnh nhân. Trong hầu hết các tình huống, Dilaudid được ưa thích hơn morphin hoặc fentanyl ở bệnh nhân không đặt nội khí quản. Giảm đau ngoài màng cứng có thể được xem xét cho những bệnh nhân bị viêm tụy cấp nặng và cấp tính, những người cần dùng opioid liều cao trong thời gian dài [63].
Mặc dù có một số bằng chứng từ RCT, vẫn không chắc chắn về thuốc giảm đau thích hợp và phương pháp quản lý tốt nhất. Đó là lý do tại sao khuyến cáo tốt nhất hiện nay là tuân thủ các nguyên tắc quản lý đau cấp tính hiện hành nhất trong môi trường phẫu thuật [63].
Tuyên bố đồng thuận (thở máy)
1. Thông khí cơ học phải được thiết lập nếu cung cấp oxy, ngay cả khi thở bằng oxy ở mũi cao, hoặc áp lực đường thở dương liên tục trở nên không hiệu quả trong việc điều trị thở nhanh và khó thở. Cả hai kỹ thuật không xâm lấn và xâm lấn đều có thể được sử dụng, nhưng thông khí xâm lấn là bắt buộc khi khạc dịch tiết phế quản bắt đầu không hiệu quả và / hoặc bệnh nhân mệt mỏi, hay dự đoán sẽ mệt mỏi. Các chiến lược bảo vệ phổi nên được sử dụng khi cần thông khí xâm lấn (1C).
Thảo luận: Không có vấn đề gì đối với việc kiểm soát suy hô hấp chuyên biệt đối với chủ đề này. Cung cấp oxy, ngay cả với lưu lượng cao hoặc các thiết bị áp lực dương liên tục, có thể trở nên không đủ để hỗ trợ suy hô hấp. Mức độ khác nhau của thở nhanh và khó thở chỉ được chứng minh một phần bởi tình trạng thiếu oxy. Đau, có thể tăng áp lực trong ổ bụng và tràn dịch màng phổi, có thể gây ra các triệu chứng này mặc dù oxy hóa động mạch đầy đủ. Tăng tính thấm hệ thống có thể thúc đẩy phù phổi sau khi hồi sức dịch [86, 87].
Tuyên bố đồng thuận (tăng áp lực trong ổ bụng)
1. Giới hạn của thuốc an thần, dịch truyền và thuốc vận mạch để đạt được mục tiêu hồi sức ở giới hạn bình thường thấp hơn được đề xuất. An thần sâu và dãn cơ có thể cần thiết để hạn chế tăng áp lực trong ổ bụng, nếu tất cả các phương pháp điều trị không phẫu thuật khác bao gồm dẫn lưu qua da qua màng bụng là không đủ để cải thiện, trước khi thực hiện phẫu thuật giải nén ổ bụng (1B).
Thảo luận: Tăng tính thấm hệ thống gây ra bởi viêm toàn thân và các nỗ lực điều trị như hồi sức truyền dịch và thuốc vận mạch có liên quan đến suy chức năng ruột và làm xấu đi áp lực trong ổ bụng. Thuốc an thần quá mức có thể làm nặng thêm tình trạng rối loạn chức năng đường ruột với sự gia tăng áp lực trong ổ bụng sau đó. Hạn chế các loại thuốc ICU thông thường khác khi các tác dụng phụ vượt quá lợi ích là rất quan trọng [88].
Tuyên bố đồng thuận (điều trị dược lý)
1. Không điều trị dược lý cụ thể nào ngoại trừ hỗ trợ tạng và dinh dưỡng nên được đưa ra (1B). Thảo luận: Mặc dù có rất nhiều nghiên cứu, nhưng không có phương pháp điều trị dược lý hiệu quả nào được tìm thấy [89].
Tuyên bố đồng thuận (dinh dưỡng đường ruột)
1. Dinh dưỡng đường ruột được khuyến cáo để ngăn ngừa suy chức năng ruột và các biến chứng nhiễm trùng. Nên tránh dinh dưỡng toàn phần qua đường tĩnh mạch (TPN) nhưng cần cân nhắc tích hợp dinh dưỡng một phần để đạt được nhu cầu calo và protein nếu đường ruột không được dung nạp hoàn toàn. Cả cho ăn dạ dày và hỗng tràng có thể được cung cấp một cách an toàn (1A).
Thảo luận: Nuôi dưỡng đường ruột duy trì hàng rào niêm mạc ruột, ngăn ngừa sự mất toàn vẹn niêm mạc và ngăn chặn sự di chuyển của vi khuẩn đường ruột tấn công vào mô hoại tử của tụy. Trong hầu hết các tình huống, truyền liên tục được ưa thích hơn cho ăn theo chu kỳ hoặc bolus. Dinh dưỡng qua đường ruột so với dinh dưỡng toàn phần qua đường tĩnh mạch làm giảm các biến chứng nhiễm trùng, suy tạng và tử vong [90]. Trong một nghiên cứu đa trung tâm, nghiên cứu ngẫu nhiên so sánh cho ăn qua ống thông mũi-dạ dày sớm trong vòng 24 giờ sau khi ngẫu nhiên với chế độ ăn uống bắt đầu 72 giờ sau khi nhập khoa cấp cứu với viêm tụy hoại tử, cho ăn sớm không làm giảm tỷ lệ nhiễm trùng hoặc tử vong. Trong nhóm có chế độ ăn bằng miệng, 69% bệnh nhân dung nạp chế độ ăn và không cần cho ăn bằng ống [91].
Điều trị ngoại khoa
Câu hỏi:
- Những chỉ định nào cho ERCP cấp cứu trong trường hợp viêm tụy cấp nặng?
- Chiến lược phẫu thuật / phẫu thuật điều chỉnh nào trong viêm tụy cấp nặng ?
- Những chỉ định nào cho dẫn lưu qua da / nội soi của tụ dịch tuyến tụy ( hoại tử vô trùng, hoại tử nhiễm trùng, những biến chứng khác)?
- Những chỉ định can thiệp phẫu thuật?
- Thời gian phẫu thuật là gì và chiến lược phẫu thuật thích hợp (mổ nội soi so với mổ mở, trong phúc mạc so với ngoài phúc mạc, sớm so với trì hoãn)?
- Khi nào nên cắt bỏ túi mật và thời điểm chính xác là gì?
Tuyên bố đồng thuận (chỉ dẫn cho ERCP cấp cứu)
1. ERCP thường quy với viêm tụy sỏi mật cấp tính không được chỉ định (độ 1A).
2. ERCP ở bệnh nhân viêm tụy sỏi mật cấp tính và viêm đường mật được chỉ định (độ 1B).
3. ERCP trong viêm tụy sỏi mật cấp tính với tắc nghẽn ống mật chung được chỉ định (độ 2B).
4. ERCP ở bệnh nhân viêm tụy sỏi mật cấp tính nặng dự đoán không có viêm đường mật hoặc tắc nghẽn ống mật chủ có thể không được khuyến cáo tại thời điểm này (độ 2B).
Thảo luận: Một tổng quan hệ thống về bảy thử nghiệm ngẫu nhiên có đối chứng (RCT) bao gồm 757 người tham gia không tìm thấy bằng chứng hỗ trợ ERCP thường quy cho tất cả các bệnh nhân bị viêm tụy sỏi mật cấp tính (AGP-acute gallstone pancreatitis) [92]. Không có bằng chứng nào cho thấy kết quả phụ thuộc vào mức độ nghiêm trọng dự đoán của AGP. Tuy nhiên, những lo ngại đã được đặt ra về các hạn chế thiết kế nghiên cứu, thiếu kích thước mẫu gộp cùng với mức tiên lượng AGP nặng và thời gian và kỹ thuật ERCP. Trong cùng một phân tích gộp, trong số các thử nghiệm bao gồm các bệnh nhân bị viêm đường mật, ERCP thường quy sớm làm giảm đáng kể tỷ lệ tử vong cũng như các biến chứng tại chỗ và toàn thân.
Ở những bệnh nhân bị tắc nghẽn đường mật, ERCP thường quy sớm có liên quan đến việc giảm đáng kể các biến chứng tại chỗ và xu hướng không đáng kể đối với việc giảm các biến chứng toàn thân. Trong trường hợp tiên lượng AGP nặng, các hướng dẫn còn gây tranh cãi [93]. Tổng quan hệ thống này đã nghiên cứu tám phân tích tổng hợp và 12 hướng dẫn và kết luận rằng thiếu sự đồng thuận ERCP thường quy đối với AGP tiên lượng nặng. Một RCT đang diễn ra, thử nghiệm APEC, được thiết kế để trả lời câu hỏi này [94]. Việc thu thập mẫu đã kết thúc nhưng kết quả vẫn chưa được công bố.
Tuyên bố đồng thuận (chỉ định cho dẫn lưu qua da / nội soi của tụ dịch tuyến tụy)
1. Lâm sàng xấu đi với các dấu hiệu hoặc nghi ngờ mạnh về viêm tụy hoại tử bị nhiễm trùng là một chỉ định để thực hiện can thiệp (dẫn lưu qua da / nội soi).
Sau 4 tuần sau khi phát bệnh:
- Suy tạng đang diễn ra mà không có dấu hiệu hoại tử bị nhiễm bệnh.
- Tắc nghẽn đường ra dạ dày, đường mật hoặc ruột đang phát triển do tụ dịch hoại tử vách hóa lớn.
- Hội chứng tắt nghẽn ống tụy chung.
- Nang giả tụy có triệu chứng hoặc đang phát triển .
Sau 8 tuần sau khi phát bệnh:
- Đau liên tục và / hoặc khó chịu (độ 1C).
Thảo luận: Bằng chứng về chỉ định dựa trên sự hiểu biết về quá trình tự nhiên của bệnh, lý luận dựa trên cơ chế và các nghiên cứu không ngẫu nhiên. Các biện pháp can thiệp điều trị viêm tụy hoại tử tốt nhất nên được thực hiện khi hoại tử đã thành vách, thường là sau 4 tuần sau khi phát bệnh [2].
Dấu hiệu hoặc nghi ngờ mạnh về hoại tử nhiễm trùng ở bệnh nhân có triệu chứng đòi hỏi phải can thiệp, mặc dù một số ít bệnh nhân đã được chứng minh chỉ phục hồi bằng kháng sinh [1]. Khi một bệnh nhân xấu đi, bước tiếp cận tăng cường bắt đầu bằng dẫn lưu qua da hoặc nội soi được chỉ định [20, 95 – 97].
Phần lớn bệnh nhân bị viêm tụy hoại tử vô trùng có thể được kiểm soát mà không cần can thiệp [1]. Tuy nhiên, cần lưu ý rằng gần một nửa số bệnh nhân được phẫu thuật do suy tạng đang diễn ra mà không có dấu hiệu hoại tử bị nhiễm trùng có nuôi cấy vi khuẩn dương tính trong mẫu vật phẫu thuật [98]. Do đó, các biện pháp can thiệp nên được xem xét khi rối loạn chức năng nội tạng kéo dài hơn 4 tuần.
Các tụ dịch hoại tử hoặc nang giả tụy có thể gây ra các triệu chứng và / hoặc tắc nghẽn cơ học và nếu chúng không giải quyết khi hết viêm, một cách tiếp cận tăng cường được chỉ định. Một ống tụy bị ngắt kết nối có triệu chứng dẫn đến tụ dịch xung quanh tụy và là một chỉ định cho các can thiệp [99, 100].
Tuyên bố đồng thuận (chỉ định can thiệp phẫu thuật)
Sau đây là các chỉ định can thiệp phẫu thuật:
- Là một tiếp cận liên tục tăng cường sau thủ thuật qua da / nội soi với cùng chỉ định.
- Hội chứng tăng áp lực khoang bụng.
- Chảy máu cấp tính khi tiếp cận nội mạch không thành công.
- Thiếu máu cục bộ ruột hoặc viêm túi mật hoại tử cấp tính trong viêm tụy cấp.
- Lỗ dò ruột kéo dài vào một khoang tụ dịch xung quanh tụy (1C).
Thảo luận: Bằng chứng về chỉ định dựa trên sự hiểu biết về quá trình tự nhiên của bệnh, lý luận dựa trên cơ chế và các nghiên cứu không ngẫu nhiên. Khi các chiến lược qua da hoặc nội soi không cải thiện bệnh nhân, các chiến lược phẫu thuật tiếp theo nên được xem xét. Hội chứng tăng áp lực khoang bụng trước tiên nên được quản lý bằng các phương pháp bảo tồn [101]. Phẫu thuật bằng phẫu thuật nội soi nên được xem xét nếu phương pháp bảo tồn không đủ hay không hiệu quả [102].
Biến chứng chảy máu trong viêm tụy nặng cấp tính có thể đảm bảo can thiệp phẫu thuật nếu phương pháp nội mạch không thành công. Ruột và các biến chứng bên ngoài tụy khác tương đối hiếm nhưng có thể phải can thiệp bằng phẫu thuật.
Tuyên bố đồng thuận (thời gian phẫu thuật)
1. Trì hoãn các can thiệp phẫu thuật trong hơn 4 tuần sau khi bệnh khởi phát dẫn đến tỷ lệ tử vong ít hơn (2B).
Thảo luận: Phẫu thuật sớm được so sánh với phẫu thuật trì hoãn trong một tổng quan hệ thống gần đây và phân tích tổng hợp từ Hiệp hội Phẫu thuật Chấn thương Miền Đông [103]. Nghiên cứu bao gồm chín nghiên cứu, trong đó một nghiên cứu ngẫu nhiên có đối chứng. Thời gian của các can thiệp phẫu thuật được so sánh trong ba lần cắt khác nhau (72 h, 12 ngày và 30 ngày). Trong tất cả các lần cắt, phẫu thuật muộn mang lại lợi ích sống sót rõ ràng. Với phẫu thuật bị trì hoãn, việc phân chia mô hoại tử với mô sống quan trọng dẫn đến ít tổn thương cho các mô còn lại. Do đó, trong phẫu thuật muộn, ít chảy máu và cắt bỏ hoại tử hiệu quả hơn.
Người ta không biết phẫu thuật có thể trì hoãn bao lâu, nếu bệnh nhân có thể chịu đựng được và trì hoãn lâu hơn dẫn đến nhiều biến chứng, chẳng hạn như tăng tỷ lệ rò ruột hoặc tắc ruột. Nếu cần phẫu thuật khẩn cấp sớm hơn cho các chỉ định khác, chẳng hạn như hội chứng tăng áp lực khoang bụng hoặc hoại tử ruột, dẫn lưu hoặc cắt bỏ hoại tử không được khuyến cáo thường qui [20, 97].
Tuyên bố đồng thuận (chiến lược phẫu thuật)
1. Trong hoại tử tụy bị nhiễm trùng, dẫn lưu qua da là phương pháp điều trị đầu tiên (phương pháp tiếp cận) trì hoãn điều trị phẫu thuật chờ đến thời điểm thuận lợi hơn hoặc thậm chí dẫn đến giải quyết hoàn toàn nhiễm trùng ở 25 – 60% bệnh nhân và được khuyến cáo điều trị đầu tiên (1A).
2. Các chiến lược phẫu thuật xâm lấn tối thiểu, chẳng hạn như phẫu thuật cắt bỏ qua ngã dạ dày nội soi hoặc cắt bỏ từ khoang sau phúc mạc qua video(VARD), dẫn đến ít suy nội tạng mới khởi phát hơn nhưng cần phải can thiệp nhiều hơn (1B).
3. Xét tỷ lệ tử vong, không đủ bằng chứng để ủng hộ phương pháp phẫu thuật mở, xâm lấn nhỏ hoặc nội soi (1B).
4. Trong các trường hợp được lựa chọn với hoại tử vách hóa và ở bệnh nhân có ống tụy bị ngắt kết nối, phẫu thuật cắt bỏ hoại tử qua dạ dày là một lựa chọn (2C). 5. Một nhóm các chuyên gia đa ngành nên điều trị phẫu thuật dựa trên từng cá thể bệnh nhân có tính đến điều kiện sẵn có (2C).
Thảo luận: Một tổng quan hệ thống về dẫn lưu catheter qua da như là một điều trị cơ bản cho viêm tụy hoại tử bao gồm 11 nghiên cứu và 384 bệnh nhân [97]. Hoại tử nhiễm trùng đã được chứng minh ở 71% và 56% bệnh nhân không cần phẫu thuật sau khi dẫn lưu qua da. Ngoài ra, dẫn lưu qua da cho phép trì hoãn can thiệp phẫu thuật sau này để thời gian thuận lợi hơn.
Một câu hỏi quan trọng là chiến lược thích hợp nào sẽ được lựa chọn khi dẫn lưu qua da không giải quyết nhiễm trùng. Các lựa chọn quản lý bao gồm phẫu thuật mở, phẫu thuật xâm lấn tối thiểu, phẫu thuật nội soi và kết hợp những biện pháp này. Người ta thường cho rằng phẫu thuật mở gây ra phản ứng viêm nặng hơn. Có nhiều RCT khác nhau và đánh giá so sánh các chiến lược khác nhau [104 – 106]. Tóm lại, các chiến lược xâm lấn tối thiểu (ví dụ: phương pháp xâm lấn tối thiểu tăng cường, phẫu thuật ngã sau phúc mạc được hỗ trợ bằng video, VARD, hoặc nội soi) làm suy tạng ít khởi phát hơn nhưng cần phải can thiệp nhiều hơn. Tuy nhiên, không có sự khác biệt về tỷ lệ tử vong đã được tìm thấy. Những kết luận này được hỗ trợ bởi một tổng quan hệ thống [107]. Khi diễn giải kết quả, cần lưu ý rằng có sự không đồng nhất đáng kể ở bệnh nhân, suy tạng và kích thước cũng như sự khu trú rõ ràng của mô hoại tử. Ngoài ra, các kỹ thuật phẫu thuật và chỉ định can thiệp không đồng nhất.
Trong một loạt 178 trường hợp được lựa chọn với hoại tử đã vách hóa, 96% bệnh nhân đã trải qua phẫu thuật cắt bỏ mô hoại tử, phẫu thuật một lần với tỷ lệ tử vong sau phẫu thuật và tỷ lệ mắc bệnh lần lượt là 2% và 38% [108]. Nó cũng là một lựa chọn tốt ở những bệnh nhân mắc hội chứng ống tụy bị ngắt kết nối.
Khi xét tỷ lệ tử vong, điều quan trọng cần lưu ý là tỷ lệ tử vong liên quan đến viêm tụy hầu hết không phải do hoại tử nhiễm trùng. Do đó, trong các nghiên cứu trong tương lai, các biện pháp kết quả khác nên được xem xét. Các biện pháp kết quả này sẽ có thể phát hiện giải quyết hoàn toàn các triệu chứng, chất lượng cuộc sống, thời gian để trở lại các hoạt động hoặc công việc hàng ngày bình thường và cần được can thiệp thêm. Chuyên môn địa phương về các phương pháp phẫu thuật khác nhau nên được tính đến, vì chỉ một tỷ lệ nhỏ bệnh nhân cần phẫu thuật và ngay cả ở các trung tâm lớn, số lượng phẫu thuật vẫn còn ít. Chúng tôi khuyên rằng một nhóm các chuyên gia đa ngành địa phương nên cá nhân hóa chiến lược phẫu thuật.
Tuyên bố đồng thuận (thời gian cắt bỏ túi mật)
1. Phẫu thuật cắt túi mật nội soi trong suốt thời gian nhập viện được khuyến cáo trong viêm tụy sỏi mật cấp tính nhẹ (1A).
2. Khi ERCP và phẫu thuật cắt bỏ cơ vòng được thực hiện trong khi nhập viện, nguy cơ viêm tụy tái phát sẽ giảm, nhưng vẫn nên cắt bỏ túi mật trong lúc nhập viện vì có nguy cơ biến chứng đường mật khác (1B).
3. Trong viêm tụy sỏi mật cấp tính có tụ dịch xung quanh tụy, nên trì hoãn cắt bỏ túi mật cho đến khi tụ dịch được giải quyết hoặc ổn định và ngừng viêm cấp tính (2C).
Thảo luận: Hai tổng quan hệ thống khác nhau cho thấy rằng phẫu thuật cắt bỏ túi mật ở AGP nhẹ là an toàn [109, 110]. Để giảm thời gian nằm viện và chi phí tổng thể, phẫu thuật cắt túi mật có thể được thực hiện sớm là vào ngày thứ hai của đợt nhập viện, miễn là bệnh nhân được cải thiện lâm sàng [111, 112]. Chụp đường mật trong phẫu thuật thường quy dường như là không cần thiết ở những bệnh nhân bị viêm tụy do sỏi mật nhẹ và bình thường hóa nồng độ bilirubin [113]. Nếu ERCP được thực hiện trong khi nhập viện, nguy cơ cho các biến cố đường mật tái phát, đặc biệt là AGP tái phát, giảm nhưng vẫn cao hơn so với phẫu thuật cắt túi mật cùng lúc nhập viện. Một RCT đa trung tâm với 266 bệnh nhân đã kết luận rằng phẫu thuật cắt túi mật giữa chừng dẫn đến các biến chứng liên quan đến sỏi mật nhiều hơn, đặc biệt là viêm tụy tái phát và đại tràng, mà không làm tăng các biến chứng liên quan đến cắt túi mật [114]. Có một nghiên cứu hồi cứu duy nhất về thời gian cắt bỏ túi mật ở bệnh nhân AGP từ trung bình đến nặng có tụ dịch xung quanh tụy [115]. Nghiên cứu này báo cáo nhiều biến chứng sau phẫu thuật cắt túi mật sớm.
Mở bụng
Câu hỏi
- Những chỉ định cho mở bụng trong trường hợp viêm tụy cấp nặng?
- Hệ thống đóng bụng kín tạm thời tốt nhất cho bụng mở là gì?
- Thời gian chính xác để thay đổi miếng che bụng là gì?
- Thời điểm chính xác để đóng bụng là gì?
Tuyên bố đồng thuận (mở bụng)
1. Ở những bệnh nhân bị viêm tụy cấp nặng không đáp ứng với điều trị bảo tồn IAH / ACS, giải áp bằng phẫu thuật và sử dụng phẫu thuật mở bụng có hiệu quả trong điều trị hội chứng tăng áp lực khoang bụng (2C).
2. Chúng tôi đề nghị các bác sĩ lâm sàng nên thận trọng không hồi sức dịch quá mức cho bệnh nhân SAP sớm và đo áp lực trong ổ bụng thường xuyên (1C).
3. Chúng tôi khuyên nên tránh mở bụng (OA) nếu các chiến lược khác có thể được sử dụng để giảm thiểu hoặc điều trị tăng áp trong ổ bụng nghiêm trọng ở SAP (1C).
4. Chúng tôi khuyên không nên sử dụng OA sau khi cắt bỏ mô hoại tử cho SAP (trừ khi IAH nghiêm trọng bắt buộc OA) (1C).
5. Chúng tôi khuyên không nên cắt bỏ hoặc tiến hành phẫu thuật cắt bỏ mô hoại tử sớm nếu buộc phải tiến hành mở bụng do hội chứng tăng áp lực khoang bụng hoặc thiếu máu cục bộ tạng (1A).
Thảo luận: Cơ sở lý luận để sử dụng khả năng quản lý mở bụng ở bệnh nhân viêm tụy cấp nặng (SAP) là có khả năng giảm thiểu IAH / ACS, cải thiện dẫn lưu dịch viêm, cho phép bơm rửa tụy nhiều lần và có khả năng cho phép phẫu thuật cắt bỏ tụy nhiều lần [116-118].
Tuy nhiên, trong SAP, không có bằng chứng cấp 1 nào liên quan đến hiệu quả của mở bụng đối với SAP, không có thử nghiệm ngẫu nhiên có đối chứng (RCT) và không có phân tích tổng hợp. Có một protocol được công bố cho một nghiên cứu như vậy [119], nhưng những người đánh giá có thể không có bằng chứng nào cho thấy nghiên cứu này đã từng được thực hiện hiệu quả.
Như là cấp độ bằng chứng tốt nhất tiếp theo, có các khuyến nghị đồng thuận hiện có từ Hiệp hội Phẫu thuật Cấp cứu Thế giới [120] và Hiệp hội Tụy Quốc tế / Hiệp hội Tụy Hoa Kỳ [20], cả hai đều khuyến nghị quản lý y tế và xâm lấn tối thiểu trong điều trị tăng áp bụng nặng (IAH) dẫn đến hội chứng tăng áp khoang bụng (ACS) theo lượt đồ quản lý hội chứng khoang bụng [101]. Tuy nhiên, việc nhận ra rằng ACS quá mức gây tử vong nếu không được điều trị, phẫu thuật giải áp mở bụng (DCL) sẽ được yêu cầu và được khuyến cáo nếu các biện pháp ít xâm lấn không hiệu quả. Khi DCL được thực hiện, khoang sau phúc mạc và hậu cung mạc nối nên được giữ nguyên để giảm nguy cơ nhiễm trùng hoại tử xung quanh tụy và tụy [20, 121].
Liên quan đến khuyến cáo chính này, có những tuyên bố liên quan đến các nguyên tắc cơ bản là hồi sức dịch quá nhiệt dường như có liên quan chặt chẽ với sự xuất hiện của IAH / ACS trong sốc nặng và việc cắt bỏ mô hoại tử sớm không nên được tiến hành trong SAP. Một nghiên cứu cổ điển hiện nay lưu ý rằng phẫu thuật cắt bỏ hoại tử sớm (< 72 giờ) so với muộn (> 12 ngày) có 56% trong các can thiệp sớm đến 27% trong các ca phẫu thuật muộn và mất máu trong phẫu thuật đã giảm đáng kể trong cách tiếp cận chậm, kết quả chỉ tiếp tục cải thiện với những cải tiến liên tục trong phẫu thuật và chăm sóc tích cực [122, 111].
Tuyên bố đồng thuận (quản lý mở bụng và đóng bụng tạm thời)
1. Chúng tôi khuyên bạn nên sử dụng liệu pháp phúc mạc áp lực âm để quản lý mở bụng (1B).
2. Chúng tôi đề nghị lực kéo được thêm vào các phương thức NPWT (2B).
3. Chúng tôi đề nghị rằng các nghiên cứu đối chứng sâu hơn được tiến hành trên các liệu pháp thẩm thấu trong phúc mạc trong SAP (không có khuyến cáo).
Thảo luận: Không có RCT hoặc phân tích tổng hợp nào đưa ra bằng chứng so sánh trực tiếp về các kỹ thuật OA trong SAP, do đó tất cả các bằng chứng liên quan gián tiếp đến nghiên cứu về mở bụng trong các môi trường liên quan khác như nhiễm trùng màng bụng [125, 126], hoặc nhóm dân số chấn thương-y tế hỗn hợp [127-130] với mối quan tâm về phương pháp.
Nghiên cứu của Pliakos là đáng chú ý vì sự ngẫu nhiên bao gồm chỉ định lực kéo them vào trị liệu máy hút chân không được chứng minh có hiệu quả vượt trội về thời gian mở bụng ngắn hơn, giảm số lần thay băng, giảm tỷ lệ tái khám, tỷ lệ đóng bụng thành công cao hơn và giảm dò ruột khí quyển [125]. Một RCT so sánh điều trị phúc mạc áp lực âm tích cực với áp lực thụ động hơn chứng tỏ lợi ích tử vong với áp lực phúc mạc tăng cường [129], chứng thực kết quả không ngẫu nhiên [130], nhưng cơ chế sinh học không rõ ràng. Một số phân tích tổng hợp bao gồm dữ liệu thử nghiệm không ngẫu nhiên đã được tiến hành mà không có sự vượt trội rõ ràng nào được thể hiện trong bất kỳ một phương pháp nào [131, 132]. Hiện tại nhất trong số này đã kết luận “Mặc dù kết quả tốt nhất về việc đạt được sự đóng bụng trì hoãn và nguy cơ dò ruột khí quyển đã được chứng minh cho NPWT với lực kéo liên tục, chất lượng tổng thể của bằng chứng có sẵn là kém, và các khuyến cáo thống nhất không thể được thực hiện” [131].
Một liệu pháp cuối cùng được xem xét cẩn thận trong quản lý OA là hồi sức trực tiếp qua phúc mạc (DPR), thấm qua màng bụng của dịch thẩm tách, đã được chứng minh là có hiệu quả trong nhóm dân số chấn thương [133]. Trong một RCT từ Smith và đồng nghiệp, các biến chứng trong ổ bụng (8% so với 18%), tỷ lệ áp xe (3% so với 14%) và tỷ lệ tử vong trong 30 ngày thấp hơn mặc dù điểm số thương tật tương tự (13% so với 28 %; p = 0,06) (20). Vì không có bằng chứng trực tiếp ở bệnh nhân SAP, nên không có khuyến cáo nào được đưa ra liên quan đến DPR.
Tuyên bố đồng thuận (thời gian thay tấm phủ màng bụng)
1. Việc thăm dò lại bụng mở nên được tiến hành không muộn hơn 24-48 giờ sau chỉ số và bất kỳ hoạt động tiếp theo nào, với sự rút ngắn khoảng thời gian phẫu thuật trước đó, với mức độ không cải thiện bệnh nhân và không ổn định huyết động (1C).
Thảo luận: Không có RCT hoặc phân tích tổng hợp nào liên quan đến thời điểm khi một bệnh nhân có bụng mở nên được đưa trở lại phòng mổ đặc biệt khi chỉ định OA là SAP, cũng không phải cho bất kỳ chỉ định nào khác. Cũng không có hướng dẫn nào khác từ các hiệp hội được công nhận đưa ra bằng chứng về việc khi nào mở lại OA sẽ diễn ra [101, 131, 134, 135]. Tuy nhiên, trong một lần xem xét, thăm dò lại thực hiện hơn 48 giờ sau lần phẫu thuật ban đầu dẫn đến tỷ lệ tử vong cao hơn đáng kể; và tỷ lệ tử vong thấp nhất (9%) đã đạt được ở những bệnh nhân được mở lại trong vòng 48 giờ [136].
Dữ liệu hiện thời cho thấy mối tương quan tuyến tính tồn tại giữa các ngày của OA và các biến chứng nghiêm trọng như phát triển lỗ dò ruột [137]. Một loạt dữ liệu khác lưu ý rằng, mỗi giờ chậm trễ trở lại phòng mổ 24 giờ sau phẫu thuật nội soi ban đầu, và có giảm 1,1% trong đóng bụng nguyên phát và xu hướng tăng các biến chứng trong ổ bụng sau 48 giờ [138].
Trong trường hợp không có bất kỳ dữ liệu mới nào, các nhà đánh giá SAP OA đề nghị áp dụng tuyên bố hướng dẫn quản lý WSES về OA hiện đại trước đó để duy trì tính nhất quán trong các khuyến cáo của WSES cho đến khi dữ liệu mới đảm bảo đủ sức để điều chỉnh [120]. Vì kết quả tổng thể được cải thiện rõ rệt bằng cách tránh các can thiệp sớm và không cần thiết [124], các bác sĩ phẫu thuật nên chống lại mọi cám dỗ đối với “vụ lộn xộn với tuyến tụy” mà có thể được đưa ra trong quá trình mở lại OA không có sẵn trong OA trường hợp SAP ít phức tạp hơn.
Tuyên bố đồng thuận (thời gian đóng bụng)
1. Đóng bụng sớm và / hoặc đóng bụng dứt khoát nên là chiến lược để quản lý vùng bụng mở một khi mọi yêu cầu về hồi sức đang diễn ra đã chấm dứt, việc kiểm soát nguồn nhiễm đã đạt được một cách dứt khoát, không còn lo ngại về khả năng sống sót của đường ruột, không cần phẫu thuật thêm là cần thiết, và không có mối quan tâm cho hội chứng tăng áp lực khoang bụng (1B).
Thảo luận: Có nguy cơ có thể bị coi là vô dụng, nhóm viết nhấn mạnh tầm quan trọng của việc cố gắng tối ưu hóa các chiến lược phòng ngừa cho IAH mặc dù hồi sức cẩn thận và siêng năng, giới thiệu sớm về quản lý y tế và xâm lấn tối thiểu IAH [101, 139, 140], để cố gắng để tránh tiến tới ACS với yêu cầu về DCL.
Tương tự như câu hỏi trước, cho đến khi có dữ liệu mới về việc đóng OA dứt khoát trong SAP hoặc bất kỳ điều kiện nào khác, các nhà đánh giá đề nghị áp dụng tuyên bố hướng dẫn quản lý WSES hiện thời trước đó để duy trì tính nhất quán trong các khuyến cáo WSES cho đến khi dữ liệu mới được điều chỉnh [120].
Kết luận
Những hướng dẫn này trình bày các tuyên bố đồng thuận quốc tế dựa trên bằng chứng về việc quản lý viêm tụy cấp tính nặng từ sự cộng tác của một nhóm chuyên gia. Nó chứa 55 tuyên bố về chẩn đoán, quản lý trong ICU, quản lý phẫu thuật và phẫu thuật, mở bụng và điều trị bằng kháng sinh. Đối với một số tuyên bố như phân loại mức độ nghiêm trọng, hình ảnh, sử dụng kháng sinh dự phòng và hầu hết các khía cạnh của quản lý trong ICU, bằng chứng là mạnh mẽ. Đối với những vấn đề khác, chẳng hạn như chẩn đoán trong phòng thí nghiệm và chiến lược phẫu thuật, ví dụ, bằng chứng khá yếu đòi hỏi phải nghiên cứu thêm. Với sự tích lũy kiến thức, các báo cáo cần phải được cập nhật thường xuyên.
Các từ viết tắt
ACS: Abdominal compartment syndrome; AGP: Acute gallstone pancreatitis; AKI: Acute kidney injury; ANC: Acute necrotic collection; AP: Acute pancreatitis; APACHE: Acute Physiology and Chronic Health Evaluation; BISAP: Bedside index of severity of acute pancreatitis; BMI: Body mass index; BUN: Blood urea nitrogen; CECT: Contrast-enhanced computed tomography; CRP: C-reactive protein; CT: Computed tomography; CTSI: CT severity index; DBC: Determinant-Based Classification of Acute Pancreatitis Severity; DCL: Decompressive laparotomy; DPR: Direct peritoneal resuscitation; ERCP: Endoscopic retrograde cholangiopancreatography; EUS: Endoscopic ultrasound; FNA: Fine-needle aspiration; GRADE: Grading of Recommendations Assessment, Development and Evaluation; HCT: Hematocrit; IAH: Intra-abdominal hypertension; IAP: Intra-abdominal pressure; ICU: Intensive care unit; LDH: Lactate dehydrogenase; MIC: Minimal inhibitory concentration; MRCP: Magnetic resonance cholangiopancreatography; MRI: Magnetic resonance imaging; NPWT: Negative pressure wound therapy; NS: Normal saline; NSAID: Nonsteroidal anti-inflammatory drug; OA: Open abdomen; OF: Organ failure; PCA: Patient-controlled analgesia; PCT: Procalcitonin; POF: Persistent organ failure; PPV: Positive predictive value; RAC: Revised Atlanta Classification; RCT: Randomized controlled trial; RL: Ringer’s lactate; SAP: Severe acute pancreatitis; SAPS: Simplified Acute Physiology Score; SIRS: Systemic inflammatory response syndrome; SOFA: Sequential Organ Failure Assessment; TPN: Total parenteral nutrition; US: Ultrasound; VARD: Videoassisted retroperitoneal debridement; WBC: White blood cell; WON: Walledoff necrosis; WSES: World Society of Emergency Surgery.
Acknowledgements Not applicable.
Funding Not applicable. Availability of data and materials The authors are responsible for the data described in the manuscript and assure full availability of the study material upon request to the corresponding author. Authors’ contributions Each author wrote a chapter of the manuscript. All the authors reviewed the manuscript and approved the final draft. Ethics approval and consent to participate Not applicable. Consent for publication Not applicable. Competing interests The authors declare that they have no competing interests. Publisher’s Note Springer Nature remains neutral with regard to jurisdictional claims in published maps and institutional affiliations. Author details 1 Abdominal Center, Helsinki University Hospital Meilahti, Haartmaninkatu 4, FI-00029 Helsinki,, Finland. 2Department of Emergency Surgery, Parma Maggiore Hospital, Parma, Italy. 3Hospital de Clinicas, Universidad Nacional de Asuncion, Asuncion, Paraguay. 4Anesthesia and Intensive Care Medicine, Maurizio Bufalini Hospital, Cesena, Italy. 5Foothills Medical Centre & the University of Calgary, Calgary, AB, Canada. 6London Health Sciences Centre, London, ON, Canada. 7Department of Surgery, Macerata Hospital, Macerata, Italy. 8Radboud University Nijmegen, Nijmegen, The Netherlands. 9Surgical Clinic, Department of Experimental and Clinical Sciences, University of Brescia, Brescia, Italy. 10General, Emergency and Trauma Surgery Department, Bufalini hospital, Cesena, Italy. 11Trauma and Acute Care Surgery, Scripps memorial Hospital, La Jolla, CA, USA. 12Cambridge University Hospitals NHS Foundation Trust, Cambridge, UK. 13Division of General Surgery, Rambam Health Care Campus, Haifa, Israel. 14Trauma Surgery, Denver Health Medical Center, Denver, CO, USA.
Received: 23 April 2019 Accepted: 27 May 2019.
Tài liệu tham khảo
1. van Santvoort HC, Bakker OJ, Bollen TL, Besselink MG, Ali UA, Am S, et al. A conservative and minimally invasive approach to necrotizing pancreatitis improves outcome. Gastroenterology. 2011;141:1254– 63.
2. Banks PA, Bollen TL, Dervenis C, Gooszen HG, Johnson CD, Sarr MG, et al. Classification of acute pancreatitis—2012: revision of the Atlanta classification and definitions by international consensus. Gut. 2013;62:102– 11.
3. Werge M, Novovic S, Schmidt PN, Gluud LL. Infection increases mortality in necrotizing pancreatitis: a systematic review and meta- analysis. Pancreatology. 2016;16:698–707.
4. Mentula P, Leppäniemi A. Position paper: timely interventions in severe acute pancreatitis are crucial for survival. World J Emerg Surg. 2014;9:15.
5. Guyatt G, Gutterman D, Baumann MH, Addrizzo-Harris D, Hylek EM, Phillips B, et al. Grading strength of recommendations and quality of evidence in clinical guidelines: report from an American College of Chest Physicians task force. Chest. 2006;129:174–81.
6. Garber A, Frakes C, Arora Z, Chahal P. Mechanisms and management of acute pancreatitis. Gastroenterol Res Pract. 2018;2018:6218798. https://doi. org/10.1155/2018/6218798. eCollection 2018
7. Banks PA, Freeman ML, Practice Parameters Committee of the American College of Gastroenterology. Practice guidelines in acute pancreatitis. Am J Gastroenterol. 2006;101:2379–400.
8. van Dijk SM, Hallensleben NDL, van Santvoort HC, et al. Acute pancreatitis: recent advances through randomised trials. Gut. 2017;66:2024–32.
9. Bollen TL, van Santvoort HC, Besselink MG, et al. The Atlanta classification of acute pancreatitis revisited. Br J Surg. 2008;95:6–21.
10. Johnson CD, Abu-Hilal M. Persistent organ failure during the first week as a marker of fatal outcome in acute pancreatitis. Gut. 2004;53:1340–4.
11. Mofidi R, Duff MD, Wigmore SJ, Madhavan KK, Garden OJ, Parks RW. Association between early systemic inflammatory response, severity of multiorgan dysfunction and death in acute pancreatitis. Br J Surg. 2006;93: 738–44.
12. Johnson CD. Organ failure and acute pancreatitis. In: Forsmark CE, Gardner TB, editors. Prediction and management of severe acute pancreatitis. New York: Springer; 2014. p. 15–27. ISBN 978-1-4939- 0970-4.
13. Dellinger EP, Forsmark CE, Layer P, et al. Determinant-based classification of acute pancreatitis severity: an international multidisciplinary consultation. Ann Surg. 2012;256:875–80. https://doi.org/10.1097/SLA.0b013e318256f778.
14. Yadav D. Acute pancreatitis: too many classifications-what is a clinician or researcher to do? Clin Gastroenterol Hepatol. 2014;12:317–9. https://doi.org/ 10.1016/j.cgh.2013.09.051.
15. Bansal SS, Hodson J, Sutcliffe RS, Marudanayagam R, Muiesan P, Mirza, et al. Performance of the revised Atlanta and determinant- based classifications for severity in acute pancreatitis. Br J Surg 2016;103:427–433. doi: https://doi. org/10.1002/bjs.10088.
16. Nawaz H, Mounzer R, Yadav D, Yabes JG, Slivka A, Whitcomb DC, Papachristou GI. Revised Atlanta and determinant-based classification: application in a prospective cohort of acute pancreatitis patients. Am J Gastroenterol. 2013;108:1911–7. https://doi.org/10.1038/ajg.2013.348.
17. Chen Y, Ke L, Tong Z, Li W, Li J. Association between severity and the determinant-based classification, Atlanta 2012 and Atlanta 1992, in acute pancreatitis: a clinical retrospective study. Medicine (Baltimore). 2015;94: e638. https://doi.org/10.1097/MD.0000000000000638.
18. Choi JH, Kim MH, Oh D, Paik WH, Park DH, Lee SS, Seo DW, Lee SK. Clinical relevance of the revised Atlanta classification focusing on severity stratification system. Pancreatology. 2014;14:324–9. https://doi.org/10.1016/j. pan.2014.08.001.
19. Acevedo-Piedra NG, Moya-Hoyo N, Rey-Riveiro M, Gil S, Sempere L, Martínez J, et al. Validation of the determinant-based classification and revision of the Atlanta classification systems for acute pancreatitis. Gastroenterol Hepatol. 2014;12:311–6. https://doi.org/10.1016/j.cgh.2013.07.042.
20. Working Group IAP/APA Acute Pancreatitis Guidelines. IAP/APA evidencebased guidelines for the management of acute pancreatitis. Pancreatology. 2013;13(4 Suppl 2):e1–15. https://doi.org/10.1016/j.pan.2013.07.063. 21. Working Party of the British Society of Gastroenterology. Association of Surgeons of Great Britain and Ireland; Pancreatic Society of Great Britain and Ireland; Association of Upper GI Surgeons of Great Britain and Ireland. UK guidelines for the management of acute pancreatitis. Gut. 2005;54(Suppl 3):iii1–9.
22. Yokoe M, Takada T, Mayumi T, Yoshida M, Isaji S, Wada K, et al. Japanese guidelines for the management of acute pancreatitis: Japanese guidelines 2015. J Hepatobiliary Pancreat Sci. 2015;22:405– 32. https://doi.org/10.1002/ jhbp.259.
23. Tenner S, Baillie J, DeWitt J, Vege SS. American College of Gastroenterology. American College of Gastroenterology guideline: management of acute pancreatitis. Am J Gastroenterol. 2013;108:1400–15; 1416. https://doi.org/10. 1038/ajg.2013.218.
24. McPherson SJ, O’Reilly DA, Sinclair MT, Smith N. The use of imaging in acute pancreatitis in United Kingdom hospitals: findings from a national quality of care study. Br J Radiol. 2017;90(1080):20170224. https://doi.org/10. 1259/bjr.20170224.
25. Aycock RD, Westafer LM, Boxen JL, Majlesi N, Schoenfeld EM, Bannuru RR. Acute kidney injury after computed tomography: a meta- analysis. Ann Emerg Med. 2018;71:44–53.e4.
26. Balthazar EJ. Acute pancreatitis: assessment of severity with clinical and CT evaluation. Radiology. 2002;223:603–13.
27. Balthazar EJ, Robinson DL, Megibow AJ, Ranson JH. Acute pancreatitis: value of CT in establishing prognosis. Radiology. 1990;174:331–6.
28. Shyu JY, Sainani NI, Sahni VA, Chick JF, Chauhan NR, Conwell DL, et al. Necrotizing pancreatitis: diagnosis, imaging, and intervention. Radiographics. 2014;34:1218–39. https://doi.org/10.1148/rg.345130012.
29. Ball CG, Correa-Gallego C, Howard TJ, Zyromski NJ, House MG, Pitt HA, et al. Radiation dose from computed tomography in patients with necrotizing pancreatitis: how much is too much? J Gastrointestinal Surg. 2010;14:1529–35.
30. Shanmugam V, Beattie GC, Yule SR, Reid W, Loudon MA. Is magnetic resonance cholangiopancreatography the new gold standard in biliary imaging? Br J Radiol. 2005;78:888–93.
31. Toouli J, Brooke-Smith M, Bassi C, Carr-Locke D, Telford J, Freeny P, et al. Guidelines for the management of acute pancreatitis. J Gastroenterol Hepatol. 2002;17(Suppl):S15–39.
32. Lippi G, Valentino M, Cervellin G. Laboratory diagnosis of acute pancreatitis: in search of the holy grail. Crit Rev Clin Lab Sci. 2012;49:18–31. https://doi. org/10.3109/10408363.2012.658354.
33. Rompianesi G, Hann A, Komolafe O, Pereira SP, Davidson BR, Gurusamy KS. Serum amylase and lipase and urinary trypsinogen and amylase for diagnosis of acute pancreatitis. Cochrane Database Syst Rev. 2017;4: CD012010. https://doi.org/10.1002/14651858.CD012010.pub2.
34. Chang K, Lu W, Zhang K, Jia S, Li F, Wang F, et al. Rapid urinary trypsinogen-2 test in the early diagnosis of acute pancreatitis: a metaanalysis. Clin Biochem. 2012;45:1051–6.
35. Zhu HH, Jiang LL. Serum inter-cellular adhesion molecule 1 is an early marker of diagnosis and prediction of severe acute pancreatitis. World J Gastroenterol. 2012;18:2554–60. https://doi.org/10.3748/wjg.v18.i20.2554.
36. Staubli SM, Oertli D, Nebiker CA. Laboratory markers predicting severity of acute pancreatitis. Crit Rev Clin Lab Sci. 2015;52:273–83. https://doi.org/10. 3109/10408363.2015.1051659.
37. Sternby H, Hartman H, Johansen D, Thorlacius H, Regner S. IL-6 and CRP are superior in early differentiation between mild and non-mild acute pancreatitis. Pancreatology. 2017;17:550–4.
38. Kibar YI, Albayrak F, Arabul M, Dursun H, Albayrak Y, Ozturk Y. Resistin: new serum marker for predicting severity of acute pancreatitis. J Int Med Res. 2016;44:328–37. https://doi.org/10.1177/0300060515605428.
39. Yu P, Wang S, Qiu Z, Bai B, Zhao Z, Hao Y, et al. Efficacy of resistin and leptin in predicting persistent organ failure in patients with acute pancreatitis. Pancreatology. 2016;16:952–7. https://doi.org/10.1016/j.pan. 2016.09.002.
40. Koutroumpakis E, Wu BU, Bakker OJ, Dudekula A, Singh VK, Besselink MG, et al. Admission hematocrit and rise in blood urea nitrogen at 24 h outperform other laboratory markers in predicting persistent organ failure and pancreatic necrosis in acute pancreatitis: a post hoc analysis of three large prospective databases. Am J Gastroenterol. 2015;110:1707–16. https://doi. org/10.1038/ajg.2015.370.
41. Brown A, James-Stevenson T, Dyson T, Grunkenmeier DJ. The panc 3 score: a rapid and accurate test for predicting severity on presentation in acute pancreatitis. Clin Gastroenterol. 2007;41:855–8.
42. Yang CJ, Chen J, Phillips AR, Windsor JA, Petrov MS. Predictors of severe and critical acute pancreatitis: a systematic review. Dig Liver Dis. 2014;46: 446–51. https://doi.org/10.1016/j.dld.2014.01.158.
43. Zeng YB, Zhan XB, Guo XR, Zhang HG, Chen Y, Cai QC, Li ZS. Risk factors for pancreatic infection in patients with severe acute pancreatitis: an analysis of 163 cases. J Dig Dis. 2014;15:377–85. https://doi.org/10.1111/1751-2980.12150.
44. Valverde-Lopez F, Matas-Cobos AM, Alegria-Motte C, Jimenez-Rosales R, Ubeda-Munoz M, Redondo-Cerezo E. BISAP, RANSON, lactate and other biomarkers in prediction of severe acute pancreatitis in a European cohort. J Gastroenterol Hepatol. 2017;32:1649–56.
45. Räty S, Pulkkinen J, Nordback I, et al. Can laparoscopic cholecystectomy prevent recurrent idiopathic acute pancreatitis? A prospective randomized multicenter trial. Ann Surg. 2015;262:736– 41.
46. Gurusamy KS, Debray TPA, Rompianesi G. Prognostic models for predicting the severity and mortality in people with acute pancreatitis. Cochrane Database Syst Rev 2018;2018, Issue 5. Art. No.: CD013026. DOI: https://doi. org/10.1002/14651858.CD013026.
47. Papachristou GI, Muddana V, Yadav D, O’Connell M, Sanders MK, Slivka A, et al. Comparison of BISAP, Ranson’s, APACHE-II, and CTSI scores in predicting organ failure, complications, and mortality in acute pancreatitis. Am J Gastroenterol. 2010;105:435–41.
48. Wu BU. Prognosis in acute pancreatitis. CMAJ. 2011;183:673–7. https://doi. org/10.1503/cmaj.101433.
49. Harrison DA, D’Amico G, Singer M. The pancreatitis outcome prediction (POP) score: a new prognostic index for patients with severe acute pancreatitis. Crit Care Med. 2007;35:1703–8.
50. Thandassery RB, Yadav TD, Dutta U, Appasani S, Singh K, Kochhar R. Hypotension in the first week of acute pancreatitis and APACHE II score predict development of infected pancreatic necrosis. Dig Dis Sci. 2015;60: 537–42. https://doi.org/10.1007/s10620-014-3081-y.
51. Cho JH, Kim TN, Chung HH, Kim KH. Comparison of scoring systems in predicting the severity of acute pancreatitis. World J Gastroenterol. 2015;21: 2387–94. https://doi.org/10.3748/wjg.v21.i8.2387.
52. Wu BU, Johannes RS, Sun X, Tabak Y, Conwell DL, Banks PA. The early prediction of mortality in acute pancreatitis: a large population-based study. Gut. 2008;57:1698–703. https://doi.org/10.1136/gut.2008.152702.
53. Park JY, Jeon TJ, Ha TH, Hwang JT, Sinn DH, Oh TH, et al. Bedside index for severity in acute pancreatitis: comparison with other scoring systems in predicting severity and organ failure. Hepatobiliary Pancreat Dis Int. 2013;12: 645–50.
54. Wang SQ, Li SJ, Feng QX, Feng XY, Xu L, Zhao QC. Overweight is an additional prognostic factor in acute pancreatitis: a meta-analysis. Pancreatology. 2011;11:92–8. https://doi.org/10.1159/000327688.
55. Fei Y, Gao K, Tu J, Wang W, Zong GQ, Li WQ. Predicting and evaluation the severity in acute pancreatitis using a new modeling built on body mass index and intra-abdominal pressure. Am J Surg. 2018;216:304–9. https://doi. org/10.1016/j.amjsurg.2017.04.017.
56. Pederzoli P, Bassi C, Vesentini S, et al. A randomized multicenter clinical trial of antibiotic prophylaxis of septic complications in acute necrotizing pancreatitis with imipenem. Surg Gynecol Obstet. 1993;176:480–3.
57. Isenmann R, Runzi M, Kron M, et al. Prophylactic antibiotic treatment in patients with predicted severe acute pancreatitis: a placebo- controlled, double blind trial. Gastroenterology. 2004;126:997–1004.
58. Dellinger EP, Tellado JM, Soto NE, et al. Early antibiotic treatment for severe acute necrotizing pancreatitis: randomized, double-blind, placebo-controlled study. Ann Surg. 2007;245:674–83.
59. Jiang K, Huang W, Yang XN, et al. Present and future of prophylactic antibiotics for severe acute pancreatitis. World J Gastroenterol. 2012;18:279– 84.
60. Villatoro E, Mulla M, Larvin M. Antibiotic therapy for prophylaxis against infection of pancreatic necrosis in acute pancreatitis. Cochrane Database Syst Rev. 2010;12(5):CD002941.
61. Sakorafas GH, Lappas C, Mastoraki A, Delis SG, Safioleas M. Current trends in the management of infected necrotizing pancreatitis. Infectious Disorders Drug Targets. 2010;10:9–14.
62. De Waele JJ. Rational use of antimicrobials in patients with severe acute pancreatitis. Semin Respir Crit Care Med. 2011;32:174–80.
63. Stigliano S, Sternby H, de Madaria E, Capurso G, Petrov MS. Early management of acute pancreatitis: a review of the best evidence. Dig Liver Dis. 2017;49:585–94.
64. Assicot M, Gendrel D, Carsin H, et al. High serum procalcitonin concentrations in patients with sepsis and infection. Lancet. 1993;341:515–8.
65. Mofidi R, Suttie SA, Patil PV, Ogston S, Parks RW. The value of procalcitonin at predicting the severity of acute pancreatitis and development of infected pancreatic necrosis: systematic review. Surgery. 2009;146:72–81.
66. Chen HZ, Ji L, Li L, Wang G, Bai XW, Cheng CD, Sun B. Early prediction of infected pancreatic necrosis secondary to necrotizing pancreatitis. Medicine (Baltimore). 2017;96:e7487.
67. Rau B, Steinbach G, Baumgart K, Gansauge F, Grünert A, Beger HG. The clinical value of procalcitonin in the prediction of infected necrosis in acute pancreatitis. Intensive Care Med. 2000;26(Suppl 2):S159–64.
68. Adachi T, Kishihara Y, Okano H, et al. The utility of procalcitonin for the patients with infected pancreatic necrotic and pancreatic abscess. Intensive Care Med Exp. 2015;3(Suppl 1):A113.
69. Eloubeidi MA, Tamhane A, Varadarajulu S, et al. Frequency of major complications after EUS-guided FNA of solid pancreatic masses: a prospective evaluation. Gastrointest Endosc. 2006;63:622–9.
70. Guarner-Argente C, Buchner A, Ahmad NA, et al. Use of antimicrobials for EUS-guided FNA of pancreatic cysts: a retrospective, comparative analysis. Gastrointest Endosc. 2011;74:81–6.
71. Buchler M, Malfertheiner P, Friess H, et al. Human pancreatic tissue concentration of bactericidal antibiotics. Gastroenterology. 1992;103:1902–8.
72. Otto W, Komorzycki K, Krawczyk M. Efficacy of antibiotic penetration into pancreatic necrosis. HPB: The Official Journal of the International Hepato Pancreato Biliary Association. 2006;8:43–8. https://doi.org/10.1080/ 13651820500467275.
73. Brattström C, Malmborg AS, Tyden G. Penetration of imipenem into human pancreatic juice following single intravenous dose administration. Chemotherapy. 1989;35:83–7.
74. Wittau M, Wagner E, Kaever V, et al. Intraabdominal tissue concentration of ertapenem. J Antimicrob Chemother. 2006;57:312– 6.
75. Wacke R, Forster S, Adam U, et al. Penetration of moxifloxacin into the human pancreas following a single intravenous or oral dose. J Antimicrob Chemother. 2006;58:994–9.
76. Schubert S, Dalhoff A. Activity of moxifloxacin, imipenem, and ertapenem against Escherichia coli, Enterobacter cloacae, Enterococcus faecalis, and Bacteroides fragilis in monocultures and mixed cultures in an in vitro pharmacokinetic/pharmacodynamic model simulating concentrations in the human pancreas. Antimicrob Agents Chemother. 2012;56:6434–6.
77. Mourad MM, Evans R, Kalidindi V, Navaratnam R, Dvorkin L, Bramhall SR. Prophylactic antibiotics in acute pancreatitis: endless debate. Ann R Coll Surg Engl. 2017;99:107–12.
78. Reuken PA, Albig H, Rödel J, Hocke M, Will U, Stallmach A, et al. Fungal infections in patients with infected pancreatic necrosis and pseudocysts: risk factors and outcome. Pancreas. 2018;47:92–8.
79. Schwender BJ, Gordon SR, Gardner TB. Risk factors for the development of intra-abdominal fungal infections in acute pancreatitis. Pancreas. 2015;44: 805–7.
80. Lytras D, Manes K, Triantopoulou C, et al. Persistent early organ failure: defining the high risk group of patients with severe acute pancreatitis. Pancreas. 2008;36:249–54.
81. de-Madaria E, Soler-Sala G, Sanchez-Paya UJ, Lopez-Font I, Martinez J, Gomez-Escolar L, et al. Influence of fluid therapy on the prognosis of acute pancreatitis: a prospective cohort study. Am J Gastroenterol. 2011; 106:1843–50.
82. Wu BU, Hwang JQ, Gardner TH, Repas K, Delee R, Yu S, et al. Lactated Ringer’s solution reduces systemic inflammation compared with saline in patients with acute pancreatitis. Clin Gastroenterol Hepatol. 2011;9:710–7.
83. Lipinski M, Rydzewska-Rosolowska A, Rydzewski A, Rydzewska G. Fluid resuscitation in acute pancreatitis: normal saline or lactated Ringer’s solution? World J Gastroenterol. 2015;21:9367–72.
84. Iqbal U, Anwar H, Scribani M. Ringer’s lactate versus normal saline in acute pancreatitis: a systematic review and meta-analysis. J Digest Dis. 2018;19: 335–41.
85. Myburgh JA, et al. Hydroxyethyl starch or saline for fluid resuscitation in intensive care. N Engl J Med. 2012;367:1901–11.
86. Zhao X, et al. Noninvasive positive-pressure ventilation in acute respiratory distress syndrome in patients with acute pancreatitis: a retrospective cohort study. Pancreas. 2016;45:58–63.
87. Wu X, et al. Effect of transpulmonary pressure-directed mechanical ventilation on respiration in severe acute pancreatitis patient with intraabdominal hypertension. Zhonghua Yi Xue Za Zhi. 2015;95:3168– 72.
88. Cordemans C. Fluid management in critically ill patients: the role of extravascular lung water, abdominal hypertension, capillary leak, and fluid balance. Ann Intensive Care. 2012;2(Suppl 1):S1.
89. Yasunaga H, Horiguchi H, Hashimoto H, Matsuda S, Fushimi K. Effect and cost of treatment for acute pancreatitis with or without gabexate mesylate: a propensity score analysis using a nationwide administrative database. Pancreas. 2013;42:260–4.
90. Yi F , Ge L, Zhao J e t al. Meta-analysis: total parenteral nutrition versus total enteral nutrition in predicted severe acute pancreatitis. Intern Med 2012;51: 523–530.
91. Bakker OJ, van Brunschot S, van Santvoort HC, Besselink MG, Bollen TL, Boermeester MA, et al. Early versus on-demand nasoenteric tube feeding in acute pancreatitis. N Emgl J Med. 2014;371:1983–93.
92. Tse F, Yuan Y. Early routine endoscopic retrograde cholangiopancreatography strategy versus early conservative management strategy in acute gallstone pancreatitis. Cochrane Database Syst Rev. 2012;39:CD009779. Cochrane Upper GI and Pancreatic Diseases Group, editor. Wiley & Sons, Ltd
93. van Geenen E-JM, van Santvoort HC, Besselink MGH, van der Peet DL, van Erpecum KJ, Fockens P, et al. Lack of consensus on the role of endoscopic retrograde cholangiography in acute biliary pancreatitis in published metaanalyses and guidelines: a systematic review. Pancreas. 2013;42:774–80.
94. Schepers NJ, Bakker OJ, Besselink MGH, Bollen TL, Dijkgraaf MGW, van Eijck CHJ, et al. Early biliary decompression versus conservative treatment in acute biliary pancreatitis (APEC trial): study protocol for a randomized controlled trial. Trials BioMed Central. 2016;17:5.
95. van Grinsven J, van Santvoort HC, Boermeester MA, Dejong CH, van Eijck CH, Fockens P, et al. Timing of catheter drainage in infected necrotizing pancreatitis, vol. 13: Nature Publishing Group. Nat Rev Gastroenterol Hepatol. 2016;13:306–12.
96. van Baal MC, van Santvoort HC, Bollen TL, Bakker OJ, Besselink MG, Gooszen HG. Systematic review of percutaneous catheter drainage as primary treatment for necrotizing pancreatitis. Br J Surg. 2010;98:18– 27.
97. Diaz JJ Jr, Cullinane DC, Khwaja KA, Tyson GH, Ott M, Jerome R, et al.Eastern Association for the Surgery of trauma. J Trauma Acute Care Surg. 2013;75:376–86.
98. Rodriguez JR, Razo AO, Targarona J, Thayer SP, Rattner DW, Warshaw AL, et al. Debridement and closed packing for sterile or infected necrotizing pancreatitis. Ann Surg. 2008;247:294–9.
99. Dua MM, Jensen CW, Friedland S, Worth PJ, Poultsides GA, Norton JA, et al. Isolated pancreatic tail remnants after transgastric necrosectomy can be observed. J Surg Res. 2018;231:109–15.
100. Bang JY, Wilcox CM, Navaneethan U, Hasan MK, Peter S, Christein J, et al. Impact of disconnected pancreatic duct syndrome on the endoscopic management of pancreatic fluid collections. Ann Surg. 2018;267:561–8.
101. Kirkpatrick AW, Roberts DJ, De Waele J, Jaeschke R, Malbrain MLNG, De Keulenaer B, et al. Intra-abdominal hypertension and the abdominal compartment syndrome: updated consensus definitions and clinical practice guidelines from the World Society of the Abdominal Compartment Syndrome. Intensive Care Med. 2013;39:1190–206.
102. Mentula P, Hienonen P, Kemppainen E, Puolakkainen P, Leppäniemi A. Surgical decompression for abdominal compartment syndrome in severe acute pancreatitis. Arch Surg. 2010;145:764–9.
103. Mowery NT, Bruns BR, MacNew HG, Agarwal S, Enniss TM, Khan M, et al. Surgical management of pancreatic necrosis. J Trauma Acute Care Surg. 2017;83:316–27.
104. van Santvoort HC, Besselink MG, Bakker OJ, Hofker HS, Boermeester MA, Dejong CH, et al. A step-up approach or open necrosectomy for necrotizing pancreatitis. N Engl J Med. 2010;362:1491–502.
105. Bakker OJ, van Santvoort HC, van Brunschot S, Geskus RB, Besselink MG, Bollen TL, et al. Endoscopic transgastric vs surgical necrosectomy for infected necrotizing pancreatitis: a randomized trial. JAMA. 2012;307:1053–61.
106. van Brunschot S, van Grinsven J, van Santvoort HC, Bakker OJ, Besselink MG, Boermeester MA, et al. Endoscopic or surgical step-up approach for infected necrotising pancreatitis: a multicentre randomised trial. Lancet. 2018;391:51–8.
107. Gurusamy KS, Belgaumkar AP, Haswell A, Pereira SP, Davidson BR. Interventions for necrotising pancreatitis. Cochrane upper GI and pancreatic diseases group. Cochrane Database Syst Rev. 2016;137:201–53.
108. Driedger M, Zyromski NJ, Visser B, et al. Surgical transgastric necrosectomy for necrotizing pancreatitis—a single-stage procedure for walled-off pancreatic necrosis. Ann Surg. 2018; https://doi.org/10.1097/ SLA00000000000003048. [Epub ahead of print]
109. van Baal MC, Besselink MG, Bakker OJ, van Santvoort HC, Schaapherder AF, Nieuwenhuijs VB, et al. Timing of cholecystectomy after mild biliary pancreatitis. Ann Surg. 2012;255:860–6.
110. Gurusamy KS, Nagendran M, Davidson BR. Early versus delayed laparoscopic cholecystectomy for acute gallstone pancreatitis. Cochrane Database Syst Rev. 2013;2(9):CD010326.
111. Falor AE, de Virgilio C, Stabile BE, Kaji AH, Caton A, Kokubun BA, et al. Early laparoscopic cholecystectomy for mild gallstone pancreatitis. Time for a paradigm shift. Arch Surg. 2012;147:1031–5.
112. Dubina ED, de Virgilio C, Simms ER, Kim DY, Moazzez A. Association of early vs delayed cholecystectomy for mild gallstone pancreatitis with perioperative outcomes. JAMA Surgery. 2018;153:1057–9.
113. Pham X-BD, de Virgilio C, Al-Khouja L, Bermudez MC, Schwed AC, Kaji AM, et al. Routine intraoperative cholangiography seems is unnecessary in patients with mild gallstone pancreatitis and normalizing bilirubin levels. Amer J Surg. 2016;212:1047–53.
114. da Costa DW, Bouwense SA, Schepers NJ, Besselink MG, van Santvoort HC, van Brunschot S, et al. Same-admission versus interval cholecystectomy for mild gallstone pancreatitis (PONCHO): a multicentre randomised controlled trial. Lancet. 2015;386:1261–8.
115. Nealon WH, Bawduniak J, Walser EM. Appropriate timing of cholecystectomy in patients who present with moderate to severe gallstone-associated acute pancreatitis with peripancreatic fluid collections. Ann Surg. 2004;239:741–51.
116. Jaipuria J, Bhandari V, Chawla AS, Singh M. Intra-abdominal pressure: time ripe to revise management guidelines of acute pancreatitis? World J Gastrointest Pathophysiol. 2016;7:186–98.
117. De Waele JJ, Hesse UJ, Pattyn P, Decruyenaere J, de Hemptinne B. Postoperative lavage and on demand surgical intervention in the treatment of acute necrotizing pancreatitis. Acta Chir Belg. 2000;100:16–20.
118. Harris JA, Jury RP, Catto J, Glover JL. Closed drainage versus open packing of infected pancreatic necrosis. Am Surg. 1995;61:612–7; discussion 7-8.
119. Radenkovic DV, Bajec D, Ivancevic N, Bumbasirevic V, Milic N, Jeremic V, et al. Decompressive laparotomy with temporary abdominal closure versus percutaneous puncture with placement of abdominal catheter in patients with abdominal compartment syndrome during acute pancreatitis: background and design of multicenter, randomised, controlled study. BMC Surg. 2010;10:22.
120. Coccolini F, Roberts D, Ansaloni L, Ivatury R, Gamberini E, Kluger Y, et al. The open abdomen in trauma and non-trauma patients: WSES guidelines. World J Emerg Surg. 2018;13:7.
121. Butte JM, Hameed M, Ball CG. Hepato-pancreato-biliary emergencies for the acute care surgeon: etiology, diagnosis and treatment. World J Emerg Surg. 2015;10:13.
122. Mier J, Leon EL, Castillo A, Robledo F, Blanco R. Early versus late necrosectomy in severe necrotizing pancreatitis. Am J Surg. 1997;173:71–5.
123. Ball CG, Hameed SM, Dixon E, Lillemoe KD. Severe acute pancreatitis for the acute care surgeon. J Trauma Acute Care Surg. 2016;80:1015– 22.
124. Howard TJ, Patel JB, Zyromski N, Sandrasegaran K, Yu J, Nakeeb A, et al. Declining morbidity and mortality rates in the surgical management of pancreatic necrosis. J Gastrointest Surg. 2007;11:43– 9.
125. Pliakos I, Papavramidis TS, Mihalopoulos N, Koulouris H, Kesisoglou I, Sapalidis K, et al. Vacuum-assisted closure in severe abdominal sepsis with or without retention sutured sequential fascial closure: a clinical trial. Surgery. 2010;148:947–53.
126. Robledo FA, Luque-de-Leon E, Suarez R, Sanchez P, de-la-Fuente M, Vargas A, et al. Open versus closed management of the abdomen in the surgical treatment of severe secondary peritonitis: a randomized clinical trial. Surg Infect. 2007;8:63–72.
127. Correa JC, Mejia DA, Duque N, J MM, Uribe CM. Managing the open abdomen: negative pressure closure versus mesh-mediated fascial traction closure: a randomized trial. Hernia. 2016;20:221–9.
128. Bee TK, Croce MA, Magnotti LJ, Zarzaur BL, Maish GO 3rd, Minard G, et al. Temporary abdominal closure techniques: a prospective randomized trial comparing polyglactin 910 mesh and vacuum- assisted closure. J Trauma. 2008;65:337–42. discussion 42-4
129. Kirkpatrick AW, Roberts DJ, Faris PD, Ball CG, Kubes P, Tiruta C, et al. Active negative pressure peritoneal therapy after abbreviated laparotomy: the intraperitoneal vacuum randomized controlled trial. Ann Surg. 2015;262:38–46.
130. Cheatham ML, Demetriades D, Fabian TC, Kaplan MJ, Miles WS, Schreiber MA, et al. Prospective study examining clinical outcomes associated with a negative pressure wound therapy system and Barker’s vacuum packing technique. World J Surg. 2013;37:2018–30.
131. Atema JJ, Gans SL, Boermeester MA. Systematic review and meta- analysis of the open abdomen and temporary abdominal closure techniques in nontrauma patients. World J Surg. 2015;39:912–25.
132. Roberts DJ, Zygun DA, Grendar J, Ball CG, Robertson HL, Ouellet JF, et al. Negative-pressure wound therapy for critically ill adults with open abdominal wounds: a systematic review. J Trauma Acute Care Surg. 2012;73:629–39.
133. Smith JW, Matheson PJ, Franklin GA, Harbrecht BG, Richardson JD, Garrison RN. Randomized controlled trial evaluating the efficacy of peritoneal resuscitation in the management of trauma patients undergoing damage control surgery. J Am Coll Surg. 2017;224:396– 404.
134. Sartelli M, Abu-Zidan FM, Ansaloni L, Bala M, Beltran MA, Biffl WL, et al. The role of the open abdomen procedure in managing severe abdominal sepsis: WSES position paper. World J Emerg Surg. 2015;10:35.
135. Beckman M, Paul J, Neideen T, Weigelt JA. Role of the open abdomen in critically ill patients. Crit Care Clin. 2016;32:255–64.
136. Koperna T, Schulz F. Relaparotomy in peritonitis: prognosis and treatment of patients with persisting intraabdominal infection. World J Surg. 2000;24:32–7.
137. Coccolini F, Catena F, Montori G, Ceresoli M, Manfredi R, Nita GE, et al. IROA: the international register of open abdomen: an international effort to better understand the open abdomen: call for participants. World J Emerg Surg. 2015;10:37.
138. Pommerening MJ, DuBose JJ, Zielinski MD, Phelan HA, Scalea TM, Inaba K, et al. Time to first take-back operation predicts successful primary fascial closure in patients undergoing damage control laparotomy. Surgery. 2014; 156:431–8.
139. Bjorck M, Wanhainen A. Management of abdominal compartment syndrome and the open abdomen. Eur J Vasc Endovasc Surg. 2014;47:279– 87.
140. De Keulenaer B, Regli A, De Laet I, Roberts D, Malbrain ML. What’s new in medical management strategies for raised intra-abdominal pressure: evacuating intra-abdominal contents, improving abdominal wall compliance, pharmacotherapy, and continuous negative extra- abdominal pressure. Anaesthesiol Intensive Ther. 2015;47:54–62.
141. Godat L, Kobayashi L, Costantini T, Coimbra R. Abdominal damage control surgery and reconstruction: world society of emergency surgery position paper. World J Emerg Surg. 2013;8:53.
142. Chen Y, Ye J, Song W, Chen J, Yuan Y, Ren J. Comparison of outcomes between early fascial closure and delayed abdominal closure in patients with open abdomen: a systematic review and meta-analysis. Gastroenterol Res Pract. 2014;2014:784056.