Bài viết Bệnh sinh và điều trị loạn sản phế quản phổi được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Pathogenesis and Treatment of Bronchopulmonary Dysplasia
Tóm tắt
Mục đích đánh giá: Loạn sản phế quản phổi (BPD, Bronchopulmonary dysplasia) là một bệnh phổi mãn tính ở trẻ nhỏ ảnh hưởng đến hầu hết trẻ sinh non với tỷ lệ mắc bệnh và tử vong đáng kể. Cải thiện khả năng sống sót của trẻ sơ sinh rất non nớt đã dẫn đến số trẻ sơ sinh mắc chứng rối loạn này tăng lên. Tổn thương phổi cấp tính và mãn tính và suy giảm phát triển phổi sau sinh được cho là nguyên nhân gây ra bệnh BPD. Mặc dù những thay đổi trong thực hành lâm sàng đã cải thiện tiến trình lâm sàng và kết quả cho trẻ sơ sinh mắc bệnh BPD, trong thập kỷ qua, tỷ lệ mắc bệnh BPD nói chung không thay đổi. Tổng quan này sẽ mô tả các yếu tố trước và sau khi sinh góp phần vào sinh bệnh học của BPD cũng như các liệu pháp điều trị hiện tại và thử nghiệm để điều trị BPD.
Những phát hiện gần đây: Các yếu tố góp phần vào sinh bệnh học của BPD được mô tả rõ ràng, tuy nhiên các nghiên cứu gần đây đã xác định rõ hơn cách thức các yếu tố này điều chỉnh sự phát triển của phổi. Viêm, các cytokine tiền viêm và thay đổi tín hiệu gen sinh mạch máu góp phần gây tổn thương phổi và làm suy giảm sự phát triển phổi trước và sau sinh dẫn đến BPD, tuy nhiên cho đến nay chưa có liệu pháp nào được xác định rằng có thể ngăn chặn hoặc đảo ngược tác động của chúng đối với sự phát triển của phổi. Chúng tôi sẽ thảo luận về các con đường truyền tín hiệu tế bào bị ảnh hưởng trong BPD và các liệu pháp hiện tại có sẵn để điều chỉnh các con đường này.
Tóm lược: Mặc dù những tiến bộ hiện tại trong chăm sóc trẻ sơ sinh, BPD vẫn là một gánh nặng lớn đối với các nguồn lực chăm sóc sức khỏe. Các phương pháp điều trị mới nhằm giảm tổn thương phổi hoặc cải thiện sự phát triển của phổi đang được nghiên cứu.
Giới thiệu
Loạn sản phế quản phổi (BPD) là một bệnh phổi mãn tính thường xảy ra ở trẻ sinh non cần thở máy và điều trị oxy cho bệnh suy hô hấp cấp tính (1-3), nhưng cũng có thể xảy ra ở trẻ sơ sinh chưa trưởng thành, có ít dấu hiệu của phổi ban đầu bị bệnh (4). Mặc dù rối loạn này thường liên quan đến sinh non, nhưng nó cũng có thể xảy ra ở trẻ sơ sinh đủ tháng cần điều trị máy thở tích cực cho bệnh phổi nặng, cấp tính. Sự ra đời của việc sử dụng steroid trước khi sinh, điều trị bằng surfactant (surfactant), chiến lược máy thở mới, cải thiện dinh dưỡng và các phương pháp điều trị khác đã dẫn đến những cải thiện lớn trong quá trình lâm sàng và kết quả của trẻ sơ sinh bị hội chứng suy hô hấp trong 40 năm qua (5,6). Tuy nhiên, mặc dù các phương pháp điều trị này, tỷ lệ mắc bệnh BPD nói chung, không thay đổi trong thập kỷ qua (7).
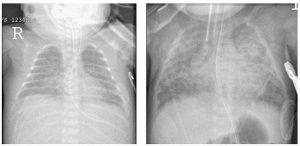
Các đặc trưng lần đầu tiên được mô tả bởi Northway et al. vào 1967, BPD theo truyền thống được định nghĩa là sự hiện diện của các dấu hiệu và triệu chứng hô hấp dai dẳng, cần oxy bổ sung để điều trị thiếu oxy và chụp X quang ngực bất thường ở tuổi 36 tuần sau tuổi kinh nguyệt (post menstrual age) (tuổi thai cộng với tuổi sau sinh (8) (Bảng 1). Hiện nay đã có sự công nhận rằng trẻ sơ sinh mắc bệnh phổi mãn tính sau khi sinh non có một quá trình lâm sàng và bệnh lý khác với ghi nhận trước khi sử dụng surfactant (5,6,10,11). Các giai đoạn tiến triển kinh điển với tình trạng xơ hóa nổi bật mà đặc trưng là bệnh BPD trước đây thường ít gây ấn tượng hơn và hiện tại bệnh được xác định chủ yếu bằng sự gián đoạn của sự phát triển phổi ở xa và được gọi là chứng loạn sản phế quản phổi mới (4) (Bảng 2, hình 1) Không giống như dạng ban đầu của bệnh, dạng mới này thường phát triển ở trẻ sơ sinh non tháng, những người có thể cần ít hoặc không cần hỗ trợ thở máy, và đã nồng độ oxy khí hít vào thấp trong những ngày đầu sau sinh (5,6). Khi khám nghiệm tử thi, mô học phổi dạng mới của những trẻ này có các vùng tổn thương đồng đều hơn và nhẹ hơn, nhưng sự phát triển của phế nang và mạch máu bị suy yếu vẫn còn nổi bật (bảng 1). Ở đây chúng tôi xem xét cơ chế bệnh sinh BPD, và cung cấp một cái nhìn tổng quan về các phương pháp điều trị dự phòng hiện có và tiềm năng.
Sinh bệnh học
Mặc dù BPD có nguyên nhân đa yếu tố (hình 2), các yếu tố trước và sau sinh chịu trách nhiệm cho sự tăng trưởng phế nang bị phá vỡ vẫn được xác định khá rõ. Trong khi mối liên quan mạnh nhất là sinh non, các yếu tố khác như nhiễm trùng và viêm trước khi sinh, thở máy, nhiễm độc oxy với giảm khả năng chống oxy hóa của vật chủ, còn ống động mạch và nhiễm trùng sau sinh đều góp phần gây bệnh cho bệnh BPD.
| Bảng 1 Tiêu chuẩn chẩn đoán NIH cho chứng loạn sản phế quản phổi (9). | ||
| Tuổi thai | ||
| <32 tuần | >32 tuần | |
| Thời điểm đánh giá | 36 tuần tuổi sau kỳ kinh nguyệt hoặc xuất viện | > 28 ngày nhưng <56 ngày tuổi sau sinh hoặc xuất viện |
| Loạn sản phế quản phổi | ||
| Nhẹ | Hít thở không khí phòng ở tuần 36 tuổi sau kỳ kinh nguyệt hoặc xuất viện | Hít thở không khí phòng sau 56 ngày tuổi sau sinh hoặc xuất viện |
| Vừa phải | Cần <30% O2 sau 36 tuần tuổi sau kỳ kinh nguyệt hoặc xuất viện | Cần <30% O2 đến 56 ngày tuổi sau sinh hoặc xuất viện |
| Nặng | Cần> 30% O2, có hoặc không có thông khí áp lực dương hoặc áp lực dương liên tục ở tuổi 36 sau kỳ kinh | Cần> 30% O2, có hoặc không có thông khí áp lực dương hoặc áp lực dương liên tục ở ngày tuổi 56 sau sinh, hoặc xuất viện |
Gần đây tiền sản giật đã được xác định là một yếu tố rủi ro cho sự phát triển tiếp theo của BPD (12). Trong khi antiangiogenesis được biết là góp phần đáng kể vào sự gián đoạn phát triển phổi ở mô hình động vật (13,14), các nghiên cứu gần đây đã cho thấy sự hình thành mạch bị suy yếu trong sự phát triển của tiền sản giật (15,16,17). Tiền sản giật có liên quan đến tăng chất fms-like tyrosine kinase 1 (sFlt-1) gắn màng tế bào, là một thụ thể cho VEGF và yếu tố tăng trưởng nhau thai (PlGF), một protein pro-angiogen liên quan với hoạt động đối kháng của cả VEGF và PIGF. Nó được sản xuất với số lượng quá mức bởi trophoblast trong tiền sản giật và vô hiệu hóa VEGF và PlGF [15,16,17]. Trẻ sơ sinh ở người mẹ bị tiền sản giật đã chứng minh sFlt-1 trong máu cuống rốn cao hơn nhưng mức PlGF và VEGF trong máu thấp hơn tương ứng với sự phát triển tiếp theo của BPD (18).
| Bảng 2 Sự khác biệt về đặc điểm bệnh lý của chứng loạn sản phế quản “cũ” và “mới” (10) | |
| Pre-surfactant (cũ) | Post-surfactant (mới) |
| Thay thế xẹp phổi với căng phồng phổi | Sự không đồng nhất trong khu vực của bệnh phổi |
| Tổn thương biểu mô đường thở nặng (ví dụ, tăng sản, dị sản tế bào vảy) | Hiếm tổn thương biểu mô đường thở |
| Tăng sản cơ trơn đường thở rõ rệt |
Dày cơ trơn đường thở nhẹ |
| Tăng sinh sợi xơ hóa, lan tỏa | Hiếm thay đổi tăng sinh sợi |
| Động mạch phổi tái tạo tăng huyết áp | Ít động mạch hơn nhưng “bất thường hình dạng” |
| Giảm phế nang hóa và diện tích bề mặt | Phế nang ít hơn, lớn hơn và đơn giản hơn |
Gần đây tiền sản giật đã được xác định là một yếu tố rủi ro cho sự phát triển tiếp theo của BPD (12). Trong khi antiangiogenesis được biết là góp phần đáng kể vào sự gián đoạn phát triển phổi ở mô hình động vật (13,14), các nghiên cứu gần đây đã cho thấy sự hình thành mạch bị suy yếu trong sự phát triển của tiền sản giật (15,16,17). Tiền sản giật có liên quan đến tăng chất fms-like tyrosine kinase 1 (sFlt-1) gắn màng tế bào, là một thụ thể cho VEGF và yếu tố tăng trưởng nhau thai (PlGF), một protein pro-angiogen liên quan với hoạt động đối kháng của cả VEGF và PIGF. Nó được sản xuất với số lượng quá mức bởi trophoblast trong tiền sản giật.

Thay đổi tín hiệu yếu tố tăng trưởng nội mô mạch máu (VEGF) góp phần gây ra bệnh mạch máu do tăng oxy máu ở cả BPD và bệnh võng mạc do sinh non (ROP) (19,20,21). Trong các nghiên cứu ở người về BPD, VEGF đã giảm trong các mẫu dịch khí quản từ trẻ sơ sinh có nguy cơ sớm mắc bệnh BPD, và biểu hiện VEGF và VEGF của thụ thể VEGF-1 (VEGFR-1) đã giảm ở trẻ sơ sinh tử vong với BPD (22,23). Trong các nghiên cứu trên động vật, hyperoxia làm giảm biểu hiện VEGF phế nang (24) và ức chế thụ thể VEGF chọn lọc làm giảm sự phát triển mạch máu phổi và phế nang (14,25). Những kết quả này cho thấy rằng việc tương tác chéo giữa biểu mô phế nang và nội mô mạch máu, đặc biệt là qua tín hiệu VEGF, rất quan trọng đối với sự phát triển của phổi bình thường sau khi sinh và sự gián đoạn của tín hiệu VEGF làm suy yếu sự phát triển của mạch máu phổi và sự phế nang hóa.
Viêm màng ối-màng đệm (chorioamnionitis) và viêm trước khi sinh là những yếu tố đóng góp cho sự phát triển của BPD (26-29). Thay đổi cả hai loại cytokine gây viêm như yếu tố hoại tử khối u (TNFa), Interleukin-1beta (IL-1β), Interleukin-6 (IL-6), Interleukin-8 (IL-8), chất biến đổi cytokine (p55) và chất đối kháng thụ thể IL-1 (IL-1RA) và protein phản ứng C đã được tìm thấy trong huyết thanh rốn của trẻ sơ sinh có mẹ bị viêm màng não nặng (30). Nồng độ cytokine tăng cao trong bối cảnh viêm màng đệm có tương quan với sự phát triển tiếp theo của BPD (31,32). Nhiều nghiên cứu gần đây đã mở rộng về những phát hiện này chứng minh rằng môi trường viêm này có thể thay đổi đường dẫn tín hiệu tế bào quan trọng trong hình thái phân nhánh phổi. Yếu tố tăng trưởng nguyên bào sợi 10 (FGF- 10) là một trong những yếu tố tăng trưởng trung mô quan trọng cho sự phát triển của phổi, thúc đẩy mở rộng đường thở và phân nhánh (33). Yếu tố hạt nhân kappa B (NF-B), thúc đẩy sự biểu hiện của nhiều gen, bao gồm các cytokine tiền viêm liên quan đến sự phát triển của BPD. Nó được kích hoạt bởi một loạt các yếu tố, bao gồm các kích thích nhiễm trùng, các cytokine gây viêm, biến dạng, chất oxy hóa và các nguyên nhân khác gây stress tế bào (34). Hoạt hóa IL-1β và TNF-α của NF-κB phá vỡ biểu hiện bình thường của FGF-10 trong trung mô phổi của thai nhi và ức chế sản sinh hình thái phổi (35).
Ngay cả khi không có viêm màng đệm, tổn thương phổi cấp tính trung gian cytokine, (36) sẽ làm trầm trọng thêm tổn thương phổi liên quan đến máy thở (37) và điều hòa đối kháng của vật chủ (38). Nồng độ cytokine tăng cao đã được quan sát thấy ở dịch hút khí quản (39,40) và huyết thanh (41,42) của trẻ sơ sinh mắc hội chứng suy hô hấp và dự đoán sự phát triển tiếp theo của BPD. Cụ thể hơn, nồng độ IL-1, IL-6, Il-8, IL 10 và INF gamma tăng cao và nồng độ interleukin 17 thấp hơn là tiên đoán của BPD.
Sự thay đổi trong tín hiệu TGF-β1 đã được chứng minh là rất quan trọng trong cơ chế bệnh sinh của BPD. Trong dịch rửa phế quản phế nang, tăng TGF- β1 đã được báo cáo để dự đoán tiến triển thành BPD, hoặc nhu cầu bổ sung oxy [43] và ở phổi chuột sơ sinh, việc chuyển dạng hoạt động của gen TGF-β1 tạo ra sự thay đổi mô học phù hợp với BPD [44]. Một nghiên cứu gần đây đã chứng minh mối quan hệ giữa nồng độ TGF-β1nước ối, viêm màng đệm và tổn thương phổi thai nhi (45), liên kết nhiễm trùng tiền sản và viêm nhiễm với BPD.
Phơi nhiễm hyperoxia sau sinh làm tăng sản xuất các gốc tự do oxy gây độc tế bào, có thể lấn át các cơ chế bảo vệ chống oxy hóa của vật chủ và gây tổn thương phổi (46,47). Trẻ sinh non bị thiếu hệ thống enzyme chống oxy hóa khi sinh và có hàm lượng chất chống oxy hóa thấp như vitamin C và E, làm tăng tính dễ bị tổn thương của chúng đối với độc tính oxy. Hyperoxia cũng làm giảm biểu hiện VEGF (24) và tăng biểu hiện TGF-β1 (48) cũng như mức độ của các cytokine tiền viêm (49). Nhu cầu thở máy sau sinh có mối tương quan mật thiết với sự phát triển của BPD. Thông khí cơ học làm tăng sản xuất TNFa, IL-1 beta, IL6, IL8 và IL1ra (50) và làm thay đổi rõ rệt hồ sơ gen angiogen trong phổi. Các gen chống ung thư được điều chỉnh tăng trong phổi thông khí bao gồm thrombospondin-1, collagen XVIII alpha-1 và chất ức chế mô của metallico- proteinase-1 (TIMP1), cũng như endoglin, biến đổi yếu tố tăng trưởng-alpha và monocyte chemo- attractant protein-1. Các gen điều hòa giảm pro- angiogen bao gồm angiogenin và midkine, cũng như yếu tố tăng trưởng nội mô mạch máu (VEGF) – B, thụ thể VEGF-2 và thụ thể angiopoietin TEK / Tie- 2 (19). Sự gia tăng các cytokine tiền viêm và sự thay đổi trong các gen tạo mạch từ tổn thương phổi liên quan đến máy thở có thể một phần là do volutrauma. Sự phát triển của BPD thứ phát sau volutrauma được đề xuất một phần bởi mối quan hệ nghịch đảo giữa mức PaCO2 thấp và nguy cơ phát triển của BPD (51). Do đó, cần tránh thể tích khí lưu thông cao trong quá trình thở máy sớm và ngay cả khi hồi sức trong phòng sinh. Trong một nghiên cứu thực nghiệm về mối liên hệ giữa kích thước của bơm phồng thủ công và tổn thương phổi ở cừu, tác dụng phụ đã được ghi nhận ngay cả khi bơm 8 ml/kg (52).
Thông khí cơ học là một điều trị thiết yếu cho trẻ cực kỳ non tháng ở biên giới khả năng sống. Các nghiên cứu gần đây so sánh thông khí nhắm mục tiêu thể tích đến thông khí áp lực đã cho thấy một số hứa hẹn. Việc sử dụng thông khí mục tiêu thể tích dẫn đến giảm kết quả tử vong hoặc loạn sản phế quản phổi, tràn khí màng phổi, ngày thông khí và hypocarbia (53). Những phát hiện này được hỗ trợ bằng cách giảm nồng độ IL-6 và IL-8 từ dịch hút khí quản của bệnh nhân được điều trị bằng thông khí nhắm mục tiêu thể tích khi so sánh với thông khí nhắm mục tiêu áp lực (54). Các chiến lược thông khí thay thế cũng có thể đóng một vai trò trong việc giảm BPD. Mặc dù sớm, việc sử dụng HFOV thường xuyên chưa được chứng minh là cải thiện kết quả phổi ở trẻ sơ sinh non tháng, Courtney và cộng sự cho thấy rằng sử dụng HFOV như một chiến lược giải cứu (ở trẻ sơ sinh có yêu cầu thở máy thông thường cao mặc dù điều trị bằng surfactant), đã giảm tỷ lệ mắc bệnh BPD (55).
Cũng có thể có một mối liên quan giữa còn ống động mạch (PDA) và BPD. Tiếp xúc lâu dài với một PDA có triệu chứng, làm xấu đi tình trạng bệnh phổi (56). Một PDA với shunting từ trái sang phải làm tăng dòng chảy dịch và protein từ hệ mạch máu phổi vào nhu mô phổi. Việc tăng dịch và protein vào mô kẽ phổi làm tăng áp lực lọc vi mạch phổi và tăng lưu lượng bạch huyết phổi giúp loại bỏ dịch và protein dư thừa từ phổi. Sự gia tăng bù này trong bạch huyết phổi ức chế sự tích tụ chất lỏng trong phổi (57). Với tồn tại của ống động mạch kéo dài, cơ chế bù này bị quá tải và phù phổi phát triển. Với sự hiện diện của nhiễm trùng huyết và RDS, cơ chế này dễ bị áp đảo hơn (5). Mặc dù có mối quan hệ giữa PDA và BPD, nhưng việc điều trị tích cực cho PDA bằng cách sử dụng phương pháp nội khoa hoặc phẫu thuật đã không được chứng minh là làm giảm tỷ lệ mắc bệnh BPD. Trên thực tế, trong một nghiên cứu, phẫu thuật thắt ống động mạch của PDA đã làm tăng tỷ lệ mắc bệnh BPD (58).
Các mô hình động vật của hyperoxia gây ra tổn thương phổi đã chứng minh vai trò của các tế bào tiền thân (nội mô và trung mô) trong sinh bệnh học của BPD và cho rằng các tế bào này góp phần sửa chữa sau tổn thương (59,60). Các tế bào tiền thân nội mô (EPC) và tế bào gốc trung mô (MSC) dễ dàng được phân lập từ máu cuống rốn ở 24-28 tuần tuổi thai, máu mang lại chủ yếu là MSC và máu thai kỳ 32-36 tuần mang lại EPCs (61) (Hình 3 (62)). Ở chuột con sơ sinh, sau khi tủy xương tiếp xúc hyperoxia, EPC trong tuần hoàn và tại phổi giảm rõ rệt (59) và ở trẻ sơ sinh cực kỳ non tháng, giảm số lượng tế bào tiền thân nội mô dây rốn sau khi sinh non cực kỳ có thể liên quan đến nguy cơ phát triển mạch máu phổi đặc tính non nớt của BPD mới (63). Sự hiện diện của các tế bào tiền thân lưu hành giảm và sự liên kết của nó với BPD có thể có tiềm năng điều trị rất lớn cho các tế bào có nguồn gốc từ máu cuống rốn này. Các nghiên cứu trên động vật cho đến nay cho thấy các liệu pháp dựa trên tế bào gốc có thể cung cấp các phương pháp điều trị mới cho các bệnh phổi hiện đang thiếu phương pháp điều trị hiệu quả.
![Hình 3 Phân biệt hemangioblasts thành tế bào tạo máu và tế bào nội mô. Các tế bào có nguồn gốc từ tủy xương có thể biệt hóa các dòng tế bào khác nhau để tạo ra các tế bào nội mô có thể tham gia vào quá trình vận mạch sau sinh hoặc tạo mạch máu (21). Vì lý do này, các tế bào có nguồn gốc từ tủy xương có tiềm năng điều trị lớn trong chứng loạn sản phế quản phổi. Chỉnh sửa với sự cho phép từ [62]](https://www.healcentral.org/wp-content/uploads/2020/09/benh_sinh_va_dieu_tri_loan_san_phe_quan_phoi_3-300x230.jpg)
Điều trị loạn sản phế quản phổi
Các yếu tố góp phần vào sinh bệnh học của BPD là vô số và các chiến lược điều trị cho đến nay đối với BPD đã không chứng minh được việc giảm tỷ lệ mắc bệnh BPD. Vì lý do này, các chiến lược nhằm ngăn chặn sự phát triển của BPD là chìa khóa. Việc sử dụng steroid trước sinh ở những bà mẹ có nguy cơ sinh con sớm làm giảm 50% tỷ lệ tử vong ở trẻ sơ sinh và hội chứng suy hô hấp, nhưng ngay cả khi kết hợp với surfactant sau sinh, vẫn không làm giảm tỷ lệ mắc bệnh BPD. Liệu pháp surfactant ngoại sinh làm giảm tỷ lệ tử vong do BPD, nhưng không ngăn ngừa được bệnh; có thể nói, điều này có thể là do sự gia tăng tỷ lệ sống sót của trẻ sơ sinh rất non nớt có nguy cơ mắc bệnh BPD cao. Sự kết hợp của barotrauma hoặc volutrauma với BPD đã dẫn đến việc sử dụng các chiến lược như hypercapnia cho phép (65) để giảm thiểu tổn thương phổi. Bằng chứng gần đây cho thấy một số lợi ích đối với thông khí đảm bảo thể tích như một chế độ máy thở để ngăn ngừa bệnh BPD và giảm viêm liên quan đến thở máy (54,55). Các thử nghiệm ngẫu nhiên lớn hơn nữa sẽ cần thiết để xác nhận phát hiện này. Mặc dù cho đến nay vẫn chưa có chế độ thông khí lý tưởng nào xuất hiện, nhưng rõ ràng từ các nghiên cứu sinh lý cho thấy thể tích khí lưu thông và nồng độ oxy được hít vào nên được giữ ở mức thấp nhất có thể để tránh hypocarbia, volutrauma và độc tính oxy, và nên sử dụng chiến lược huy động phổi.
Một cách tiếp cận khác để giảm BPD là tránh đặt nội khí quản và thở máy bằng cách sử dụng áp lực dương liên tục qua mũi sớm (CPAP). Một nghiên cứu so sánh kết quả của trẻ sinh non nặng 500 – 1500 g khi sinh được điều trị ở Boston hoặc New York, Hoa Kỳ, báo cáo rằng tỷ lệ mắc bệnh BPD cao hơn ở Boston (22%) so với ở New York (4%) và nguy cơ mắc bệnh tăng lên có liên quan đến đặt nội khí quản sớm và thở máy (66). Nhiều trung tâm hiện nay giảm thiểu việc sử dụng thở máy, thích CPAP qua mũi có hoặc không có surfactant ngoại sinh, và báo cáo tỷ lệ mắc bệnh BPD thấp ở trẻ sơ sinh có nguy cơ cao. Tuy nhiên, các thử nghiệm lâm sàng có kiểm soát lớn vẫn chưa thể nhân đôi trải nghiệm trung tâm duy nhất. Thử nghiệm COIN đã chọn ngẫu nhiên 610 trẻ sinh từ 25 đến 28 tuần tuổi để điều trị CPAP hoặc đặt nội khí quản và thở máy vào lúc 5 phút sau khi sinh và phát hiện CPAP mũi sớm không làm giảm đáng kể tỷ lệ tử vong hoặc loạn sản phế quản phổi so với đặt nội khí quản (67). Nghiên cứu này một lần nữa chứng minh hiệu quả của surfactant trong việc giảm airleak, vì CPAP có liên quan đến việc tăng đáng kể nguy cơ tràn khí màng phổi. Một nghiên cứu gần đây đã chọn ngẫu nhiên 1316 trẻ sơ sinh đặt nội khí quản và điều trị bằng surfactant (trong vòng 1 giờ sau khi sinh) hoặc điều trị CPAP được bắt đầu trong phòng sinh, với việc sử dụng chiến lược thông khí hạn chế theo giao thức và cũng không tìm thấy sự khác biệt nào trong kết cục chính của tử vong hoặc loạn sản phế quản phổi như được xác định bởi yêu cầu oxy bổ sung ở tuần 36 (68). Dựa trên những phát hiện này, cần thận trọng trong việc lựa chọn một dân số có thể hưởng lợi từ phương pháp này và các tác dụng phụ, như mất ổn định huyết động và viêm ruột hoại tử, cần được theo dõi cẩn thận.
Một phân tích tổng hợp của bảy thử nghiệm ngẫu nhiên cho thấy rằng bổ sung vitamin A toàn thân với số lượng đủ để thiết lập nồng độ retinol trong huyết thanh bình thường làm giảm sự phụ thuộc oxy ở 36 tuần tuổi sau kỳ kinh nguyệt (69), nhưng không thay đổi kết quả lâu dài. Tuy nhiên, nồng độ vitamin A phải được theo dõi cẩn thận và trong khi có lợi trong thời gian ngắn, việc thiếu tác dụng lâu dài có lợi đã được chứng minh đối với kết quả phổi và thần kinh đã hạn chế sử dụng liệu pháp này.
Liệu pháp corticosteroid, mặc dù hướng vào việc giảm viêm phổi thấy ở trẻ sơ sinh mắc bệnh BPD tiến triển hoặc thành lập, có lẽ là lĩnh vực chăm sóc gây tranh cãi nhất. Các nghiên cứu lâm sàng đã liên tục chỉ ra rằng steroid cải thiện sâu sắc cơ học phổi và trao đổi khí, và giảm các tế bào viêm và các sản phẩm của chúng trong các mẫu dịch hút khí quản của bệnh nhân mắc bệnh BPD (70,71). Một phân tích tổng hợp các thử nghiệm ngẫu nhiên cho thấy corticosteroid làm giảm sự phụ thuộc oxy mãn tính ở 28 ngày và 36 tuần sau tuổi kinh nguyệt, nếu được sử dụng một cách có hệ thống trong 96 giờ đầu, (72) nhưng có những lo ngại quan trọng về việc tăng tỷ lệ tử vong và tác dụng phụ tăng trưởng đầu, kết quả phát triển thần kinh và cấu trúc phổi (72-74). Việc sử dụng steroid liều cao thường xuyên ở trẻ sơ sinh non tháng rất không được khuyến khích, như được phản ánh trong các bài xã luận của Học viện Nhi khoa Hoa Kỳ và những người khác (75,76). Tuy nhiên, những phát hiện bất lợi thường dựa trên dữ liệu từ các nghiên cứu đã sử dụng liều cao dexamethasone bắt đầu trong vài ngày đầu đời và dùng trong thời gian dài. Nhiều câu hỏi vẫn tồn tại liên quan đến mối quan hệ lợi ích – rủi ro trong việc sử dụng các steroid khác trong thời gian nghiên cứu ngắn hơn. Do đó, một số trung tâm khuyên bạn nên sử dụng steroid ngoài tuần đầu tiên với liều thấp hơn và trong thời gian ngắn hơn (5-7 ngày) ở trẻ sơ sinh phụ thuộc máy thở bị bệnh phổi nặng, dai dẳng. Do các tác dụng phụ được quan sát của dexamethasone, sử dụng steroid sau sinh bằng hydrocortison đã được nghiên cứu để phòng ngừa bệnh BPD. Mặc dù không có nghiên cứu nào cho thấy lợi ích rõ ràng khi sử dụng hydrocortison, nhưng hướng tác dụng ủng hộ hydrocortisone trong tất cả các nghiên cứu và trong nghiên cứu lớn nhất cho đến nay, đối với trẻ sơ sinh bị viêm màng não, hydrocortisone giảm đáng kể tỷ lệ tử vong và tăng tỷ lệ sống sót khi không mắc bệnh BPD (77). Không có tác dụng ngắn hoặc dài hạn bất lợi đã được chứng minh khi sử dụng hydrocortison trong mọi nghiên cứu. Đối với trẻ sơ sinh mắc bệnh BPD và bệnh phổi mãn tính phụ thuộc vào máy thở, hydrocortison dùng với liều 5 mg/kg mỗi ngày, giảm dần trong 3 tuần có hiệu quả như dexamathasone để cai máy cho trẻ từ máy thở và giảm liệu pháp oxy bổ sung, với thời gian ngắn hơn và giảm liệu pháp oxy bổ sung. không có tác dụng phụ lâu dài (78). Những tác dụng có lợi của liệu pháp hydrocortison cần phải được cân nhắc với tỷ lệ tăng của thủng đường tiêu hóa, đặc biệt là khi sử dụng đồng thời indomethacin (77). Để tránh các tác dụng phụ liên quan đến dùng đường toàn thân, steroid cũng đã được sử dụng qua đường hô hấp, nhưng không có lợi ích quan trọng nào được ghi nhận với phương pháp này. Tác dụng chính của betamethasone dạng hít trong một thử nghiệm ngẫu nhiên đa trung tâm là làm giảm nhu cầu nhận thức về việc sử dụng steroid toàn thân (79-81). Một phân tích gần đây đã chứng minh tỷ lệ rút ống thành công tăng lên sau 1 – 4 tuần sử dụng steroid dạng hít, mà không làm giảm tỷ lệ mắc bệnh BPD (82).
Nitric oxide dạng hít (NO) đã được chứng minh là có hiệu quả trong việc cải thiện cấu trúc phổi trong nhiều mô hình thí nghiệm của BPD. Những nghiên cứu này bao gồm chuột sơ sinh và chuột con sau khi tiếp xúc với hyperoxia (83,84), bleomycin gây ra BPD ở chuột con sơ sinh (85) và cừu non bị RDS (86). Ba nghiên cứu đối chứng ngẫu nhiên lớn về hít NO để phòng ngừa cũng như điều trị bệnh BPD đã thành lập đã được công bố (47,48,49). Nghiên cứu đầu tiên đã chọn ngẫu nhiên 793 trẻ sơ sinh dưới 34 tuần tuổi thai cần thở máy trong vòng 48 giờ đầu đời để nhận khí NO (5ppm) hoặc khí giả dược trong 21 ngày hoặc cho đến khi rút ống. Trong thử nghiệm này, iNO đã giảm 50% tỷ lệ mắc bệnh BPD cho trẻ sơ sinh có cân nặng khi sinh lớn hơn 1000g. NO hít cũng làm giảm tỷ lệ chấn thương não ở trẻ sơ sinh non tháng (87). Tuy nhiên, một nghiên cứu tiếp theo cho thấy rằng việc bắt đầu sớm với liều thấp NO không ngăn cản sự phát triển tiếp theo của BPD (88). Một nghiên cứu khác đã chọn ngẫu nhiên 582 trẻ sơ sinh có cân nặng khi sinh dưới 1250 g cần hỗ trợ thở máy trong khoảng từ 7 đến 21 ngày tuổi. Trẻ sơ sinh được điều trị đã nhận được nồng độ oxit nitric giảm, bắt đầu từ 20 ppm trong 48 đến 96 giờ và các liều sau đó đã giảm xuống liều 10, 5 và 2 ppm trong khoảng thời gian hàng tuần, trong tối thiểu 24 ngày. KHÔNG làm tăng tỷ lệ sống sót mà không có BPD thêm 7% và cũng cải thiện chức năng phổi ngắn và dài hạn (89). Mặc dù các bằng chứng hiện tại không hỗ trợ việc sử dụng iNO thường quy để phòng ngừa bệnh BPD ở trẻ non tháng (90), một thử nghiệm lâm sàng về điều trị iNO không xâm lấn ở trẻ sinh non có nguy cơ mắc bệnh BPD và một thử nghiệm được thiết kế để nghiên cứu tác dụng của iNO trong trẻ sơ sinh mắc bệnh BPD tiến triển (sau tuần đầu tiên) đang diễn ra. Những nghiên cứu này sẽ tiếp tục thông tin về cuộc tranh luận.
Một điều cũng quan trọng là phải nhận ra rằng đối với trẻ sơ sinh dưới 34 tuần trong tình trạng giảm sản phổi và tăng áp phổi (ví dụ, trẻ sinh ra sau khi vỡ ối sớm và kéo dài), hít NO là một lựa chọn điều trị quan trọng. Trong số các chiến lược có sẵn để điều trị tăng áp phổi, iNO là phương pháp điều trị an toàn và hiệu quả nhất. Một số trẻ sơ sinh non tháng bị thiếu oxy nghiêm trọng liên quan đến tăng áp phổi và iNO là phương pháp điều trị tối ưu. Có thể là liều NO cao ở trẻ sinh non có cân nặng khi sinh < 750g trong những ngày đầu đời có thể liên quan đến tăng nguy cơ xuất huyết nội sọ (91). Tuy nhiên, sự an toàn của 5ppm trong tuần đầu tiên của cuộc đời đã được thiết lập.
Phương pháp điều trị dự phòng mới nổi
Một phương pháp đầy hứa hẹn để ngăn chặn sự phát triển của BPD là bổ sung dự phòng các enzyme chống oxy hóa tái tổ hợp của con người (92). Trong các nghiên cứu sơ bộ ở trẻ sinh non, việc sử dụng cả hai liều đơn và nhiều liều trong khí quản tái tổ hợp CuZn superoxide effutase (rh superoxide effutase) dường như làm giảm các thay đổi viêm và tổn thương phổi nghiêm trọng do thở oxy và thở máy. Trong một thử nghiệm ngẫu nhiên, có đối chứng giả dược, điều trị dự phòng, rhSOD trong khi sinh cho trẻ sinh non (cân nặng 600 -1200 g) có nguy cơ cao mắc bệnh BPD có liên quan đến các đợt bệnh hô hấp ít hơn (thở khò khè, hen suyễn, nhiễm trùng phổi) đủ để yêu cầu điều trị bằng thuốc giãn phế quản hoặc corticosteroid khi 1 tuổi điều chỉnh (93). Điều này cho thấy rằng rhSOD có thể ngăn ngừa tổn thương phổi lâu dài từ các loại oxy phản ứng ở trẻ sơ sinh có nguy cơ cao.
Mặc dù tiềm năng điều trị của các tế bào tiền thân (cả MSC và tế bào tiền thân angiogen) đã được chứng minh trên các mô hình động vật của BPD, đặc biệt là sau khi tiếp xúc với hyperoxia, cho đến nay chưa có thử nghiệm nào trên người. Dùng qua nội khí quản của MSC và tiêm tế bào angiogen có nguồn gốc từ tủy xương ngăn ngừa sự phát triển của bệnh BPD sau khi tiếp xúc với tăng oxy máu ở chuột sơ sinh (60,94). Vẫn còn những lo ngại về tác dụng lâu dài của các tế bào tiền thân mặc dù tiềm năng điều trị của chúng. Các nghiên cứu trong tương lai sẽ làm sáng tỏ nếu lợi ích điều trị an toàn tồn tại với các liệu pháp tế bào gốc.
Phần kết luận
Gần 40 năm sau mô tả ban đầu, BPD vẫn là một biến chứng lớn của sinh non và là thách thức cho tương lai. BPD đã phát triển được đặc trưng bởi sự ức chế phát triển phổi. Các chiến lược trong tương lai cải thiện kết quả lâu dài sẽ phụ thuộc vào sự tích hợp thành công của nghiên cứu cơ bản về cơ chế phát triển phổi cơ bản và đáp ứng với chấn thương, cũng như các nghiên cứu thử nghiệm các can thiệp mới để giảm sự xuất hiện và mức độ nghiêm trọng của di chứng tim phổi của BPD. Những cách mới để ngăn ngừa hoặc điều chỉnh BPD đang diễn ra, và hy vọng sẽ tiếp tục cải thiện kết quả lâu dài của trẻ sơ sinh non tháng.
Những điểm chính
BPD là một biến chứng chính của sinh non với nguyên nhân đa yếu tố.
Những thay đổi trong tín hiệu sFlt-1, VEGF, TGF-B1 và NF-B cũng như sự gia tăng các cytokine tiền viêm góp phần vào sinh bệnh học của BPD.
Các chiến lược điều trị cho BPD đã không chứng minh được việc giảm tỷ lệ mắc bệnh BPD.
Các chiến lược ngăn chặn sự phát triển của BPD là chìa khóa.
Tích hợp các nghiên cứu cơ bản và lâm sàng sẽ dẫn đến các liệu pháp mới có hiệu quả trong phòng ngừa và điều trị BPD.





