Khả năng nhận biết và tương tác với môi trường xung quanh (tức là, ý thức) là yếu tố tự nhiên mà có chứ không phải là kinh nghiệm sống, và mất khả năng này là một trong những dấu hiệu chính của một bệnh đe dọa đến tính mạng. Chương này mô tả các rối loạn chính của ý thức, nhấn mạnh vào mê sảng, hôn mê và chết não.
Tác giả: Bác sĩ Nguyễn Thành Luân – Khoa hồi sức tích cực bệnh viện Hoàn Mỹ Cửu Long.
Thay đổi ý thức
Ý thức
Ý thức có hai thành phần: sự tỉnh táo và nhận thức.
- Sự tỉnh táo là khả năng trải nghiệm môi trường xung quanh bạn.
- Nhận thức là khả năng hiểu mối quan hệ của bạn với môi trường xung quanh.
- Hai thành phần này được sử dụng để xác định các trạng thái ý thức thay đổi được mô tả tiếp theo.
Trạng thái thay đổi ý thức
Lo lắng và thờ ơ là những tình trạng mà sự sự tỉnh táo và nhận thức còn nguyên vẹn, nhưng có một sự thay đổi trong sự chú ý (tức là mức độ nhận thức).
Hội chứng khóa trong là một tình trạng trong đó sự tỉnh táo và nhận thức còn nguyên vẹn, nhưng hầu như không có sự đáp ứng của vận động. Tình trạng này được gây ra bởi tổn thương hai bên của các đường vận động ở phần bụng cầu não, làm gián đoạn tất cả các chuyển động tự ý ngoại trừ chuyển động mắt lên xuống và chớp mắt (1).
Mê sảng và mất trí nhớ là những tình trạng mà sự tỉnh táo còn nguyên vẹn, nhưng nhận thức bị thay đổi. Sự thay đổi trong nhận thức có thể dao động (như trong cơn mê sảng) hoặc tiến triển chậm (như mất trí nhớ).
Trạng thái thực vật là một tình trạng mà có một số mức độ của sự tỉnh táo (mắt có thể mở), nhưng không có nhận thức. Cử động tự phát và đáp ứng vận động với đau sâu có thể xảy ra, nhưng các chuyển động là không có mục đích. Sau một tháng, tình trạng này được gọi là trạng thái thực vật dai dẳng (2).
Hôn mê được đặc trưng bởi mất hoàn toàn sự tỉnh táo và nhận thức. Chuyển động tự phát và đáp ứng vận động với đau sâu có thể xảy ra, nhưng các chuyển động là không có mục đích.
Chết não tương tự như hôn mê ở chỗ hoàn toàn không có sự sự tỉnh táo và nhận thức, nhưng nó khác với hôn mê theo hai cách: (a) nó liên quan đến việc mất tất cả các chức năng của thân não, bao gồm hoạt động thần kinh sọ và hô hấp tự phát, và ( b) nó luôn luôn không thể đảo ngược.
Các nguyên nhân thay đổi ý thức
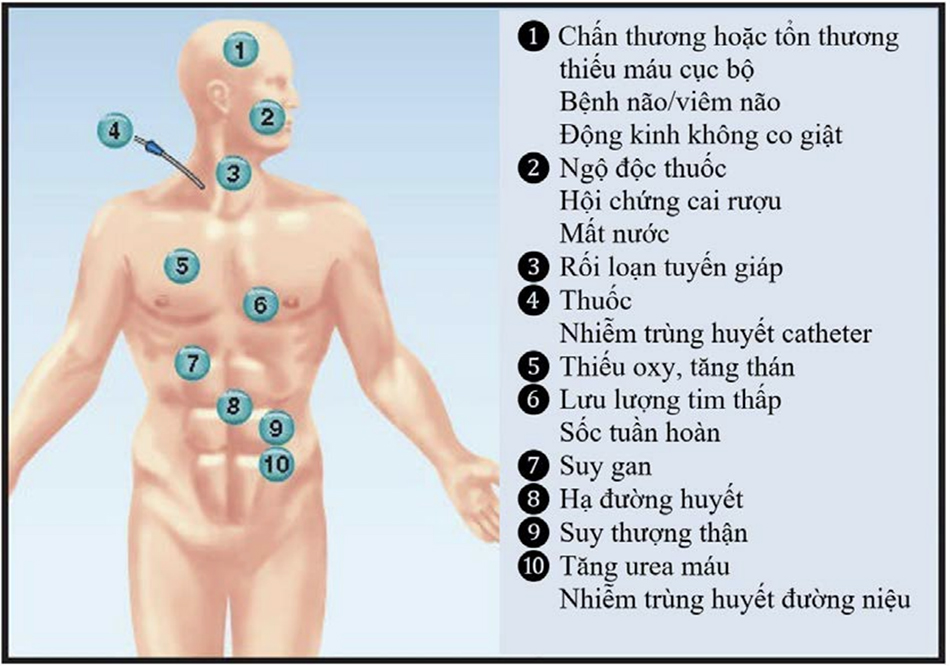
Các nguyên nhân có thể xác định của thay đổi ý thức được chỉ ra trong Hình 40.1. Trong một khảo sát tiến cứu về các biến chứng thần kinh ở ICU nội khoa (3), thì đột quỵ thiếu máu cục bộ là nguyên nhân thường gặp nhất của thay đổi ý thức khi nhập ICU, và bệnh não nhiễm trùng là nguyên nhân thường gặp nhất của thay đổi ý thức mắc phải trong ICU.
Mê sảng liên quan ICU
Mê sảng được báo cáo ở 16-89% bệnh nhân ICU (4), và có ảnh hưởng xấu đến kết cục (5).
Đặc điểm lâm sàng
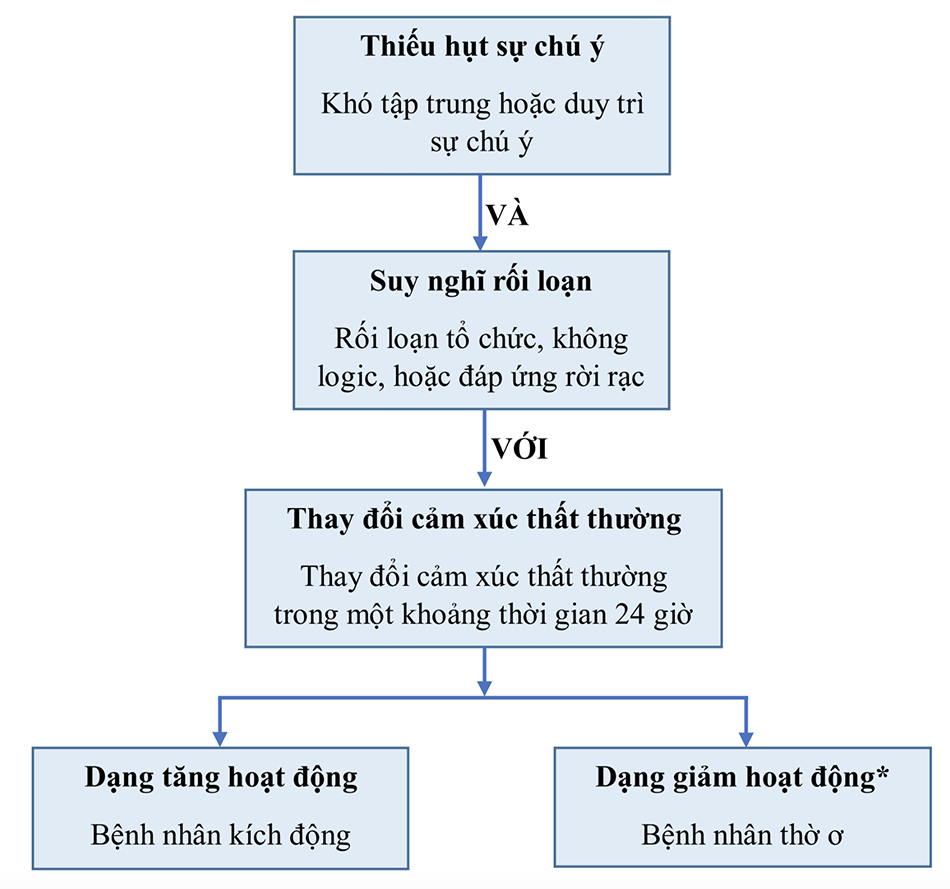
Các đặc điểm lâm sàng của mê sảng được tóm tắt trong Hình 40.2 (4.6).
- Mê sảng là một trạng thái lú lẫn cấp tính với sự thiếu hụt sự chú ý, suy nghĩ rối loạn, và một diễn biến thất thường (sự thất thường trong hành vi xảy ra trong khoảng thời gian 24 giờ).
- Hơn 40% bệnh nhân nhập viện bị mê sảng có triệu chứng loạn thần (ví dụ, ảo giác thị giác) (7); do đó, mê sảng thường được gọi bằng một tình trạng không thích hợp “loạn thần ICU”(8).
- Các kiểu phụ của mê sảng Các kiểu phụ sau đây của mê sảng được công nhận:
a. Mê sảng tăng động được đặc trưng bởi kích động không ngừng nghỉ. Loại mê sảng này thường gặp trong cai rượu, nhưng nó không thường gặp trong mê sảng mắc phải tại bệnh viện, chiếm 2% hoặc ít hơn các trường hợp (4).
b. Mê sảng giảm động được trưng bởi sự thờ ơ và buồn ngủ. Đây là dạng mê sảng mắc phải tại bệnh viện thường gặp nhất, chiếm 45-64% trường hợp (4). Loại mê sảng này thường bị bỏ qua, và có thể giải thích tại sao chẩn đoán mê sảng thường bị thiếu sót.
c. Mê sảng hỗn hợp liên quan đến các đợt xen kẽ giữa mê sảng tăng động và giảm động. Loại mê sảng này được báo cáo ở 6-55% bệnh nhân mê sảng mắc phải tại bệnh viện (4).
Mê sảng so với mất trí nhớ Mê sảng và mất trí nhớ là những rối loạn tâm thần riêng biệt thường bị nhầm lẫn bởi vì chúng có các đặc điểm lâm sàng chồng chéo nhau (nghĩa là, thiếu sự chú ý và suy nghĩ rối loạn). Các đặc điểm chính của mê sảng để phân biệt nó với mất trí nhớ là sự khởi phát đột ngột và diễn biến thất thường.
Điều kiện thuận lợi
Một số tình trạng thúc đẩy mê sảng ở bệnh nhân nằm viện, bao gồm: (a) tuổi cao, (b) thiếu ngủ, (c) đau không giảm, (d) nghỉ ngơi kéo dài trên giường bệnh, (e) phẫu thuật lớn, (f) bệnh não, và (g) thuốc (xem tiếp) (4,9,10).
Thuốc gây mê sảng: Các loại thuốc thúc đẩy mê sảng bao gồm:
- (a) thuốc kháng cholinergic,
- (b) thuốc dopaminergic,
- (c) thuốc seritonergic và
- (d) benzodiazepine (10,11).
- Các loại thuốc chủ yếu thúc đẩy mê sảng trong ICU là các benzodiazepine (11).
Biện pháp phòng ngừa
Các biện pháp được khuyến cáo để làm giảm nguy cơ mê sảng bao gồm:
- (a) điều trị đau đầy đủ,
- (b) duy trì chu kỳ thức-ngủ đều đặn,
- (c) tăng cường thời gian ra khỏi giường bệnh,
- (d) khuyến khích sự thăm nuôi của gia đình và
- (e) hạn chế sử dụng thuốc gây mê sảng, nếu có thể (4,11).
Dexmedetomidine An thần với dexmedetomidine có liên quan đến ít cơn mê sảng hơn so với các loại thuốc benzodiazepine (12,13). Thuốc này cung cấp một giải pháp thay thế cho benzodiazepine để an thần ở bệnh nhân ICU có nguy cơ mê sảng. Để biết thêm thông tin về dexmedetomidine, xem Chương 43, Phần II-D.
Chẩn đoán
Các hướng dẫn hiện hành về quản lý kích động và mê sảng (11) khuyến cáo kiểm tra định kỳ đối với mê sảng bằng các công cụ sàng lọc đã được chứng nhận như Confusion Assessment Method for the ICU (CAM-ICU) (6), hiện có sẵn tại www.icudelirium.org.
Quản lý
Không có thuốc điều trị được thừa nhận trên toàn cầu cho mê sảng mắc phải tại bệnh viện.
- Các hướng dẫn hiện tại về thuốc an thần ở bệnh nhân ICU (11) khuyên dùng dexmedetomidine hơn benzodiazepine để điều trị mê sảng không liên quan đến cai nghiện rượu hoặc cai nghiện benzodiazepine. Tuy nhiên, không có bằng chứng để hỗ trợ cho khuyến cáo này (11).
- Haloperidol là một loại thuốc phổ biến để điều trị mê sảng, mặc dù không có bằng chứng ủng hộ hoặc chống lại việc sử dụng nó (11). (Để biết thông tin về sử dụng haloperidol, xem Chương 43, Phần II-E.)
- Có một số bằng chứng về sự thành công trong điều trị mê sảng bằng thuốc “chống loạn thần không điển hình” (ví dụ, quietiapine, olanzapine, risperidone) (14), mà không có nguy cơ tác dụng phụ ngoại tháp liên quan đến haloperidol. Tuy nhiên, không có đủ bằng chứng để đảm bảo khuyến cáo về các loại thuốc này (11).
Mê sảng do cai rượu
Mê sảng do cai rượu được đặc trưng bởi tăng hoạt động vận động và tăng hoạt động trên điện não đồ (EEG), trong khi mê sảng mắc phải tại bệnh viện được đặc trưng bởi giảm hoạt động vận động và làm chậm hoạt động trên điện não đồ (4).
Đặc điểm lâm sàng
Các đặc điểm lâm sàng của cai rượu được tóm tắt trong Bảng 44.1.
- Sảng rượu Khoảng 5% bệnh nhân trải qua cai rượu sẽ bị sảng rượu (DTs), được đặc trưng bởi mê sảng kích động, ảo giác, sốt, nhịp tim nhanh, tăng huyết áp, mất nước, và cũng có thể bao gồm co giật và nhiều bất thường điện giải (đặc biệt là hạ kali máu và hạ magne máu) (15). Khởi phát thường muộn (2 ngày sau lần uống rượu cuối cùng) và hội chứng có thể kéo dài trong 5 ngày hoặc lâu hơn. Tỷ lệ tử vong được báo cáo là 5-15% (15).
- Bệnh não Wernicke Bệnh nhân nghiện rượu được nhập viện với dự trữ thiamine ở mức tối thiểu và được truyền tĩnh mạch glucose có thể phát triển bệnh não Wernicke cấp do thiếu thiamine (18). Những thay đổi cấp tính về tình trạng tâm thần có thể xảy ra vài ngày sau khi nhập viện, và có thể bị nhầm lẫn với mê sảng do cai rượu. Sự hiện diện của rung giật nhãn cầu hoặc liệt liếc ngang sẽ giúp xác định bệnh não Wernicke. (Để biết thêm về sự thiếu hụt thiamine, xem Chương 36, Phần III- A.)
| Bảng 40.1 Các Đặc điểm lâm sàng của Hội chứng Cai rượu | ||
| Đặc điểm | Khởi phát sau lần uống cuối cùng | Kéo dài |
Dấu hiệu sớm:
|
6-8 giờ | 1-2 ngày |
| Co giật toàn thể | 6-48 giờ | 2-3 ngày |
Ảo giác:
|
12-48 giờ | 1-2 ngày |
| Sảng rượu (1) | 48-96 giờ | 1-5 ngày |
| (1) Mê sảng kích động, ảo giác, sốt, nhịp tim nhanh, tăng huyết áp, co giật, mất nước, và rối loạn nhiều chất điện giải. Vẽ lại từ Tài liệu tham khảo 15. | ||
Điều trị
- Tác dụng ức chế hệ thần kinh trung ương của ethanol là kết quả, một phần, của việc kích thích thụ thể gamma-aminobutyric (GABA), là một con đường ức chế chính trong não. Đây cũng là cơ chế tác dụng của các benzodiazepine, và đây là cơ sở cho việc sử dụng benzodiazepine như là thuốc được lựa chọn đối với mê sảng và kích động trong cai rượu (17). Một lợi ích thêm nữa của benzodiazepine là bảo vệ chống lại các cơn động kinh toàn thể.
- PHÁC ĐỒ: Đối với những bệnh nhân cần chăm sóc trong ICU, lorazepam tĩnh mạch là một lựa chọn thích hợp để quản lý DTs (17). Để kiểm soát ban đầu, cho 2-4 mg tĩnh mạch mỗi 5-10 phút cho đến khi bệnh nhân bình tĩnh. Sau đó, dùng lorazepam tĩnh mạch mỗi 1-2 giờ (hoặc truyền liên tục) ở liều duy trì sự bình tĩnh. (Có thể cần đặt ống nội khí quản và thở máy.)
-
-
- Điều quan trọng là phải giảm benzodiazepine càng sớm càng tốt bởi vì chúng tích tụ và có thể tạo ra tình trạng an thần kéo dài và kéo dài thời gian nằm ICU.
- Một lo ngại khác với việc truyền tĩnh mạch lorazepam kéo dài là gây ngộ độc propylene glycol (xem Chương 24, Mục I-A-5).
-
-
- Để biết thêm thông tin về các benzodiazepine, xem Chương 43, Phần II-B.
- Do nguy cơ thiếu hụt thiamine đã đề cập, thiamine được dùng thường quy cho bệnh nhân DTs. Liều thường dùng là 50-100 mg mỗi ngày, có thể tiêm tĩnh mạch mà không gây hại.
Hôn mê
Hôn mê dai dẳng là một trong những tình trạng thách thức nhất trong thực hành săn sóc đặc biệt, và đòi hỏi không chỉ chú ý đến bệnh nhân mà còn cả gia đình bệnh nhân và cả những người thân thiết khác.
Bệnh nguyên
Hôn mê có thể là kết quả của bất kỳ tình trạng nào sau đây:
- Tổn thương não do thiếu máu cục bộ, lan tỏa.
- Bệnh não do ngộ độc hoặc chuyển hóa (bao gồm quá liều thuốc).
- Chèn ép thân não do một khối tổn thương trên lều với thoát vị xuyên liều, hoặc từ một khối tổn thương ở hố sau.
- Trạng thái động kinh không co giật.
- Hôn mê rõ ràng (nghĩa là, hội chứng khóa trong, phản ứng hysteria (chứng cuồng loạn)).
- Lưu ý: đột quỵ do thiếu máu cục bộ không dẫn đến hôn mê trừ khi có một hiệu ứng khối choáng chổ một bên gây đẩy lệch đường giữa và chèn ép bán cầu não đối bên, hoặc tổn thương vùng thân não.
Đánh giá tại giường
Đánh giá tình trạng hôn mê tại giường nên bao gồm đánh giá các phản xạ thần kinh sọ, chuyển động mắt và cơ thể tự phát và phản xạ vận động (18,19). Các yếu tố sau đây của đánh giá đáng được đề cập:
Đáp ứng vận động
a. Giật cơ tự phát (chuyển động không đều, giật) có thể là một dấu hiệu không đặc hiệu của rối loạn chức năng não lan tỏa, hoặc có thể đại diện cho hoạt động động kinh (cơn động kinh giật cơ), trong khi tứ chi mềm có thể chỉ ra tổn thương não lan tỏa hoặc tổn thương đến thân não.
b. Cử động giật cơ được phát hiện ra khi gấp bàn tay hoặc bàn chân (dấu run vẫy) là một dấu hiệu của bệnh não chuyển hóa lan tỏa (20).
c. Với tổn thương vùng đồi thị, các kích thích đau gây ra co chi trên, được gọi là tư thế mất vỏ.
d. Với tổn thương não giữa và cầu não cao, cánh tay và chân duỗi và sấp khi đáp ứng đau; điều này được gọi là tư thế mất não.
e. Cuối cùng, với tổn thương liên quan đến thân não thấp, các chi vẫn mềm trong khi kích thích đau.
Khám đồng tử

Các tình trạng ảnh hưởng đến kích thước đồng tử và độ đáp ứng ánh sáng được thể hiện trong Bảng 40.2 (18,19,21). Các phát hiện về đồng tử có thể được tóm tắt như sau:
- a. Đồng tử dãn và phản ứng ánh sáng có thể là do thuốc (ví dụ, thuốc kháng cholinergic) hoặc cơn động kinh không co giật, trong khi dãn đồng tử và không phản ứng ánh sáng là một dấu hiệu của tổn thương não lan tỏa, tăng áp lực nội sọ hoặc chèn ép thân não do khối trong sọ to ra.
- b. Đồng tử một bên, dãn và cố định có thể là do chấn thương mắt, phẫu thuật mắt gần đây, hoặc rối loạn chức năng dây thần kinh sọ thứ ba do một khối nội sọ to ra.
- c. Đồng tử có kích thước trung bình, phản ứng ánh sáng, có thể là do một bệnh não chuyển hóa, quá liều thuốc an thần, hoặc các loại thuốc ngăn chặn thần kinh cơ, trong khi đồng tử có kích thước trung bình, không phản ứng ánh sáng có thể gặp trong suy gan cấp, bệnh não sau thiếu oxy, hoặc chết não.
- d. Đồng tử nhỏ, phản ứng ánh sáng có thể là do bệnh não chuyển hóa, trong khi đồng tử co nhỏ có thể do quá liều thuốc phiện (đồng tử có phản ứng) hoặc tổn thương ở cầu não (đồng tử không phản ứng).
Chuyển động mắt
Chuyển động mắt tự phát là một dấu hiệu không đặc hiệu ở bệnh nhân hôn mê, nhưng hay liếc về một hướng cố định là gợi ý nhiều đến một tổn thương dạng khối hoặc hoạt động cơn động kinh.
Phản xạ mắt
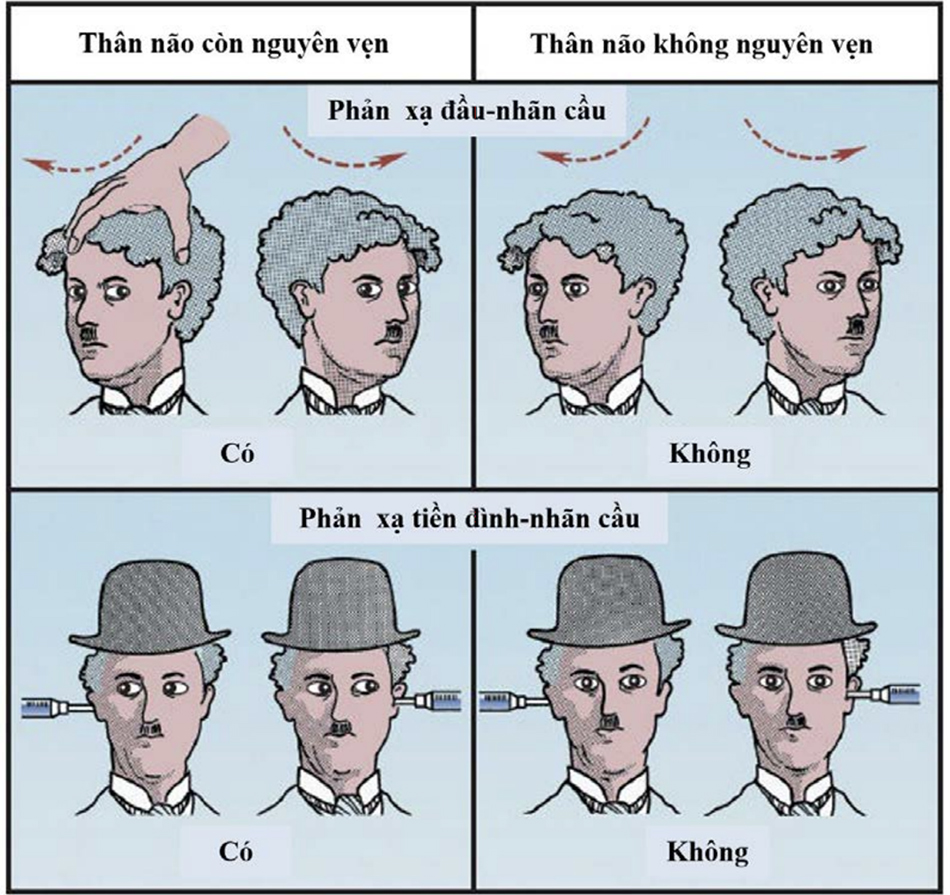
Các phản xạ mắt được sử dụng để đánh giá tính toàn vẹn chức năng của thân não thấp (19). Những phản xạ này được minh họa trong Hình 40.3.
- a. PHẢN XẠ ĐẦU-NHÃN CẦU: Phản xạ mắt búp bê được đánh giá bằng cách xoay nhanh đầu từ bên này sang bên kia. Khi bán cầu não bị ảnh hưởng nhưng thân não thấp vẫn còn nguyên vẹn, mắt sẽ xoay ngược hướng với quay đầu và duy trì tầm nhìn về phía trước. Khi thân não thấp bị tổn thương, mắt sẽ xoay theo hướng quay đầu.
- b. PHẢN XẠ TIỀN ĐÌNH-NHÃN CẦU: Phản xạ tiền đình-nhãn cầu được thực hiện bằng cách tiêm 50 ml nước muối lạnh vào ống tai ngoài của mỗi tai. Khi chức năng thân não còn nguyên vẹn, cả hai mắt sẽ liếc chậm về phía tai bị làm ướt. Chuyển động mắt liên hợp này bị mất khi thân não thấp bị tổn thương.
Điểm hôn mê Glasgow
1. Thang đo hôn mê Glasgow trong Bảng 40.3 được giới thiệu để đánh giá mức độ nghiêm trọng của chấn thương sọ não (22), nhưng nó cũng đã được áp dụng để sử dụng trong các tổn thương sọ não không chấn thương.
2. Thang đo bao gồm ba thành phần: 1) mở mắt, 2) giao tiếp bằng lời nói và 3) đáp ứng vận động với lời nói hoặc kích thích đau. Điểm hôn mê Glasgow (GCS) là tổng của ba thành phần; điểm tối thiểu 3 cho thấy hoàn toàn không có nhận thức và đáp ứng, và điểm tối đa 15 là bình thường.
3. Hôn mê được xác định là GCS ≤8.
4. Một trong những thiếu sót lớn của Thang điểm Glasgow là không có khả năng đánh giá đáp ứng lời nói ở bệnh nhân đặt nội khí quản. Những bệnh nhân này được quy định một “điểm giả” của lời nói là 1 (GCS tối đa là 11). GCS cũng không đáng tin cậy ở những bệnh nhân bị liệt, an thần nặng hoặc tụt huyết áp.
Điện não đồ
1. Trạng thái động kinh không co giật có thể là một nguyên nhân bị che lấp của hôn mê; ví dụ, trong một nghiên cứu, nó chiếm 8% các trường hợp hôn mê (23).
2. Điện não đồ được khuyến cáo cho tình trạng hôn mê không rõ nguyên nhân hoặc kéo dài.
| Bảng 40.3 Thang đo hôn mê Glasgow và điểm số | |
| Điểm | |
Mở mắt:
|
|
Giao tiếp lời nói:
|
|
Đáp ứng vận động:
|
|
| Điểm hôn mê Glasgow (tổng 3 thang đo) (1) | |
| (1) Điểm thấp nhất là 3 điểm, và cao nhất là 15 điểm. Khi có ống nội khí quản, điểm cao nhất là 11 điểm. | |
Chết não
The Uniform Determination of Death Act tuyên bố rằng “Một cá thể được xác nhận một trong hai tình trạng, hoặc 1) sự chấm dứt không thể đảo ngược của các chức năng tuần hoàn và hô hấp, hoặc 2) sự chấm dứt không thể đảo ngược của tất cả các chức năng của toàn bộ não, bao gồm thân não, là đã chết. (24). Tình trạng thứ hai là mục đích của việc xác định chết não được mô tả ở đây.
Xác định chết não
Một liệt kê về chẩn đoán chết não ở người trưởng thành được thể hiện trong Bảng 40.4 (25). Vẫn còn thiếu đồng thuận về những khía cạnh nhỏ của việc xác định chết não, nhưng những thành phần thiết yếu được liệt kê ở đây:
| Bảng 40.4 Bảng kiểm tra để Xác định chết não ở người lớn | |
| Hướng dẫn: Bệnh nhân có thể được tuyên bố là chết theo pháp luật nếu các Bước 1-4 được xác nhận. | Tic ✓ nếu Mục được xác nhận |
Bước 1: Điều kiện tiên quyết để kiểm tra: Tất cả các điều kiện sau đây phải được thỏa mãn trước khi bắt đầu đánh giá chết não.
|
|
| Bước 2: Xác định nguyên nhân của hôn mê: Nguyên nhân của hôn mê đã được biết, và đủ để giải thích cho chết não không thể đảo ngược. | |
| Bước 3: Không có chức năng của thân não và vỏ não:
A. Bệnh nhân hôn mê. B. Không nhăn mặt trong đáp ứng kích thích đau. C. Không có các phản xạ thân não sau đây:
|
|
| Bước 4: Không có gắng sức thở tự phát: Không có gắng sức thở tự phát khi PCO2 động mạch cao hơn 20 mm Hg so với mức nền của bệnh nhân. | |
| Trích the Clinical Practice Guidelines trong Tài liệu tham khảo 25. | |
1. Hôn mê không hồi phục.
2. Không có phản xạ thân não.
3. Không có hô hấp tự phát trong một thử thách CO2.
4. Việc xác định chết não phải được tiến hành theo các điều kiện sau:
a. Huyết áp tâm thu ≥100 mm Hg và nhiệt độ cơ thể >36°C.
b. Không có thuốc an thần hoặc thuốc ức chế thần kinh cơ.
c. Đường huyết và chức năng tuyến giáp bình thường.
5. Một lần kiểm tra thần kinh là đủ để chẩn đoán chết não ở hầu hết các tiểu bang Hoa Kỳ, nhưng một số tiểu bang yêu cầu 2 lần kiểm tra.
Nghiệm pháp ngưng thở
Chết não được xác nhận bằng việc không có các nỗ lực thở tự phát khi đối mặt với sự gia tăng cấp tính của PCO2 động mạch (PaCO2). Điều này được đánh giá bằng nghiệm pháp ngưng thở, bao gồm việc đưa bệnh nhân ra khỏi máy thở và quan sát các nỗ lực thở tự phát khi PaCO2 tăng. Các bước sau đây có liên quan đến nghiệm pháp ngưng thở (25):
- Trước nghiệm pháp, bệnh nhân được thở O2 100% trong ít nhất 10 phút. Tần số thở trên máy thở giảm xuống còn 10 nhịp thở/phút và mức PEEP giảm xuống còn 5 cm H2O. Nếu độ bão hòa O2 đo bằng máy đo oxy mạch đập (SpO2) >95%, một khí máu động mạch được lấy để thiết lập mức nền PaCO2.
- Sau đó, bệnh nhân được tách ra khỏi máy thở, và O2 100% được đưa vào đường thở qua một ống thông đưa sâu vào ống nội khí quản (oxy hóa khi ngưng thở).
- Mục đích của nghiệm pháp ngưng thở là cho phép PaCO2 tăng 20 mm Hg trên mức nền. PaCO2 tăng khoảng 3 mm Hg mỗi phút khi ngưng thở ở nhiệt độ cơ thể bình thường (26), do đó, thời gian nghiệm pháp 6-7 phút là đủ để đạt được mục tiêu PaCO2. Lấy lại một khí máu động mạch vào cuối nghiệm pháp, và bệnh nhân được đặt trở lại với máy thở.
- Nếu ngưng thở vẫn tồn tại mặc dù tăng PaCO2 ≥20 mm Hg, chẩn đoán chết não được xác nhận.
- Hủy bỏ nghiệm pháp khi một trong những điều sau đây xảy ra (25):
-
- a. Huyết áp tâm thu xuống dưới 90 mm Hg.
- b. SpO2 giảm xuống dưới 85% trong hơn 30 giây.
-
Cận lâm sàng phụ trợ
1. Các cận lâm sàng phụ trợ để chẩn đoán chết não bao gồm chụp cộng hưởng từ và chụp động mạch (MRI và MRA), chụp cắt lớp vi tính động mạch (CTA) và kiểm tra cảm giác xúc giác.
2. Các kiểm tra này thường được sử dụng khi khám thần kinh là không rõ ràng, hoặc nghiệm pháp ngưng thở không thể được thực hiện một cách an toàn.
3. Tuy nhiên, không đủ bằng chứng để xác định xét nghiệm phụ trợ có thể xác định chết não đáng tin cậy (25) hay không và các hướng dẫn hiện hành về xác định chết não cảnh báo bác sỹ thận trọng sử dụng cận lâm sàng này (25).
Dấu hiệu Lazarus
1. Bệnh nhân chết não có thể biểu hiện các cử động ngắn, tự phát của đầu, thân hoặc các chi trên (Dấu hiệu Lazarus), đặc biệt là sau khi họ được lấy ra khỏi máy thở (27).
2. Những chuyển động này là kết quả của việc dẫn điện của tế bào thần kinh ở tủy sống cổ, có thể là để đáp ứng với thiếu oxy máu.
Người hiến nội tạng tiềm năng
Hiến tặng nội tạng là một phần không thể thiếu trong quá trình xác định chết não. Chủ đề này nằm ngoài phạm vi của văn bản này, nhưng các hướng dẫn được công bố gần đây về lấy nội tạng trong ICU (28) được đưa vào danh mục tài liệu ở cuối chương.
Tài liệu tham khảo
1. Leon-Carrion J, van Eeckhout P, Dominguez-Morales Mdel R. The locked-in syndrome: a syndrome looking for a therapy. Brain Inj 2002; 16:555–569.
2. The Multi-Society Task Force on PVS. Medical aspects of the persistent vegetative state (Part 1). N EnglJ Med 1994; 330:1499–1508.
3. Bleck TP, Smith MC, Pierre-Louis SJ, et al. Neurologic complications of critical medical illnesses. Crit Care Med 1993; 21:98–103.
4. Zaal IJ, Slooter AJC. Delirium in critically ill patients: epidemiology, pathophysiology, diagnosis and management. Drugs 2012; 72:1457–1471.
5. Ely EW, Shintani A, Truman B, et al. Delirium as a predictor of mortality in mechanically ventilated patients in the intensive care unit. JAMA 2004; 291:1753–1762.
6. Ely EW, Margolin R, Francis J, et al. Evaluation of delirium in critically ill patients: validation of the Confusion Assessment Method for the Intensive Care Unit (CAM-ICU). Crit Care Med 2001; 29:1370–1379.
7. Webster R, Holroyd S. Prevalence of psychotic symptoms in delirium. Psychosomatics 2000; 41:519–522.
8. McGuire BE, Basten CJ, Ryan CJ, et al. Intensive care unit syndrome: a dangerous misnomer. Arch InternMed 2000; 160:906–909.
9. Inouye SK. Deliriumin older persons. N Engl J Med 2006; 354:1157–1165.
10. Reade MC, Finfer S. Sedation and delirium in the intensive care unit. N Engl J Med 2014; 370:444– 454.
11. Barr J, Fraser GL, Puntillo K, et al. Clinical practice guidelines for the management of pain, agitation, and deliriumin adult patients in the intensive care unit. Crit Care Med 2013; 41:263–306.
12. Pandharipande PP, Pun BT, Herr DL, et al. Effect of sedation with dexmedetomidine vs lorazepam on acute brain dysfunction on mechanically ventilated patients: the MENDS randomized controlled trial. JAMA 2007; 298:2644–2653.
13. Riker RR, Shehabi Y, Bokesch PM, et al. Dexmedetomidine vs midazolam for sedation of critically ill patients: a randomized trial. JAMA 2009; 301:489–499.
14. Gilchrist NA, Asoh I, Greenberg B. Atypical antipsychotics for the treatment of ICU delirium. J Intensive Care Med 2012; 27:354–361.
15. Tetrault JM, O’Connor PG. Substance abuse and withdrawal in the critical care setting. Crit Care Clin 2008; 24:767–788.
16. Attard O, Dietermann JL, Diemunsch P, et al. Wernicke enceph-alopathy: a complication of parenteral nutrition diagnosed by magnetic resonance imaging. Anesthesiology 2006; 105:847–848.
17. Mayo-Smith MF, Beecher LH, Fischer TL, et al. Management of alcohol withdrawal delirium: an evidence-based practice guideline. Arch Intern Med 2004; 164:1405–1412.
18. Stevens RD, Bhardwaj A. Approach to the comatose patient. Crit Care Med 2006; 34:31–41.
19. Bateman DE. Neurological assessment of coma. J Neurol Neurosurg Psychiatry 2001; 71:i13–17.
20. Kunze K. Metabolic encephalopathies. J Neurol 2002; 249:1150–1159.
21. Wijdicks EFM. Neurologic manifestations of pharmacologic agents commonly used in the intensive care unit. In: Neurology of critical illness. Philadelphia: F.A. Davis, Co., 1995:3–17.
22. Teasdale G, Jennett B. Assessment of coma and impaired consciousness. A practical scale. Lancet 1974; 2:81–84.
23. Towne AR, Waterhouse EJ, Boggs JG, et al. Prevalence of nonconvulsive status epilepticus in comatose patients. Neurology 2000; 54:340–345.
24. National Conference of Commissioners on Uniform State Laws. Uniform Determination of Death Act. Approved July, 1980.
25. Wijdicks EFM, Varelas PNV, Gronseth GS, Greer DM. Evidence-based guideline update: determining brain-death in adults. Report of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology 2010; 74:1911–1918.
26. Dominguez-Roldan JM, Barrera-Chacon JM, Murillo-Cabezas F, et al. Clinical factors influencing the increment of blood carbon dioxide during the apnea test for the diagnosis of brain death. Transplant Proc 1999; 31:2599–2600.
27. Ropper AH. Unusual spontaneous movements in brain-dead patients. Neurology 1984; 34:1089– 1092.
28. Kotloff RM, Blosser S, Fulda GJ, et al. Management of the potential organ donor in the ICU: Society of Critical Care Medi-cine/American College of Chest Physicians/Association of Organ Procurement Organizations Consensus Statement. Crit Care Med 2015; 43:1291–1325.



![[Cảnh báo] Để cải thiện thiếu máu não nên ăn gì? Kiêng ăn gì? Thiếu máu não nên ăn gì?](https://www.healcentral.org/wp-content/uploads/2020/11/thieu_mau_nao_nen_an_gi1-218x150.jpg)


Tôi có thể mua thuốc này ơ đâu>?