Bài viết Thông khí cơ học trong quá trình oxy hoá màng ngoài cơ thể ở bệnh nhân suy hô hấp cấp tính được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Mechanical Ventilation during Extracorporeal Membrane Oxygenation in Patients with Acute Severe Respiratory Failure
Tóm tắt
Thông thường, một số lượng đáng kể các bệnh nhân suy hô hấp cấp cần thông khí cơ học (MV) để ngăn ngừa thiếu oxy máu và tăng CO2 máu. Tuy nhiên, thở máy có thể gây tổn thương phổi, đẩy nhanh sự tiến triển của bệnh. Oxy hóa màng ngoài cơ thể (ECMO) cung cấp một giải pháp thay thế cứu hộ cho các bệnh nhân bị suy hô hấp nặng mà thông khí cơ học thông thường không duy trì được sự trao đổi khí đầy đủ. Sinh lý học đằng sau ECMO và sự tương tác của nó với MV đã được xem xét. Tiếp theo, chúng tôi thảo luận về thời gian bắt đầu ECMO dựa trên những rủi ro và lợi ích của ECMO. Trong quá trình chạy ECMO, chiến lược thông khí bảo vệ có thể được sử dụng mà không phải lo lắng về tình trạng thiếu oxy máu trầm trọng và ứ carbon dioxide. Có rất nhiều bằng chứng cho thấy rằng thông khí bảo vệ có thể tích khí lưu thông thấp, áp lực dương cuối kỳ thở ra cao, và tư thế nằm sấp có thể mang lại lợi ích cho kết cục tử vong. Gần đây hơn, ngày càng phổ biến về việc sử dụng hô hấp tự nhiên và cho các bệnh nhân đang trải qua ECMO được thức tỉnh, được cho là có lợi trong việc phục hồi chức năng.
Giới thiệu
Oxy hóa màng ngoài cơ thể (ECMO) là một kỹ thuật quan trọng để điều trị suy hô hấp nghiêm trọng, tạo cơ hội phục hồi phổi hoặc cấy ghép [1, 2]. Hill và các đồng nghiệp đã mô tả lần đầu tiên ECMO hỗ trợ cho các trường hợp suy hô hấp nặng cách đây bốn thập kỷ [3]. Kể từ đó, một số lượng lớn các nghiên cứu quan sát và các thử nghiệm ngẫu nhiên được thực hiện [4, 5]. Trong thực tiễn chung, ECMO được chỉ định khi thông khí cơ học thông thường không cải thiện được oxy hóa động mạch và/hoặc loại bỏ carbon dioxide [6]. Một dấu hiệu khác là suy tuần hoàn và/hoặc suy tim. Tuy nhiên, ECMO chưa được thiết lập (ví dụ như trong khuôn khổ y học bằng chứng) về hiệu quả của nó trong điều trị suy hô hấp nghiêm trọng, đặc biệt trong một số trường hợp đặc biệt như bệnh nhân suy giảm miễn dịch [7]. Mặc dù ECMO không chắc chắn hiệu quả hơn so với thông khí cơ học đối với kết cục tử vong, ECMO vẫn còn được sử dụng rộng rãi cho những bệnh nhân bị suy hô hấp.
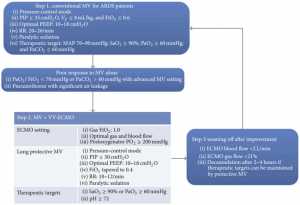
Lưu ý rằng oxy hóa màng ngoài cơ thể được cung cấp sau khi thất bại với thông khí thông thường. Bước 1 là việc sử dụng MV thông thường cho bệnh nhân ARDS. Thông thường sử dụng thông khí bảo vệ. Nếu bệnh nhân đáp ứng kém với thiết lập MV ban đầu, chiến lược sẽ bắt đầu VV-ECMO với mục tiêu điều trị để duy trì SaO2 và pH huyết thanh. Ngưng ECMO được xem xét khi lưu lượng máu và lưu lượng khí giảm lần lượt là 2 L/phút và 21%. Hình này được trích từ Reference [9]. MV: thông khí cơ học; VV-ECMO: oxy hóa màng tế bào tĩnh mạch – tĩnh mạch; MAP: Áp lực đường thở trung bình; PEEP: áp lực dương cuối kỳ thở ra; RR: tần số hô hấp.
Vì ECMO rất khó khăn về mặt kỹ thuật, và có những biến chứng nặng nề, nó không được coi là phương pháp điều trị đầu tiên cho bệnh nhân suy hô hấp [8]. Một phác đồ điều trị điển hình của hội chứng suy hô hấp cấp tính nghiêm trọng (ARDS) được biểu diễn trong Hình 1 [9]. Phương pháp điều trị đầu tiên (bước 1) đối với ARDS nặng là thông khí cơ học với nhiều phương thức [10-13]. Thông thường sử dụng thông khí bảo vệ. Nếu bệnh nhân đáp ứng kém với thiết lập MV ban đầu, chiến lược sẽ bắt đầu VV-ECMO với mục tiêu điều trị để duy trì SaO2 và pH huyết thanh. Ngưng ECMO được xem xét khi lượng máu và lưu lượng khí giảm xuống còn 2 L/phút và 21% [9]. Trong khi chạy ECMO, thông khí cơ học vẫn đang được sử dụng. Do đó, hỗ trợ hô hấp của những bệnh nhân này bao gồm phổi tự nhiên và phổi nhân tạo. Cài đặt thông khí cơ học ở bệnh nhân đang ECMO là một lĩnh vực hoạt động nghiên cứu. Có tranh cãi về mức độ tối ưu của hỗ trợ thông khí cơ học. Trong khi thông khí siêu an toàn cung cấp đủ để cho phổi nghỉ ngơi, thì việc huy động phổi có thể làm tăng khả năng hồi phục phổi [14]. Trong bài tổng quan này chúng tôi tóm tắt bằng chứng hiện tại về thông khí cơ học trong ECMO.
Sinh lý học ECMO
Vì đánh giá này tập trung chủ yếu vào thở máy trong ECMO, trước tiên chúng ta cần phải hiểu một số thay đổi về sinh lý trong ECMO. Oxy hóa màng ngoài cơ thể TM-TM (VV-ECMO) thường được sử dụng để điều trị bệnh nhân suy hô hấp và ổn định huyết động. Máu tĩnh mạch có độ bão hòa oxy thấp (SvO2) thường được rút ra từ TM chủ trên, TM chủ dưới, và/hoặc tĩnh mạch lớn như tĩnh mạch đùi hoặc tĩnh mạch dưới đòn. Nó đi qua màng oxy hóa – oxygenator [15] và sau đó quay trở lại bệnh nhân trong hoặc gần tâm nhĩ phải [16]. Máu trở lại với hàm lượng oxy cao được trộn lẫn với máu tĩnh mạch hệ thống và đi vào tim phải. Các máu tĩnh mạch hỗn hợp được oxy hóa thêm trong phổi tự nhiên. Tuy nhiên, do thiết lập thông khí cơ học thấp, việc oxy hóa đó luôn luôn không đáng kể. Thông khí cơ học trong vấn đề này để giữ cho phổi mở hơn là để cung cấp oxy [16]. Tuy nhiên, chức năng phổi tự nhiên không phải lúc nào cũng không đáng kể; điều này có thể xảy ra đối với việc loại bỏ CO2 ở phổi tự nhiên. Trung khu hô hấp không thể được kiểm soát hoàn toàn bằng cách loại bỏ CO2 ngoài cơ thể, đặc biệt là ở những bệnh nhân thiếu oxy máu cấp tính.
Vì ECMO có thể cung cấp oxy và loại bỏ khí cácbon điôxit, nên có thể kiểm soát được trung tâm kiểm soát hô hấp và nỗ lực gắng sức trigger của bệnh nhân. Một vài nghiên cứu trên động vật cho thấy ECMO đã loại bỏ carbon dioxide có thể gây ngưng thở [17, 18]. Trong nghiên cứu ở con người, khi lưu lượng khí (ví dụ, kiểm soát CO2) giảm từ 100% xuống 0%, áp lực tạo ra trong 100 ms đầu tiên của thì hít vào đối với thủ thuật bịt đường hô hấp tăng từ 0.9 ± 0.5 đến 2.8 ± 2.7 cmH2O (p < 0.001); áp lực cơ hít vào tối đa tăng từ 4.5 ± 3.1 đến 8.5 ± 6.3 cmH2O. Các tác giả kết luận rằng việc loại bỏ carbon dioxide có tác động đáng kể đến nỗ lực hít thở tự nhiên [19].
Một tính năng quan trọng của VV-ECMO là tác động huyết động nhẹ lên tuần hoàn. Điều này đặc biệt quan trọng đối với những bệnh nhân huyết động không ổn định với suy hô hấp cấp (ARF). Trong mô hình động vật, Shen và các đồng nghiệp đã phát hiện ra rằng mặc dù có sự thay đổi nhẹ về siêu cấu trúc và chức năng của tế bào cơ tim và ty thể, nhưng huyết động học toàn phần vẫn ổn định [20]. Ngoài ra, có bằng chứng cho thấy việc cài đặt VV-ECMO làm giảm nhịp tim, nhưng áp lực động mạch trung bình không bị ảnh hưởng đáng kể [21]. Với các tính năng huyết động thuận lợi của VV-ECMO, nó có thể được sử dụng cho bệnh nhân có bệnh nhân huyết động không ổn định. Tuy nhiên, nếu một bệnh nhân cho thấy ARF kết hợp với sốc kháng trị, ECMO của TM-ĐM (VA-ECMO) nên được khuyến cáo sử dụng.
Thời điểm bắt đầu ECMO: Chỉ định dựa vào các thông số thở máy
Vì thông khí cơ học thường đi trước ECMO và thông số thông khí cơ học cung cấp thông tin quan trọng cho việc bắt đầu ECMO, trong phần này, chúng ta sẽ thảo luận khi nào ECMO bắt đầu ở bệnh nhân suy hô hấp nặng.
Nguyên tắc để bắt đầu ECMO là khi thông khí cơ học thông thường không thể cung cấp đủ oxy hóa và/hoặc giảm điôxít cacbon hoặc thiết lập thông khí cơ học quá cao có thể gây ra tổn thương phổi đáng kể. Một điều kiện nữa là khoảng thời gian thở máy cơ học không quá dài để bệnh lý cơ bản có thể đảo ngược được. Thời gian ECMO thường dựa trên mức độ nghiêm trọng của ARDS, như giảm oxygen máu trầm trọng mặc dù PEEP cao (PaO2/FiO2 < 80 mmHg) và tăng CO2 máu không bù (pH < 7.2) [22]. Có bằng chứng cho thấy việc bắt đầu sớm ECMO (1.9 ± 1.4 ngày sau khi ARDS nặng được xác định bởi định nghĩa của Berlin) cải thiện sự sống còn của bệnh nhân chấn thương [23]. Tuy nhiên, nghiên cứu này bị hạn chế bởi quy mô mẫu nhỏ và sử dụng kiểm soát lịch sử. Một thử nghiệm lâm sàng ngẫu nhiên lớn do Peek và cộng sự thực hiện có thể là nền tảng để khám phá các chỉ định ECMO cho bệnh nhân ARDS [24]. Trong nghiên cứu này, bệnh nhân ARDS có điểm số Murray > 3.0 hoặc pH < 7.20 được phân ngẫu nhiên để nhận ECMO hoặc thông khí cơ học thông thường. Tỷ lệ sống sót 6 tháng là 63% ở nhóm ECMO so với 47% ở nhóm đối chứng. Với thành công của thử nghiệm này, các tiêu chí đã được thông qua bởi mạng ECMO ở Ý. Việc sử dụng các tiêu chí trong các bệnh nhân ARDS do virus cúm A (H1N1) cho thấy tỷ lệ sống sót là 68% [25]. Trong một nghiên cứu thuần tập, VV-ECMO sớm kết hợp với tỷ lệ tử vong thấp ở bệnh nhân suy hô hấp giảm oxygen máu nghiêm trọng [26]. Một ngưỡng áp lực cao nguyên thường được sử dụng để tránh tổn thương phổi trong quá trình thông khí cơ học. Tuy nhiên, áp lực cao nguyên tạo ra bởi sự đàn hồi của phổi và thành ngực. Đó là áp lực xuyên phổi cái có thể gây tổn thương phổi. Grasso và các đồng nghiệp đã báo cáo các tiêu chí bắt đầu ECMO sử dụng áp lực xuyên phổi ước tính với áp lực thực quản. Ở 14 bệnh nhân có ARDS liên quan đến cúm A (H1N1) có chỉ định ECMO, một nửa trong số họ đã tránh được ECMO khi áp dụng giới hạn trên áp lực xuyên phổi lên tới 25 cmH2O [27].
Cũng có những tình huống trong đó việc sử dụng ECMO có thể không có lợi. Về thông khí cơ học, người ta đã khuyên rằng những bệnh nhân thở máy trong hơn 7 ngày không dùng cho ECMO [24]. Trong khi người ta biết rằng thông khí cơ học kéo dài là một dấu hiệu của kết cục bất lợi, những ngày này không được chứng minh bằng bằng chứng thực nghiệm. Ví dụ, Cheng và các đồng nghiệp đã phát triển điểm số tử vong VV-ECMO để phân loại bệnh nhân trước khi chạy ECMO, trong đó Pre-ECMO MV ngày > 4 là yếu tố tiên đoán quan trọng nhất của tử vong với hệ số 2 (các dự đoán khác có hệ số là 1) [28]. Các nghiên cứu quan sát khác cũng xác định mối quan hệ tương tự giữa thời kỳ Pre-ECMO MV và kết cục tử vong [9, 29-31]. Điều quan trọng nhất, MV trước khi bắt đầu ECMO là một thành phần quan trọng trong việc tính điểm RESP (Respiratory ECMO Survival Prediction). Điểm này đã được xác nhận để hỗ trợ dự đoán sự sống còn của những bệnh nhân người lớn trải qua ECMO vì suy hô hấp [4, 32]. Tuy nhiên, vẫn khó xác định một thời điểm cụ thể sau thời điểm bắt đầu ECMO có thể được coi là vô ích. Có lẽ, điều này phụ thuộc vào sự tinh tế của các trung tâm cá nhân, và ở đây lựa chọn cá nhân của bệnh nhân nên được thực hiện.
Thông khí bảo vệ trong ECMO
Nên hiểu rằng chế độ thông thường có thể gây tổn thương phổi do thở máy gây ra (VILI). Các cơ chế cơ bản của VILI bao gồm sự quá căng phế nang (volutrauma), sự mất ổn định của phế nang dẫn đến xẹp phế nang và mở lại với mỗi nhịp thở (atelectrauma) và viêm thứ phát do các chấn thương cơ học được gọi là biotrauma [33]. Volutrauma là do thông khí ở thể tích khí lưu thông cao. Ảnh hưởng của lượng khí thở vào tổn thương là độc lập với áp lực đỉnh đường thở. Các mô hình chuột cho thấy, ở cùng một áp lực đỉnh đường thở (45 cmH2O), những người thông khí với lượng khí lưu thông thấp đã bị tăng tính thẩm thấu và phù phổi ít trầm trọng hơn [34]. Trong thực hành lâm sàng, thông khí ở áp lực đường thở cao được quan sát thấy gây ra tổn thương phổi biểu hiện như tràn khí màng phổi hoặc tràn khí dưới da. Tuy nhiên, vì áp lực đường thở cao không gây ra VILI trừ khi chúng có liên quan đến thể tích phổi cao, thuật ngữ barotrauma là một sự nhầm lẫn [35]. Để cải thiện VILI, khái niệm thông khí bảo vệ phổi được đưa vào thực hành lâm sàng. Các đoạn sau xem xét việc sử dụng thông khí bảo vệ ở bệnh nhân đang trải qua ECMO.
Thông khí bảo vệ có thể tích khí lưu thông thấp từ lâu đã được biết đến như một thành phần chính của chiến lược thông khí cho cả phổi bị thương và khỏe mạnh [10, 36, 37]. Một nghiên cứu bước ngoặt về thông khí khối lượng thấp được tiến hành gần hai thập kỉ trước [38]. Nghiên cứu cho thấy những bệnh nhân nhận được thông khí bảo vệ so với nhóm thông thường có tỷ lệ tử vong 28 ngày thấp hơn đáng kể (38% so với 71%;). Một phân tích gộp gần đây cho thấy rằng thông khí có lượng khí lưu thông thấp cộng với tư thế nằm sấp có liên quan đến giảm nguy cơ tử vong (hazards ratio: 0.62, 95% CI: 0.42-0.98) [39]. Tuy nhiên, một số nghiên cứu không xác định được tác động có lợi trên tỷ lệ tử vong [40, 41] hoặc ảnh hưởng ít hơn nhiều so với nghiên cứu của Amato [42]. Trong khi lợi ích của thông khí thể tích khí lưu thông thấp là để làm giảm tổn thương phổi, nó có thể gây ra sự tích tụ carbon dioxide và giảm oxy máu do thông khí giảm. Nói cách khác, sự cân bằng giữa phổi nghỉ và làm việc rất khó xác định. Bệnh nhân có ARDS nặng thực sự là một nhóm cực kỳ không đồng nhất mà một kích thước không phù hợp với tất cả (one size does not ft all), và tầm quan trọng tương đối của phổi còn lại so với nhu cầu chuyển hóa có thể khác nhau trong dân cư. Trong quá trình VV-ECMO, cần phải có thông khí cơ học do các lý do (1) tốc độ lưu thông máu của ECMO thường không đủ và trong tình trạng tăng động (hyperdynamic) một lượng đáng kể lượng máu vẫn truyền qua phổi tự nhiên, không phải đi qua phổi nhân tạo trước tiên; (2) phổi nên được thông khí nhẹ và giữ trong tình trạng mở. Sự xẹp hoàn toàn của phổi có thể làm chậm sự hồi phục của nó. Có bằng chứng cho thấy mức PEEP đầy đủ là có lợi [43].
Trở ngại chính đối với việc thông khí thể tích khí lưu thông thấp là ứ cacbon đioxit, oxy hóa trở nên tồi tệ hơn, và shunt trong phổi [44]. Khi thể tích khí lưu thông giảm xuống dưới 6 mL/kg, mức PaCO2 tăng đáng kể và giá trị pH giảm xuống dưới 7,2. Một thủ tục như vậy đối với phổi nghỉ ngơi được thực hiện với cái giá là rối loạn chuyển hóa và giảm ôxy mô. May mắn thay, ECMO có thể cung cấp cơ hội để phổi nghỉ ngơi trong khi duy trì cung cấp oxy mô và thải carbon dioxide. Với việc loại bỏ carbon dioxide ngoài cơ thể, Ranieri và các cộng sự cho thấy thể tích khí lưu thông < 6 mL/kg được tăng cường bảo vệ phổi trong điều kiện cân bằng cơ acid-base, tiết cytokine, và hình thái phổi [45]. Vì vậy, khôn ngoan là phổi nghỉ ngơi ở những bệnh nhân nặng ARDS, những người cũng được hỗ trợ với ECMO. Trong một cuộc khảo sát quốc tế về thiết lập máy thở trong ECMO, 77% các trung tâm ECMO báo cáo ” phổi nghỉ ” là mục tiêu chính của thông khí cơ học; một thể tích khí lưu thông 6 mL/kg hoặc ít hơn được nhắm mục tiêu trong 76% trung tâm [46]. Mặc dù thiếu một thử nghiệm đối chứng ngẫu nhiên trong chủ đề này, có một lượng lớn các bằng chứng quan sát ủng hộ ý tưởng rằng thông khí bảo vệ có liên quan đến kết quả tốt hơn [47]. Trong nghiên cứu của Schmidt và các cộng sự, thông khí bảo vệ được sử dụng thường xuyên ở các trung tâm ECMO thể tích lớn (high-volume ECMO). Mức tăng PEEP cao trong suốt 3 ngày đầu của ECMO được kết hợp với tỉ lệ tử vong thấp hơn (odds ratio 0.75, 95% CI, 0.64-0.88) [43]. Với mô hình hồi quy đa biến, mỗi một cmH2O tăng áp lực bình nguyên (plateau pressure) có liên quan đến giảm 14,4% tỷ lệ sống sót trong bệnh viện (95% CI = 1,75% – 25,4%, p = 0.027). Ngược lại, mỗi cmH2O tăng trong PEEP có liên quan đến sự giảm tỷ lệ sống sót trong 30 ngày là 36,2% (95% CI = 10,8% – 54,4%, p = 0.009) [48]. Đại dịch cúm A là một bi kịch đối với con người, nhưng nó cung cấp cơ hội tốt để khám phá cơ chế thở máy cơ học trong các bệnh nhân ECMO [49]. Những người sống sót đã có áp lực bình nguyên thấp hơn đáng kể ở ECMO so với những người không sống (25 ± 3 vs 29 ± 5 cmH2O; p < 0.01); Kết quả vẫn không thay đổi ngay cả sau khi điều chỉnh đa biến (OR: 1,33, 95% CI: 1,14-1,59; p < 0.01). Gần đây, một số tác giả cũng khám phá việc sử dụng thông khí siêu bảo vệ (nghĩa là thể tích khí lưu thông giảm xuống còn 4 ml/kg trọng lượng cơ thể dự đoán trong khi PEEP tăng lên nhằm mục tiêu áp lực cao nguyên giữa 23 và 25 cmH2O) với sự trợ giúp của loại bỏ cácbon điôxit ngoài cơ thể dòng chảy thấp (ECCO2R) với ARDS vừa phải [50].
Một thành phần khác của thông khí bảo vệ là tần số hô hấp thấp [51]. Lý do của thủ tục này là để phổi nghỉ ngơi bằng cách giảm chuyển động của nó. Phổi được thông khí 3 đến 5 lần/phút, với áp lực đường thở giới hạn ở mức 35-45 cmH2O. Một dòng oxy liên tục được cung cấp. Thải trừ carbon dioxide được thực hiện bằng phương pháp ngoài cơ thể [51].
Thông khí vòng kín (closed-loop ventilation) đóng vai trò là một chế độ thông khí bảo vệ mới [52]. Nó tự động điều chỉnh một số cài đặt theo mục tiêu sinh lý của các bác sĩ, cho phép lựa chọn một thiết lập máy thở riêng lẻ [53]. IntelliVent-ASV TM là một mở rộng và phát triển hệ thống thông khí hỗ trợ thích ứng (ASV, adaptive support ventilation) tự động điều chỉnh các thiết lập thông khí như thể tích phút, thể tích khí lưu thông (VT) và tần số hô hấp (RR) để đạt được PetCO2 mục tiêu ở những bệnh nhân thở thụ động và RR mục tiêu ở những bệnh nhân tự thở. Hơn nữa, FiO2 và PEEP được điều chỉnh tự động để đạt được SpO2 mục tiêu. Mặc dù chế độ thông khí vòng kín đã được chứng minh là an toàn và hiệu quả ở những bệnh nhân ARDS, nhưng việc sử dụng nó ở những bệnh nhân đang điều trị ECMO chưa được điều tra đầy đủ [54, 55]. Trong 6 bệnh nhân, Karagiannidis và các đồng nghiệp báo cáo rằng chế độ thông khí vòng kín đáp ứng nhanh chóng tới lưu lượng khí ECMO giảm. Nó kết luận rằng sự kết hợp của hệ thống thở thông khí điều chỉnh tự nhiên (NAVA) và ECMO có thể cho phép thông khí vòng kín với thông khí bảo vệ tự động [56].
Thủ thuật huy động
Thủ thuật huy động là thành phần không thể thiếu của thông khí bảo vệ, và có nhiều phương pháp để thực hiện thủ thuật huy động. Trong phần này, chúng tôi nhằm mục đích mô tả một số động tác huy động thường được sử dụng. Grasso và các đồng nghiệp đã đề xuất việc chuẩn độ PEEP theo chỉ số căng thẳng (stress index). Chỉ số căng thẳng (b) có thể được ước lượng dựa trên áp lực đường thở và thời gian hít vào theo phương trình sau:
Airway pressure = α.Inspiratory time^b + c, (1)
ở đây hệ số b là chỉ số căng thẳng mô tả hình dạng của áp lực mở đường thở (Pao) tương ứng với thời kỳ bơm phống với lưu lượng hằng định. Đối với b < 1, đường cong Pao thể hiện sự lõm xuống, cho thấy sự giảm liên tục trong độ đàn hồi trong thời gian bơm phồng với lưu lượng hằng định. Đối với b> 1, đường cong cho thấy một sự cong lên phía trên cho thấy sự gia tăng liên tục trong độ đàn hồi. Đối với b = 1, đường này thẳng, cho thấy không có sự thay đổi độ đàn hồi theo bơm phồng thể tích khí lưu thông. Mức PEEP được điều chỉnh để xác định chỉ số căng thẳng giữa 0,9 và 1,1 [57]. Cụ thể, PEEP giảm nếu chỉ số căng thẳng cao hơn 1,1 và tăng nếu chỉ số căng thẳng thấp hơn 0,9. PEEP không thay đổi nếu chỉ số căng thẳng là giữa 0,9 và 1,1 [58].
Talmor và các đồng nghiệp đã đề xuất thiết lập mức PEEP theo mức áp lực thực quản. Bệnh nhân cần an thần sâu và thuốc chẹn thần kinh cơ. Cơ cấu huy động được thực hiện bằng cách tăng áp lực đường thở lên 40 cmH2O trong 30 giây. Sau đó, PEEP đã được thiết lập để đạt được áp lực xuyên phổi từ 0 đến 10 cmH2O khi cuối thì thở ra, theo thang trượt dựa trên PaO2 và FiO2 (Bảng 1) [59]. Thiết lập thông khí thở được điều chỉnh trong một cột tại một thời điểm để giữ PaO2 từ 55 đến 120 mmHg. Ngoài ra, độ bão hòa ôxyđược giữ từ 88 đến 98% bằng cách sử dụng thiết lập thông khí trong một cột tại một thời điểm. PEEP được thiết lập ở mức áp lực xuyên phổi trong suốt quá trình tắc nghẽn cuối thì thở ra (PLexp) nằm giữa 0 và 10 cmH2O và giữ áp lực xuyên phổi trong thời gian tắc nghẽn cuối thì hít vào ở dưới 25 cmH2O. Thể tích khí lưu thông được thiết lập ở mức 6 mL/kg trọng lượng cơ thể dự đoán. Trọng lượng cơ thể dự đoán được ước tính theo phương trình sau:
=50(if male, 45.5 if female) + 0,91 x (centimeters of height – 152,4) (2)

”Bảng được điều chỉnh từ reference [59]. Cài đặt thông khí được điều chỉnh từng cột một lần để giữ áp lực từng phần của ôxy động mạch (PaO2) từ 55 đến 120 mmHg. Ngoài ra, độ bão hòa oxy, được đo bằng pulse oximeter, được giữ từ 88 đến 98% bằng cách sử dụng các thiết lập thông khí trong một cột tại một thời điểm. Áp lực dương cuối thì thở ra (PEEP) được đặt ở mức áp lực xuyên phổi trong quá trình tắc nghẽn cuối thì thở ra (PLexp) nằm giữa 0 và 10 cmH2O và giữ áp lực xuyên phổi trong quá trình tắc nghẽn cuối thì hít vào ở dưới 25 cmH2O.”
Trong thử nghiệm EXPRESS, “phương pháp phổi mở” được sử dụng để điều trị những bệnh nhân ARDS nặng [60]. Các cài đặt thở máy bao gồm chế độ kiểm soát áp lực, nhắm mục tiêu thể tích khí lưu thông là 6 mL/kg trọng lượng cơ thể dự đoán và áp lực đường thở bình nguyên dưới 40 cmH2O. Thủ thuật huy động bao gồm một nhịp thở 40 giây với áp lực đường thở là 40 cmH2O và một FIO2 là 1.0. Sự oxy hóa được duy trì ở một phạm vi đích như mô tả trước đây sử dụng một thang điểm kết hợp PEEP/FiO2 (Bảng 2) [42].

Tư thế nằm sấp trong thời gian ECMO
Tư thế nằm sấp là một liệu pháp thay thế hoặc cứu hộ cho bệnh nhân ARDS nặng. Tư thế nằm sấp có thể giúp làm giảm sự xẹp của các phần phổi lưng với việc tránh căng quá mức của vùng phổi phía trước ngực. Mục đích là làm đồng nhất áp lực phổi và làm giảm shunt trong phổi. Ở những bệnh nhân ARDS nặng, tư thế nằm sấp đã được chứng minh là có lợi trong một số kết cục lâm sàng như tử suất (nguy cơ tương đối [RR]: 0.9, 95% CI: 0.82-0.98) [61] PaO2/FiO2 (63.0 ± 66.8 vs 44.6 ± 68.2, p = 0.02) [62], và viêm phổi liên quan đến thở máy (1,66 vs 2,14 trên 100 bệnh nhân – ngày đặt nội khí quản, p = 0.045) [63]. Nghiên cứu PROSEVA nổi tiếng là nghiên cứu đa trung tâm lớn nhất điều tra tác động của việc tư thế nằm sấp lên kết cục tử vong. Nghiên cứu khẳng định rằng việc áp dụng sớm tư thế nằm sấp kéo dài đã làm giảm đáng kể 28 ngày (16,0% so với 32,8%) và tử vong 90 ngày (23,6% so với 41,0%) ở bệnh nhân ARDS nặng [64].
Việc tư thế nằm sấp có thể được thực hiện thành công trong ECMO và nó liên quan đến cải thiện các thông số hô hấp. Trong 17 đối tượng VV-ECMO cũng thất bại ít nhất một lần cai máy, tư thế nằm sấp kéo dài (24 giờ) đã được thực hiện [65]. Độ giãn nở của hệ hô hấp tăng từ 18 (12-36) đến 32 (15-36) mL/cmH2O (p < 0.0001), và tỷ số PaO2/FiO2 tăng từ 111 (84-128) đến 173 (120-203) mmHg (p < 0.0001). Những phát hiện tương tự được báo cáo trong một vài trường hợp và các nghiên cứu đoàn hệ quan sát [66-69]. Chỉ định tư thế nằm sấp trong khi ECMO bao gồm tình trạng thiếu oxy nặng (PaO2/FiO2 <70) và cài đặt thông khí có thể gây tổn thương như áp lực bình nguyên cao hơn 32 cmH2O [70].
Một vấn đề thách thức trong việc tư thế nằm sấp là nguy cơ có thể có thể xảy ra khi xoay bệnh nhân. Do đó, một số tác giả đề xuất rằng ECMO có thể là một chống chỉ định của tư thế nằm sấp [67]. Các tác dụng ngoại ý được báo cáo bao gồm cannula kém chức năng, tụt nội khí quản không chủ ý, loét do chèn ép và tụt các đường động mạch và tĩnh mạch [71]. Chảy máu từ cannula và ống dẫn lưu ngực cũng được ghi nhận trong một số nghiên cứu [72, 73]. Một quy trình quay chuẩn phải được thực hiện trong các trung tâm chuyên sâu để tránh những biến chứng có hại này. Có bằng chứng cho thấy tư thế nằm sấp trong ECMO là an toàn nếu được thực hiện đúng [74, 75].
Thở tự nhiên trong thời gian ECMO
Thở tự nhiên thường không được phép trong giai đoạn đầu của ARDS nặng, chủ yếu là do các bệnh nhân nặng cần phải thông khí bảo vệ (ví dụ, thể tích khí lưu thông thấp, PEEP cao, và thủ thuật huy động) [76]. Để thực hiện việc thông khí bảo vệ, bệnh nhân thường cần an thần sâu và thuốc liệt cơ. Trong thử nghiệm ACURASYS (ARDS et Curarisation Systematique), việc sử dụng các thuốc chống thần kinh cơ để ức chế nhịp thở tự nhiên đã được thấy là có lợi trên các kết cục lâm sàng quan trọng như thời gian không nằm ICU và tử vong (tỷ số nguy cơ ở 90 ngày: 0,68; 95% CI: 0,48-0,98). Ảnh hưởng có ý nghĩa thống kê trong ARDS nặng (tỷ lệ tử vong 90 ngày: 30,8% so với 44,6%,) [77]. Các kết quả tương tự đã được báo cáo trong các nghiên cứu khác [78-82]. Tuy nhiên, những ảnh hưởng bất lợi của thuốc an thần sâu và thuốc liệt cơ, bao gồm nhịp tim chậm, chứng liệt liên quan ICU, viêm phổi liên quan đến thở máy, vẫn là mối quan tâm quan trọng. Để tránh những tác động có hại tiềm ẩn của an thần sâu và liệt cơ, một số trung tâm tiên phong bắt đầu sử dụng ECMO làm phương pháp điều trị đầu tiên chứ không phải là liệu pháp cứu hộ sau khi thất bại. Vì vậy, có tích lũy bằng chứng về việc sử dụng ECMO trong bệnh nhân còn tỉnh, thở tự nhiên [83-85]. Ở những bệnh nhân chờ đợi cấy ghép phổi, những người trải qua ECMO thở tự nhiên đã cho thấy sự sống còn được cải thiện khi so sánh với các chiến lược khác [84].
ECMO có thể cung cấp một giải pháp thay thế để cung cấp thông khí bảo vệ. Như đã đề cập ở trên, việc loại bỏ cácbon điôxit có thể kiểm soát nỗ lực thở tự nhiên. Với việc giảm lượng khí cácbon điôxit bằng cách gia tăng lượng khí và lưu lượng máu, có thể gây ngưng thở ở động vật [17, 18]. Các kết quả tương tự đã được tìm thấy trong các nghiên cứu của con người [19, 86]. Trong giai đoạn muộn của ARDS nặng, hít thở tự nhiên có thể được cho phép để ngăn ngừa tác động bất lợi của thông khí kiểm soát kéo dài. Ví dụ, teo cơ hô hấp thường gặp ở bệnh nhân thở máy kéo dài, và tác dụng phụ này có thể xảy ra chỉ sau 18 giờ thở máy [87]. Hồi phục hoạt động cơ hô hấp giúp giảm hoặc ngăn ngừa bệnh cơ lan tỏa [88]. Một lợi ích khác của việc thở tự nhiên là tăng lưu lượng máu của cơ thể và các tạng. Trong một nghiên cứu trên động vật, Hering và các đồng nghiệp cho thấy lưu lượng máu dạ dày tăng lên từ 0.13 ± 0.01 đến 0.29 ± 0.05 mL/g⋅min với nhịp thở tự phát. Các xu hướng tương tự cũng được tìm thấy ở các cơ quan nội tạng khác [89]. Nên biết rằng sự tưới máu các cơ quan nội tạng là một yếu tố quyết định quan trọng cho các kết cục lâm sàng trong giai đoạn bệnh nặng. Trong trường hợp có sáu người tham gia, Karagiannidis và các đồng nghiệp phát hiện ra rằng bệnh nhân có thể điều chỉnh ngay PaCO2 theo hướng sinh lý. Thể tích khí lưu thông tăng từ 2-5 mL/kg lên 8 mL/kg với ECMO bất hoạt, và áp lực hít vào tăng từ 19-29 cmH2O đến 21-45 cmH2O [56]. Hít thở tự nhiên ở những động vật ARDS nặng được hỗ trợ ECMO có liên quan đến việc cải thiện oxy hóa và shunt trong phổi và thông khí phân bố lại đối với vùng lưng, so với những người có thông khí có kiểm soát [44]. Chế độ thông khí cơ học cho phép thở tự nhiên có thể được sử dụng như chế độ hỗ trợ, CPAP cộng với hỗ trợ áp lực và thông khí cơ học điều chỉnh thần kinh (NAVA).
Hơn nữa, cho phép thở tự phát trong thời gian ECMO có thể có lợi trong điều trị hồi phục sớm, bởi vì những bệnh nhân này cần ít thuốc an thần và thuốc liệt cơ hơn. Có thể thực hiện phục hồi sớm cho nhóm bệnh nhân này. Trong một nghiên cứu liên quan đến 100 bệnh nhân ECMO, các nhà nghiên cứu nhận thấy rằng 35% (35/100 bệnh nhân nhận ECMO) có thể tham gia vào việc cử động sớm và 51% (18/35) có thể đi lại được [90]. Như vậy, cử động sớm được coi là an toàn và khả thi. Có bằng chứng cho thấy bệnh nhân đang được huấn luyện thể lực có thể có thời gian lưu trú ở ICU ngắn hơn [91].
Tóm lại, không cho phép thở tự nhiên vào giai đoạn đầu của ARDS nặng, nhằm thực hiện việc thông khí bảo vệ. Với sự hỗ trợ của ECMO, không có gì đáng lo ngại về tình trạng thiếu oxy máu và tăng CO2 máu và có thể dễ dàng thông khí bảo vệ. Ở giai đoạn phục hồi ARDS nghiêm trọng, có thể khôn ngoan để hạ thấp lưu lượng khí và tốc độ dòng máu ECMO, cho phép hồi phục hơi thở tự nhiên. Sự phục hồi có thể rất nhanh.
Cai máy
Một số tác giả đề nghị cai máy VV-ECMO nên bắt đầu với cai máy của máy thở. Thủ tục này có thể bắt đầu khi bệnh nhân có thể duy trì trao đổi khí đầy đủ với giảm các thông số ECMO và cài đặt máy thở tối thiểu. Bệnh nhân có thể được cai từ thông khí cơ học trong khi vẫn dùng liệu pháp ECMO. Việc sử dụng ống thông đơn, ống thông kép trong tĩnh mạch cổ trong cho phép các bệnh nhân rút ống nội khí quản, bệnh nhân tập đi trong khi đang kết nối với hệ thống ECMO. Một chiến lược như vậy đòi hỏi sự phối hợp tốt giữa các y tá, bác sĩ, và các nhân viên y tế khác [92]. Sau đó, khi FiO2 cai máy trên ECMO, tốc độ dòng chảy có thể giảm xuống dưới 2,5 L/phút. Có thể xem xét việc giải ngưng khi bệnh nhân được điều trị với lưu lượng FiO2 và ECMO thấp nhất.
Các tác giả khác thích sử dụng phác đồ bảo vệ phổi và sau đó quyết định ưu tiên cai máy VV- ECMO trên MV [47]. Trong một cuộc khảo sát quốc tế liên quan đến 141 phản ứng cá nhân, Marhong và các đồng nghiệp báo cáo rằng phần lớn các trung tâm ưu tiên cai máy VV-ECMO trên nền thông khí cơ học [46]. Quy trình cai máy có thể được thực hiện theo hướng dẫn của tổ chức ELS (https://www.elso.org): Các lưu lượng ECMO giảm dần theo bước tối thiểu là 1 L/phút trong khi vẫn duy trì sweep ở 100%. Ngoài ra, khi lưu lượng được giảm xuống còn 2 L/phút và sau đó FiO2 sweep được giảm. Cả hai cách tiếp cận này đều nhằm mục đích duy trì SaO2 lớn hơn 95%. Khi SaO2 ổn định trên thiết lập này, sweep có thể được kẹp trên cài đặt thông khí của thông khí hỗ trợ áp lực (PSV) hoặc áp lực đường thở dương liên tục (CPAP) là 20 cmH2O. Nếu SaO2 > 95% và PaCO2 < 50 mmHg có thể được duy trì trong 60 phút, ECMO có thể được cai máy.
Kết luận
Mặc dù MV thường được sử dụng để tránh tình trạng thiếu oxy máu trầm trọng và tăng CO2 máu ở những bệnh nhân ARDS nặng nhưng MV có thể gây tổn thương phổi và đẩy nhanh sự tiến triển của bệnh. Oxy hóa màng ngoài cơ thể (ECMO) cung cấp một giải pháp thay thế cho các bệnh nhân cứu hộ bị suy hô hấp nghiêm trọng mà MV không thể duy trì trao đổi khí đầy đủ. Thời điểm bắt đầu ECMO dựa trên những rủi ro và lợi ích của ECMO đã được điều tra rộng rãi. Trong quá trình chạy ECMO, chiến lược thông khí bảo vệ có thể được sử dụng mà không phải lo lắng về tình trạng thiếu oxy máu trầm trọng và ứ carbon dioxide. Có rất nhiều bằng chứng cho thấy rằng thông khí bảo vệ có lượng khí lưu thông thấp, PEEP cao và tư thế nằm sấp có thể mang lại lợi ích cho kết cục tử vong. Gần đây hơn, ngày càng có sự phổ biến về việc sử dụng hô hấp tự phát cho những bệnh nhân trải qua ECMO. Cuối cùng, chúng tôi thảo luận về cai máy ECMO. Đa số các trung tâm ưu tiên cai máy VV-ECMO trên nền thở máy, trong khi những người khác lại ưu tiên cai máy thở trước ECMO.





