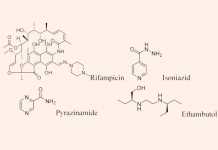
Giới thiệu chung về Kháng sinh nhóm Lipopeptide
Lịch sử ra đời
Cũng giống như các kháng sinh nhóm Glycopeptide, các kháng sinh nhóm Lipopeptide cũng là các kháng sinh quan trọng trên lâm sàng trong điều trị các chủng vi khuẩn kháng thuốc. Trong bài viết này, chúng ta sẽ tập trung vào các kháng sinh quan trọng hiện đang được sử dụng trên lâm sàng, đó là Daptomycin và các Polymyxin.
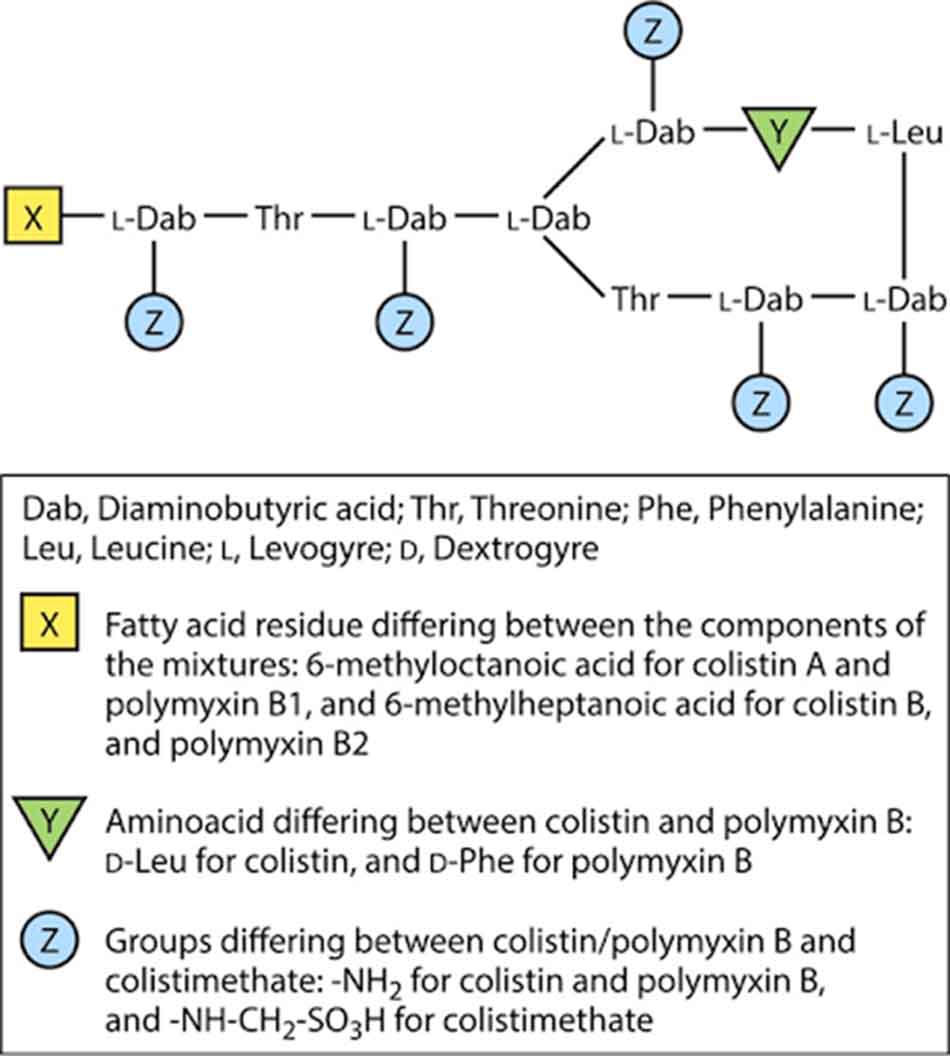
Hiện tại có hai loại kháng sinh nhóm Polymyxin đang được sử dụng thường xuyên trên lâm sàng là Polymyxin B (bao gồm Polymyxin B1 và B2, chỉ dùng đường tại chỗ) và Polymyxin E (Colistin, bao gồm Colistin A và Colistin B, có thể dùng theo đường toàn thân). Dạng dược dụng được dùng toàn thân của Colistin là Colistimethate natri, hay còn có tên gọi khác là Colistin methanesulfonate, thu được bằng cách xử lý Colistin với formaldehyde và natri bisulfite. Dạng dược dụng này là tiền thuốc không hoạt động ít độc hơn so với Colistin sulfate, nó sẽ được chuyển thành Colistin khi được hòa tan trong nước, vì vậy bột pha tiêm đông khô chứa Colistimethate natri cần được sử dụng ngay sau khi pha để tránh độc tính của Colistin. Colistin được sử dụng phổ biến trên lâm sàng hơn nhiều so với Polymyxin B.
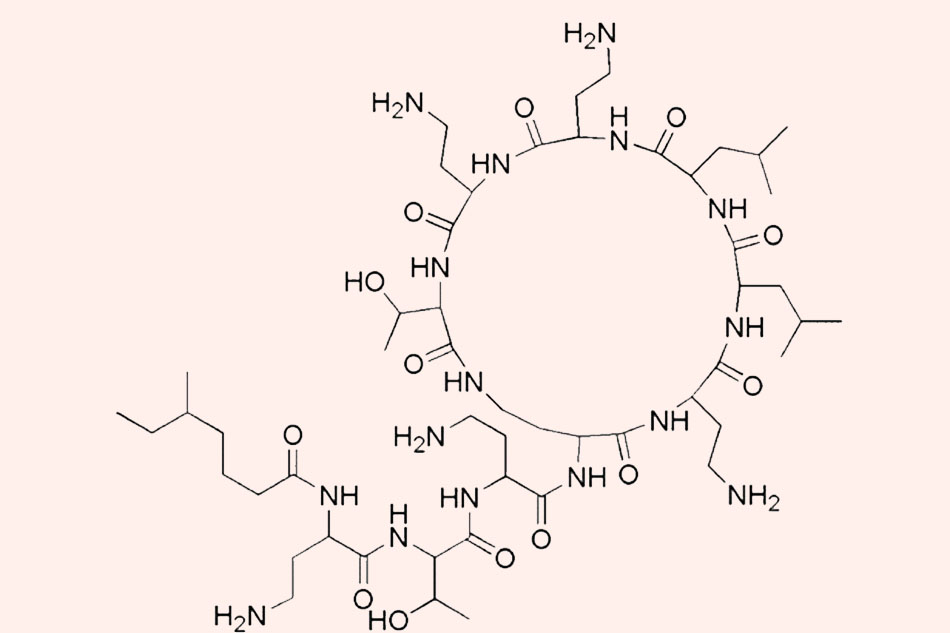
Colistin được xác định lần đầu năm 1947, nó được phân lập từ quá trình lên men của chủng vi khuẩn sống trong đất Paenibacillus polymyxa subsp. colistinus, được tổng hợp không thông qua ribosome như con đường tổng hợp các peptide thông thường, và do đó trong cấu trúc của chúng có sự xuất hiện của một số acid amin “lạ” như 2,4-diaminobutyric acid (Dab) và các acid amin cấu hình D (bình thường các acid amin cấu tạo nên protein trong các cơ thể sống có cấu hình L). Nó được sử dụng tại châu Âu và Nhật Bản từ những năm 1950 và tới năm 1959, Colistimethate đã thay thế Colistin trong điều trị sau khi được Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) Hoa Kỳ phê duyệt. Tuy nhiên, độc tính không nhỏ của Colistin, đặc biệt là độc tính trên thận, đã khiến cho việc sử dụng nó được xem xét lại vào những năm 1970. Colistin dần bị thay thế bằng những kháng sinh mới có phổ rộng hơn, ít độc tính hơn như Aminoside, Quinolone và β-lactam. Trong suốt 20 năm sau đó, Colistin được sử dụng rất hạn chế trên người, chủ yếu là sử dụng theo đường tại chỗ hoặc nhãn khoa. Colistin đường toàn thân hoặc khí dung chỉ được sử dụng cho những bệnh nhân xơ nang. Tuy nhiên, cùng với sự phát triển ngày càng cao của các chủng vi khuẩn gram âm đa kháng, đặc biệt là các chủng vi khuẩn sản xuất carbapenemase khiến cho kháng sinh Carbapenem mất đi tác dụng, Colistin đường toàn thân đã dần được đưa trở lại trên lâm sàng. Hiện nay nó đã trở thành tuyến phòng thủ cuối cùng của các bác sĩ để chống lại các vi khuẩn gram âm đa kháng.
Ngược lại với các Polymyxin được tìm ra khá sớm và có tác dụng tốt trên vi khuẩn gram âm, Daptomycin lại là một kháng sinh Lipopeptide được tìm ra khá muộn (được sử dụng chính thức trên lâm sàng từ năm 2003) và chỉ có tác dụng tốt trên các vi khuẩn gram dương. Daptomycin có nguồn gốc từ loài Streptomyces roseosporus. Sự ra đời của Daptomycin đã giúp ích rất nhiều trong cuộc chiến chống lại các vi khuẩn gram dương đa kháng, đặc biệt là tụ cầu vàng kháng Methicillin (MRSA), trong bối cảnh mà tỷ lệ MRSA đề kháng với Vancomycin ngày càng cao.
Cấu trúc hóa học
Các Polymyxin có cấu trúc polypeptide tích điện dương, bao gồm một vòng heptapeptide nối với chuỗi bên tripeptide mà đầu N của nó được acyl hóa bằng một acid béo.
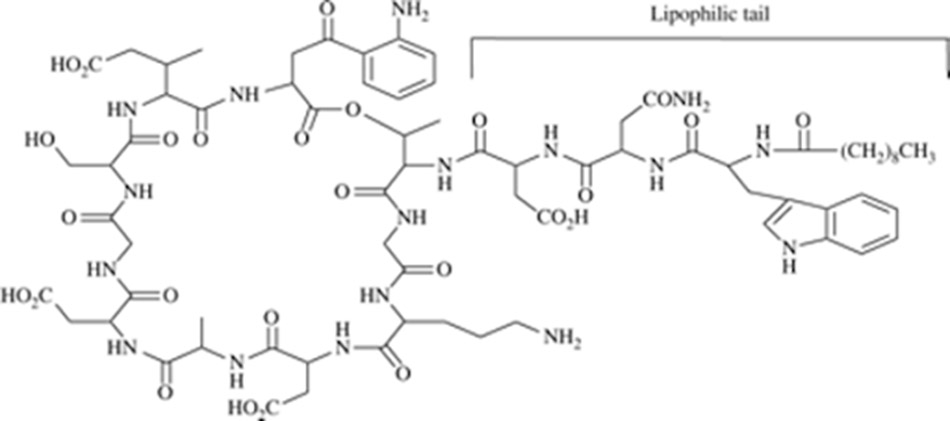
Daptomycin có cấu trúc độc đáo với peptide vòng chứa 13 acid amin và chuỗi bên decanoyl.
Dược lực học
Cơ chế tác dụng
– Các kháng sinh nhóm Polymyxin là các cation (tích điện dương) có khả năng tương tác với lớp màng ngoài tế bào vi khuẩn (lớp màng này chỉ có ở vi khuẩn gram âm) tích điện âm, cụ thể là tương tác tĩnh điện giữa phần Dab tích điện dương của kháng sinh với nhóm phosphate tích điện âm của lipid A. Điều này làm cho các cation hóa trị II là Ca2+ và Mg2+ đi ra khỏi nhóm phosphate của lipid màng. Từ đó, thành phần lipopolysaccharide (LPS) màng ngoài tế bào bị mất ổn định, màng ngoài tế bào vi khuẩn tăng tính thấm, gây ra rò rỉ các thành phần trong bào tương, dẫn đến chết tế bào. Không những vậy, khả năng liên kết với LPS còn giúp kháng sinh trung hòa được nội độc tố của vi khuẩn. Một cơ chế khác cũng được đề xuất với các Polymyxin là chúng ức chế một enzyme hô hấp quan trọng của vi khuẩn có tên gọi là NADH-quinone oxidoreductase type II (NDH-2) ở lớp màng trong của vi khuẩn.
– Trong khi đó, Daptomycin lại có cơ chế tác dụng độc nhất và cho đến nay vẫn chưa hoàn toàn được hiểu rõ. Cơ chế được đề xuất cho Daptomycin là nó đưa chuỗi bên kỵ nước vào màng tế bào, gây ra sự khử cực màng nhanh chóng cùng với thoát ion K+ ra ngoài tế bào thông qua sự oligomer hóa tạo thành một kênh xuyên màng tế bào. Tiếp theo sau đó, các quá trình tổng hợp DNA, RNA cùng với protein cũng bị đình trệ. Kết cục cuối cùng là vi khuẩn chết. Daptomycin có tác dụng diệt khuẩn cực mạnh, tới hơn 99.9% số vi khuẩn (3 log) bị tiêu diệt trong chưa tới 1 giờ.
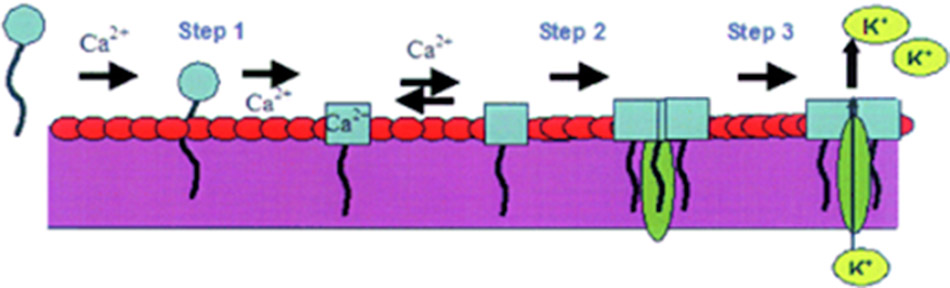
Mô tả: Daptomycin ban đầu sẽ gắn với màng tế bào (quá trình phụ thuộc ion Ca2+), sau đó nó được oligomer hóa và hình thành một lỗ xuyên màng, lỗ này sẽ làm tế bào mất các ion nội bào quan trọng và cuối cùng là chết.
Một số cơ chế khác được đề xuất với Daptomycin bao gồm ức chế quá trình vận chuyển tích cực các acid amin, ức chế tổng hợp peptidoglycan và/hoặc lipoteichoic acid.
Nồng độ cardiolipin trong màng tế bào vi khuẩn tăng lên có thể làm giảm tác dụng diệt khuẩn của Daptomycin.
Phổ tác dụng
– Các Polymyxin có phổ tác dụng rộng trên nhiều vi khuẩn gram âm như E. coli, Klebsiella spp., Enterobacter spp., Pseudomonas aeruginosa (trực khuẩn mủ xanh) và Acinetobacter spp. Chúng cũng có tác dụng trên Salmonella spp., Shigella spp., Pasteurella spp. và Haemophilus spp. Các vi khuẩn Proteus spp., Providencia spp. và hầu hết các chủng Serratia spp. có khả năng đề kháng nội tại với Polymyxin. Ngoài ra, các chủng vi khuẩn khác cũng có khả năng đề kháng với Polymyxin bao gồm Brucella spp., Neisseria spp., Chromobacterium spp. và Burkholderia spp.
Các Polymyxin không có tác dụng trên vi khuẩn gram dương và vi khuẩn kỵ khí.
– Ngược lại với các Polymyxin, phổ tác dụng của Daptomycin lại chỉ tập trung trên nhóm vi khuẩn gram dương, tương tự như các Glycopeptide. Các vi khuẩn mà Daptomycin có tác dụng tốt bao gồm Staphylococcus aureus nhạy cảm (MSSA) hoặc kháng Methicillin (MRSA), S. aureus đề kháng trung gian Glycopeptide (GISA) hoặc kháng Vancomycin (VRSA), Staphylococcus spp. có coagulase âm tính kháng Methicillin (CoNS), Enterococci kháng Vancomycin (VRE), S. aureus và E. faecium kháng Linezolid và Quinupristin/Dalfopristin, các liên cầu tan huyết β bao gồm Streptococcus pyogenes (nhóm A), S. agalactiae (nhóm B) và các Streptococcus khác. Các vi khuẩn khác cũng nằm trong phổ tác dụng của Daptomycin gồm có Corynebacterium jeikeium, Peptostreptococcus spp., Clostridium perfringens, C. difficile và Propionibacterium acnes.
Đã quan sát thấy tác dụng hiệp đồng khi phối hợp Daptomycin với các Aminoside hoặc Rifampicin.
Cơ chế đề kháng
– Cơ chế đề kháng với các Polymyxin:
Một số vi khuẩn như P. mirabilis và S. marcescens có khả năng đề kháng nội tại với các Polymyxin là nhờ sự biểu hiện của operon arnBCADTEF và/hoặc gene eptB, điều này dẫn đến sự thay đổi cấu trúc của LPS màng ngoài vi khuẩn gram âm thông qua sự bổ sung các nhóm cation phosphoethanolamine (pEtN) và/hoặc 4-amino-4-deoxy-L-arabinose (L-Ara4N) vào LPS. Sự thay đổi này làm thay đổi điện tích âm của LPS, làm giảm ái lực gắn của phân tử kháng sinh với LPS, từ đó tạo ra đề kháng.
Các trực khuẩn gram âm đường ruột Enterobacteriaceae như Klebsiella, Escherichia, Enterobacter và Salmonella lại chủ yếu có đề kháng đạt được với các Polymyxin. Một số cơ chế đề kháng ở mức độ phân tử đã được biết là tương tự như các vi khuẩn có khả năng đề kháng nội tại với Polymyxin, đó là thông qua sự bổ sung các nhóm cation pEtN và L-Ara4N vào LPS. Có nhiều gene cũng như operon tham gia vào cơ chế đề kháng với các Polymyxin, ví dụ: các gene và operon quy định tổng hợp nhóm cation và/hoặc gắn nhóm cation vào LPS như gene pmrC, pmrE và operon pmrHFIJKLM, các gene điều hòa mã hóa cho các protein tham gia vào hệ thống hai thành phần PmrAB và PhoPQ, gene mgrB điều hòa âm tính hệ thống PhoPQ và hệ thống hai thành phần crrAB điều hòa hệ thống PmrAB.
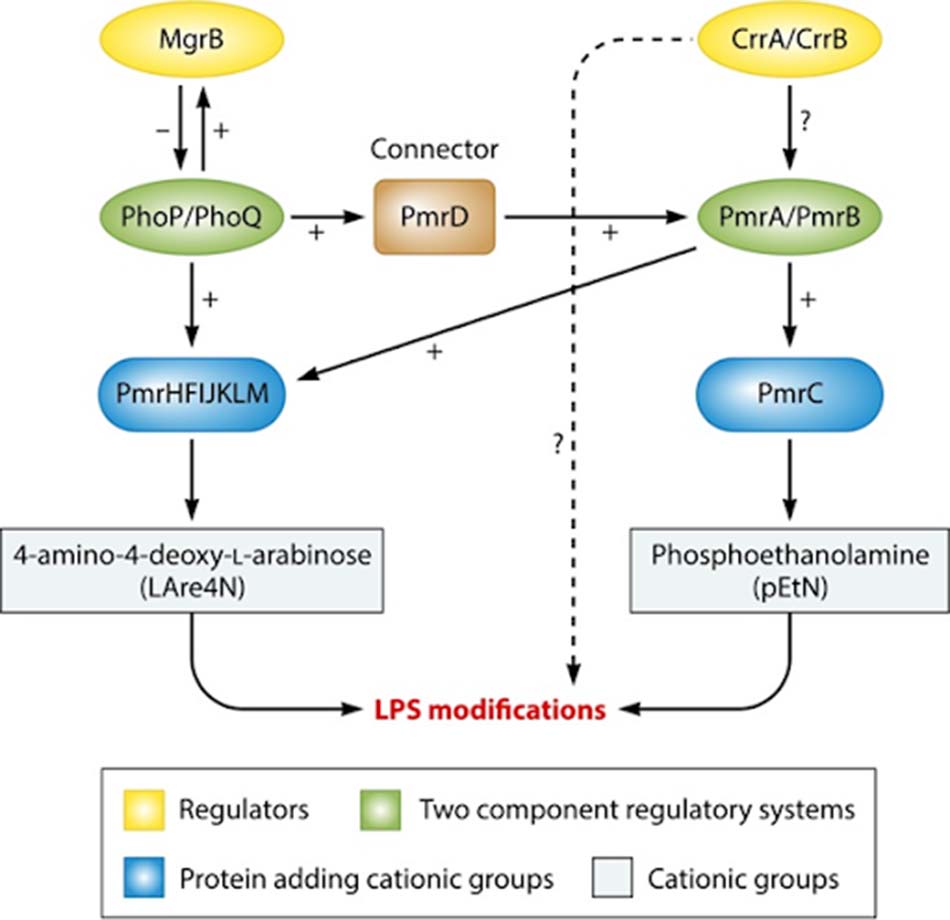
Operon pmrCAB mã hóa cho ba protein: pEtN phosphotransferase PmrC, PmrA điều hòa đáp ứng (tên gọi khác: BasR) và protein kinase PmrB cảm biến (tên gọi khác: BasS). pEtN phosphotransferase PmrC chịu trách nhiệm gắn nhóm pEtN vào LPS.
Operon pmrHFIJKLM (tên gọi khác: operon arnBCADTEF hoặc operon pbgPE) mã hóa cho bảy protein. Gene pmrE và operon pmrHFIJKLM quy định tổng hợp nhóm L-aminoarabinose (L-Ara4N) và gắn nó vào lipid A.
Môi trường phagosome của đại thực bào chứa các ion Fe3+, Al3+ và pH thấp (5.5) là điều kiện cần thiết cho sự hoạt hóa PmrB. Hệ thống hai thành phần PmrAB và PhoPQ được hoạt hóa khi vi khuẩn bị thực bào bởi đại thực bào, cho phép chúng có thể tồn tại trong môi trường của phagosome. PmrB là một protein có hoạt tính tương tự tyrosine kinase, có khả năng hoạt hóa PmrA thông qua phosphoryl hóa. PmrA hoạt hóa quá trình phiên mã operon pmrCAB, operon pmrHFIJKLM và gene pmrE, điều này làm gắn pEtN và L-Ara4N vào LPS.
Những đột biến ở các gene pmrA và pmrB là nguyên nhân gây ra đề kháng đạt được với Colistin ở các chủng K. pneumoniae, E. aerogenes và S. enterica.
Môi trường trong phagosome đại thực bào đồng thời cũng kích thích quá trình hoạt hóa PhoQ. Hệ thống hai thành phần PhoPQ (được mã hóa bởi operon phoPQ) cũng cho phép thay đổi cấu trúc LPS, từ đó giúp vi khuẩn chống lại các tác nhân kháng khuẩn có bản chất cation. Cụ thể: PhoQ là một protein có hoạt tính tyrosine kinase, nó phosphoryl hóa PhoP, PhoP đến lượt nó lại hoạt hóa phiên mã operon pmrHFIJKLM, từ đó gắn nhóm L-Ara4N vào LPS. PhoQ cũng đồng thời hoạt hóa PmrA thông qua PmrD, từ đó gắn nhóm pEtN vào LPS.
Những đột biến ở các gene phoP và phoQ là nguyên nhân gây ra đề kháng đạt được với Colistin ở K. pneumoniae và E. coli.
mgrB là gene quy định tổng hợp protein xuyên màng MgrB. mgrB được điều hòa lên khi hoạt hóa PhoP. Khi hoạt hóa mgrB, MgrB được tăng tổng hợp, điều này dẫn đến ngăn chặn biểu hiện của các gene mã hóa PhoQ. Nếu gene mgrB bị bất hoạt, operon phoPQ sẽ được biểu hiện quá mức, dẫn đến hoạt hóa operon pmrHFIJKLM, từ đó sản xuất L-Ara4N và gây ra đề kháng Colistin. Hoặc nếu protein MgrB vì một lý do nào đó bị mất hoạt tính (đột biến gene mgrB), vi khuẩn có thể đề kháng với Colistin (cơ chế ở K. pneumoniae). Một nguồn gây đề kháng Colistin đáng chú ý gần đây, đó là sự chuyển vị của các gene quy định ESBLs (các β-lactamase phổ rộng) hoặc carbapenemase gây phá vỡ gene mgrB trên nhiễm sắc thể.
Operon crrAB (crr: colistin resistance regulation) mã hóa cho hai protein là protein điều hòa CrrA và protein kinase cảm biến CrrB. Nếu crrAB bị bất hoạt, operon pmrAB sẽ được biểu hiện quá mức, từ đó hoạt hóa operon pmrHFIJKLM và gene pmrC và pmrE, sản xuất L-Ara4N và pEtN và gây ra đề kháng Colistin. Ngoài ra, sự bất hoạt crrAB cũng có thể hoạt hóa protein tương tự glycosyltransferase làm thay đổi cấu trúc lipid A.
Ngoài các cách làm thay đổi đích tác dụng của kháng sinh nhóm Polymyxin thông qua các đột biến nhiễm sắc thể như ở trên, còn phải kể đến một cơ chế đề kháng nữa vô cùng quan trọng với các kháng sinh nhóm này, đó là đề kháng trung gian thông qua plasmid, mà cụ thể ở đây chúng ta quan tâm nhiều đến gene mcr-1. Gene mcr-1 lần đầu được phát hiện tại Trung Quốc trong giai đoạn 2011-2014 trên các chủng vi khuẩn E. coli và K. pneumoniae. mcr-1 chịu trách nhiệm mã hóa cho protein MCR-1, đây là một loại enzyme phosphoethanolamine transferase. Enzyme này chịu trách nhiệm gắn nhóm phosphoethanolamine vào LPS, và từ đó gây ra đề kháng với Polymyxin tương tự như các cơ chế đã được nêu ở trên (MCR-1 làm MIC của E. coli với kháng sinh tăng từ 4-8 lần). MCR-1 ngoài việc giúp vi khuẩn đề kháng với kháng sinh, nó còn giúp chúng đề kháng với cả lysozyme. Ở thời điểm hiện tại, vi khuẩn mang gene mcr-1 đã được phát hiện thấy trên toàn thế giới, đặc biệt là ở các Enterobacteriaceae như E. coli, Klebsiella, Enterobacter, Salmonella và Shigella.
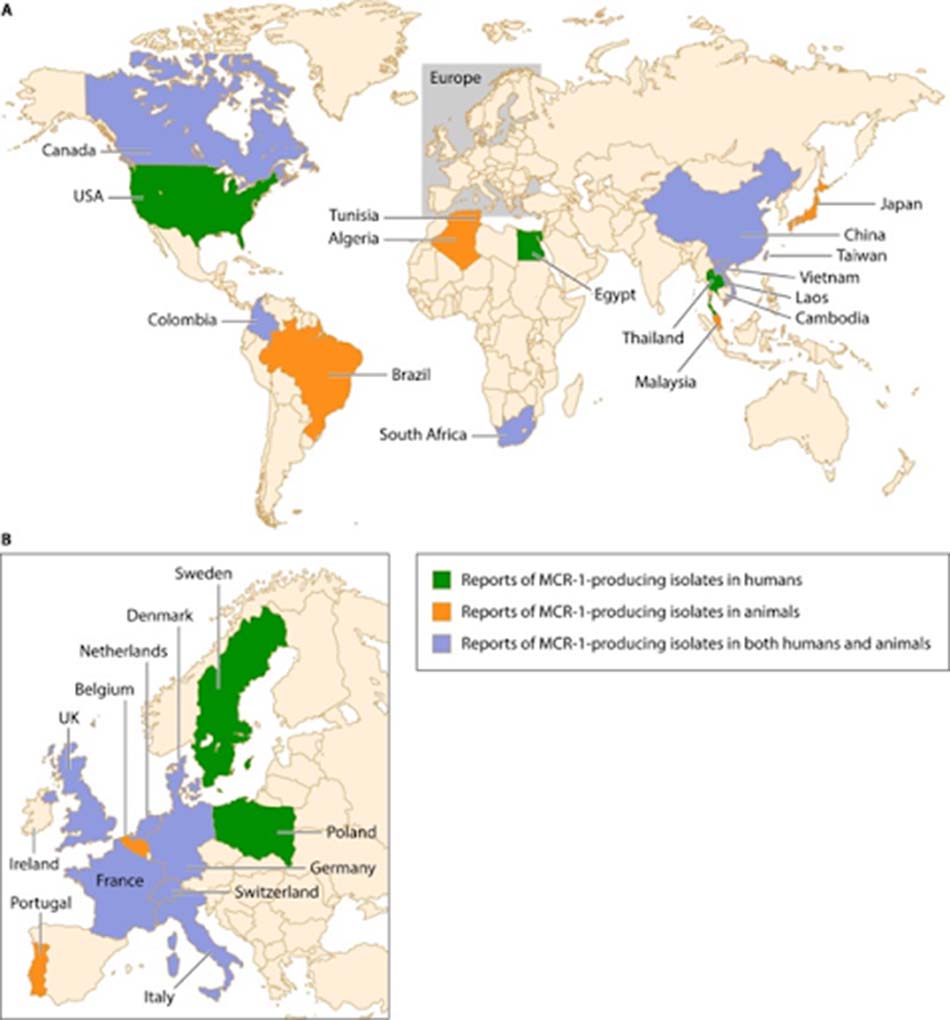
Có giả thuyết cho rằng, nguồn gốc của các vi khuẩn có gene mcr-1 này có thể bắt nguồn từ việc sử dụng kháng sinh thiếu hợp lý trong ngành chăn nuôi gia súc, đặc biệt là lợn. Sử dụng kháng sinh rộng rãi trên vật nuôi sẽ tạo ra áp lực chọn lọc cao, đẩy nhanh sự xuất hiện của các chủng vi khuẩn đề kháng. Ở một số vi khuẩn, gene mcr-1 tồn tại trên các plasmid đa kháng thuốc cùng một số gene kháng các nhóm kháng sinh khác, chẳng hạn như gene mã hóa các carbapenemase.
Ngoài ra, gene kháng Colistin qua trung gian plamid mcr-2 cũng đã được tìm thấy ở E. coli trên lợn con tại Bỉ, với 77% trình tự nucleotide giống với mcr-1.
Một số cơ chế khác đề kháng với các Polymyxin ở các chủng Enterobacteriaceae bao gồm: Sản xuất quá mức polysaccharide vỏ (CPS) có bản chất anion tạo thành hàng rào bảo vệ vi khuẩn, thông qua các kênh porin (S. enterica) và bơm tống thuốc (đột biến kpnEF và acrAB).
Ở P. aeruginosa, cơ chế đề kháng với các Polymyxin có liên quan đến ít nhất năm hệ thống hai thành phần làm thay đổi LPS, bao gồm PmrAB, PhoPQ, ParRS, ColRS và CprRS. Trong khi đó, A. baumannii đề kháng với kháng sinh theo hai cơ chế: Đột biến các gene pmrA và pmrB, từ đó điều hòa lên operon pmrCAB, làm tăng tổng hợp pEtN (không làm tăng tổng hợp L-Ara4N) hoặc đột biến các gene lpxA, lpxC và lpxD, từ đó làm thay đổi cấu trúc LPS.
– Cơ chế đề kháng với Daptomycin:
+ Bacillus subtilis: Hệ thống Lia được cảm ứng mạnh khi có mặt Daptomycin làm tăng khả năng chống chịu của vi khuẩn với kháng sinh. Khi loại bỏ operon liaIH, MIC của vi khuẩn với kháng sinh giảm đi, nhưng điều này không đúng với operon liaF. Cơ chế đề kháng này chỉ được nghiên cứu in vitro và không có nhiều ý nghĩa lâm sàng vì B. subtilis không phải là một vi khuẩn gây bệnh nguy hiểm. Cơ chế này có thể gây ra sự đề kháng chéo với Vancomycin và Bacitracin. Ở vi khuẩn có cơ chế đề kháng này, phosphatidylglycerol trong màng tế bào giảm rõ rệt. Ngoài ra, gene mprF cũng góp phần vào đề kháng với Daptomycin ở B. subtilis. Gene này chịu trách nhiệm mã hóa cho enzyme có khả năng lysinyl hóa phosphatidylglycerol, làm tăng cường sự tích điện dương của màng tế bào, từ đó làm giảm ái lực tương tác với Daptomycin.
+ S. aureus: Cơ chế đầy đủ của đề kháng Daptomycin ở tụ cầu vàng chưa hoàn toàn được hiểu đầy đủ. Tuy nhiên có một số cơ chế mà các nhà khoa học đã phát hiện ra. Cơ chế thứ nhất là thông qua gene mprF tương tự như B. subtilis. Cơ chế thứ hai xảy ra ở các tụ cầu vàng đề kháng trung gian với Vancomycin (VISA): Các chủng vi khuẩn này có độ dày thành tế bào gia tăng rõ rệt do sự điều hòa lên các tác nhân kích thích thành tế bào, cản trở hoạt động của Daptomycin. Hai cụm gene quan trọng liên quan đến sự đề kháng Daptomycin ở VISA là vraSR và yycFG (walKR). VraSR tương đương với LiaSR ở các vi khuẩn gram dương khác. Cơ chế thứ ba là thông qua sự tăng cường tổng hợp cardiolipin trên màng tế bào (gene cls mã hóa cho enzyme chịu trách nhiệm tổng hợp cardiolipin). Một gene khác cũng liên quan đến đề kháng Daptomycin thông qua thay đổi phospholipid màng là pgsA, gene này mã hóa cho CDP-diacylglycerol-glycerol-3-phosphate 3-phosphatidyltransferase. Cơ chế thứ tư liên quan đến một số yếu tố khác, ví dụ như gene tagA chịu trách nhiệm cho tổng hợp teichoic acid thành tế bào, hoặc cảm ứng plasmid ở MSSA làm tăng sản xuất staphyloxanthin (một sắc tố carotenoid làm cho S. aureus có màu vàng đặc trưng) dẫn đến tăng MIC của vi khuẩn với Daptomycin (staphyloxanthin ảnh hưởng đến tính lưu động màng tế bào), hay giảm hoạt động của chu trình Krebs, tăng hoạt động của con đường pentose phosphate và chuyển hóa purine/pyrimidine.
+ E. faecalis: Cơ chế đề kháng Daptomycin ở E. faecalis cũng có nhiều điểm tương tự như các vi khuẩn gram dương đã nới ở trên, bao gồm thành tế bào dày lên và làm tăng điện tích dương màng tế bào. Những thay đổi ở gene liaFSR là bước quan trọng đầu tiên tham gia vào cơ chế đề kháng. Một cơ chế đề kháng khác của vi khuẩn là thông qua các enzyme cardiolipin synthase (Cls, chịu trách nhiệm tổng hợp cardiolipin) và glycerol-phosphodiester phosphodiesterase (GdpD, chịu trách nhiệm luân chuyển glycerol để sinh tổng hợp phospholipid). Đột biến các gene cls và gdpD có thể gây ra đề kháng Daptomycin trên lâm sàng và chúng có thể cộng gộp tác dụng với nhau.
+ E. faecium: Cơ chế đề kháng Daptomycin ở E. faecium cũng có những điểm tương đồng với E. faecalis đã nói ở trên. Màng tế bào của vi khuẩn kháng Daptomycin có hàm lượng phosphatidylglycerol giảm rõ rệt trong khi cardiolipin thay đổi không đáng kể. Đột biến liaFSR là thay đổi phổ biến nhất ở các chủng kháng Daptomycin, trong đó thay đổi hay gặp nhất là ở LiaS (T120A) và LiaR (W73C). Đột biến gene yycFG hoặc cls cũng được tìm thấy ở chủng kháng hoặc dung nạp Daptomycin.
Dược động học
Hấp thu: Khi được sử dụng theo đường tĩnh mạch, các thuốc này không có quá trình hấp thu. Nếu sử dụng theo đường tiêm bắp, hấp thu nhanh và gần như hoàn toàn. Sử dụng thuốc theo đường hô hấp (Colistin) có tỷ lệ hấp thu vào máu rất thấp. Polymyxin B được sử dụng tại chỗ nên hầu như không có quá trình hấp thu.
Phân bố: Các kháng sinh lipopeptide đều có bản chất peptide thân nước nên phân bố tốt vào các dịch trong cơ thể và có thể tích phân bố (Vd) thấp. Khả năng vượt qua hàng rào máu não và hàng rào nhau thai kém. Colistin có tỷ lệ liên kết với protein huyết tương là 50%. Con số này ở Daptomycin là 92%.
Chuyển hóa: Trong cơ thể, không quá 20-25% lượng Colistimethate được chuyển hóa in vivo thành Colistin thông qua phản ứng thủy phân. Daptomycin hầu như không chuyển hóa.
Thải trừ: Phần lớn Colistimethate sẽ được thải trừ nhanh chóng qua thận. Không giống như Colistimethate, Colistin lại được thải trừ chủ yếu theo các con đường không qua thận bởi nó được tái hấp thu ở ống thận rất nhiều. Tuy Colistin được thải trừ qua thận kém, nồng độ Colistin trong nước tiểu vẫn khá cao do Colistimethate được chuyển dần thành Colistin trong đường tiết niệu. Daptomycin cũng được thải trừ chủ yếu qua thận (78%) với thời gian bán thải (t1/2) là 8 giờ.
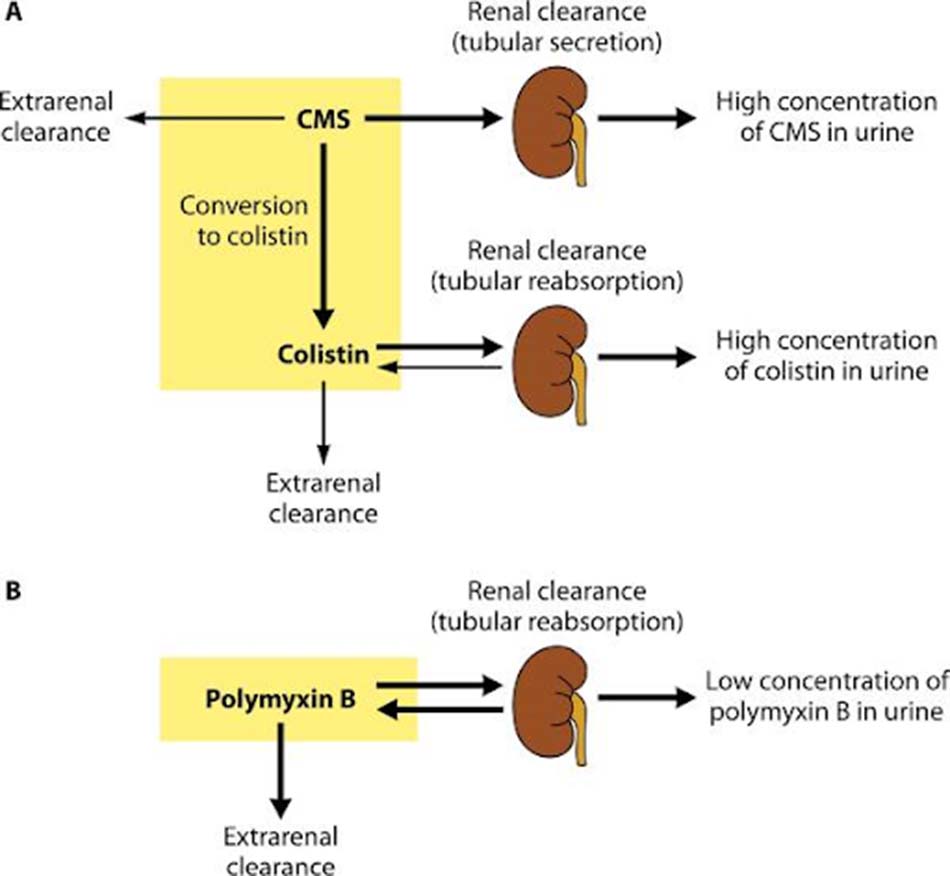
Ứng dụng dược động học/dược lực học (PK/PD) trong tối ưu hóa sử dụng thuốc
Colistin là kháng sinh diệt khuẩn phụ thuộc nồng độ. Trong thực tế lâm sàng điều trị các nhiễm khuẩn nặng do hai chủng vi khuẩn gram âm kháng thuốc nhiều nhất hiện nay là trực khuẩn mủ xanh P. aeruginosa và A. baumannii, thông số PK/PD quan trọng nhất, dự đoán tốt nhất hoạt động kháng khuẩn của Colistin là fAUC0-24/MIC (tỷ lệ của diện tích dưới đường cong nồng độ – thời gian của thuốc dạng tự do từ 0-24 giờ và nồng độ ức chế tối thiểu). Thông số này quan trọng hơn thông số Cmax/MIC (tỷ lệ của nồng độ thuốc tối đa trong huyết tương và nồng độ ức chế tối thiểu). Điều này cho thấy sự phơi nhiễm với Colistin trung bình theo thời gian quan trọng hơn việc cố gắng đạt được nồng độ thuốc cao trong máu. Để tối ưu hóa hoạt động kháng khuẩn cũng như giảm thiểu độc tính trên thận, với các chủng vi khuẩn có MIC ≤ 1 µg/mL, nồng độ Colistin trong huyết tương ở trạng thái cân bằng trung bình được đề xuất là 2 µg/mL. Các nhà lâm sàng cũng đã phát hiện tác dụng hậu kháng sinh (PAE) của Colistin với các chủng vi khuẩn K. pneumoniae, P. aeruginosa và A. baumannii.
Daptomycin cũng là kháng sinh diệt khuẩn phụ thuộc nồng độ. Thông số PK/PD quan trọng trong thực hành lâm sàng sử dụng Daptomycin là fAUC0-24/MIC và Cmax/MIC. Chế độ liều dùng 1 lần/ngày làm tăng hiệu lực và độ an toàn của Daptomycin. Daptomycin có thời gian bán hủy dài và PAE lên tới 6.8 giờ.
Tác dụng – Chỉ định của nhóm kháng sinh Lipopeptide
Tác dụng: Các kháng sinh Lipopeptide đều là các kháng sinh diệt khuẩn nhanh, mạnh và phụ thuộc nồng độ.
Colistin là kháng sinh cực kỳ quan trọng trong cuộc chiến của chúng ta chống lại các vi khuẩn gram âm đa kháng thuốc. Và vì nó được xem là kháng sinh mạnh nhất chống lại các vi khuẩn gram âm, đồng thời độc tính của kháng sinh này cũng rất lớn, Colistin chỉ được sử dụng khi các kháng sinh khác có ít độc tính hơn không còn hiệu quả (hay nói cách khác, Colistin chính là “giải pháp cuối cùng” trong điều trị các nhiễm trùng vi khuẩn gram âm nặng và đa kháng). Và điều quan trọng nhất cần lưu ý khi sử dụng kháng sinh này, đó là vi khuẩn có thể phát triển đề kháng ngay trong quá trình điều trị bằng Colistin đơn độc (còn gọi là hiện tượng dị kháng Colistin, với sự xuất hiện của một “quần thể con” các vi khuẩn đề kháng với Colistin, kể cả khi vi khuẩn nhạy cảm với Colistin [MIC ≤ 2 µg/mL] và nồng độ kháng sinh đạt tới 4 µg/mL). Ban đầu, số lượng vi khuẩn trong ổ nhiễm khuẩn có thể giảm rất nhanh, nhưng cũng rất nhanh sau đó, sự đề kháng xảy ra khiến cho số lượng vi khuẩn nhanh chóng tăng trở lại. Để khắc phục điều này, Colistin được sử dụng phối hợp với nhóm kháng sinh khác, cụ thể ở đây là các Carbapenem. Phối hợp này làm giảm đáng kể nguy cơ phát triển dị kháng trong quá trình điều trị bằng Colistin.
Chỉ định:
Colistin: Các nhiễm trùng nghiêm trọng như nhiễm khuẩn huyết, viêm màng não (tiêm vào dịch não tủy), viêm phổi (có thể sử dụng theo đường hô hấp) … do các chủng vi khuẩn còn nhạy cảm.
Polymyxin B: Các nhiễm trùng ngoài ra, nhiễm trùng tai ngoài hoặc mắt… do các chủng vi khuẩn còn nhạy cảm.
Daptomycin: Du khuẩn huyết do tụ cầu vàng, cụ thể là viêm nội tâm mạc nhiễm trùng bên phải (do MRSA hoặc MSSA) và nhiễm trùng da và cấu trúc da cấp tính (do các chủng nhạy cảm: MRSA, MSSA, S. pyogenes, S. agalactiae, S. dysgalactiae subsp equisimilis và E. faecalis nhạy cảm Vancomycin).
Cách dùng – Liều dùng
Colistin:
Liều tính theo Colistin dạng base: 2.5-5 mg/kg/ngày chia ra mỗi 6 hoặc 12 giờ tiêm bắp (IM) hoặc tĩnh mạch (IV).
Với bệnh nhân suy giảm chức năng thận:
- Khi thanh thải creatinine (ClCr) 50-79 mL/phút: 2.5-3.8 mg/kg/ngày IV/IM chia ra mỗi 12 giờ.
- Khi ClCr 30-49 mL/phút: 2.5 mg/kg/ngày IV/IM 1 lần/ngày hoặc chia ra mỗi 12 giờ.
- Khi ClCr 10-29 mL/phút: 1.5 mg/kg IV/IM mỗi 36 giờ.
Daptomycin:
Du khuẩn huyết do tụ cầu vàng: 6 mg/kg truyền IV mỗi 24 giờ trong 2-6 tuần. Nếu ClCr < 30 mL/phút, truyền IV 6 mg/kg mỗi 48 giờ.
+ Nhiễm trùng da và cấu trúc da cấp tính: 4 mg/kg truyền IV mỗi 24 giờ trong 7-14 ngày. Nếu ClCr < 30 mL/phút, truyền IV 4 mg/kg mỗi 48 giờ.
Polymyxin B: Do sử dụng tại chỗ nên không thể xác định chính xác được liều của thuốc.
Tác dụng không mong muốn
Colistin: Dị cảm, chóng mặt, ngứa ở đầu chi, đầu lưỡi, độc với thận và hệ thần kinh, có thể gây suy hô hấp cấp.
Polymyxin B: Dị ứng, mày đay là chủ yếu.
Daptomycin: Mất ngủ, đau họng, đau ngực, đau bụng, tiêu chảy, tăng creatine phosphokinase (CK) trong máu (có nguy cơ gây tiêu cơ vân), các phản ứng dị ứng từ nhẹ đến nặng…
Chống chỉ định
Quá mẫn cảm với bất cứ thành phần nào của thuốc.
Tương tác thuốc
Colistin:
+ Phối hợp với các thuốc khác có độc tính trên thận và thần kinh – cơ (Amphotericin B, kháng sinh nhóm Aminoside, lợi tiểu quai Furosemide, Cisplatin…) hoặc các thuốc giãn cơ (Atracurium, Pancuronium, Rapacuronium…): Tăng nguy cơ gặp phải các độc tính trên thận và thần kinh. Phối hợp như thế này nhìn chung nên tránh, trừ khi tình trạng nhiễm khuẩn của bệnh nhân bắt buộc phải sử dụng Colistin.
+ Colistin cho tác dụng hiệp đồng với các kháng sinh diệt khuẩn khác, bao gồm các kháng sinh ức chế tổng hợp thành tế bào (nhóm β-lactam, điển hình là các Carbapenem và nhóm Glycopeptide) và kháng sinh nhóm Aminoside. Phối hợp Colistin với các kháng sinh nhóm Quinolone đôi khi cũng được sử dụng trên lâm sàng.
Daptomycin:
+ Phối hợp với vaccin tả: Nên tránh phối hợp này do tác dụng của vaccin có thể giảm đi. Không tiêm vaccin tả cho bệnh nhân đã dùng kháng sinh trong vòng 14 ngày gần đây nhất.
+ Phối hợp với các statin (Simvastatin, Atorvastatin, Lovastatin…): Tăng nguy cơ gặp phải tiêu cơ vân do hiệp đồng dược lực học. Phối hợp này nên được theo dõi cẩn thận.
+ Phối hợp với Tobramycin: Sau phối hợp một liều duy nhất, nồng độ Tobramycin giảm và nồng độ Daptomycin tăng lên. Cơ chế chưa rõ. Nên thận trọng với phối hợp này.
+ Phối hợp với các kháng sinh nhóm Aminoside, β-lactam hoặc Glycopeptide: Hiệp đồng dược lực học. Cũng có thể phối hợp Daptomycin với các kháng sinh nhóm Quinolone.
Polymyxin B: Thường được sử dụng phối hợp trong các chế phẩm dùng đường tại chỗ với kháng sinh nhóm Aminoside (Neomycin, Tobramycin, Gentamicin), thuốc kháng nấm (Clotrimazole, Ketoconazole, Nystatin) hoặc corticoid (Dexamethasone, Betamethasone).
Lưu ý và thận trọng khi sử dụng thuốc
Colistin:
+ Ngưng sử dụng thuốc nếu BUN (nitrogen urea máu) hoặc creatinine tăng cao (đây có thể là dấu hiệu của suy thận). Liều tối đa 5 mg/kg/ngày.
+ Không sử dụng thuốc cho các nhiễm trùng do Proteus hoặc Neisseria do hầu hết các chủng này đều kháng thuốc.
+ Colistin có nguy cơ gây viêm đại tràng giả mạc do C. difficile.
+ Rất thận trọng với bệnh nhân nhược cơ, hoặc đang dùng các thuốc ức chế thần kinh – cơ do làm tăng nguy cơ suy hô hấp.
Daptomycin:
+ Ngừng thuốc ngay nếu bệnh nhân gặp phải phản ứng phản vệ hoặc viêm phổi tăng bạch cầu ái toan và điều trị thích hợp (Adrenaline và Corticoid toàn thân tương ứng).
+ Không sử dụng cho bệnh nhi dưới 12 tháng tuổi.
+ Daptomycin cũng có nguy cơ gây viêm đại tràng giả mạc do C. difficile.
+ Daptomycin có khả năng gây ra bệnh cơ cũng như tiêu cơ vân: Thận trọng ở những bệnh nhân mắc các bệnh lý thần kinh ngoại biên hoặc bệnh cơ. Ngừng sử dụng thuốc ngay khi nồng độ CK > 2000 U/L hoặc CK > 1000 U/L và có triệu chứng của bệnh cơ. Nên cân nhắc việc tạm ngừng các statin (cũng có khả năng gây tiêu cơ vân) trong quá trình điều trị bằng Daptomycin.
Nếu trong quá trình điều trị, bệnh nhân mắc phải viêm đại tràng giả mạc do C. difficile, cần ngừng ngay thuốc đang điều trị và chuyển sang điều trị nhiễm trùng C. difficile bằng Metronidazole, Vancomycin đường uống hoặc Fidaxomicin, đồng thời bổ sung nước, protein và điện giải phù hợp cho bệnh nhân, có thể phẫu thuật nếu cần.
Sử dụng thuốc trên đối tượng đặc biệt
Bệnh nhân suy giảm chức năng gan thận: Có thể cần hiệu chỉnh liều cho bệnh nhân suy giảm chức năng thận. Mức liều giảm căn cứ theo ClCr của bệnh nhân. Bệnh nhân suy giảm chức năng gan không cần hiệu chỉnh liều.
Người già và trẻ em: Có thể cần hiệu chỉnh liều cho các đối tượng này do chức năng thận của người già thường suy giảm, còn của trẻ em, đặc biệt là trẻ sơ sinh, thường chưa hoàn thiện.
Phụ nữ có thai và đang cho con bú: Phân loại an toàn trong thai kỳ của Colistin là C. Daptomycin không có đầy đủ dữ liệu. Chỉ sử dụng Colistin và Daptomycin cho phụ nữ có thai khi lợi ích đạt được là vượt trội so với rủi ro. Polymyxin B chỉ dùng theo đường tại chỗ nên có thể sử dụng cho phụ nữ mang thai. Colistin và Polymyxin B không có dữ liệu về nồng độ thuốc trong sữa mẹ, còn Daptomycin có thể vào trong sữa mẹ với lượng bằng 0.1% liều dùng. Sử dụng các kháng sinh này cho phụ nữ đang cho con bú thận trọng.
Một số nghiên cứu và thử nghiệm lâm sàng
– Phân tích gộp đánh giá hiệu lực và an toàn của điều trị bằng Colistin trong nhiễm trùng phổi do P. aeruginosa hoặc A. baumannii cho kết luận: Colistin có thể có hiệu lực và an toàn tương đương liệu pháp kháng sinh tiêu chuẩn trong điều trị nhiễm trùng phổi do hai chủng vi khuẩn trên.
– Phân tích ghép cặp đánh giá hiệu lực và an toàn của Colistin trong điều trị các nhiễm trùng gây ra bởi các chủng P. aeruginosa đa kháng ở những bệnh nhân có bệnh lý huyết học ác tính đưa ra kết luận: Colistin có hiệu quả trong điều trị các nhiễm trùng nặng do các chủng trực khuẩn mủ xanh đa kháng gây ra, với độc tính ở mức chấp nhận được.
– Nghiên cứu thuần tập so sánh đánh giá hiệu lực của Colistin dạng hít bổ trợ cho Colistin IV trong điều trị viêm phổi thở máy cho kết quả: Kết quả của những bệnh nhân sử dụng Colistin dạng hít kết hợp với Colistin IV tốt hơn những bệnh nhân chỉ sử dụng Colistin IV, tuy nhiên không có sự khác biệt về tỷ lệ tử vong nội viện cũng như ICU (đơn vị chăm sóc tích cực) do mọi nguyên nhân giữa hai nhóm.
– Thử nghiệm lâm sàng đánh giá an toàn và hiệu lực của Daptomycin trong điều trị nhiễm trùng da và cấu trúc da cấp tính (cSSSI) cho kết luận: Daptomycin với liều 4 mg/kg/ngày có an toàn và hiệu quả tương đương liệu pháp tiêu chuẩn trong điều trị cSSSI gây ra bởi các vi khuẩn gram dương.
– Thử nghiệm lâm sàng so sánh Daptomycin với liệu pháp tiêu chuẩn trong điều trị du khuẩn huyết và viêm nội tâm mạc do S. aureus đưa ra kết luận: Daptomycin với liều 6 mg/kg/ngày không thua kém liệu pháp tiêu chuẩn trong điều trị du khuẩn huyết và viêm nội tâm mạc bên phải do tụ cầu vàng.
Tài liệu tham khảo
Landman D, Georgescu C, Martin DA, Quale J. Polymyxins revisited. Clin Microbiol Rev. 2008;21(3):449-465. doi:10.1128/CMR.00006-08.
Available at https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2493081/
Poirel L, Jayol A, Nordmann P. Polymyxins: Antibacterial Activity, Susceptibility Testing, and Resistance Mechanisms Encoded by Plasmids or Chromosomes. Clin Microbiol Rev. 2017;30(2):557-596. doi:10.1128/CMR.00064-16.
Available at https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5355641/
Steenbergen JN, Alder J, Thorne GM, Tally FP. Daptomycin: a lipopeptide antibiotic for the treatment of serious Gram-positive infections. J Antimicrob Chemother. 2005 Mar;55(3):283-8. doi: 10.1093/jac/dkh546.
Available at https://academic.oup.com/jac/article/55/3/283/758329
Tran TT, Munita JM, Arias CA. Mechanisms of drug resistance: daptomycin resistance. Ann N Y Acad Sci. 2015;1354:32-53. doi:10.1111/nyas.12948.
Available at https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4966536/
Zhang H, Zhang Q. Clinical efficacy and safety of colistin treatment in patients with pulmonary infection caused by Pseudomonas aeruginosa or Acinetobacter baumannii: a meta-analysis. Arch Med Sci. 2015;11(1):34-42. doi:10.5114/aoms.2015.48158.
Available at https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4379367/
Durakovic N, Radojcic V, Boban A, Mrsic M, Sertic D, Serventi-Seiwerth R, Nemet D, Labar B. Efficacy and safety of colistin in the treatment of infections caused by multidrug-resistant Pseudomonas aeruginosa in patients with hematologic malignancy: a matched pair analysis. Intern Med. 2011;50(9):1009-13. doi: 10.2169/internalmedicine.50.4270.
Available at https://pubmed.ncbi.nlm.nih.gov/21532223/
Arbeit RD, Maki D, Tally FP, Campanaro E, Eisenstein BI; Daptomycin 98-01 and 99-01 Investigators. The safety and efficacy of daptomycin for the treatment of complicated skin and skin-structure infections. Clin Infect Dis. 2004 Jun 15;38(12):1673-81. doi: 10.1086/420818.
Available at https://academic.oup.com/cid/article/38/12/1673/303768
Fowler VG Jr, Boucher HW, Corey GR, Abrutyn E, Karchmer AW, Rupp ME, Levine DP, Chambers HF, Tally FP, Vigliani GA, Cabell CH, Link AS, DeMeyer I, Filler SG, Zervos M, Cook P, Parsonnet J, Bernstein JM, Price CS, Forrest GN, Fätkenheuer G, Gareca M, Rehm SJ, Brodt HR, Tice A, Cosgrove SE; S. aureus Endocarditis and Bacteremia Study Group. Daptomycin versus standard therapy for bacteremia and endocarditis caused by Staphylococcus aureus. N Engl J Med. 2006 Aug 17;355(7):653-65. doi: 10.1056/NEJMoa053783.
Available at https://www.nejm.org/doi/full/10.1056/NEJMoa053783
Korbila IP, Michalopoulos A, Rafailidis PI, Nikita D, Samonis G, Falagas ME. Inhaled colistin as adjunctive therapy to intravenous colistin for the treatment of microbiologically documented ventilator-associated pneumonia: a comparative cohort study. Clin Microbiol Infect. 2010 Aug;16(8):1230-6. doi: 10.1111/j.1469-0691.2009.03040.x.
Available at https://pubmed.ncbi.nlm.nih.gov/19732088/
Tham khảo thêm: