Bài viết Liệu pháp tăng thông khí để kiểm soát tăng áp lực nội sọ sau chấn thương được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Hyperventilation Therapy for Control of Posttraumatic Intracranial Hypertension
Tóm tắt
Trong chấn thương sọ não, tăng áp lực nội sọ (ICH, intracranial hypertension) có thể trở thành một tình trạng đe dọa tính mạng nếu nó không được xử trí nhanh chóng và đầy đủ. Các bác sĩ sử dụng phương pháp điều trị tăng thông khí để giảm áp lực nội sọ (ICP, intracranial pressure) bằng cách điều khiển các chức năng tự điều hòa liên kết đáp ứng với CO2 của mạch máu não. Gây giảm CO2 máu thông qua tăng thông khí làm giảm áp lực một phần của carbon dioxide động mạch (PaCO2), gây ra co mạch trong các tiểu động mạch đề kháng của não (cerebral resistance arterioles). Sự co thắt này làm giảm lưu lượng máu não, làm giảm thể tích máu não và cuối cùng, làm giảm ICP của bệnh nhân. Tác dụng của tăng thông khí trị liệu (HV, therapeutic hyperventilation) là thoáng qua, nhưng những nguy cơ đi kèm với những thay đổi này trong sinh lý não và hệ thống phải được xem xét cẩn thận trước khi điều trị có thể được khuyến nghị. Những chỉ trích nổi bật nhất của phương pháp này là khả năng bị thiếu máu não và thiếu oxy mô. Mặc dù đúng là các biện pháp nhất định, như theo dõi oxy hóa não, là cần thiết để giảm thiểu các tình trạng nguy hiểm này, sử dụng bằng chứng có sẵn về kết quả kém tiềm năng liên quan đến HV như biện minh để bác bỏ việc thực hiện HV trị liệu vẫn còn gây tranh cãi giữa các bác sĩ. Tổng quan này nhấn mạnh các vấn đề khác nhau xung quanh việc sử dụng HV như một biện pháp kiểm soát ICH sau chấn thương, bao gồm chỉ định điều trị, nguy cơ tiềm ẩn và lợi ích, và thảo luận về những kỹ thuật nào có thể được thực hiện để tránh các biến chứng bất lợi.
Giới thiệu
Các bác sĩ bắt đầu khám phá sự tăng thông khí (HV, hyperventilation) như một cách để giảm thể tích máu não (CBV, cerebral blood volume) trong những năm 1920 (1). Một trong những mô tả sớm nhất được ghi nhận về phương pháp điều trị này có từ năm 1959, khi Lundberg báo cáo việc sử dụng HV để giảm mức độ tăng áp lực nội sọ (ICP, intracranial pressure) (2). HV gây co mạch máu động mạch, dẫn đến giảm lưu lượng máu não (CBF, cerebral blood flow) và do đó, làm giảm CBV (3-5). Thời gian trôi qua, liệu pháp dễ thực hiện này đã được sử dụng rộng rãi để kiểm soát tăng áp lực nội sọ (ICH, intracranial hypertension) thứ phát sau chấn thương sọ não nặng (sTBI, severe traumatic brain injury) (6-8). Vào giữa những năm 1990, tại các trung tâm phẫu thuật thần kinh ở Hoa Kỳ và Vương quốc Anh, tỷ lệ sử dụng HV lần lượt là 83 và 97% (6, 7). Một phân tích cơ sở dữ liệu châu Âu được công bố vào năm 2008 chỉ ra rằng trong 24 giờ đầu tiên sau khi bị tổn thương, các bác sĩ đã sử dụng HV dự phòng trong hơn một nửa các trường hợp TBI của họ (9).
Mặc dù HV làm giảm nhanh chóng và hiệu quả ICP, nhưng hiệu quả chỉ là nhất thời và không liên quan đến việc cải thiện kết quả bệnh nhân cuối cùng (10, 11). Bởi vì HV có khả năng có thể kích hoạt các tổn thương thiếu máu não thứ phát và tạo ra hậu quả bất lợi ảnh hưởng đến các hệ cơ quan khác, và liệu pháp này vẫn là một chủ đề tranh cãi và tranh luận mạnh mẽ (10, 11). Bằng chứng sẵn có chỉ ra rằng HV dự phòng mức độ cao hoặc kéo dài là bất lợi và nên tránh, đặc biệt là trong giai đoạn cấp tính của sTBI; tuy nhiên, liệu pháp này vẫn được khuyến nghị như một cách để tạm thời xử trí mức độ đe dọa tính mạng của ICP (12). Mục tiêu của tổng quan này là cung cấp một bản cập nhật đánh giá các nghiên cứu hiện tại mô tả HV về kiểm soát ICP để xác định xem HV có vai trò trong việc kiểm soát chấn thương não cấp tính hay không.
Sinh lý CO2: Các khái niệm cơ bản
Tăng thông khí dẫn đến tăng thông khí phế nang (AV, alveolar ventilation) (13, 14), thể tích phút đi vào vùng hô hấp (phế quản, phế nang, v.v.) cũng có sẵn để trao đổi khí (13). Do một phần của thể tích đó vẫn nằm trong khu vực mà khí không khuếch tán vào máu, AV có thể được xác định theo phương trình sau (13):
AV = RR × (VT – VD)
Thông khí phế nang có mối quan hệ nghịch đảo với mức CO2 phế nang; khi AV tăng, nồng độ CO2 phế nang giảm (13, 14). Tuy nhiên, CO2 phế nang có mối liên hệ trực tiếp với áp suất riêng phần của CO2 động mạch (PaCO2), phản ánh sự cân bằng giữa sản xuất và loại bỏ CO2 (13, 14):
PaCO2 = CO2 sản xuất – CO2 loại bỏ.
Sản xuất CO2 của tế bào của bệnh nhân có thể phụ thuộc vào một số biến số, bao gồm chế độ ăn uống, tập thể dục, nhiệt độ và hoạt động của hormone (tuyến giáp) (13). Sản xuất CO2 vẫn tương đối ổn định và không đổi, ngoại trừ trong các trạng thái tăng chuyển hóa nghiêm trọng. Nếu vận chuyển CO2 và cung lượng tim không thay đổi, nồng độ PaCO2 sẽ được xác định ngược lại bằng tốc độ loại bỏ CO2 thông qua AV (13).
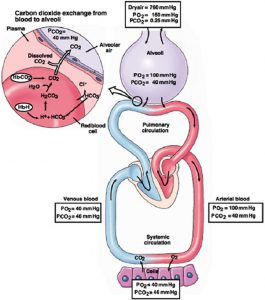
CO2 là một loại khí hòa tan và khuếch tán được vận chuyển theo ba cách khác nhau: 10- 15% trong số đó được hòa tan theo PaCO2 (Luật Henry); 20-30% của nó liên kết với protein huyết tương và huyết sắc tố tạo thành phức hợp carbaminic và 65-70% được chuyển thành axit bicarbonate/carbonic trong hồng cầu và huyết tương (13). Đáp ứng phức tạp thứ ba này giúp duy trì trạng thái cân bằng giữa bicarbonate và các ion hydro (H+) (13, 14) (Hình1).
Giá trị PaCO2 bình thường dao động trong khoảng 35 đến 45 mmHg (4,7-6 kPa) ở nhiệt độ cơ thể bình thường và ở mực nước biển với áp suất khí quyển là 760 mmHg (13, 14).
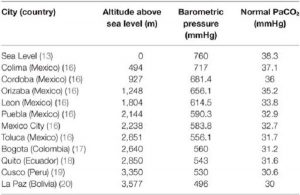
Nếu nhiệt độ cơ thể giảm, độ hòa tan của CO2 tăng và PaCO2, giảm (13, 15). PaCO2 giảm 4,5% cho mỗi mức giảm nhiệt độ C. Điều ngược lại xảy ra khi nhiệt độ tăng (Bảng 1) (15). Ở độ cao cao hơn, áp suất khí quyển giảm, kích thích AV, do đó mức PaCO2 bình thường thấp hơn (Bảng 2) (16-20).
![Bảng 1 Sửa đổi giá trị PaCO2 bình thường theo sự thay đổi của nhiệt độ trung tâm ([ref] 15).](https://www.healcentral.org/wp-content/uploads/2020/09/lieu_phap_tang_thong_khi_de_kiem_soat_tang_ap_luc_noi_so_sau_chan_thuong_2-300x160.jpg)
Những thay đổi về sinh lý não trong quá trình giảm PaCO2
Não là một trong những cơ quan hoạt động chuyển hóa mạnh nhất trong toàn bộ cơ thể. Bởi vì nó thiếu dự trữ oxy và glucose, hai chất dinh dưỡng rất quan trọng để duy trì hoạt động hóa lý mạnh mẽ, điều quan trọng là não phải có một số hệ thống cung cấp liên tục mà qua đó các chất nền này có thể được nhận (21). Hệ thống phân phối này xảy ra thông qua CBF. CBF rất quan trọng đến mức não bộ đã phát triển các cơ chế thích nghi để duy trì dòng chảy đầy đủ và liên tục mặc dù có sự thay đổi về các biến số sinh lý hoặc yêu cầu chuyển hóa (21-23). Việc duy trì CBF được gọi là tự điều hòa não bộ (“cerebral autoregulation”), và được thực hiện chủ yếu bởi các tiểu động mạch đề kháng (22-23). Bằng cách làm giãn hoặc co để đáp ứng với những thay đổi về huyết áp, độ nhớt, khí máu và nhu cầu chuyển hóa, các tiểu động mạch có thể điều chỉnh CBF (22, 23).
Lưu lượng máu não
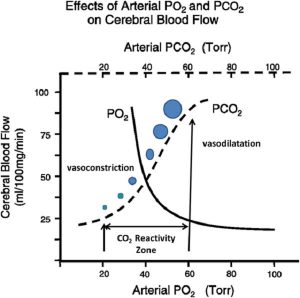
Khả năng đáp ứng của CO2 là khả năng đề kháng động mạch não có thể giãn nở hoặc co lại để đáp ứng với những thay đổi trong PaCO2. Sự giãn nở xảy ra khi PaCO2 tăng (PaCO2 > 44 mmHg biểu thị tăng PaCO2 máu, hypercapnia); các mạch máu co lại nếu mức PaCO2 giảm (PaCO2 <35 mmHg biểu thị giảm PaCO2 máu, hypocapnia) (3- 5, 10, 11). Tuy nhiên, hoạt động mạch máu này chỉ xảy ra trong phạm vi 20-60 mmHg của PaCO2 (24). Đường kính của các mạch máu sẽ không thay đổi nếu mức PaCO2 tăng lên trên hoặc giảm xuống dưới ngoài phạm vi cụ thể đó. Do những hạn chế này, khi được vẽ trên đồ thị, đường cong tự động mô tả CBF theo sự dịch chuyển PaCO2 giống như một hàm sigmoid (Hình 2) (4, 25).
Những thay đổi trong đường kính mạch máu được gây ra bởi hypocapnia so với những thay đổi được gây ra bởi hypercapnia không tỷ lệ thuận (5). Nếu PaCO2 tăng lên 80 mmHg, sự giãn mạch sẽ tăng CBF thêm 100-200%, gây ra sự giải phóng catecholamine và tăng hoạt động chuyển hóa. Mặt khác, cứ mỗi milimét thủy ngân mà PaCO2 giảm, CBF sẽ giảm 3%; do đó, mức PaCO2 trong khoảng từ 20 đến 25 mmHg có liên quan đến việc giảm CBF 40-50% (5, 24).
Các tiểu động mạch của pial chịu trách nhiệm cho những trường hợp giãn nở và co lại này có đường kính nhỏ hơn 50 μm. Nội mạc mạch máu đáp ứng với những thay đổi pH xảy ra trong khoảng quanh mạch máu bằng cách giải phóng các chất trung gian điều hòa nội mô và cơ trơn mạch máu (5, 26). Các yếu tố vận mạch này được cho là bao gồm oxit nitric, prostaglandin, nucleotide tuần hoàn, kali và canxi (5).
Lưu lượng máu não thường không đồng nhất; nó thay đổi theo tốc độ chuyển hóa và hoạt động của từng vùng (27). Đáp ứng mạch máu não với CO2 cũng có thể khác nhau, tùy thuộc vào vị trí hoặc hoàn cảnh (28). Trong sTBI, đặc biệt là trong vài giờ đầu tiên, đáp ứng CO2 bị thái quá hơn, đặc biệt là ở các khu vực tiếp giáp với các vùng dập não hoặc tụ máu dưới màng cứng (29- 32). Vì những lý do này, những thay đổi về mức độ bình thường của CO2 là những tổn thương thứ cấp nguy hiểm tiềm tàng có thể ảnh hưởng mạnh đến sinh lý não (11).
Thể tích máu não
Ở người trưởng thành, CBV bình thường là 3-4 ml trên 100 g mô nhu mô (5). Mặc dù những thay đổi về đường kính của các mạch máu não có thể làm thay đổi tổng CBV, nhưng 70% tổng lượng máu chứa trong não tương ứng với hệ thống tĩnh mạch (33, 34). Do các tĩnh mạch và mao mạch không đáp ứng với sự dao động của PaCO2, nên bất kỳ thay đổi nào trong CBV sau các sự cố của hypercapnia hoặc hypocapnia chỉ có thể được quy cho sự thay đổi về thể tích máu động mạch (33, 34). Người ta ước tính rằng HV làm giảm CBV khoảng 0,049 ml/100 g trên mỗi milimet giảm CO2 thủy ngân (5). Nếu chỉ có 30% tổng số CBV nằm trong các động mạch và chỉ các mạch pial đáp ứng với những thay đổi trong PaCO2, thì việc giảm CBF do giảm hypocapnia là 30% sẽ chỉ khiến CBV giảm 7% (35). Theo cách này, việc giảm CO2 rõ rệt có thể tạo ra sự sụt giảm đáng kể về CBF, nhưng ít ảnh hưởng đến CBV và ICP tương ứng (35). Có ý kiến cho rằng đáp ứng của CBV đối với hypocapnia sẽ giảm hơn nữa khi hạ huyết áp động mạch, đặc biệt khi phạm vi huyết áp động mạch trung bình (MABP, mean arterial blood pressure) giảm từ 154 xuống còn 114 mmHg (5).
Áp lực nội sọ
Theo giả thuyết Monro-Kellie, những thay đổi trong CBV sẽ tạo ra những thay đổi ICP chỉ sau khi các cơ chế bù trừ khoảng trống (spatial compensatory mechanisms) bị cạn kiệt (10, 11, 14). Các cơ chế bù trừ này bao gồm những thay đổi trong dịch não tủy (CSF, cerebrospinal fluid) và lượng máu chủ yếu thông qua việc tăng trở lại tĩnh mạch cho tim và lệch CSF vào kênh cột sống. Hypercapnia kích hoạt sự giãn mạch, dẫn đến tăng CBV và tăng ICP sau đó; hypocapnia gây ra co mạch, dẫn đến giảm CBV và giảm ICP sau đó (10, 11, 14). HV là một liệu pháp sử dụng các điều kiện của hypocapnia để kích hoạt co mạch trong các tiểu động mạch đề kháng trong nhu mô não để giảm ICP. Làm điều này sẽ sửa đổi giá trị tuyệt đối và hình thái của sóng xung ICP bằng cách giảm thành phần P2 (sóng thủy triều) (36).
Chuyển hóa não
Hypocapnia làm tăng hoạt động chuyển hóa của não thông qua các cơ chế khác nhau. Nó gây ra sự giải phóng các axit amin kích thích (N- Methyl-d-aspartate và glutamate) và làm tăng tính kích thích thần kinh, tiêu thụ glucose và tốc độ chuyển hóa của O2 (CMRO2) (11, 14). Nó cũng làm mạnh và kéo dài hoạt động co giật (11, 14).
Oxygen hóa não
Tình trạng thiếu oxy xảy ra khi cơ thể hoặc một vùng cụ thể của cơ thể không nhận được hoặc không thể xử lý một lượng oxy thích hợp để đáp ứng nhu cầu chuyển hóa của nó (37- 39). Thiếu oxy mô có thể là cục bộ hoặc toàn thể, nhưng cả hai biến thể đều có thể được phát hiện bằng cách sử dụng theo dõi não ở đầu giường để đo áp lực mô của O2 (ptiO2, tissular pressure of O2) hoặc độ bão hòa tĩnh mạch của O2 trong tĩnh mạch cảnh (SvjO2) (40). Có bốn con đường khác nhau mà qua đó hypocapnia có thể gây ra hoặc góp phần vào tình trạng thiếu oxy mô (37-39):
- Sự co mạch do hypocapnia mang lại có thể làm giảm CBF, dẫn đến tình trạng thiếu oxy máu thiếu máu cục bộ (“ischemic hypoxia”) (3, 5, 10, 11, 14).
- Việc giảm nồng độ carbon dioxide có thể làm giảm trao đổi khí trong phổi, kích hoạt tình trạng thiếu oxy mô do thiếu oxy (“hypoxemic hypoxia”) (10, 11).
- Đường cong phân ly oxy oxy hemoglobin (Hgb) có thể dịch chuyển sang trái do hypocapnia, làm tăng ái lực của Hgb đối với O2 và cản trở sự giải phóng O2 vào các tế bào còn được gọi là hypoxia ái lực cao (“high affinity hypoxia”) (10, 11).
- Tăng tính hưng phấn thần kinh và chuyển hóa não do hypocapnia mang lại làm tăng nhu cầu chuyển hóa, dẫn đến thiếu oxy (11, 14).
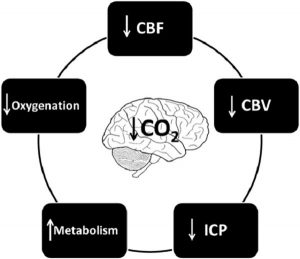
Những thay đổi khác nhau mà hypocapnia gây ra liên quan đến sinh lý não được mô tả trong Hình 3.
Tác dụng toàn thân của Hypocapnia
Tác động hypocapnia ảnh hưởng đến tất cả các hệ thống cơ quan (10, 11, 14). Khi đánh giá hypocapnia cho sử dụng HV điều trị, người ta cũng nên tính đến ảnh hưởng của thở máy (10, 11, 41, 42). Bởi vì bệnh nhân bị sTBI có thể đồng thời xuất hiện các tổn thương bị dập trong nhu mô phổi, các vi hít sặc dịch dạ dày hoặc hội chứng suy hô hấp cấp tính (ARDS), họ có thể yêu cầu thông khí bảo vệ với VT thấp và PEEP cao (10, 11, 41, 42). HV trị liệu đạt được bằng cách tăng RR hoặc VT. Tăng VT có thể gây bất lợi vì sự căng thẳng (stress) mà nó đặt lên cơ thể; nó gây ra sự kéo căng phế nang, gây ra sự giải phóng cytokine và yếu tố gây viêm cả cục bộ và hệ thống (10, 11, 41-43).
Hypocapnia làm giảm tưới máu đến mô thận, mô tiêu hóa và mô da và cơ xương; nó cũng gây ra sự gia tăng sự kết dính và kết tập tiểu cầu (10, 11, 14). Nồng độ PaCO2 thấp kích thích co thắt phế quản, làm giảm co mạch phổi do thiếu oxy, ức chế sản xuất chất hoạt động bề mặt và tăng tính thấm của màng phế nang và đường dẫn khí trên (11, 14). Một số biến số có thể làm ảnh hưởng đến trao đổi khí và làm tăng tính nhạy cảm của bệnh nhân đối với các bệnh nhiễm trùng. Chúng bao gồm: xẹp phổi, phù phổi, giảm độ giãn nở, thay đổi cơ chế bảo vệ phổi, thay đổi tỷ lệ thông khí/tưới máu và thay đổi tỷ lệ shunt (11, 14). Nhiễm kiềm hô hấp (rối loạn cân bằng axit/bazơ liên quan đến giảm nồng độ kali, canxi và phốt phát trong huyết tương) làm biến chứng oxy hóa mô bằng cách dịch chuyển đường cong phân ly O2/Hgb sang trái (10, 11).
Hypocapnia gây ra co mạch gây tổn thương lưu lượng máu mạch vành và làm tăng nguy cơ co thắt mạch vành. Nó cũng làm tăng nhu cầu chuyển hóa của cơ tim, có thể làm tăng nguy cơ bệnh nhân mắc bệnh thiếu máu cơ tim. Điều này đặc biệt đúng nếu bệnh nhân có các yếu tố ảnh hưởng hoặc có tiền sử bệnh tim (10, 11, 14). Hypocapnia cũng thúc đẩy chấn thương tái tưới máu và thúc đẩy sự phát triển của loạn nhịp tim, đặc biệt là rung nhĩ (11).
Hypocapnia và độc tính thần kinh
Nồng độ PaCO2 thấp tạo ra tác dụng gây độc thần kinh bằng cách tạo ra sự giải phóng các axit amin kích thích gây độc tế bào, làm tăng nồng độ dopamine trong hạch nền và thúc đẩy sự kết hợp của choline vào phospholipid của màng tế bào (44-46).
Tăng thông khí và hạn chế thời gian
Đáp ứng động mạch não với CO2 phụ thuộc vào thay đổi pH quanh mạch máu (26). HV gây ra nhiễm kiềm hypocapnic, nhanh chóng kích hoạt các cơ chế đệm cố gắng bình thường hóa các thay đổi được thực hiện đối với khoang ngoại bào và CSF (10, 11). Trong thời gian này, có một dòng tế bào nhanh chóng của các ion hydro (H+) liên kết với bicarbonate và tạo ra axit carbonic (H2CO3), phân ly trong nước (H2O) và CO2 (10, 11). Đồng thời, bicarbonate ngoại bào được trao đổi với clorua từ khoang nội bào (10, 11). Các cơ chế đệm này không hiệu quả vì chúng nhanh chóng cạn kiệt; Nếu tình trạng hypocapnia kéo dài, nhiễm kiềm sẽ kéo dài.
Một bộ đệm chậm hơn nhưng hiệu quả hơn xảy ra ở cấp độ ống thận gần, trong đó tái hấp thu bicarbonate bị ức, chế đồng thời bài tiết H+ được kích thích (10, 11). Những đáp ứng này bắt đầu vài phút sau khi nhiễm kiềm hypocapnic bắt nguồn và được duy trì trong nhiều giờ hoặc thậm chí vài ngày, cho phép CSF và pH quanh mạch máu bình thường hóa 6 giờ sau khi bắt đầu hypocapnia; HV tự nhiên trở nên kém hiệu quả hơn sau khi con đường đệm này được kích hoạt (10, 11). Các nghiên cứu lâm sàng đã chứng minh giảm 40% CBF khi nồng độ PaCO2 là 20 mmHg; nhưng, sau 4 giờ HV, CBF bắt đầu bình thường hóa (47). Nồng độ CO2 sau khi điều trị bằng HV cũng cần có thời gian để bình thường hóa; Nếu PaCO2 tăng nhanh, pH quanh mạch máu (bình thường hóa bởi hệ thống đệm) sẽ giảm, gây nhiễm toan cục bộ, giãn mạch và tăng CBV và ICP (còn được gọi là “rebound hyperemia”) (11, 48).
Bằng chứng lâm sàng về điều trị tăng thông khí trong quản lý sTBI
Trong nhiều năm, HV là một liệu pháp quan trọng trong việc kiểm soát và phòng ngừa ICH sau chấn thương (6-8, 49-51). Oertel et al. báo cáo rằng HV là một công cụ mạnh mẽ và hiệu quả hơn để giảm mức ICP tăng khi so sánh với tăng áp lực động mạch trung bình (MABP) hoặc giảm chuyển hóa não với propofol (52). Nhiều nghiên cứu chỉ ra rằng cơ chế mà HV làm giảm ICP là co mạch và giảm CBF (3-5, 10, 11). Khi CBF giảm, nguy cơ thiếu máu cục bộ là một mối nguy hiểm tiềm ẩn (8, 10-12). Đây là một vấn đề gây tranh cãi là chủ đề của nhiều cuộc tranh luận.
Ngay sau khi bị chấn thương, CBF giảm xuống còn khoảng 40% và CMRO2 cũng có thể giảm theo (53-56). Sau ít nhất 48 giờ, giai đoạn này được theo sau bởi hai giai đoạn liên tiếp của tình trạng tăng lưu lượng máu tương đối (“relative hyperemia”) (trong đó CBF tăng trên nhu cầu chuyển hóa) và co thắt mạch máu (57). Não sau chấn thương cực kỳ dễ bị tổn thương do thiếu máu cục bộ (58-61). Trong gần một nửa số trường hợp sTBI được báo cáo, cơ chế tự điều hòa áp lực bị tổn hại; do đó, CBF trở thành phụ thuộc vào áp lực (58-61). Trong các trường hợp khác nhau, đường cong tự điều hòa áp lực có thể dịch chuyển sang phải, điều này sẽ làm tăng giới hạn áp lực tưới máu não (CPP) để giúp ngăn ngừa thiếu máu cục bộ (58-61). Bởi vì não cần phải đạt được CPP cao hơn trong giai đoạn cấp tính của sTBI, rất khuyến khích rằng nên tránh hạ huyết áp trong giai đoạn này.
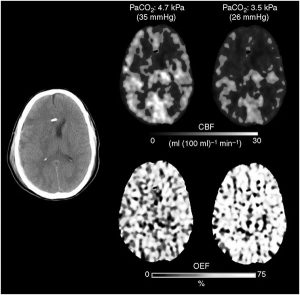
Giống như CBF, sự co mạch của động mạch đối với CO2 có thể thay đổi tùy theo khu vực. Đáp ứng CO2 được duy trì theo thói quen và trầm trọng hơn trong giai đoạn chấn thương ban đầu, đặc biệt là ở các khu vực lân cận với các vùng dập não hoặc tụ máu dưới màng cứng; sự gần gũi với các khu vực này làm tăng khả năng thiếu máu cục bộ xảy ra ở những khu vực đó (Hình 4) (31, 33, 62). Nếu đáp ứng CO2 trở nên bị tổn hại, thông thường là do một sự kiện cuối cùng, liên quan đến kết cục kém (53, 62-64). Vì những lý do này, điều quan trọng ở giai đoạn này trong điều trị là duy trì CBF trong giới hạn bình thường để cung cấp CPP đầy đủ (CPP = MABP – ICP) và độ nhớt của máu trong khi tránh co thắt mạch đề kháng (12, 58).
Tăng thông khí và thiếu máu não
Davis là người đầu tiên quan sát thấy sự chậm lại của sóng điện não đồ sau HV và quy kết hành vi này là do thiếu máu cục bộ (65). Cold đã đánh giá CBF khu vực (rCBF) bằng cách sử dụng kỹ thuật Xenon (Xe-CT) trước và sau HV giữa ngày đầu tiên nhập viện và 3 tuần sau sTBI (66). Trong các điều kiện này, ICP trung bình được báo cáo là 19 mmHg và mức PaCO2 thay đổi từ 36 thành 26 mmHg. Nhóm tăng thông khí đã chứng minh vùng thiếu máu nhiều gấp ba lần (được xác định bằng CBF < 20 ml/100 g/phút) và các khu vực giảm CBF nghiêm trọng của họ (<15 ml/100 g/m) tăng từ 0,1 đến 3%. Những quan sát này đã rõ ràng hơn ở bán cầu não với CBF cơ bản thấp hơn. Cũng có một mối tương quan mạnh mẽ giữa HV, giảm rCBF và kết cục bệnh nhân xấu (66).
Nhiều nghiên cứu lâm sàng kiểm tra sTBI đã xác nhận rằng HV gây ra sự giảm đáng kể CBF (67-69). Nhưng quan sát giảm CBF là không đủ để chẩn đoán chính xác thiếu máu cục bộ. Để xác định chẩn đoán hợp lệ, tình trạng thiếu oxy mô phải liên quan đến bất kỳ sự giảm CBF nào được quan sát thấy (37-40). Mặc dù chúng không có sẵn trong thời gian thực ở đầu giường, nhưng điều quan trọng là phải thực hiện các nghiên cứu chuyển hóa, chẳng hạn như chụp cắt lớp phát xạ positron (PET) (70).
Một nhóm từ Cambridge đã tiến hành một loạt các nghiên cứu trong đó họ đã phân tích tác động của HV ở bệnh nhân mắc sTBI bằng PET (71-73). Một mẫu số chung trong số các bệnh nhân là sự vắng mặt của ICH (71-73). Trong nghiên cứu đầu tiên của nhóm, 33 bệnh nhân đã được thử nghiệm trong tuần đầu tiên của chấn thương và bốn bệnh nhân được đánh giá trong vòng 24 giờ đầu tiên nhập viện (71). Các nhà nghiên cứu đã giảm mức PaCO2 từ mức cơ bản là 36-29 mmHg. HV tăng CPP và giảm ICP và CBF, làm tăng số lượng và thể tích của các khu vực đạt đến phạm vi giảm tưới máu. Tuy nhiên, những thay đổi này không liên quan đến thiếu máu cục bộ toàn thể do SvjO2 và sự khác biệt tĩnh mạch động mạch của O2 (AVDO2) vẫn ở trong giới hạn bình thường (71).
Trong một nghiên cứu tiếp theo, 13 bệnh nhân đã được phân tích trong cùng giai đoạn sau chấn thương để kiểm tra giả thuyết rằng sự thay đổi khuếch tán trong vi tuần hoàn góp phần vào tình trạng thiếu oxy mô (72). Các bệnh nhân được theo dõi với PET, tỷ lệ trích xuất O2 (OEF, O2 extraction fraction), ptiO2 và pvO2 (72). Một lần nữa, sau khi gây ra HV ở mức PaCO2 29 mmHg, CBF đã giảm. Các khu vực trong phạm vi giảm tưới máu và thiếu oxy (ptiO2 <10 mmHg) cho thấy khả năng dự trữ ít hơn để trích xuất O2, làm tăng nguy cơ tổn thương do thiếu máu cục bộ ở những vùng này (72).
Sử dụng một kỹ thuật PET đã được sửa đổi, Coles et al. đã đánh giá CBF, CMRO2, CBV và OEF ở 30 bệnh nhân sTBI trong vòng 10 ngày sau chấn thương (73). Hypocapnia (PaCO2 = 29 mmHg) gây ra giảm CBF, tăng thể tích vùng thiếu máu cục bộ và tăng OEF. CMRO2 tăng, nhưng đáp ứng không đồng nhất. 28% các cá nhân bị tăng thông khí cho thấy CMRO2 giảm rõ rệt. CMRO2 tương quan với kết quả theo dõi sinh lý thần kinh (73).
Trong một loạt bệnh nhân sTBI khác có giá trị ICP bình thường, ảnh hưởng của HV và mannitol đối với CBF và các biến số chuyển hóa được đo bằng thiết bị siêu âm Doppler và mẫu máu được lấy từ ống thông động mạch cảnh (74). Thời gian của nghiên cứu không được chỉ định. Các tác giả đã báo cáo rằng, khi so sánh với nhóm mannitol 20% (0,5 g/kg), nhóm này được điều hòa ở mức PaCO2 mục tiêu là 32 mmHg có CBF và CMRO2 thấp hơn; việc sử dụng glucose (CMRGlu) và sản xuất lactate (CMRL) cũng tăng lên trong nhóm này, được các tác giả giải thích là dấu hiệu của tăng ly giải glycogen kỵ khí (74).
Sử dụng Xe-CT, Stringer đã phân tích rCBF ở 12 cá nhân với nhiều nguyên nhân khác nhau, bốn trong số đó là bệnh nhân TBI (75). HV được tạo ra không đồng nhất với các giá trị CO2 cuối thì thở ra (ETCO2) khác nhau, ba trong số chúng thấp hơn 20 mmHg. Nghiên cứu cho thấy sự giảm rCBF. Không có thông số chuyển hóa được đo (75).
Sử dụng phương pháp đo khuếch tán nhiệt và vi lọc (thermodiffusion and microdia- lysis), Marion đã phân tích rCBF và các dấu hiệu thiếu oxy mô trong dịch ngoại bào của 20 cá nhân có sTBI trước và sau HV với mục tiêu 24,6 mmHg (76). Bệnh nhân duy trì giá trị ICP bình thường. Các tác giả đã phân tích các khu vực rõ ràng khỏe mạnh, liền kề với các khu vực dập não hoặc tụ máu dưới màng cứng trong khoảng thời gian hai lần: 24-36 h và 3-4 ngày sau chấn thương (76). Sau HV, sự gia tăng của glutamate, lactate và mối quan hệ giữa lactate/pyruvate (L/P) đã được quan sát là 10% so với giá trị cơ bản. CBF giảm theo tỷ lệ tương tự. Những thay đổi này đã được nhìn thấy trong cả hai khoảng thời gian, nhưng chúng thường được quan sát nhiều hơn trong giai đoạn đầu sau TBI (76).
Sử dụng PET, Diringer đã kiểm tra sự thay đổi của CBF, CBV, CMRO2, OEF và CvO2 sau HV theo mục tiêu PaCO2 được chỉ định trước là 30 mmHg. Bệnh nhân được phân tích trung bình 11 giờ sau sTBI. Trong số chín cá nhân được nghiên cứu, chỉ có năm người có ICP lớn hơn 20 mmHg (77). Việc giảm CBV, CBF và CvO2 đã được quan sát. Không có thiếu máu cục bộ hoặc rối loạn chức năng năng lượng rõ ràng do CMRO2 không thay đổi với tiêu tốn là tăng OEF (77). Hai năm sau, cùng một nhóm đã sử dụng cùng một phương pháp để so sánh ảnh hưởng của HV đối với bệnh nhân và không có ICH trong các ngày 1 và 5 sau chấn thương (78). Kết quả họ thu được và kết luận họ đạt được không khác với kết quả được báo cáo trong nghiên cứu trước đó (78).
Tăng thông khí và oxy hóa não
PaCO2 ảnh hưởng đến các phép đo được thực hiện bởi cả hai phương pháp theo dõi oxy hóa toàn thể (SvjO2) và khu vực (ptiO2). HV làm giảm mức độ ICP và các nghiên cứu lâm sàng đã chứng minh giảm đồng thời các giá trị SvjO2 (79- 81). Khi phân tích tác động của mức ETCO2 đối với CBF và ptiO2, mối quan hệ trực tiếp đã được quan sát giữa các biến này, đặc biệt là trong phạm vi ETCO2 từ 20 đến 60 mmHg (82). Khi HV mạnh hơn và mức ETCO2 thấp hơn, khả năng phát hiện tình trạng thiếu oxy mô bằng cách sử dụng theo dõi ptiO2 tăng (83). Hypocapnia là một trong những tổn thương thứ cấp có khả năng kích hoạt tình trạng thiếu oxy mô (84). Hiệu quả của HV đối với quá trình oxy hóa mô trở nên kịch tính hơn khi thời gian trôi qua; nó có tác động mạnh nhất trong khoảng 5 ngày sau chấn thương (85, 86). Hiện tượng này có liên quan đến kết cục kém (86-88). Nhiều nghiên cứu lâm sàng đã xác định được tác dụng phụ của HV đối với nồng độ ptiO2. Trong sTBI, ptiO2 thấp hơn rõ ràng đã trở thành một yếu tố dự báo độc lập về tỷ lệ tử vong và kết cục xấu của bệnh nhân (86- 89).
Tăng thông khí và Kết cục sTBI
Chỉ có một vài nghiên cứu đã thiết lập mối tương quan giữa kết cục của bệnh nhân và HV. Hai nghiên cứu nhỏ kết luận rằng tỷ lệ tử vong và kết cục chức năng kém có liên quan đến HV khi tăng thể tích vùng có CBF thấp vào vùng thiếu máu cục bộ (66) hoặc khi mức ptiO2 giảm cùng với tăng đáp ứng CO2 5 ngày sau chấn thương (86).
Gordon đã báo cáo một loạt các bệnh nhân hồi cứu lớn được điều trị bằng tăng thông khí kéo dài (90). 251 bệnh nhân bị sTBI đã được nghiên cứu, 51 trong số đó được tăng thông khí (PaCO2 trong khoảng từ 25 đến 30 mmHg). Khoảng thời gian của HV thay đổi trong khoảng từ 6 h đến 41 ngày (trung bình là 10 ngày). Nhóm HV có tỷ lệ tử vong thấp hơn (9,8 so với 32,8%); tuy nhiên, số người sống sót với di chứng thần kinh nghiêm trọng tăng đáng kể. Bệnh nhân đã hồi phục hoàn toàn không khác nhau giữa các nhóm (90). Các tác giả của bài báo đã đưa ra một vài chi tiết về phương pháp của họ; dữ liệu lâm sàng báo cáo của họ cũng không đầy đủ.
Chỉ có một nghiên cứu ngẫu nhiên, có kiểm soát đánh giá kết cục cuối cùng của bệnh nhân sTBI được điều trị bằng HV sâu và kéo dài (5 ngày) (91). Ba nhóm được đánh giá trong nghiên cứu này: bệnh nhân dùng chỉ tiêu thông thường (PaCO2 35 mmHg), bệnh nhân dùng HV ở mức PaCO2 25 mmHg và bệnh nhân dùng HV và THAM (tromethamine). THAM hoạt động như một bộ đệm, ngăn chặn sự thay đổi pH trong dịch não và ngoại bào để kéo dài thời gian HV có hiệu quả. Trước khi ngẫu nhiên, bệnh nhân được phân tầng thành hai nhóm theo thành phần vận động của Thang điểm hôn mê Glasgow (GCS): ≤ 3 hoặc > 3 điểm. Kết quả thuận lợi ở 3 và 6 tháng của sự kiện thấp hơn đáng kể ở nhóm HV, đặc biệt là đối với những bệnh nhân có tình trạng lâm sàng tốt hơn tại thời điểm nhập viện (vận động GCS 4-6). Sau một năm trôi qua kể từ ngày chấn thương, sự khác biệt giữa các nhóm không còn đáng kể. Khi đánh giá CBF (Xe133) và AVDO2, không có bằng chứng thiếu máu cục bộ ở bất kỳ nhóm nào trong số ba nhóm (91).
Các kết luận nghiên cứu nên được giải thích một cách thận trọng. Đầu tiên, các đặc điểm lâm sàng và chụp cắt lớp của bệnh nhân không được cân bằng tốt giữa các nhóm. Số lượng bệnh nhân trong mỗi nhóm cũng ít, do đó có thể có các lỗi thống kê thuộc loại α (dương tính giả). Nhóm đối chứng cũng được tăng thông khí với PaCO2 trung bình ở mức 31 mmHg. Thứ ba, rõ ràng là HV đã được sử dụng trong điều trị dự phòng vì chỉ có 14% cá nhân trong nhóm kiểm soát và nhóm HV và 5% nhóm HV và THAM có giá trị ICP cao. Cuối cùng, khi phân tích kết quả sau 12 tháng sau chấn thương, kết quả tốt nhất tương ứng với nhóm HV + THAM.
Mục tiêu PaCO2 trong xử trí sTBI
Cochrane kết luận rằng không có đủ bằng chứng để xác định rõ liệu liệu điều trị tăng thông khí trong xử trí sTBI là có lợi hay bất lợi (92). Trong các tình huống khẩn cấp, các hướng dẫn của Tổ chức chấn thương não (BTF, Brain Trauma Foundation) khuyến nghị một khoảng thời gian tăng thông khí ngắn (HV) (15-30 phút để nhắm mục tiêu PaCO2 30-35 mmHg) để điều trị suy giảm thần kinh cấp tính phản ánh việc tăng ICP (12). Tuy nhiên, ở những bệnh nhân mắc TBI, PaCO2 được nhắm mục tiêu của quá trình chuẩn hóa là 35-40 mmHg với độ oxy hóa xung từ 95% trở lên và/hoặc PaO2 từ 80 mmHg trở lên (12). Nếu bệnh nhân kháng trị với tất cả các phương pháp điều trị khác, bao gồm nước muối ưu trương, an thần và liệt cơ, thời gian điều trị HV kéo dài với theo dõi oxy hóa não có thể được yêu cầu để làm giảm ICH (12).
Các quy tắc cần tính đến trước khi tăng thông khí một bệnh nhân bị sTBI
Tăng thông khí có một vị trí trong xử trí ICP. Để các bác sĩ xác định liệu có chỉ định chính xác và đủ để điều trị với nguy cơ tối thiểu cho bệnh nhân hay không, phải thực hiện một phương pháp có hệ thống dựa trên bằng chứng khoa học hiện tại. Các tác giả khuyến nghị các hướng dẫn sau, trong Hình 5:
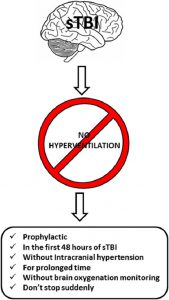
- KHÔNG tăng thông khí dự phòng. HV sẽ không ngăn chặn sự gia tăng ICP, và cũng sẽ không cải thiện kết quả cuối cùng.
- KHÔNG tăng thông khí khi không có ICH.
- KHÔNG tăng thông khí trong thời gian dài. Ở 4-6 giờ, các hệ thống đệm bình thường hóa độ pH của khoang quanh mạch máu, do đó phủ nhận những ảnh hưởng của tăng thông khí đối với hệ thống mạch máu não.
- KHÔNG tăng thông khí trong vòng 24 giờ đầu tiên của sTBI, khi nguy cơ thiếu máu cục bộ là lớn nhất.
- KHÔNG tăng thông khí mà không theo dõi oxy. Cân nhắc sử dụng Doppler xuyên sọ và đo nồng độ CO2 thông qua việc xác định mức ETCO2 cuối thở ra hoặc khí động mạch. Vì thiếu oxy máu cục bộ là một nguy cơ tiềm ẩn và nguy hiểm, nên theo dõi quá trình oxy hóa não trên toàn thể (SvjO2), cục bộ (ptiO2) hoặc cả hai mặc dù mức độ bằng chứng thấp của khuyến nghị này.
- KHÔNG đột ngột dừng HV. Ngừng đột ngột sẽ làm tăng nguy cơ phục hồi mức độ tăng ICP.
Điều kiện lý tưởng để tăng thông khí
Cơ chế tự điều hòa não bị ảnh hưởng xấu trong hơn một nửa các trường hợp sTBI được báo cáo, nhưng HV có thể giúp cải thiện những trường hợp đó (93, 94). Tuy nhiên, lợi ích thu được từ HV là nhất thời và chỉ có thể đạt được thông qua HV vừa phải. Một nghiên cứu Doppler kiểm tra 10 bệnh nhân mắc sTBI đã chứng minh rằng HV ở mức PaCO2 là 28 mmHg đã cải thiện đáng kể khả năng tự điều hòa não, nhưng lợi ích đã mất khi HV giảm xuống còn PaCO2 là 23 mmHg (95). Một nhóm khác bao gồm 30 cá nhân sTBI có giá trị ICP bình thường được chứng minh là cải thiện khả năng tự điều hòa khi mức PaCO2 tạm thời giảm từ 38 xuống 33 mmHg (96).
Tăng thông khí được khuyến cáo là biện pháp tạm thời để giảm mức ICP cao trong các tình huống sau:
- Các hội chứng thoát vị. Đây là những hội chứng liên quan đến sự suy giảm của tình trạng thần kinh (dãn đồng tử, tư thế vận động bất thường) thứ phát sau các tổn thương lan rộng (tụ máu ngoài màng cứng, dưới màng cứng, v.v.) như một cầu nối để giải quyết phẫu thuật (12).
- Mức độ cao đe dọa tính mạng của ICP. Ví dụ, loại sóng cao nguyên loại A, trong khi điều tra các yếu tố kích hoạt và mong đợi hiệu quả của liệu pháp thẩm thấu (12).
- ICH kháng trị. HV được sử dụng kết hợp với các biện pháp cấp độ thứ hai, chẳng hạn như phẫu thuật mở hộp sọ giải áp, hạ thân nhiệt hoặc dùng barbiturat liều cao (12).
- ICH thứ phát sau tăng lưu lượng máu.
- Trong khoảng 20% trường hợp sTBI, mức độ cao ICP tương quan với CBF cao vượt quá nhu cầu chuyển hóa, chủ yếu ở những người trẻ tuổi (53, 97, 98). Trong các tình huống này, dựa trên nguyên tắc ghép nối giữa CBF và CMRO2, khái niệm tối ưu hóa HVR xuất hiện để hạ thấp CBF và do đó, ICP mà không sửa đổi CMRO2 (99-102). Bằng cách thực hiện phương pháp này cùng với theo dõi oxy hóa não thông qua SvjO2 và các biến liên quan, Cruz et al. hiệu chỉnh HV thành PaCO2 mục tiêu thay đổi từ 18 đến 30 mmHg. Do đó, ICP đã giảm mà không sửa đổi trong CMRO2 trong khi OEF tăng (98-102). Trong một loạt bệnh nhân sTBI khác, đã có báo cáo rằng HV đã góp phần ổn định và cải thiện sự hấp thu glucose của não (101).
- Tối ưu hóa HV có những hạn chế của nó. Nó dựa trên sự giám sát toàn thể không tính đến sự khác biệt trong khu vực về CBF, chuyển hóa hoặc đáp ứng CO2. Khoang hóa ICP và loại tổn thương (khu trú hoặc lan tỏa) tương tự như vậy theo cách này. Không tồn tại một định nghĩa nhất quán về tăng lưu lượng máu, đặc biệt là về các phương pháp theo dõi có sẵn ở đầu giường. Cũng có nhiều hạn chế đối với phương pháp theo dõi oxy, điều này có thể gây khó khăn cho việc diễn giải dữ liệu thu được từ giám sát nói trên.
Kỹ thuật tăng thông khí
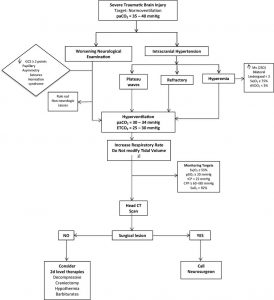
Trong Hình 6,6, chúng tôi phác thảo một thuật toán thực tế tóm tắt các khái niệm mà người ta nên xem xét khi làm thông khí cho bệnh nhân.
Kết luận
Bệnh nhân có ICP tăng cao đòi hỏi phải can thiệp khẩn cấp để ngăn ngừa hậu quả nghiêm trọng. Trong một số điều kiện nhất định, khi đáp ứng CO2 của mạch máu não còn nguyên vẹn, HV có thể được sử dụng tạm thời để gây ra hypocapnia để gây co mạch máu với mục đích giảm CBF và cuối cùng là ICP. Các tác dụng tại não của hypocapnia là thoáng qua. Bởi vì HV sâu và kéo dài có nguy cơ thiếu máu cục bộ, điều quan trọng là liệu pháp này phải được theo dõi chặt chẽ để ngăn ngừa bất kỳ tác dụng phụ bất lợi nào.
HV có hậu quả hệ thống nghiêm trọng. Không nên thực hiện trong 24 giờ đầu tiên của chấn thương khi CBF giảm rõ rệt. Dự phòng HV hoặc HV mà không có dấu hiệu tăng ICP sẽ không mang lại bất kỳ lợi ích nào. Các khuyến nghị hiện tại cho thấy rằng một khoảng thời gian ngắn của HV (15-30 phút) với mục tiêu PaCO2 là 30-35 mmHg và mục tiêu CPP là 60-70 mmHg kết hợp với giám sát oxygen hóa thần kinh gần như là một phương pháp hiệu quả để kiểm soát ICH trong giai đoạn cấp tính của sTBI.



![[Cảnh báo] Để cải thiện thiếu máu não nên ăn gì? Kiêng ăn gì? Thiếu máu não nên ăn gì?](https://www.healcentral.org/wp-content/uploads/2020/11/thieu_mau_nao_nen_an_gi1-218x150.jpg)

