Tác giả: Bác sĩ Đặng Thanh Tuấn
Tóm tắt
Bệnh phổi tắc nghẽn mạn tính (COPD) và hen phế quản thường làm phức tạp các bệnh nhân phẫu thuật, dẫn đến tình trạng bệnh lý và tử vong sau phẫu thuật. Nhiều tác giả đã cố gắng dự đoán các biến chứng phổi sau phẫu thuật nhưng không đặc hiệu với COPD. Mục đích của tổng quan này là cung cấp các hướng dẫn dựa trên bằng chứng gần đây về dự đoán và chiến lược thông khí cho thở máy ở COPD và bệnh nhân hen phế quản. Sử dụng tìm kiếm của Google cho các cơ sở dữ liệu lập chỉ mục, việc tìm kiếm các bài báo được xuất bản đã được thực hiện bằng cách sử dụng các kết hợp khác nhau của các cụm từ tìm kiếm sau: “predictors”; “mechanical ventilation”; “COPD”; “bronchial asthma”; “recent strategies”. Các nguyên nhân khác cũng được xác định bằng cách khám phá danh sách tham khảo chính.
Keywords: Bronchial asthma, chronic obstructive pulmonary disease, heliox, mechanical ventilation, risk
MỞ ĐẦU
Bệnh phổi tắc nghẽn mạn tính (COPD) bao gồm nhiều loại bệnh cũng gộp luôn cả viêm phế quản và khí phế thũng. Nó đang trở thành vấn đề chính về sức khoẻ và kinh tế trên toàn thế giới; vào năm 1990, đó là nguyên nhân tử vong thứ sáu phổ biến nhất, được cho là nguyên nhân thứ ba phổ biến nhất vào năm 2020. Tử vong liên quan đến hen cũng rất đáng kể, với 1-8 tử vong trên một lakh trên toàn thế giới; tuy nhiên, mức độ thực tế của vấn đề ở nước ta (Ấn độ) không được biết rõ. [1] Vì vậy, để tối ưu hóa các bệnh nhân này trước khi phẫu thuật để tránh các biến chứng trong giai đoạn hậu phẫu, thông khí cơ học có thể là vấn đề hơn là một giải pháp. Thông khí cho bệnh nhân COPD thường rất khó vì bệnh có thể không có thành phần có thể đảo ngược. Hơn nữa, việc định lượng và quản lý quá căng phổi động (DH, dynamic hyperinflation) tại giường là rất khó khăn. Theo thời gian, nó đang trở thành một vấn đề sức khoẻ quan trọng vì ngày càng có nhiều bệnh nhân bị bệnh tắc nghẽn được đưa vào phẫu thuật [2].
Obstructive lung disease
Bệnh phổi tắc nghẽn chủ yếu bao gồm rối loạn đường thở như COPD, hen suyễn, co thắt phế quản và viêm phế quản (bronchiilitis) [3].
CÁC THAY ĐỔI SINH LÝ TRONG COPD DẪN ĐẾN THỞ MÁY
Expiratory flow limitation – Giới hạn lưu lượng thở ra
Đó là sự thay đổi sinh lý chính trong COPD và được bù đắp bằng cách tăng lưu lượng khí hít vào và thể tích phổi. Mặc dù tải trọng là thở ra, sự bù trừ này về cơ bản là hít vào, điều này kết hợp với điều hòa hô hấp cao sẽ dẫn đến sự mỏi mệt mỏi của cơ hô hấp có ý nghĩa sinh lý trung tâm trong sự phát triển của suy hô hấp cấp (ARF) ở những bệnh nhân này.
Dynamic hyperinflation and auto-positive end-expiratory pressure – Quá căng phổi động và PEEP tự động
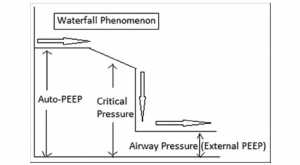
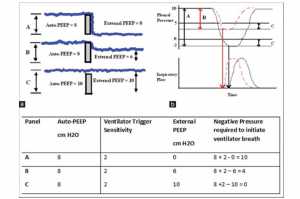
Tắc nghẽn luồng dẫn khí, độ đàn hồi thấp, nhu cầu thông khí cao và thời gian thở ra ngắn dẫn đến bẫy khí và kết quả là quá căng phổi động (DH, dynamic hyperinflation). Ở bệnh nhân COPD với ARF, DH là yếu tố chính giải thích tăng áp suất trong lồng ngực, tăng công thở (WOB), sự phụ thuộc của máy thở và sự thất bại của cai máy [4]. Theo lý thuyết thác nước (waterfall theory), tăng áp suất hạ lưu từ vị trí đường thở nhỏ đóng hoặc xẹp không làm giảm lưu lượng thở ra cho đến khi dòng nước hạ lưu (áp suất dương cuối kỳ thở ra bên ngoài [PEEP]) đạt đến áp suất tới hạn (critical pressure) [Hình 1] [4] Vì vậy, PEEP bên ngoài nên được giữ ở mức dưới 75% đến 85% PEEP tự động (auto-PEEP) để tránh tình trạng quá căng phổi (hyperinflation) hoặc ức chế tuần hoàn nặng hơn [6,7]. Xác định DH, tuy nhiên không dễ thực hiện trong ICU. Nó đòi hỏi phải đặt một catheter bóng thực quản và đánh giá các cơ bụng nơi có thể được huy động trong quá trình thở ra. [8] Tuy nhiên, có thể thấy sự thay đổi dung tích hít vào (IC, inspiratory capacity) phỏng theo của quá căng phổi, dung tích hít vào càng lớn thì thể tích phổi cuối kỳ thở ra càng thấp, giả định là dung tích phổi toàn phần không đổi [9,10].
Types of auto-positive end-expiratory pressure and their measurement – Các loại PEEP tự động và cách đo
Static auto-positive end-expiratory pressure – PEEP tự động tĩnh
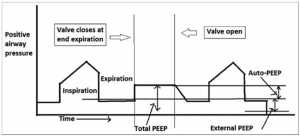
Nó chỉ được đo ở bệnh nhân mà không có nỗ lực hô hấp hoạt động bằng cách sử dụng sự ngưng thở cuối thì thở ra của máy thở. PEEP tự động sau đó được tính bằng cách loại bỏ PEEP bên ngoài khỏi tổng PEEP [Hình 2]. [11]
Dynamic auto-positive end-expiratory pressure – PEEP tự động động
Nó được đo bằng cách ghi đồng thời luồng không khí (airflow) và áp suất đường thở cuối thì thở ra. Ở những bệnh nhân thở tự nhiên, PEEP tự động được xác định bằng việc ghi lại cùng với áp lực thực quản và luồng không khí. Nó được đo tại thời điểm cuối thì thở ra như là chổ lõm âm của áp suất thực quản lúc giá trị của lưu lượng là zero. Nó nhỏ hơn PEEP tự động tĩnh vì nó phản ánh áp suất cuối thì thở ra của các đơn vị phổi với các hằng số thời gian ngắn và sự thở ra nhanh chóng trong khi các đơn vị có hằng số thời gian dài vẫn trống.
Diagnosis of dynamic hyperinflation
1. Làm chậm tốc độ của bóp bóng bằng tay
2. Đường biểu diễn capnography không đạt tới cao nguyên
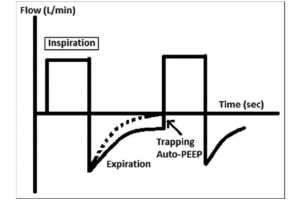
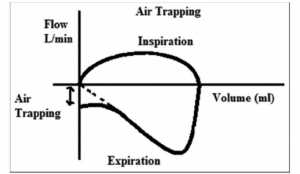
3. Lưu lượng thở ra không đạt tới zero trong biểu đồ lưu lượng/thể tích (Hình 3 và 4)
4. Đo PEEP nội tại (PEEPi). [12]
Xử trí cho phép kéo dài thời gian thở ra
Giảm tần số hô hấp (RR) hoặc I: E (thường là 1:3 – 1:5) để cho phép thở ra nhiều thời gian hơn và giảm bớt khó thở. Tuy nhiên, điều này sẽ dẫn đến thông khí phút giảm gây ra chứng tăng CO2 máu, giảm oxy máu hoặc nhiễm toan. Điều này dẫn đến sự gia tăng sức đề kháng mạch máu phổi và sự bất ổn định huyết động nặng hơn. Nếu điều này là đáng lo ngại, có thể sử dụng một tốc độ thở nhanh hơn với áp suất đỉnh cao, nhưng điều này sẽ làm cho bệnh nhân tăng nguy cơ bị barotrauma.
Áp dụng áp lực dương cuối kỳ thở ra (PEEP)
Việc sử dụng PEEP bên ngoài ở bệnh nhân thông khí với COPD có lợi ích lý thuyết bằng cách giữ cho đường thở nhỏ mở ra trong quá trình thở ra sau đó, vì vậy có thể làm giảm PEEPi hoặc PEEP tự động. Thêm vào đó, người ta đã thấy rằng nếu PEEP bên ngoài được giữ dưới PEEPi, không có sự gia tăng đáng kể áp lực phế nang và sự ảnh hưởng xấu lên tim mạch xảy ra. [13]
Điều trị với thuốc giãn phế quản Lưu lượng khí trong các đường dẫn khí nhỏ có thể bị tổn hại nghiêm trọng do co thắt phế quản, thường xảy ra khi gây mê hoặc trong dụng cụ khí thở. Cần được điều trị kịp thời bằng thuốc giãn phế quản dạng hít hoặc bằng cách gây mê sâu bằng propofol hoặc tăng nồng độ thuốc mê hít.
CÁC CHỈ SỐ DỰ ĐOÁN THỞ MÁY HẬU PHẪU BỆNH NHÂN COPD HOẶC HEN
Dự báo các biến chứng phổi sau phẫu thuật (PPCs, post-operative pulmonary complications) vẫn là một thách thức đối với hầu hết các nhà nghiên cứu. Mặc dù nhiều nghiên cứu đã cố gắng để dự đoán PPCs, nhưng chúng không dành riêng cho bệnh nhân COPD. Bệnh nhân COPD rõ ràng là có nguy cơ gia tăng về PPCs. Một đánh giá gần đây ước tính tỷ lệ mắc phải của PPCs không điều chỉnh là 18,2% ở bệnh nhân COPD trải qua phẫu thuật. [14] Mức độ nghiêm trọng của COPD gia tăng nguy cơ cao hơn, từ 10% với bệnh nhẹ đến trung bình đến 23% ở bệnh nhân bị bệnh nặng [15].
Bằng chứng cho thấy rằng bệnh sử và khám lâm sàng là yếu tố dự báo kém về tắc nghẽn đường thở và mức độ nghiêm trọng của nó. Tuy nhiên, sự xuất hiện của bệnh sử hút thuốc > 55 gói/năm, thở khò khè khi nghe phổi và bệnh nhân thở khò khè tự báo cáo có thể được xem là tiên đoán tắc nghẽn dòng khí, được định nghĩa là forced expiratory volume 1 (FEV1)/forced vital capacity < 0.70 sau khi dùng thuốc giãn phế quản. [2] Spirometry rất hữu ích để xác định tắc nghẽn khí ở bệnh nhân có triệu chứng, nhưng tiện ích của nó ở bệnh nhân không có triệu chứng hô hấp là đáng ngờ. Những người hút thuốc lá có spirometry bình thường chỉ có 4% nguy cơ bị PPCs. [16] Các bệnh nhân có triệu chứng với FEV1 < 60% dự đoán sẽ có lợi từ điều trị bằng thuốc dạng hít nhưng chứng cứ không hỗ trợ điều trị cho người không triệu chứng, bất kể các yếu tố nguy cơ và tắc nghẽn dòng không khí [2]. Tuy nhiên, không giống như phẫu thuật cắt phổi, không có giá trị điểm cắt (cut-off) của FEV1 hoặc bất kỳ chỉ số spirometric khác để xem xét những bệnh nhân này không phù hợp cho phẫu thuật.
Phân tích khí máu động mạch (ABG) không được chỉ định trừ khi bệnh sử của bệnh nhân cho thấy thiếu oxy máu hoặc mức COPD nghiêm trọng mà người ta nghi ngờ ứ CO2. Sau đó, ABG nên được sử dụng theo cách tương tự như người ta có thể sử dụng các xét nghiệm tiền phẫu thuật, tức là để tìm các bệnh có thể đảo ngược hoặc để xác định mức độ nghiêm trọng của bệnh nền. Xác định đường cơ sở PaO2 và PaCO2 đặc biệt quan trọng nếu người ta dự đoán được việc thở máy sau khi phẫu thuật một bệnh nhân bị COPD nặng [17]. Nhìn chung, các yếu tố nguy cơ độc lập khác nhau [Bảng 1] và chỉ số nguy cơ đã được phát triển để dự đoán PPCs [15,18,19,20,21,22].

CÁC CHỈ SỐ NGUY CƠ THƯỜNG SỬ DỤNG ĐỂ DỰ ĐOÁN NGUY CƠ BIẾN CHỨNG PHỔI SAU MỔ TRÊN BỆNH NHÂN COPD VÀ HEN
A. Tỷ số cho dự báo các biến chứng hô hấp sau mỗ (SPORC) [18]. Các yếu tố nguy cơ và điểm số tương ứng (trong ngoặc đơn) là ASA score ≥ 3 (3), thủ thuật cấp cứu, (3) dịch vụ có nguy cơ cao, (2), suy tim sung huyết (2) và bệnh phổi mãn tính (1 ).
(Xác suất tái đặt lại nội khí quản: 0 points = 0.1%; 1–3 points = 0.4%; 4–6 points = 1.6%; 7–11 points = 6.4%)
B. Respiratory failure risk index – chỉ số nguy cơ suy hô hấp:[23]
a. Loại phẫu thuật
b. Cấp cứu
c. Albumin (<30 g/L)
d. Blood urea nitrogen > 30 mg/dl
e. Phụ thuộc chức năng
f. COPD
g. Tuổi
Xác suất suy hô hấp (PRF): Class 1 (≤ 10 points) = 0.5%; Class 2 (11–19 points) = 2.2%; Class 3 (20–27 points) = 5%; Class 4 (28–40 points) = 11.6%; Class 5 (>40 points) = 30.5%
C. PRF risk calculator: Tính toán nguy cơ suy hô hấp [20]
D. Cardiopulmonary risk index: Chỉ số nguy cơ tim phổi [24]
HỖ TRỢ THÔNG KHÍ CƠ HỌC CHO BỆNH PHỔI TẮC NGHẼN
Bằng cách sử dụng bằng chứng hiện tại, thông khí áp lực dương không xâm lấn (NIPPV) là chọn lựa đầu tiên của việc điều trị cho những bệnh nhân này, tuy nhiên cần phải thông khí áp lực dương xâm lấn ở những bệnh nhân có bệnh nặng hơn. Một trong những nguyên nhân chính của bệnh suất và tử vong phát sinh trong quá trình thông khí cơ học ở những bệnh nhân này là quá mức DH với PEEPi, làm tăng nặng WOB. Mục tiêu chính của thông khí cơ học là cải thiện trao đổi khí phổi và làm giảm các cơ hô hấp bị suy yếu đủ để phục hồi từ tình trạng mệt mỏi.
Các chiến lược cải thiện trao đổi khí
Tình trạng thiếu oxy máu do các bệnh gây tắc nghẽn đường thở cơ bản là do một trong ba nguyên nhân chung: shunt, bất tương xứng thông khí/tưới máu (V/Q mismatching) và các khiếm khuyết khuếch tán [Bảng 2]. Nói chung, những người bị COPD cấp tính có mức độ khiếm khuyết thông khí cao hơn (gây tăng CO2 máu) so với bệnh nhân mãn tính, những người chủ yếu bị khiếm khuyết tưới máu (gây ra tình trạng thiếu oxy máu). Tuy nhiên, tình trạng co mạch do thiếu oxy và tăng CO2 máu ở bệnh nhân mãn tính làm giảm sự không phù hợp V/Q như dự kiến [25]. Vì vậy, xử trí nguyên nhân có tầm quan trọng hàng đầu trong điều trị thiếu oxy máu ở COPD. Hơn nữa, các bằng chứng cho thấy những ảnh hưởng có ích của các kỹ thuật thở có kiểm soát như: thở ra hoạt động, thở chậm và sâu, thở bằng miệng thở, liệu pháp thư giãn, các tư thế cụ thể và tập luyện cơ hít vào. Hơi thở bằng cơ hoành không thể hiện sự lợi ích [26].
| Bảng 2: Các yếu tố ảnh hưởng đến trao đổi khí tại phổi | ||
| Các yếu tố ảnh hưởng đến thông khí | Các yếu tố ảnh hưởng đến tưới máu | Các yếu tố ảnh hưởng đến khuếch tán |
|
|
|
Các chiến lược cho cơ hô hấp nghỉ ngơi và giảm công thở
Ở bệnh nhân COPD và hen suyễn, kiểm soát hô hấp cao và lợi thế cơ học kém gây ra sự mệt mỏi của cơ hít vào có thể được cải thiện bằng cách giảm tải hô hấp, tăng cường khả năng cơ bắp và hỗ trợ thông khí cơ học [Bảng 3].
| Bảng 3: Các yếu tố ảnh hưởng đến hiệu quả của cơ hô hấp | |
| Các yếu tố ảnh hưởng đến tải hô hấp | Các yếu tố ảnh hưởng đến năng lực cơ bắp |
| Tải sức cản (co thắt phế quản, tắc nghẽn đường thở trên) | Ức chế trung tâm hô hấp (thuốc an thần, nhược giáp) |
| Tải độ đàn hồi của phổi (viêm phổi, phù phổi, xẹp phổi) | Yếu cơ (hạ kali máu, hạ phosphate máu)
Suy dinh dưỡng |
| Tải độ đàn hồi của thành ngực (béo phì, tràn dịch màng phổi, tràn khí màng phổi, chướng bụng) | |
| Tải thông khí phút (tăng sản xuất CO2 quá mức, tăng tỉ lệ VD/VT) | Quá căng chướng phổi động và PEEP tự động |
|
Các yếu tố liên quan đến máy thở Ống nội khí quản bị hẹp PEEP cài đặt bên ngoài Trigger không nhạy/giảm ngưỡng trigger của máy thở |
|
VAI TRÒ THÔNG KHÍ KHÔNG XÂM LẤN TRONG ĐIỀU TRỊ BỆNH PHỔI TẮC NGHẼN
NIPPV đã được chấp nhận rộng rãi như là chế độ thông khí được lựa chọn đầu tiên trong điều trị bệnh nhân bệnh tắc nghẽn đường thở có suy hô hấp. Nó làm giảm đáng kể nhu cầu đặt nội khí quản và do đó giảm các biến chứng của nó (ví dụ: viêm phổi liên quan đến thở máy, biến chứng thanh quản và khí quản) nếu được xem xét sớm trong diễn tiến của bệnh [27,28,29,30,31]
Cơ chế tác động của thông khí không xâm lấn
Áp suất đường thở dương thì thở ra (EPAP) áp dụng cho PEEPi do tắc nghẽn khí thở ra [Hình 5]. Áp suất đường thở dương thì hít vào (IPAP) làm tăng thể tích khí lưu thông dẫn đến giảm bất lợi về cơ học, giảm RR, giảm WOB và cải thiện thông khí (thường giảm PaCO2). [32]
Chỉ định của thông khí không xâm lấn
1. Bệnh nhân có pH từ 7.30 – 7.25
2. Không đáp ứng với điều trị nội khoa: PaO2 < 50 mmHg, PaCO2 > 80–90 mmHg, pH ≤7.2, with following:
a. Bệnh nhưng không tử vong
b. Có khả năng bảo vệ đường thở
c. Có ý thức và hợp tác
d. Huyết động động học ổn định
e. Không có chất bài tiết qua đường hô hấp quá mức
f. Ít bệnh tật đi kèm
3. Bệnh nhân từ chối đặt nội khí quản
4. Tạo dễ dàng cai máy thở
5. NPPV tại nhà cho bệnh nhân tái nhập viện nhiều lần.
Kỹ thuật thông khí không xâm lấn [33,34]
Cài đặt ban đầu:
- Pressure support (PS) ở 10 cm H2O của IPAP và 5 cm H2O của EPAP
- Áp lực < 8 cm/4 cm H2O (IPAP/EPAP) không được khuyến cáo do không đầy đủ
- Điều chỉnh (IPAP và hoặc EPAP) để đạt tidal volume là 5–7 ml/kg.
Điều chỉnh dựa vào kết quả khí máu:
- Tăng IPAP 2 cm H2O nếu tăng CO2 máu kéo dài
- Tăng IPAP và EPAP 2 cm H2O nếu thiếu oxygen máu kéo dài
- Tối đa IPAP giới hạn ở 20–25 cm H2O (tránh căng dạ dày, cải thiện sự dễ chịu cho bệnh nhân)
- Tối đa EPAP giới hạn ở 10–15 cm H2O. Có thể tăng nếu thấy có nhịp 3 bị mất
- FiO2 điều chỉnh xuống mức thấp nhất với trị số SpO2 chấp nhận được
- Tần số RR dự phòng 12–16 lần/phút
- Nếu bệnh nhân không thể trigger, có rò rỉ lớn dẫn đến auto-cycling với PS, bệnh nhân có thể chuyển sang pressure controlled mode. Proportional assist ventilation (PAV) cũng có thể được sử dụng với kết quả đầy hứa hẹn.
Các chỉ số dự đoán thành công của thông khí không xâm lấn (1–2 h)
a) Giảm PaCO2 > 8 mmHg
b) Cải thiện pH > 0.06
c) Điều chỉnh được toan hô hấp.
Các chỉ số dự đoán thất bại
a) Độ nặng của bệnh
- Acidosis (pH < 7.25)
- Hypercapnia (> 80 and pH < 7.25)
- APACHE II score > 20
b) Mức độ trí giác [34,35]
- Thang điểm thần kinh/Kellye–Matthay score > 4 (li bì, chỉ thức tỉnh khi kích thích mạnh, làm theo y lệnh không thường xuyên)
- Encephalopathy score > 3 (lú lẫn nặng, ngủ ngày hoặc kích thích)
- Glasgow Coma Scale score < 8
c) Kém cải thiện với thông khí không xâm lấn sau 12–24h
Chỉ định của thông khí xâm nhập
Tiêu chuẩn chính (bất kỳ 1 tiêu chuẩn sau) [36,37]
- Ngừng thở
- Mất ý thức
- Đông kinh tâm thần đòi hỏi sự an thần
- Sự bất ổn định huyết động, huyết áp tâm thu < 70 hoặc > 180 mmHg
- Nhịp tim < 50 nhịp/phút với sự mất tỉnh táo
- Thở ngáp.
Tiêu chuẩn phụ (bất kỳ 2 tiêu chuẩn sau)
- RR > 35 lần/phút
- Toan máu hoặc pH <7.25
- PaO2 <40 mmHg hoặc PaO2/FiO2 < 200 mmHg mặc dù có oxy
- Giảm mức độ ý thức.
CỐ ĐỊNH ĐƯỜNG THỞ
Những bệnh nhân phải đặt nội khí quản (dựa trên mức độ nghiêm trọng của suy hô hấp hơn là bất kỳ giá trị tuyệt đối nào của PaCO2 hoặc RR), hỗ trợ hô hấp sau 24 giờ hoặc đến khi các cơ hô hấp mệt mỏi nghỉ ngơi đầy đủ. Các chế độ được kiểm soát nên được sử dụng càng ngắn càng tốt để tránh việc teo các cơ hô hấp và kéo dài thời gian thông khí cơ học không cần thiết.
Có thể gây mê bằng ketamine, propofol hoặc fentanyl với midazolam. Trước khi dẫn đầu, tình trạng dịch phải được tối ưu hóa ở những bệnh nhân này vì ảnh hưởng xấu huyết động có thể xảy ra do tăng DH và PEEPi. Nếu một bệnh nhân bị hạ huyết áp sau khi đặt nội khí quản không đáp ứng với truyền dịch, máy thở có thể bị ngắt kết nối và nếu BP cải thiện, có thể thực hiện việc bóp bóng bằng tay để giảm DH và có thể đánh giá trên SpO2. [38]
THÔNG KHÍ BỆNH NHÂN THỤ ĐỘNG
Thông khí phải được điều chỉnh dựa trên mức độ DH và auto-PEEP chứ không phải PaCO2. Chỉ có ba yếu tố xác định PEEP tự động: (1) Thông khí phút, (2) Tỷ lệ I:E, (3) Hằng số thời gian thở ra. Trong ba yếu tố, thông khí phút là yếu tố quan trọng nhất gây ra DH. Do đó, khi thông khí với bệnh nhân COPD, nên sử dụng VT nhỏ hơn, RR chậm, lưu lượng đỉnh cao nên được sử dụng với mục đích nhắm đến độ pH bình thường và không phải PaCO2 (tăng PaCO2 cho phép).
Các cài đặt ban đầu:
- Đặt FiO2 để nhắm mục tiêu SpO2 là 88-92%
- Thông khí theo chế độ điều khiển trợ giúp assist/control hoặc thông khí bắt buộc ngắt quãng (IMV ± PS)
- VT – 8 ml/kg, RR – 12-14 lần/phút, tỷ lệ I:E = 1:3 hoặc nhiều hơn tùy thuộc vào tính toán thời gian thở ra, tốc độ dòng chảy – 80-100 L/phút, áp suất thở cao điểm (PIP) < 40-45 cm H2O và Pplat < 30 cm H2O là chấp nhận được
- Điều chỉnh độ nhạy kích hoạt thường là – 1 đến 2 cm H2O cho pressure trigger và 2 L/phút cho flow trigger. Nếu kích hoạt là nhạy cảm, kiềm hô hấp có thể xảy ra trong khi kích hoạt quá ‘trơ’ sẽ làm tăng công thở (WOB)
- Cài đặt PEEP bắt đầu từ 5 cm H2O, và theo dõi thật sát Pplat hoặc PIP và huyết động học. Mức thấp nhất của PEEP cải thiện sự đồng bộ và giảm WOB từ mức A đến mức B bằng cách bù trừ được PEEP tự động ở bệnh nhân COPD (Hình 5). Tác động có lợi này của PEEP là rõ ràng nhất ở những bệnh nhân có giới hạn về lưu lượng (flow limitation) trong quá trình thở ra và có thể là do sự giảm tính không đồng nhất của phổi [1].
THÔNG KHÍ BỆNH NHÂN CÓ TỰ THỞ
- Chế độ PS/PC/PAV
- PS để tạo ra VT 8 ml/kg, trigger lưu lượng hoặc áp lực tối thiểu, lưu lượng đỉnh 80-100 L/phút
- PEEP có thể được thêm vào bắt đầu ở 5 cm H2O với mỗi bậc 2 cm H2O
- Quan sát WOB, RR và nhịp thở bị mất trong biểu đồ lưu lượng – thời gian cho thấy giảm RR và không có nhịp thở
- Theo dõi PIP và Pplat, nếu có bất kỳ sự gia tăng nào trong những áp lực này – giảm PEEP. Hiếm khi cần PEEP hơn 10 cm H2O
- Độ nhạy thở ra có thể được đặt nhiều hơn mức mặc định là 25%
- Nếu bệnh nhân vẫn không đồng bộ, cần phải tìm các nguyên nhân khác như sốt, đau, vv và trong trường hợp không tìm ra nguyên nhân khác, có thể dùng thuốc an thần.
CƠN CẤP CỦA HEN NẶNG
Ngoài các khuyến cáo tiêu chuẩn cho NPPV trong mọi tình huống, các khuyến cáo cụ thể cho bệnh nhân hen phế quản cấp tính hoặc nặng là:
- Y văn hiện tại hỗ trợ VT nhỏ (6-10 ml/kg), lưu lượng hít vào cao (80-100 L/phút) với PIP < 40- 45 cm H2O và Pplat < 25-30 cm H2O, để bảo vệ thời gian thở ra và giảm thiểu hyperinflation, barotrauma và hạ huyết áp [Hình 6]. RR cần phải có từ 8-12 lần/phút để đạt hyperinflation ít nhất có thể (PEEP < 10 cm H2O) và duy trì pH trong một phạm vi chấp nhận được, nếu có thể.
- Ngược lại với bệnh nhân COPD, áp dụng PEEP trong suốt quá trình hỗ trợ hô hấp của bệnh nhân bị hen nặng có DH do hạn chế lưu lượng cố định và không xẹp đường thở có thể gây ra nguy cơ tăng thể tích phổi, áp lực đường thở và áp lực trong lồng ngực, gây chèn ép tuần hoàn. Mặc dù một số nghiên cứu lâm sàng đã cho thấy chức năng hô hấp cải thiện (không có tác dụng không mong muốn) với CPAP hoặc với NIV và PEEP ở bệnh nhân hen cấp tính, việc sử dụng PEEP trong suốt thời gian thở máy của bệnh nhân suyễn cấp tính đang gây tranh cãi.
- Hơn nữa, vì mức độ biến đổi trong PEEP tự động theo từng nhịp thở có thể cao ở bệnh nhân hen thở máy, việc bổ sung PEEP áp dụng mà không tính đến sự biến đổi theo từng nhịp thở có thể dẫn đến sự quá căng phổi. Do đó, PEEP nên được sử dụng thận trọng ở những bệnh nhân hen, thở máy và điều chỉnh liều theo thời gian thực.
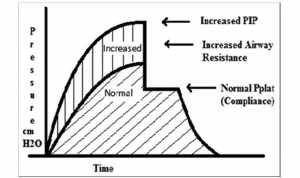
Giảm thông khí có kiểm soát dường như cải thiện kết quả lâm sàng của bệnh nhân có tình trạng hen suyễn. Khi giảm DH là một vấn đề và nếu không có tăng áp lực nội sọ và sự mất ổn định về huyết động học thì sự chấp nhận của toan máu vừa phải (pH ≥ 7.2) là hợp lý.
CAI MÁY
Một chính sách tích cực đối với cai máy là hợp lý ở bệnh nhân COPD vì không có khả năng cai máy thường liên quan đến tiên lượng xấu hơn và thông khí kéo dài. Nó bắt đầu khi các yếu tố thúc đẩy suy hô hấp là đảo ngược một phần hoặc hoàn toàn.
Cơ học hô hấp còn xấu và sự hiện diện của PEEP tự động khiến cho việc cai máy trở nên khó khăn đối với bệnh nhân COPD. Do đó, các yếu tố tăng sức đề kháng như kích cỡ ống NKQ, chất tiết đàm, kẹt ống và sự hiện diện của các bộ phận khuỷu tay hoặc HME trong mạch thở phải được tối ưu hóa để thúc đẩy cai máy sớm. Hơn nữa, bệnh nhân bị cor pulmonale có thể cần liều nhỏ thuốc tăng sức bóp cơ tim, thuốc lợi tiểu và chiến lược hạn chế dịch trong khi cai máy.
Cai máy thở có thể được thực hiện với chế độ PS cùng với thử nghiệm hít thở tự nhiên (SBTs). Việc cai máy theo trình tự (rút ngắn thời gian theo sau là NPPV) được tìm thấy là sự thay thế tốt ở những bệnh nhân có SBT thất bại [44,45]. Ngược lại, vai trò của phẫu thuật mở khí quản không chắc chắn, nhưng ở những bệnh nhân có cơ học hô hấp chưa cải thiện tốt, nó có thể giúp cai máy dễ dàng hơn.
TÓM TẮT
Hỗ trợ thở máy là một thủ thuật cứu sống bệnh nhân COPD và hen suyễn cấp tính. Mục đích điều trị là cải thiện việc trao đổi khí, giảm tải thông khí và hồi phục rối loạn hô hấp. Ngày nay, NPPV được coi là lựa chọn điều trị đầu tiên, trong khi thông khí xâm lấn được dành riêng cho suy hô hấp đe dọa tính mạng. Tuy nhiên, nó có thể làm tăng đáng kể tỷ lệ bệnh tật và tử vong nếu không được sử dụng đúng cách. Vì vậy, cần phải có một hiểu biết tốt về sinh lý bệnh học, cơ học và mô hình tắc nghẽn lưu lượng và DH để cung cấp thông khí phù hợp nhất cho những bệnh nhân này. Hình ảnh thông khí (lưu lượng, áp suất và thể tích) của hầu hết các máy thở hiện đại trở thành công cụ có giá trị trong những tình huống này và hỗ trợ chẩn đoán sớm và quản lý tình trạng của bệnh nhân trước khi trở nên diễn tiến xấu trên lâm sàng.





