Bài viết Thông khí cơ học ở bệnh nhân bị tổn thương não với tăng áp lực nội sọ được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Mechanical ventilation for raised intracranial pressure in the patient with cerebral insult
Tóm tắt
Thông khí cơ học là một can thiệp quan trọng trong việc quản lý bệnh nhân bị tổn thương não đang có dấu hiệu tăng áp lực nội sọ. Kiểm soát khí máu động mạch là điều cần thiết để duy trì lưu lượng máu não và do đó, ngăn ngừa thiếu máu não. Bài viết này tìm hiểu các tác động sinh lý của oxygengen và carbon dioxide đối với lưu lượng máu não. Thông khí cơ học được thảo luận và các chế độ được đánh giá theo quan điểm về lợi ích của bệnh nhân. Các phương pháp để thúc đẩy oxygen được xác định và kiểm soát carbon dioxide được khám phá trong nghiên cứu gần đây. Khuyến nghị về quản lý thông khí cho nhóm bệnh nhân này được đưa ra cho các điều dưỡng làm việc trong môi trường chăm sóc đặc biệt.
Kiểm soát khí máu động mạch là một thành phần thiết yếu trong quản lý hiệu quả bệnh nhân đã tăng áp lực nội sọ (ICP). Thông khí cơ học có thể được yêu cầu để đảm bảo rằng oxygen và carbon dioxide được duy trì trong phạm vi trị liệu được ủng hộ trên cơ sở kết quả nghiên cứu. Mục đích của bài viết này là để xem xét các thực hành hiện tại trong thở máy và kiểm soát tăng áp lực nội sọ.
Áp lực nội sọ
ICP được định nghĩa là áp lực tác động trong não thất bởi dịch não tủy (CSF) (Hickey, 2002). Nó cũng được xác định bởi mô não và lượng máu não trong sọ (Hickey, 2002). Một ICP bình thường là 0-10 mmHg (Hickey, 2002) và dao động trong các hoạt động sinh hoạt bình thường. Ví dụ, hắt hơi có thể tạo ra sự gia tăng áp lực thoáng qua trong đầu, thời gian tồn tại ngắn và không có tác dụng lâu dài. Tuy nhiên, ở những bệnh nhân bị chấn thương não, một sự gia tăng nhỏ có thể có những tác động hủy hoại dẫn đến thoát vị mô não từ khoang này sang khoang khác (Vos, 1993; Lindsay et al, 1998). Những tác động như vậy có thể xảy ra trước các tổn thương không thể phục hồi đối với thân não.
ICP tăng được định nghĩa là lớn hơn 15 mmHg (Hickey, 2002). Tăng áp lực nội sọ được phân loại là ICP hơn 20 mmHg (Hickey, 2002; Porth, 2003). Nếu ICP tăng lên, có các cơ chế bù có thể giúp ngăn ngừa thoát vị và do đó ngăn ngừa tổn thương thân não. Học thuyết Monroe- Kellie đã sửa đổi tuyên bố rằng trong cấu trúc cứng của hộp sọ, có ba thành phần chứa đầy, theo khả năng chứa chúng (Hickey, 2002). Ba thành phần này là mô não (80%), máu (10%) và CSF (10%). Học thuyết Monroe-Kellie tuyên bố rằng nếu có sự gia tăng ở một trong các ngăn thì phải có sự giảm đi qua lại ở một trong hai ngăn còn lại. Điều này sẽ dẫn đến việc duy trì ICP bình thường (Hickey, 2002). Để đạt được ICP bình thường, các cơ chế như tăng hấp thu CSF và chuyển dịch CSF sang khoang dưới màng cứng cột sống xảy ra (Hickey, 2002). CSF hầu hết có thể điều chỉnh sự thay đổi về thể tích để đáp ứng với sự gia tăng ICP, trong khi mô não ít có khả năng giảm thể tích.
Khả năng đối phó với sự gia tăng ICP khác nhau từ người này sang người khác và cuối cùng phụ thuộc vào độ giãn nở (compliance) của mô não (Porth, 2003). Độ giãn nở là khả năng của bộ não đối phó với áp lực gia tăng nhưng vẫn duy trì ICP ổn định. Độ giãn nở được thể hiện bằng tỷ lệ thay đổi thể tích với kết quả thay đổi về áp lực. Về cơ bản, nó có thể được coi là “sự chậm chạp” (slackness) của các thành phần trong hộp sọ. Khi được vẽ dưới dạng biểu đồ, sẽ thu được đường cong áp lực/thể tích não rất điển hình (Hình 1).
Đường cong này chứng tỏ rằng ICP có thể duy trì ổn định mặc dù tăng thể tích.
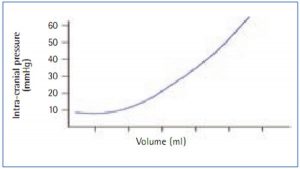
Tuy nhiên, có một điểm khi những thay đổi về thể tích tạo ra tăng ICP (Hickey, 2002). Ở giai đoạn này, độ giãn nở của não đang thay đổi và nếu nguồn tăng thể tích không được giải quyết, cuối cùng những thay đổi nhỏ về thể tích sẽ dẫn đến sự gia tăng lớn không phù hợp trong ICP. Do đó độ giãn nở của não thấp và độ đàn hồi của não (hoặc độ cứng) cao. Tại thời điểm này, khả năng có kết quả khả quan cho bệnh nhân là rất mong manh và có khả năng thoát vị não (Hickey, 2002).
Lưu lượng máu não
Tăng áp lực nội sọ dẫn đến giảm lưu lượng máu não vì lưu lượng máu bị cản trở khi nó cố gắng chảy qua các mạch máu bị nén (Brinker et al, 1992). Điều này có thể dẫn đến giảm việc cung cấp oxygen não (Cruz et al, 1993) và thiếu máu não có thể phát triển. Lưu lượng máu não bình thường là 50 ml/phút (hoặc 750 ml/phút trong não 1500 g) (Hickey, 2002) và não có thể tự động lưu lượng máu não để duy trì lưu lượng ổn định (Vander et al, 2000). Điều này thường là để đáp ứng với áp lực tưới máu não (CPP), hoặc gradient huyết áp, xuyên não (Hickey, 2002). CPP là sự khác biệt giữa áp lực động mạch trung bình toàn thân và ICP, và thường là khoảng 80-100 mmHg (Hickey, 2002), với ít nhất là 60 mmHg được yêu cầu để tưới máu thần kinh.
Tự động hóa đảm bảo lưu lượng máu não tương đối ổn định mặc dù có thay đổi huyết áp hệ thống (Vander et al, 2000). Do đó, nếu huyết áp hệ thống tăng, mạch máu não co lại; nếu huyết áp giảm, các mạch giãn ra. Tự động hóa chỉ có thể xảy ra trong một phạm vi nhất định của huyết áp động mạch trung bình toàn thân (50-150 mmHg). Ngoài phạm vi này, lưu lượng máu não trở thành áp lực thụ động khi nó thay đổi theo áp lực động mạch trung bình (Bernsten và Soni, 2003) (Hình 2). Do đó, nếu áp lực động mạch trung bình giảm, thì lưu lượng mạch máu não cũng giảm.
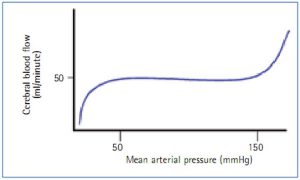
CPP không tính đến sức cản mạch máu não sẽ làm thay đổi lưu lượng máu não. Mặc dù vậy, theo dõi ICP và tính toán CPP là phương pháp thông thường để ước tính tưới máu não (Hickey, 2002), khi xem xét các ảnh hưởng đến lưu lượng máu não, thì có thể xác định được các biến số có thể được xử lý trong chăm sóc bệnh nhân. Lưu lượng máu não có thể được tính toán như sau: CBF = K x [CPP(d^4) / 8lv]
Có thể điều khiển một số biến số này như áp lực động mạch trung bình và ICP (và do đó, CPP), đường kính của mạch máu não và độ nhớt của máu. Trong số này, đường kính mạch máu có ảnh hưởng lớn nhất đến lưu lượng máu não và do đó, cung cấp oxygen cho não (Muizelaar và Schroder, 1994).
Lưu lượng máu não và khí máu động mạch
Khí máu động mạch có thể làm thay đổi đường kính của các mạch máu não và do đó, có thể ảnh hưởng đến lưu lượng máu não (Hickey, 2002). Do đó, điều cần thiết là carbon dioxide và oxygen được kiểm soát chặt chẽ.
Carbon dioxide
Nồng độ ion hydro ảnh hưởng đến cơ trơn mạch máu với sự gia tăng nồng độ (và do đó làm giảm pH hoặc nhiễm toan) dẫn đến thư giãn cơ trơn và do đó giãn mạch. Điều này sẽ làm tăng lưu lượng máu não và cả ICP theo học thuyết Monroe-Kellie đã được sửa đổi. Bởi vì các ion hydro là sản phẩm phụ của quá trình chuyển hóa carbon dioxide, do đó, việc tăng nồng độ carbon dioxide sẽ làm tăng nồng độ ion hydro và dẫn đến sự giãn mạch não (Yoshihara et al, 1995). Ngược lại, việc giảm nồng độ carbon dioxide sẽ dẫn đến co mạch và do đó làm giảm lưu lượng máu não và ICP. Theo quan điểm này, carbon dioxide được coi là một trong những yếu tố chính ảnh hưởng đến lưu lượng máu não và ICP (Hình 3). Carbon dioxide cần phải được kiểm soát cẩn thận để tránh cả tăng lưu lượng máu não (tăng thể tích máu não) và thiếu máu cục bộ.
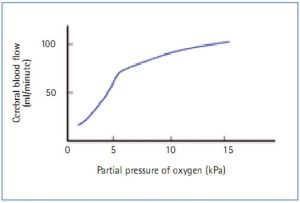
Oxygen
Nếu hàm lượng oxygen trong máu giảm, lưu lượng máu não tăng lên trong nỗ lực duy trì oxygen hóa não (Hình 4). Điều này cũng sẽ làm tăng ICP (Price et al, 2003). Lượng carbon dioxide và oxygen phần lớn có thể được kiểm soát thông qua quản lý hỗ trợ hô hấp cẩn thận và do đó quản lý khí máu động mạch thông qua chiến lược thông khí cơ học.
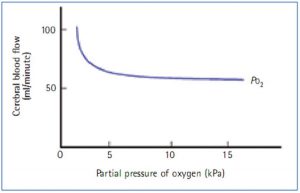
Thông khí cơ học
Thuật ngữ “thông khí” liên quan đơn giản đến sự chuyển động của không khí trong và ngoài phế nang (Hudak et al, 1998). Trong thông khí tự phát, điều này đạt được bằng sự co thắt của cơ hô hấp. Sự co thắt của cơ hoành dẫn đến sự gia tăng dung tích thẳng đứng của ngực trong khi sự co thắt của các cơ liên sườn làm tăng dung tích nằm ngang khi xương sườn được nâng lên và ra ngoài (Vander et al, 2000). Sự kết hợp của sự co thắt của hai nhóm cơ này làm giảm áp lực trong lồng ngực xuống dưới áp lực khí quyển và do đó không khí đi vào phổi để cân bằng hai áp lực; do đó thì hít vào xảy ra. Thở ra xảy ra thông qua việc thư giãn các cơ hô hấp và do đó, không khí rời khỏi phổi khi thể tích trong lồng ngực bị giảm (Vander et al, 2000). Do đó, thở tự nhiên xảy ra thông qua việc tạo ra một áp lực âm trong lồng ngực.
Tuy nhiên, máy thở cơ học hiện đại “đẩy” không khí vào phổi chống lại độ chênh lệch áp lực, do đó buộc phổi phải giãn nở. Kết quả là họ tạo ra một áp lực dương trong phổi. Điều này đòi hỏi bệnh nhân phải đặt nội khí quản bằng ống nội khí quản hoặc mở khí quản (Adam và Osbourne, 2005). Về cơ bản, thở máy là sự đảo ngược của hơi thở tự phát, và nhiều biến chứng của thở máy là kết quả của áp lực dương trong lồng ngực. Mặc dù thở máy có liên quan đến các biến chứng không mong muốn như giảm cung lượng tim và do đó giảm tưới máu mô (Adam và Osbourne, 2005), nó cho phép nhóm chăm sóc chuyên sâu cố gắng kiểm soát ICP và tưới máu não thông qua việc sử dụng các chiến lược quản lý trị liệu là không thể không thở máy.
Thông khí áp lực dương
Có hai cách chính trong đó máy thở cơ học có thể mang lại hơi thở cho bệnh nhân: thông khí theo chu kỳ thể tích và thông khí theo chu kỳ áp lực.
Thông khí theo chu kỳ thể tích
Thông khí theo chu kỳ thể tích liên quan đến thông khí cơ học trong đó thể tích khí lưu thông được xác định trước được đưa đến bệnh nhân theo nhịp hô hấp định sẵn (Adam và Osbourne, 2005). Một khi thể tích đã đạt được, thở ra xảy ra. Mặc dù thể tích được kiểm soát, áp lực nội tại về cơ bản không được kiểm soát, với độ giãn nở phổi của bệnh nhân xác định áp lực được tạo ra bởi việc cung cấp thể tích này (Adam và Osbourne, 2005). Áp lực đường thở cao có thể dẫn đến barotrauma và có khả năng tràn khí màng phổi. Ngoài ra, áp lực đường thở cao làm trầm trọng thêm các tác dụng phụ không mong muốn của thở máy. Tuy nhiên, khi thể tích phút bệnh nhân (thể tích khí lưu thông x nhịp thở) đang được kiểm soát, sự thanh thải carbon dioxide cũng được kiểm soát.
Thông khí theo chu kỳ áp lực
Trong thông khí theo chu kỳ áp lực, áp lực theo quy định được đặt ra và máy thở cho phép thì hít vào xảy ra cho đến khi đạt được áp lực đặt trước đó (Adam và Osbourne, 2005). Sau đó thở ra sẽ xảy ra. Do đó, thể tích khí lưu thông của mỗi hơi thở được xác định bởi áp lực đặt liên quan đến độ giãn nở phổi của bệnh nhân. Nếu một bệnh nhân có phổi cứng, một thể tích nhỏ hơn sẽ được cung cấp cho một áp lực nhất định so với một bệnh nhân có phổi giãn nở tốt hơn. Mặc dù thể tích khí lưu thông thay đổi (và, do đó, thể tích phút) có liên quan đến thông khí theo chu kỳ áp lực, nó được coi là bảo vệ phổi nhiều hơn và để tăng cường việc huy động phế nang bị xẹp, làm tăng trao đổi khí (Bernsten và Soni, 2003). Theo quan điểm về thể tích khí lưu thông thay đổi và do đó thể tích phút, thông khí theo chu kỳ áp lực thường không được sử dụng cho bệnh nhân bị tổn thương não vì carbon dioxide và do đó lưu lượng máu não có thể được kiểm soát kém.
Có các chế độ khác nhau của cả hai thông khí chu kỳ thể tích và thông khí chu kỳ áp lực (Bảng 2). Những chế độ cung cấp kiểm soát tốt về thể tích phút (và, do đó, trên carbon dioxide) được ủng hộ (Myburgh, 2003). Do đó, một chế độ chu kỳ thể tích thường được đề nghị. Tuy nhiên, trong các chế độ này, áp lực nội sọ không được kiểm soát, điều này có thể làm giảm lưu lượng máu não do giảm cung lượng tim và tăng ICP do giảm trở lại tĩnh mạch (Adam và Osbourne, 2005).
Một số máy thở cơ học hiện đại cho phép các chế độ thông khí kết hợp cả thông khí theo chu kỳ và áp lực. Các chế độ này bao gồm kiểm soát thể tích được điều chỉnh áp lực và thông khí bắt buộc ngắt quãng đồng bộ giới hạn áp lực. Điều này cho phép một thể tích khí lưu thông được thiết lập được phân phối nhưng trong giới hạn áp lực. Do đó, carbon dioxide có thể được kiểm soát, cũng như áp lực trong lồng ngực. Đối với bệnh nhân bị tổn thương não, cả hai tính năng này đều được mong muốn; do đó các chế độ này rất hữu ích cho nhóm bệnh nhân này.
Thiếu oxygen
Các tác động bất lợi của thiếu oxygen đã được nêu ở trên. Khuyến cáo rằng áp lực riêng phần của oxygen (PO2) trong máu ở mức bình thường là 11-13 kPa (McLeod, 2004). Do đó, lượng oxygen cung cấp cho bệnh nhân có thể được thao tác để đảm bảo PO2 đầy đủ. Tuy nhiên, các tình huống có thể phát sinh trong đó việc tăng nồng độ oxygen không duy trì PO2 trong phạm vi bình thường. Điều này có thể là kết quả của viêm phổi, xẹp phổi hoặc độ giãn nở phổi giảm (Adam và Osbourne, 2005). Trong nỗ lực tăng cường oxygen hóa, chế độ thông khí có thể được điều chỉnh thông qua một số ứng dụng, bao gồm áp lực dương cuối thì thở ra (PEEP) và tỷ lệ hít vào:thở ra (I: E).
Áp lực dương cuối thì thở ra (PEEP)
Thông thường, thể tích khí hít vào được thở ra hoàn toàn; do đó áp lực cuối thì thở ra phế nang bình thường tương đương với áp lực khí quyển (Marino, 1998). Bằng cách áp dụng PEEP, phế nang ở xa ít có khả năng sụp đổ khi thở ra. Do đó PEEP có thể mở lại phế nang bị sụp đổ. Sụp đổ phế nang làm suy yếu trao đổi khí và có thể khiến bệnh nhân bị thiếu oxygen (Marino, 1998). PEEP cải thiện trao đổi khí và tăng độ giãn nở phổi do đó làm tăng cường thông khí cơ học.
Tuy nhiên, PEEP đẩy dạng sóng áp lực dương thông khí cơ học lên trên, do đó phóng đại ảnh hưởng của thông khí cơ học đến hoạt động của tim. Do đó, xu hướng thở máy để giảm cung lượng tim và hồi lưu tĩnh mạch sẽ lớn hơn với PEEP (Marino, 1998). Myburgh (2003) khuyến cáo rằng mức độ thấp của PEEP (5-10 cmH2O) có thể được sử dụng ở những bệnh nhân bị tổn thương não để cải thiện quá trình oxygen hóa, mặc dù nên sử dụng thận trọng ở mức độ cao hơn để xem xét các tác động tim mạch. Cấp độ > 15 cmH2O có thể làm giảm trở lại tĩnh mạch não, do đó làm tăng ICP, mặc dù điều này được thừa nhận rằng điều này là không phổ biến.
Tỷ lệ hít vào: thở ra
Tỷ lệ I:E có thể được xem đơn giản là thời gian hít vào và thời gian thở ra trong một chu kỳ thở. Thông thường đây là 1:2, có nghĩa là thở ra mất gấp đôi thời gian thì hít vào (Adam và Osbourne, 2005). Trong tình huống sụp đổ phế nang và do đó giảm PO2, nó có thể có ích để kéo dài thời gian hít vào cho đến tạo tỷ lệ nghịch 2:1 (Marino, 1998). Mặc dù điều này có thể cải thiện trao đổi khí và do đó oxygen hóa, thời gian hít vào kéo dài có thể làm tăng xu hướng làm trống phổi không đủ (Marino, 1998). Điều này có khả năng có thể gây ra tự động PEEP và siêu bơm phồng phổi cũng như loại bỏ carbon dioxide không đầy đủ. Những tác dụng này có thể gây bất lợi cho bệnh nhân tăng áp lực nội sọ.
Mức độ carbon dioxide
Việc kiểm soát áp lực một phần của carbon dioxide (PCO2) là rất cần thiết trong quản lý thông khí của nhóm bệnh nhân này. PCO2 như đã chỉ ra trước đây phần lớn kiểm soát bởi thể tích phút của bệnh nhân. vì thế tăng thể tích phút sẽ làm giảm PCO2. Điều này thường đạt được thông qua việc tăng tần số hô hấp để đạt được PCO2 ở mức thấp hơn trong phạm vi bình thường là 4,5-6 kPa (McLeod, 2004). Tăng thông khí (do đó sẽ dẫn đến hypocapnia hoặc giảm PCO2) từ lâu đã được thừa nhận là một cách để giảm ICP thông qua co mạch máu não và do đó làm giảm thể tích máu não (Stocchetti et al, 2005). Tuy nhiên, nguy cơ tăng thông khí là não có thể bị thiếu máu do giảm lưu lượng máu não sau đó. Fortune et al (1995) đã chứng minh rằng giảm PCO2 xuống 26 mmHg (3,5 kPa) ở những người tình nguyện khỏe mạnh làm giảm thể tích máu não 7,2% và lưu lượng máu não giảm 30,7%.
Một số nghiên cứu đã xác nhận tác dụng phụ của tăng thông khí đối với lưu lượng máu não ở bệnh nhân chấn thương đầu (Sioutos et al, 1995; Dahl et al, 1996; Skippen et al, 1997). McLaughlin và Marion (1996) cũng đã chỉ ra rằng có sự gia tăng đáp ứng vận mạch đối với carbon dioxide trong các trường hợp dập não và mô phù xung quanh; tác dụng này, kết hợp với giảm tưới máu tương đối, có thể dẫn đến các mô dập não đặc biệt nhạy cảm với thiếu máu cục bộ có thể bị nặng thêm do giảm thông khí.
Các nghiên cứu sâu hơn đã được thực hiện để xác định xem việc giảm lưu lượng máu não sau khi tăng thông khí có dẫn đến thiếu máu cục bộ có ý nghĩa lâm sàng như đã được chứng minh qua các nghiên cứu chuyển hóa. Cruz (1998) lập luận rằng sự giảm lưu lượng máu não sau khi tăng thông khí là chấp nhận được miễn là các thông số chuyển hóa được duy trì. Diringer et al (2000) đã chỉ ra rằng tăng thông khí ngắn không làm suy yếu quá trình chuyển hóa não toàn thể và trích xuất oxygen ở những bệnh nhân bị chấn thương đầu nghiêm trọng, mặc dù lưu lượng máu não toàn thể giảm rõ rệt.
Thông tin về tình trạng trao đổi chất của não có thể thu được bằng cách theo dõi máu tĩnh mạch cảnh, từ các nghiên cứu vi phân, từ chụp cắt lớp phát xạ positron (PET) hoặc từ quang phổ chụp cộng hưởng từ (MRI) (Stocchetti et al, 2005). Nồng độ lactate cao đã được tìm thấy trong các mẫu CSF sau chấn thương đầu nghiêm trọng. Lactate là một chỉ số của hô hấp kị khí và do đó việc cung cấp oxygen không đủ đến các mô (Bernsten và Soni, 2003). Bằng cách phân tích máu tĩnh mạch cổ, nồng độ lactate đã được tìm thấy tăng tỷ lệ thuận với mức độ nghiêm trọng của chấn thương đầu trong 48 giờ đầu sau chấn thương (Robertson et al, 1987). Điều này cũng được tìm thấy bởi Murr et al (1996) trong nghiên cứu của họ cho thấy sự khác biệt về mức độ lactate não đã tăng đáng kể từ ngày đầu tiên đến ngày thứ năm sau chấn thương.
Các nghiên cứu vi phân đã chỉ ra mối tương quan giữa nồng độ oxygen mô não thấp và mức độ tăng lactate (Robertson et al, 1998). Marion et al (2002) đã báo cáo tác dụng cụ thể của tăng thông khí đối với nồng độ ngoại bào của lactate, glutamate và pyruvate. Các nghiên cứu tăng thông khí, hạ thấp PCO2 xuống 8-12 mmHg (1.06-1.6 kPa) đã được thực hiện trong 24-36 giờ sau chấn thương và một lần nữa sau 3-4 ngày sau chấn thương. Vào lúc 24-36, sự tăng thông khí dẫn đến sự gia tăng đáng kể về lượng lactate và tỷ lệ giữa lactate và pyruvate. Sau 3-4, mức độ lactate một lần nữa tăng đáng kể sau khi tăng thông khí, nhưng sự khác biệt về tỷ lệ lactate: pyruvate không đáng kể. Điều này dường như chỉ ra rằng hiệu quả của giảm thông khí rõ rệt hơn trong giai đoạn đầu sau chấn thương đầu. Điều này cho thấy nên tránh tăng thông khí trong thời gian này.
Mặc dù có rất nhiều bằng chứng xác định các tác động có thể có hại của tăng thông khí, nhưng chỉ có một thử nghiệm ngẫu nhiên tiền cứu đã nghiên cứu ảnh hưởng của tăng thông khí đến kết quả lâm sàng. Muizelaar và cộng sự (1991) đã so sánh kết quả của những bệnh nhân bị tăng thông khí với PCO2 là 25 mmHg (3,3 kPa) trong 5 ngày với những bệnh nhân có PCO2 được duy trì ở mức 35 mmHg (4,6 kPa). Ở cả 3 và 6 tháng sau chấn thương, những bệnh nhân có PCO2 ở mức cao hơn 35 mmHg có kết quả tốt hơn đáng kể. Chính nghiên cứu này đã thay đổi cách bệnh nhân tăng áp lực nội sọ được thở máy, với các khuyến nghị rằng tăng thông khí kéo dài (PCO2 = 25 mmHg (3,3 kPa)) là không có lợi, và PCO2 < 35 mmHg (<4,6 kPa) cần tránh trong 24 giờ đầu tiên sau khi tổn thương não. Myburgh (2003) khuyến nghị PCO2 nên được duy trì ở 36- 40 mmHg (4,8-5,3 kPa) trong khi Stocchetti và cộng sự (2005) đề xuất rằng nên sử dụng cẩn thận tăng thông khí để kiểm soát ngắn hạn ICP tăng có thể hữu ích, với sự đồng thuận rằng nên tránh tăng thông khí tới mức PCO2 < 30 mmHg (<4 kPa). Kết hợp với điều này, độ pH nên được duy trì ở mức bình thường là 3,5-4,5 (Price, 2003).
| Bảng 2. Các chế độ thông khí cơ học khác nhau | ||||
| Chế độ thông khí | Nguyên tắc | Chỉ định | Ưu điểm | Nhược điểm |
| Thông khí kiểm soát thể tích | Cài đặt tần số thở và Vt cung cấp. Bệnh nhân không thể tự thở | Cài đặt tần số thở và Vt cung cấp. Bệnh nhân không thể tự thở | Thể tích phút được kiểm soát, vì vậy PCO2 được kiểm soát | Không kiểm soát được áp lực trong lồng ngực. Có thể ảnh hưởng xấu đến tim mạch, nguy cơ tràn khí màng phổi, barotrauma. Cần giãn cơ, an thần. |
| SIMV theo kiểm soát thể tích | Cài đặt tần số thở và Vt cung cấp. Máy thở sẽ đồng bộ với nhịp tự thở bệnh nhân | Bệnh nhân cần thiết hỗ trợ hô hấp nhưng có thể thở tự nhiên nếu cần | Thể tích phút có thể kiểm soát nếu bệnh nhân không có nhịp thở tự nhiên nào. Không cần giãn cơ. Ít cần an thần. | Không kiểm soát được áp lực trong lồng ngực. |
| Thông khí kiểm soát áp lực | Cài đặt tần số thở và Vt cung cấp. Bệnh nhân không thể tự thở | Bệnh nhân cần thiết hỗ trợ hô hấp hoàn toàn. Trao đổi khí tổn thương nặng. ALI/ARDS | Áp lực trong lồng ngực được kiểm soát. Thông khí bảo vệ hơn. Ít tác dụng phụ tim mạch. | Thể tích khí lưu thông phụ thuộc mức giới hạn áp lực và độ giãn nở phổi bệnh nhân. Thể tích khí lưu thông và thể tích phút dao động nên kiểm soát kém PCO2. Cần giãn cơ, an thần. |
| SIMV theo kiểm soát áp lực, BiPAP | Cài đặt tần số thở và mức giới hạn áp lực. Máy thở sẽ đồng bộ với nhịp tự thở bệnh nhân | Bệnh nhân cần thiết hỗ trợ hô hấp nhưng có thể thở tự nhiên nếu cần | Áp lực trong lồng ngực được kiểm soát. Thông khí bảo vệ hơn. Ít tác dụng phụ tim mạch. Không cần giãn cơ. Ít cần an thần. | Thể tích khí lưu thông và thể tích phút dao động nên kiểm soát kém PCO2. |
| Kiểm soát thể tích điều hòa áp lực/SIMV theo kiểm soát áp lực | Cài đặt tần số và thể tích khí lưu thông, mức giới hạn áp lực | Thể tích phút và áp lực trong lồng ngực được kiểm soát. Khi độ giãn nở phổi quá kém, sẽ gây tăng áp lực quá mức với thông khí kiểm soát thể tích, hay thể tích quá thấp với thông khí kiểm soát áp lực | Thể tích phút và áp lực trong lồng ngực được kiểm soát. Ít tác dụng phụ tim mạch hơn so với kiểm soát thể tích | Có thể cần đặt mức giới hạn áp lực tương đối cao để máy thở có thể cung cấp đủ thể tích. Bệnh nhân có thể cần thuốc giãn cơ và an thần |
Can thiệp hô hấp
Bệnh nhân được đặt nội khí quản và thở máy thường xuyên sẽ yêu cầu hút đàm qua nội khí quản (hút đàm nội khí quản), trong một nỗ lực để làm sạch dịch tiết phổi và để duy trì sự thông thoáng đường thở. Đối với điều dưỡng chăm sóc bệnh nhân được đặt nội khí quản và thở máy có tăng ICP hoặc tăng áp lực nội sọ, một vấn đề nan giải xuất hiện liên quan đến việc hút qua nội khí quản (Price, 2003). Chất tiết ứ đọng có thể dẫn đến thiếu oxygen và tăng CO2 máu sẽ làm tăng ICP, nhưng hút qua nội khí quản cũng có thể dẫn đến tăng mạnh trong ICP. Thở oxygen trước với oxygen 100% trong 1 phút trước khi hút nội khí quản có thể làm giảm đáng kể tác dụng giảm oxygen của hút nội khí quản, do đó hạn chế nguy cơ thiếu máu não do hút qua nội khí quản (Wong, 2000; McLeod, 2004).
Tăng thông khí trước khi hút nội khí quản cũng có thể giúp giảm sự gia tăng ICP trong quá trình hút nội khí quản. Kerr et al (1997) đã thực hiện một nghiên cứu ngẫu nhiên, trong đó họ phát hiện ra rằng sự giảm thông khí có kiểm soát trong thời gian ngắn với 30 hơi thở mỗi phút làm giảm PCO2, làm giảm lưu lượng máu não trong một thời gian ngắn. Điều này dẫn đến ICP tăng ít hơn do hút qua nội khí quản, vẫn được duy trì tưới máu não. Tuy nhiên, các nhà nghiên cứu đặt câu hỏi liệu đây có thực sự là biện pháp bảo vệ thần kinh hay không, đặc biệt là nếu có các vùng thiếu máu cục bộ trong mô não sẽ bị thiếu máu cục bộ nhiều hơn trong thời kỳ lưu lượng máu não giảm. Một liều thuốc an thần nhỏ trước khi hút qua nội khí quản hoặc can thiệp đường hô hấp cũng có thể giúp ngăn ngừa tăng huyết áp và ICP (Adam và Osbourne, 2005). Cách tiếp cận này, tuy nhiên, sẽ phải được cân nhắc với nguy cơ gây giảm huyết áp đột ngột và do đó, giảm lưu lượng máu não.
Kết luận
Bệnh nhân tăng áp lực nội sọ đặt ra một thách thức đối với đội ngũ chăm sóc tích cực trong việc đảm bảo duy trì lưu lượng máu não và tránh được thiếu máu não. Thông khí cơ học là một thành phần cốt lõi để quản lý nhóm bệnh nhân này. Hypoxia phải tránh và carbon dioxide cần phải được kiểm soát trong phạm vi khuyến nghị. Có thể cần phải tăng thông khí cho bệnh nhân trong một thời gian ngắn để giảm sự gia tăng quan trọng của ICP trước khi can thiệp phẫu thuật hoặc các thủ tục chẩn đoán. Chế độ thông khí là một khía cạnh quan trọng để đảm bảo rằng điều này xảy ra. Một chế độ chu kỳ thể tích cho phép kiểm soát cẩn thận carbon dioxide. Tuy nhiên, những hậu quả bất lợi của thở máy như giảm cung lượng tim và tăng áp lực nội sọ cần phải được giảm thiểu. Do đó, một chế độ thông khí như điều khiển thể tích được điều chỉnh áp lực, cho phép điều này, được khuyến nghị.
Thông khí cơ học chỉ là một khía cạnh trong quản lý của nhóm bệnh nhân này. Không có nó, các chiến lược điều trị khác như hạ thân nhiệt trị liệu sẽ là không thể.
| Những điểm chính |
|



![[Cảnh báo] Để cải thiện thiếu máu não nên ăn gì? Kiêng ăn gì? Thiếu máu não nên ăn gì?](https://www.healcentral.org/wp-content/uploads/2020/11/thieu_mau_nao_nen_an_gi1-218x150.jpg)

