Bài viết Các biến chứng phổi ở bệnh nhân tổn thương não nặng được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Pulmonary complications in patients with severe brain injury
Các biến chứng về phổi phổ biến trong quần thể bị bệnh lý thần kinh nặng. Các triệu chứng của suy hô hấp, viêm phổi, tổn thương phổi cấp và hội chứng suy hô hấp cấp (ALI/ARDS), phù phổi, dập phổi và tràn khí/tràn máu màng phổi và thuyên tắc phổi thường gặp trong bệnh cảnh tổn thương não nghiêm trọng. Chấn thương não trực tiếp, giảm mức độ ý thức và không có khả năng bảo vệ đường thở, phá vỡ các hàng rào phòng vệ tự nhiên, giảm cử động, và các rối loạn thần kinh thứ phát liên quan đến tổn thương não nghiêm trọng là nguyên nhân chính gây nên biến chứng phổi ở bệnh nhân bệnh thần kinh nặng. Các chiến lược phòng ngừa và liệu pháp hiện tại và tương lai cần được thực hiện để tránh và điều trị sự phát triển của những biến chứng nội khoa đe dọa tính mạng này.
Giới thiệu
Các biến chứng về phổi rất phổ biến trong quần thể bệnh nhân bị bệnh lý thần kinh nặng. Suy hô hấp, viêm phổi, tràn dịch màng phổi và tràn mủ màng phổi, tổn thương phổi cấp tính và hội chứng suy hô hấp cấp (ALI/ARDS), phù phổi, và thuyên tắc phổi (PE) do thuyên tắc tĩnh mạch (thuyên tắc huyết khối tĩnh mạch, VTE, venous thromboembolism) thường gặp ở những bệnh nhân này [1-7]. Ngoài ra, chấn thương ngực trực tiếp và bệnh nhân tổn thương não do chấn thương (TBI) không được miễn trừ các biến chứng trực tiếp như gãy xương sườn, mảng sườn di động, dập phổi, và tràn máu/tràn khí màng phổi. Thật không may, sự hiện diện của những biến chứng này cần thiết đưa bệnh nhân vào ICU và ngăn ngừa việc cử động sớm, và điều này làm tăng khả năng phát triển khuyết tật thứ phát.
Các triệu chứng của suy hô hấp, viêm phổi, tổn thương phổi cấp và hội chứng suy hô hấp cấp (ALI/ARDS), phù phổi, dập phổi và tràn khí/tràn máu màng phổi và thuyên tắc phổi thường gặp trong bệnh cảnh tổn thương não nghiêm trọng.. Mục tiêu của ICU là ngăn ngừa, điều trị, và tối ưu hóa thiếu oxy máu và duy trì việc cung cấp oxy để hạn chế những biến chứng thần kinh thứ phát. Trong khi không có loại thuốc khả thi nào để nhắm mục tiêu này, các phương pháp dự phòng để giảm thiểu các biến chứng về phổi như sử dụng các kỹ thuật tại giường như chọc hút khoang màng phổi, dẫn lưu màng phổi, chiến lược thở máy bảo vệ phổi, chiến lược để phòng ngừa viêm phổi liên quan đến thở máy (VAP, ventilator associated pmeumonia), và dự phòng huyết khối tĩnh mạch sâu (DVT, deep venous thrombosis) là nền tảng trong việc phòng ngừa và quản lý các biến chứng phổi ở bệnh nhân bị chấn thương não nặng.
Cuối cùng, có thể cần phải xây dựng, nghiên cứu trong các thử nghiệm lâm sàng, và triển khai thực hành lâm sàng, để tối ưu hóa kết cục trong quần thể bệnh nhân này, có thể cần phải xây dựng các chiến lược bổ sung nhằm mục tiêu các điểm cuối về sinh lý học như trong điều kiện lâm sàng. Bài báo này tóm tắt những biến chứng quan trọng nhất của phổi gặp phải trong quần thể bệnh nhân bị bệnh lý thần kinh nặng.
Các biến chứng về phổi liên quan đến chấn thương ngực trực tiếp
Bệnh nhân tổn thương não do chấn thương (TBI, traumatic brain injury) thường có nguy cơ tổn thương do chấn thương khác như gãy xương sườn, dập phổi, mảng sườn di động, và tràn khí/tràn máu màng phổi. Thực hiện đánh giá theo tiêu chuẩn thông thường ở nạn nhân chấn thương cung cấp một phác đồ rất nhạy để chẩn đoán những thương tích này.
Tràn khí màng phổi do chấn thương, được xác định là sự xâm nhập của không khí vào khoang màng phổi, có thể xảy ra sau chấn thương ngực xâm nhập hoặc không xâm nhập.
- Tràn khí màng phổi đơn giản (simple pneumothorax) xảy ra khi không có thông nối với môi trường bên ngoài hay bất kỳ sự thay đổi của cấu trúc trung thất (Hình 1),
- Tràn khí màng phổi mở (open pneumothorax) xảy ra khi có thông nối hoặc rò tồn tại giữa khoang màng phổi và môi trường (vết thương hút, sucking wound), và cuối cùng,
- Tràn khí màng phổi có áp lực (tension pneumothorax) xảy ra khi chổ thoát khí ra môi trường ngoài bị ngăn chặn, và tăng áp lực trong khoang màng phổi dẫn đến sự di lệch trung thất và ảnh hưởng xấu đến huyết động.
Xử trí tràn khí màng phổi nhỏ trong một nạn nhân bị chấn thương có kèm thông khí áp lực dương đòi hỏi phải đặt ống dẫn lưu ngực. Tuy nhiên, những bệnh nhân bị chấn thương ngực kín, có thể thở tự nhiên và có nguy cơ tràn khí tiềm ẩn, phải được theo dõi trong mức an toàn tốt nhất [9]. Tràn khí màng phổi mở cần phải: (a) đặt ống dẫn lưu ngực, (b) thông khí cơ học, và (c) phẫu thuật sửa chữa vết thương ngay lập tức. Điều trị tràn khí màng phổi có áp lực đòi hỏi phải sử dụng phương pháp giải áp ngay lập tức (chọc dò khoang màng phổi giải áp bằng kim) và/hoặc đặt nhanh ống dẫn lưu màng phổi. Sự tồn tại của rò rỉ khí và tràn khí màng phổi là dấu hiệu của một rò phế quản-màng phổi và do đó đòi hỏi phải phẫu thuật sửa chữa ngay lập tức với mở ngực (Hình 1).
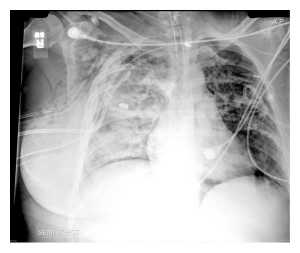
Tràn máu màng phổi là sự tích tụ máu trong khoang màng phổi và có thể là nguyên nhân gây ra tình trạng suy hô hấp, đau, giảm oxy máu và ngưng tuần hoàn. Tràn máu màng phổi lượng nhiều được xác định là có hơn 1000 cc máu hoặc lưu lượng ống dẫn lưu ngực > 200 cc/h [8].
Việc điều trị tràn máu màng phổi yêu cầu: (a) bồi hoàn thể tích máu lưu hành, nếu cần thiết, (b) cung cấp oxy và khôi phục đường thở, và (c) đặt ống dẫn lưu ngực.
Mảng sườn di động xảy ra khi ≥ 3 xương sườn liền kề bị gãy ở hai điểm khác nhau, cho phép một phần của thành ngực di chuyển tự do. Hình thức gãy xương này thường liên quan đến đau nặng, dập phổi, và suy hô hấp thứ phát do các chuyển động nghịch chiều của thành ngực. Hầu hết những bệnh nhân này cần thở máy và kiểm soát đau nhưng quyết định đặt nội khí quản có thể xem xét từng ca nhân cụ thể.
Suy hô hấp và viêm phổi
Suy hô hấp liên quan đến thần kinh do rối loạn chức năng hệ thần kinh trung ương nghiêm trọng là một trong những lý do thường gặp nhất để bắt đầu thông khí cơ học [10]. Trong số các nguyên nhân gây rối loạn chức năng thần kinh, các nguyên nhân cấu trúc như đột quỵ do thiếu máu cục bộ (AIS, ischemic stroke), xuất huyết (xuất huyết nội sọ (ICH, intracerebral hemorrhage) và xuất huyết dưới màng nhện (SAH, subarachnoid hemorrhage)) và tổn thương não do chấn thương (TBI) có tiên lượng tồi tệ nhất và là thách thức lớn nhất các chuyên gia ICU dựa trên sự tương tác giữa tình trạng thiếu oxy máu và tổn thương thần kinh thứ phát.
Trong một nghiên cứu ngẫu nhiên đa trung tâm hồi cứu gần đây, Pelosi et al. nghiên cứu dịch tễ học, đặc điểm lâm sàng và thực hành liên quan đến thông khí cơ học trong một nhóm bệnh nhân bị bệnh lý thần kinh nặng. Mặc dù bệnh nhân SAH bị loại trừ, nghiên cứu này là một mô tả tuyệt vời về thực tiễn hàng ngày thông qua các ICU khác nhau trên toàn cầu. Không có gì ngạc nhiên khi các bệnh nhân thần kinh có Glasgow Coma Scale thấp hơn (GCS) khi nhập viện, ngày ở ICU và ngày thở máy cao, mở khí quản sớm hơn, tỷ lệ VAP nhiều hơn, nhưng thú vị hơn, tỷ lệ tái đặt nội khí quản cũng tương tự như những bệnh nhân không phải là bệnh lý thần kinh. Theo nghĩa này, nghiên cứu này cung cấp hỗ trợ rằng tình trạng tinh thần và GCS có thể không quan trọng tại thời điểm rút nội khí quản [11], vì GCS đã cao hơn ở bệnh nhân không phải là bệnh lý thần kinh và tỷ lệ tái đặt NKQ là như nhau. Mặc dù nghiên cứu Pelosi rất quan trọng, nhưng nó không trả lời câu hỏi của những bệnh nhân thần kinh nào có nhiều khả năng bị “mắc kẹt” trên máy thở hoặc cần phải tái đặt NKQ sớm. Sự tương tác với mức độ nghiêm trọng của bệnh, tuổi tác, chẩn đoán thần kinh, và các biến quan trọng làm lo lắng tất cả các chuyên gia chăm sóc đặc biệt tại thời điểm rút nội khí quản như đặc điểm và xử trí chất tiết (đàm), biểu hiện xẹp phổi do giảm thông khí [12], sự tổn thương các dây thần kinh sọ (đồng tử không đều nhau, không có phản xạ hầu, ..) bị thiếu trong phân tích này. Những câu hỏi này có thể cần phải được trả lời trong các thử nghiệm lâm sàng tiền cứu khác, nhưng trong thời gian chờ đợi, chuyên môn lâm sàng có thể cần phải hướng dẫn phương pháp tiếp cận tốt nhất cho một bệnh nhân cụ thể.
Viêm phổi là một biến chứng thường gặp của tổn thương não nghiêm trọng và có thể xảy ra ở khoảng 60% bệnh nhân [13] vì những bệnh nhân này có khuynh hướng hít sặc dịch dạ dày. Tương tự như vậy, viêm phổi thở máy (VAP, ventilator associated pneumonia) là một kết quả thứ phát có thể dự phòng được do đặt nội khí quản và thông khí cơ học kéo dài. VAP là bệnh viêm phổi phát triển trong một bệnh nhân đặt nội khí quản để hỗ trợ hô hấp sau ≥ 48 giờ [14]. Bệnh nhân bệnh thần kinh trầm trọng khi thở máy có nguy cơ tăng VAP do các yếu tố như mức độ suy giảm ý thức; miệng mở, khô; sự hít sặc của các chất bài tiết [15]. Bệnh nhân bị tổn thương não nghiêm trọng có xu hướng sử dụng máy thở với thời gian dài hơn và VAP trong ICU thần kinh có thể làm tăng thêm thời gian ở lại (LOS) [16]. Ở những bệnh nhân đột quỵ nặng, sự phát triển của VAP có liên quan đến tăng tử vong trong bệnh viện gấp 3 lần [17]. Việc thực hiện các gói dự phòng VAP bao gồm chăm sóc răng miệng đã được chứng minh là làm giảm tỷ lệ VAP ở những bệnh nhân bệnh thần kinh trầm trọng [18]. Các biện pháp bổ sung để giảm VAP bao gồm ngưng điều trị thuốc an thần vào ban ngày để kiểm tra sự sẵn sàng cho việc rút nội khí quản, quản lý các chất tiết đường hô hấp trên với hệ thống hút kín và kiểm soát chặt chẽ áp lực bóng chèn, các chính sách liên quan đến vệ sinh bàn tay, nâng đầu cao ở 45◦, vệ sinh răng miệng với chlorhexidine, cùng với điều trị dự phòng loét dạ dày với H2 hoặc thuốc ức chế bơm proton [19].
Mặc dù các bệnh nhân thần kinh phải mở khí quản sớm hơn, nhưng thực hành này không liên quan đến kết cục bệnh nhân được cải thiện, đặc biệt là tử vong hoặc xuất hiện VAP [20, 21]. Tích tụ dịch trong khoang màng phổi và nhiễm trùng do vi khuẩn có thể dẫn đến chứng tràn mủ màng phổi. Điều trị tràn mủ màng phổi và tràn dịch màng phổi phức tạp đòi hỏi phải dẫn lưu dịch nhiễm trùng bằng ống dẫn lưu ngực và phác đồ kháng sinh.
ALI và ARDS
ALI và hình thức tổn thương phổi nặng hơn, ARDS, là sự liên tục của những phản ứng viêm sau tổn thương trực tiếp hoặc gián tiếp lên phổi và được nhận biết về mặt lâm sàng khi xuất hiện tình trạng thiếu oxy máu, giảm độ giãn nở phổi, và hình ảnh X quang của tổn thương thâm nhiễm phổi 2 bên [22]. Tỷ lệ mắc hội chứng ALI/ARDS đã được báo cáo ở 20-25% bệnh nhân bị tổn thương sọ não do chấn thương (TBI) [23, 24]. Ở những bệnh nhân có SAH, tỉ lệ mắc từ 20-30% cũng được báo cáo [2, 3], và đột quỵ thiếu máu cục bộ (AIS), một nghiên cứu dịch tễ học gần đây cho biết tỷ lệ ARDS từ 1994 – 2008 là 4% [6]. Trong tất cả các báo cáo, tử vong và kết cục đều xấu [3, 6, 24] (Hình 2).
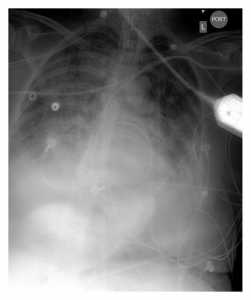
ARDS được xác định như một hội chứng đặc trưng bởi khởi phát cấp tính tổn thương thâm nhiễm hai phổi liên quan đến phù phổi (Hình 3), không có dấu hiệu tăng áp nhĩ trái (thường là áp lực động mạch phổi bít < 18 mmHg), và giảm oxy máu với PaO2/FiO2 <200. Bệnh nhân có các tiêu chí này nhưng với tỷ lệ PaO2/FiO2 < 300 được phân loại là ALI [22]. Các yếu tố nguy cơ cho sự phát triển ALI/ARDS ở bệnh nhân bị tổn thương não là mức độ nghiêm trọng của thương tích não ban đầu (điểm GCS thấp hơn), tăng huyết áp do bệnh viện [25] và các yếu tố bên ngoài như tuổi trẻ, giới tính nam, dân tộc chủng tộc trắng, tiền căn bệnh lý cao HA, tiểu đường, và COPD, và sự phát triển của nhiễm trùng huyết [6, 24].
Cơ chế sinh lý bệnh của ARDS/ALI khá phức tạp. Các nghiên cứu ban đầu cho thấy sự phát triển của phù phổi cấp do thần kinh (NPE, neurogenic pulmonary edema) ở bệnh nhân bị TBI [26] và đột quỵ xuất huyết nhiều hơn, thường gặp ở những bệnh nhân có áp lực nội sọ cao hơn và áp lực tưới máu não thấp (CPP = MAP – ICP) [27]. Bệnh nhân không có chấn thương phổi rõ ràng và X-quang ngực bình thường khi nhập viện, cho thấy chấn thương sọ não là một yếu tố nguy cơ cho hiện tượng này. Các giải thích cho những quan sát này dựa trên những gì được gọi là “chấn thương sọ mầm”, điều này giải thích bằng sự gia tăng đáp ứng adrenergic được chuyển thành tăng áp suất mao mạch ở hệ mạch máu phổi, tổn thương nội mô, và tiếp theo là sự rò rỉ mao mạch vào phế nang và mô kẽ phổi [28]. Ngoài ra, đáp ứng viêm có liên quan đến việc sản xuất các chất trung gian như IL-6 có thể giải thích sự phát triển của NPE [29, 30]. Để đạt được mục tiêu này, mô hình “double hit” đã được đề xuất khi bệnh nhân bị tổn thương não nghiêm trọng phải trải qua “cú đánh đầu tiên” với sự gia tăng adrenergic và sản xuất các hóa chất trung gian gây viêm, làm cho phổi dễ bị tổn thương hơn và “cú đánh thứ hai” từ các tác động bên ngoài, chẳng hạn như nhiễm trùng, truyền máu, và thông khí cơ học [31].
Vai trò thông khí cơ học trong sinh lý bệnh của ALI/ARDS đã được nghiên cứu rộng rãi. Sự khởi phát đáp ứng viêm hệ thống trong điều kiện chấn thương não cùng với các phương thức thông khí cơ học thông thường được sử dụng trong xử trí chấn thương não như tăng thông khí để làm giảm CO2 cho phép, có thể liên quan đến tổn thương phổi nhiều hơn [32]. Việc sử dụng các phương thức thông khí để đạt được giảm PaCO2 nhẹ (PaCO2 30-35mmHg) có thể liên quan đến việc sử dụng thể tích khí lưu thông lớn hơn 6-8ml/kg, có liên quan đến tổn thương phổi do thở máy (VILI), một hội chứng không thể phân biệt được với ARDS [33] và liên quan đến quá căng phế nang trong quá trình thông khí cơ học (volutrauma), mở-xẹp có chu kỳ các phế nang xẹp (atelectrauma), và kích hoạt quá trình viêm (biotrauma) [31].
Hỗ trợ hô hấp thông thường ở bệnh nhân bị tổn thương não nặng dựa vào việc sử dụng thông khí hỗ trợ điều khiển (assist-control ventilation) [1]. Mục tiêu thông khí với VT thấp (6- 8ml/kg PBW), áp lực bình nguyên < 30 cm H2O, và mức PEEP từ 5-10 cmH2O [34]. Trong những trường hợp giảm oxy máu không đáp ứng thông khí cứu hộ với PEEP cao hơn, tư thế nằm sấp và huy động phế nang, thông khí xả áp (APRV, airway pressure release ventilation), thở máy rung tần số cao (HFOV, high frequency oscillation), phụt khí khí quản (TGI, tracheal gas insufflation), oxy hóa màng ngoài cơ thể (ECMO, extracorporeal membrane oxygenation), và việc loại bỏ CO2 ngoài cơ thể (AV-ECCO2R) có thể cần phải được thực hiện [31,34]. Các nghiên cứu quan sát gần đây đã chứng minh rằng có thể sử dụng mức PEEP thấp hơn ở các bệnh nhân có bệnh lý thần kinh [35], mặc dù lo sợ có thể làm tăng áp lực nội sọ (ICPS). Áp dụng PEEP trong các trường hợp tổn thương não có liên quan đến ba đáp ứng: tăng hoặc giảm ICP hoặc không thay đổi, phụ thuộc vào kết quả cuối cùng ở cấp độ phổi và mức trao đổi khí.
- Nếu PEEP gây ra huy động phế nang, thì sẽ giảm được PaCO2, với sự sụt giảm của ICP.
- Nếu PEEP gây ra sự căng chướng của phế nang và không có sự cải thiện gì về thông khí, có thể tăng PaCO2, với sự gia tăng đồng thời ICP [36].
- Cuối cùng, việc áp dụng PEEP ở những bệnh nhân trong trường hợp huy động phế nang xảy ra, nhưng yếu tố chủ yếu là sự cải thiện oxy hóa thay vì giảm đáng kể PaCO2 do giảm khoảng chết, sẽ không có thay đổi đáng kể trong ICP [36].
Vào thời điểm này, có vẻ như việc sử dụng PEEP hơi cao để điều trị ALI/ARDS có thể phù hợp ở bệnh nhân bị tổn thương não nghiêm trọng, với điều kiện là MAP được duy trì và chú ý đến ICP và CPP khi có thay đổi. Một số tác giả ủng hộ việc xác định tính tự điều chỉnh của não (autoregulation) để xác định xem bệnh nhân có thể dung nạp được hay không. Nếu thay đổi đột ngột PEEP có thể dẫn đến tăng ICP, thì những bệnh nhân này mất khả năng tự điều hòa [37]. Cuối cùng, việc sử dụng steroid trong giai đoạn tăng sinh của ARDS vẫn còn là câu hỏi [35, 38-40].
Các mô hình động vật thí nghiệm hạ thân nhiệt gây ra cùng với tần số thở máy thấp đã chứng minh sự cải thiện của nhiều biến số của tổn thương phổi cấp tính như số lượng bạch cầu trung tính và các xét nghiệm phản ứng viêm, cho thấy vai trò hạ thân nhiệt trong việc xử trí ALI/ARDS có thể được nghiên cứu trong các thử nghiệm lâm sàng sắp tới [41].
Phù phổi ở bệnh nhân SAH
Sự co thắt mạch máu não có triệu chứng và thiếu tưới máu não muộn tiếp tục là một nguyên nhân chính cho bệnh suất đáng kể đối với bệnh nhân xuất huyết dưới màng cứng do phình mạch não (SAH, subarachnoid hemorrhage) [42] (Hình 3). Liệu pháp Triple H, bao gồm tăng huyết áp (hypertension), pha loãng máu (hemodilution), và tăng thể tích máu (hypervolemic), đã là một trụ cột của liệu pháp điều trị y khoa để điều trị chứng co thắt mạch máu não có triệu chứng trong vài thập niên qua [43]. Mỗi thành phần của liệu pháp này được hướng tới việc gia tăng lưu lượng máu não (CBF) và áp lực tưới máu não. Mặc dù có rất ít bằng chứng về chỉ định, nhưng liệu pháp triple H đã được sử dụng rộng rãi trên toàn thế giới, trong cả dự phòng và điều trị co thắt mạch não. Thời gian kích hoạt liệu pháp ban đầu cũng như cách mỗi thành phần được sử dụng phụ thuộc chủ yếu vào nhu cầu của mỗi bệnh nhân, vì SAH có thể không đồng nhất (tức là, SAH grade thấp so với grade cao có một bản chất bệnh lý khác nhau đáng kể) và bệnh động học (dynamic disease). Tuy nhiên, ngay cả đối với cùng một bệnh nhân, có nhiều cách thực hành khác nhau trong việc sử dụng liệu pháp này, chủ yếu là do thiếu bằng chứng cho các hướng dẫn lâm sàng. Theo một cuộc khảo sát đã được công bố gần đây, hầu hết các BS chăm sóc đặc biệt thần kinh bắt đầu điều trị triple H để điều trị co thắt mạch máu não có triệu chứng [44]. Do đó, hầu hết các tranh cãi tồn tại trong bối cảnh sử dụng dự phòng. Mặc dù dữ liệu cho hay chống lại việc sử dụng dự phòng như vậy là rất hạn chế, nhưng các tài liệu chỉ ra rằng không có sự khác biệt giữa kết quả giữa giả dược và liệu pháp Triple H khi sử dụng như là một cách dự phòng chống lại sự co thắt mạch não [45, 46]. Bất kể nó được sử dụng như là một điều trị dự phòng hoặc điều trị co thắt mạch máu não hoạt động, hypervolemia và hemodilution thường dẫn đến các biến chứng về y khoa thường gặp nhất là phù phổi và thiếu máu, có thể liên quan đến những kết cục tồi tệ nhất ở bệnh nhân SAH [47].
Sự tăng thể tích nội mạch máu và mục tiêu đạt mức độ nhất định của hemoglobin có thể cung cấp sự gia tăng cung lượng tim và do đó cuối cùng cải thiện việc cung cấp oxy. Tuy nhiên, mục tiêu tối ưu cho hemoglobin vẫn chưa được biết, nhưng các nghiên cứu về phân tách microdialysis đã cho thấy việc đặt các mức hemoglobin thấp hơn 9 mg/dL có thể liên quan đến sự suy giảm chuyển hóa trong não bị thương [48]. Tác động dương tính tiềm tàng của pha loãng máu, đặc biệt trong khi tổn thương thiếu máu cục bộ đang diễn tiến, có thể được cung cấp bởi liệu pháp triple H, nhưng cũng có một mức trần. Không biết phải tăng tiền tải đến bao nhiêu, vì cung lượng tim không tăng vĩnh viễn và do đó đạt đến một mức độ cao nhất của bình nguyên. Năng lực chuyên chở oxy cũng có cùng giới hạn. Hơn nữa, để não bộ đang bị tổn thương có thể nhận nhận được oxy đầy đủ, sự trao đổi khí trong phổi phải tối ưu. Khái niệm sinh lý học khá đơn giản và quan trọng này thường bị bỏ qua vì nhấn mạnh đến việc cứu lấy não và cho phép chấn thương phổi như phù phổi thường xảy ra. Các bác sĩ cần phải hiểu rằng sẽ có sự cân bằng giữa việc tối ưu hóa lưu lượng máu não với tình trạng pha loãng máu và mức độ phức tạp của các biến chứng về phổi, điều này có thể ảnh hưởng đến mục tiêu cuối cùng của việc cung cấp oxy và lưu lượng máu cung cấp cho não bị tổn thương. Khái niệm này đã dẫn tới sự nhấn mạnh hơn về tăng huyết áp [49] trong khi vẫn đảm bảo trạng thái đồng thể tích thay vì tạo trạng thái tăng thể tích một cách tùy tiện [50]. Ngay cả ngày nay, nhiều trung tâm dùng áp lực tĩnh mạch trung tâm (CVP) là 10 mmHg và áp lực mao mạch phổi lớn hơn 12 mmHg như điểm kết thúc huyết động. Không có biến nào trong số các biến này được xác định chính xác để đánh giá tình trạng thể tích tĩnh mạch và dẫn đến tỉ lệ phù phổi cao không thể chấp nhận, điều này lại làm giảm sự cung cấp oxy đến não thiếu máu (Hình 3). Một đánh giá gần đây có hệ thống về phân tích CVP đã cho thấy mối quan hệ giữa CVP và tình trạng thể tích tĩnh mạch thấp và báo cáo rằng làm tăng giá trị CVP lên một giá trị xác định tùy tiện không dẫn tới đáp ứng huyết động dương [51]. Cuộc tranh luận về việc sử dụng liệu pháp Triple H và cân bằng giữa việc tối đa hóa CBF và việc điều chỉnh phù phổi có thể tiếp tục, và câu trả lời có thể tương tự với nhiều chủ đề gây tranh cãi khác: quyết định từng cá nhân, từng trường hợp. Trong bất kỳ trường hợp nào, nguyên tắc trao đổi khí cần phải được chuyển tải và đạt được để tối ưu hóa thành công việc oxy hóa não. Các hướng dẫn hiện tại để quản lý SAH hỗ trợ duy trì đồng thể tích chứ không phải là tăng thể tích máu [52].
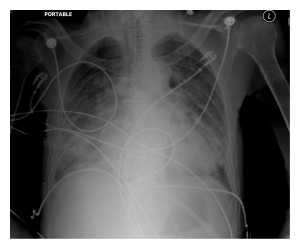
Phù phổi do nguyên nhân thần kinh
Phù phổi do thần kinh (NPE, Neurogenic pulmonary edema) đã được báo cáo với một số cơ chế đề xuất. Trong khi chưa có cơ chế rõ ràng liên quan đến hệ thần kinh trung ương (CNS), tình trạng nguy hiểm này có thể xảy ra trong các tổn thương não cấp, nghiêm trọng bao gồm chấn thương sọ não, xuất huyết não (ICH), và ngay cả trong cơn co giật. Tăng đột ngột áp lực nội sọ (ICP) như trong SAH hoặc ICH, tổn thương vùng dưới đồi, tăng đáp ứng giao cảm gây tăng sức đề kháng mạch máu (SVR) [53]. Tăng tuần hoàn và trương lực tĩnh mạch dẫn đến máu tĩnh mạch trở về tim nhiều hơn. Tăng áp suất thủy tĩnh trong hệ mạch máu phổi có thể dẫn đến sự hình thành phù mô kẽ phổi [31]. Tăng SVR gây tăng hậu tải cho tim, do đó có thể dẫn đến một sinh lý bệnh tương tự như phù phổi do tim gây ra với suy thất trái và phù khoảng. Đây là chẩn đoán loại trừ và phân biệt các nguyên nhân chính như suy tim sung huyết nặng, viêm phổi do hít, dập phổi và các bệnh khác có thể gây ra phù phổi. NPE có đặc điểm, nhanh chóng hình thành phù phổi xảy ra trong vài giờ sau khi bị thương tổn thần kinh trung ương.
Tăng áp lực nội sọ là phổ biến và điều trị nên tập trung vào việc điều trị kịp thời ICP và tối ưu hóa áp lực tưới máu não trong khi giải quyết các tổn thương não cơ bản. Vì đây là sự thất bại của nhiều hệ thống liên quan đến não, tim, phổi cũng như mạch máu ngoại biên nên cần đảm bảo đảm bảo tình trạng thể tích máu, hỗ trợ co bóp và trương lực mạch máu và đồng thời hồi sức não.
Thuyên tắc phổi
Thuyên tắc huyết khối tĩnh mạch (VTE, venous thromboembolism) là một bệnh thường gặp và nghiêm trọng bao gồm cả huyết khối tĩnh mạch sâu (DVT, deep venous thrombosis) và thuyên tắc phổi (PE, pulmonary embolism) [54] (Hình 4). Dịch tễ học của DVT và PE ở bệnh nhân bị tổn thương não nặng khác nhau tùy theo dân số nghiên cứu, mức độ thương tích, các bệnh kèm và chấn thương, và các phương pháp chẩn đoán. Ở những bệnh nhân chấn thương, tỷ lệ DVT là 18-60% [55-57] và PE là 4-22% [58]. Các nghiên cứu trong các nhóm bệnh nhân ICH cho thấy tỷ lệ hiện mắc là 2% đối với PE và 1% đối với DVT [5]. Trong SAH, tỷ lệ hiện mắc của PE là <1% và DVT là 5-7% [2]. Các tác động của VTE có thể gây bất lợi cho bệnh nhân thần kinh nặng, dẫn đến hội chứng sau viêm tĩnh mạch (postphlebitic syndrome), VTE tái phát và PE có khả năng tử vong 9-50%. Chẩn đoán lâm sàng VTE là rất khó khăn, và độ nhạy và đặc điểm của khám lâm sàng rất thấp. Vì vậy, nghiên cứu các bệnh nhân có nguy cơ cao hoặc có tỷ lệ hiện mắc cao hơn các yếu tố nguy cơ cho sự phát triển của VTE đòi hỏi phải sử dụng các xét nghiệm xâm lấn và không xâm lấn.
Ngay cả với việc sử dụng các thiết bị ép bằng khí nén (pneumatic compression devices), tỷ lệ DVT cao hơn khiến cho liệu pháp heparin dự phòng được chỉ định. Các thiết bị cơ khí để dự phòng DVT được coi là một tiêu chuẩn chăm sóc [59]. Ngược lại với điều trị dự phòng bằng thuốc, các thiết bị cơ khí có thể giảm thiểu các biến chứng xuất huyết nhưng không thể làm giảm tỉ lệ VTE. Các tỷ lệ bất lợi của các biến chứng xuất huyết với dự phòng bằng thuốc so với tỷ lệ VTE sau phẫu thuật không được nghiên cứu kỹ lưỡng, và phương pháp dự phòng tối ưu cho bệnh nhân phẫu thuật thần kinh (cơ học, thuốc, hoặc cả hai) vẫn còn nhiều tranh cãi. Một nghiên cứu gần đây ở bệnh nhân phẫu thuật thần kinh cho thấy phần lớn các DVT xảy ra trong tuần đầu tiên sau các thủ thuật về phẫu thuật thần kinh và việc sử dụng heparin dưới da sớm (24 hoặc 48 giờ) có liên quan đến việc giảm 43% việc phát triển DVT ở chi dưới, không gia tăng xuất huyết trong phẫu thuật so với không có kết hợp dự phòng bằng thuốc [59]. Nói chung, những bệnh nhân bị tổn thương não nghiêm trọng được hưởng lợi từ việc sử dụng sớm thuốc dự phòng cho VTE. Sau khi phẫu thuật nắn sọ, heparin dưới da dùng liều thấp (5000U BID hoặc TID) bắt đầu sau ngày thứ hai giảm đáng kể tần suất VTE, không tăng lượng máu trong sọ [60]. Điều trị với heparin trọng lượng phân tử thấp (tức enoxaparin 40mg mỗi ngày) là một lựa chọn hợp lý nếu chức năng thận là bình thường và kết quả của những nghiên cứu gần đây cho thấy cả hai đều tương đương nhau với tỉ lệ giảm tiểu cầu tương tự heparin [61]. Nếu chống chỉ định dùng thuốc, cần phải sử dụng bộ phận lọc tĩnh mạch chủ dưới (inferior vena cava filter) ngắn hạn [59].
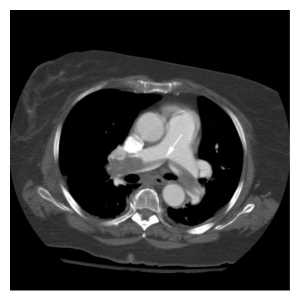
Kết luận
Các biến chứng về phổi rất phổ biến ở những bệnh nhân bệnh thần kinh trầm trọng. Các chuyên gia ICU và các chuyên gia thần kinh phải có hiểu biết sâu rộng về bệnh lý, phương pháp chẩn đoán, các phương pháp điều trị và tác động toàn diện đến kết cục của bệnh nhân.





