Những năm trước đây khi dịch cúm H5N1 khiến nhiều người tử vong bộ y tế đã ra quyết định nhập rất nhiều sản phẩm Tamiflu ( hoạt chất chính là Oseltamivir) để phòng tình trạng bùng phát dịch. Ở bài viết này https://www.healcentral.org sẽ giải thích cho các bạn vì sao Oseltamivir lại có tác dụng diệt virus? Cơ chế diệt virus của Oseltamivir là gì? Và đưa ra các bằng chứng về lâm sàng về tác dụng của Oseltamivir. Dưới đây là thông tin chi tiết.
Lịch sử nghiên cứu và phát triển
Oseltamivir (Biệt dược gốc là Tamiflu) là một thuốc kháng virus được sử dụng để điều trị và phòng ngừa cúm A và cúm B.
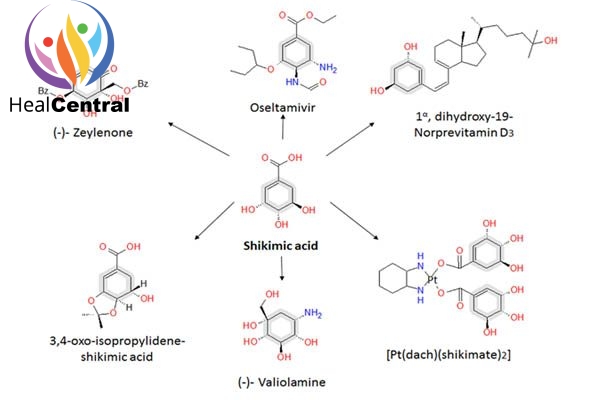
Oseltamivir được khám phá bởi các nhà khoa học tại Gilead bằng cách sử dụng chất dẫn đường là acid shikimic, một chất có nhiều trong đại hồi (bát giác hồi hương) – một loại dược liệu phổ biến ở Trung Quốc. Năm 2006, 30% nguồn cung acid shikimic là từ E.coli theo phương pháp tái tổ hợp. Gilead đã cấp bằng sáng chế độc quyền cho Roche (Thụy Sĩ) năm 1996.
Năm 1999, oseltamivir phosphate đã được FDA phê duyệt cho điều trị cúm ở người trưởng thành. Tháng 6/2002, EMA phê duyệt oseltamivir phosphate cho dự phòng và điều trị cúm. Năm 2003, một phân tích tổng hợp từ 10 thử nghiệm lâm sàng ngẫu nhiên đã kết luận rằng oseltamivir làm giảm nguy cơ nhiễm trùng đường hô hấp dưới dẫn đến sử dụng kháng sinh và nhập viện ở người trưởng thành.
Oseltamivir (Tamiflu) đã được sử dụng rộng rãi trong các dịch cúm gia cầm H5N1 ở Đông Nam Á năm 2005. Chính phủ Vương quốc Anh, Canada, Hoa Kỳ và Úc đã dự trữ một lượng lớn oseltamivir để đề phòng dịch bệnh lớn có thể xảy ra. Tháng 11/2005, Tổng thống Hoa Kỳ George W. Bush đã yêu cầu Quốc hội tài trợ 1 tỷ USD cho việc sản xuất và dự trữ oseltamivir, sau khi Quốc hội đã phê duyệt 1.8 tỷ USD cho việc sử dụng thuốc trong quân đội.
Năm 2006, một nhận xét của Cochrane đã gây tranh cãi khi đưa ra kết luận không nên sử dụng oseltamivir trong bệnh cúm mùa thông thường vì hiệu quả điều trị thấp.
Vào 12/2008, một công ty dược Ấn Độ tên là Cipla đã thắng một vụ kiện mà từ đó cho phép công ty sản xuất một phiên bản rẻ hơn của Tamiflu, đó gọi là Antiflu. Tháng 5/2009, Cipla đã nhận được sự chấp thuận của WHO xác nhận rằng thuốc Antiflu có hiệu quả tương đương Tamiflu và Antiflu được đưa vào danh sách các thuốc được sơ tuyển của WHO.
Năm 2009, một loại virus cúm A/H1N1 mới được phát hiện đang lan rộng ở Bắc Mỹ. Tháng 6/2009, WHO tuyên bố cúm A/H1N1 là đại dịch. Viện Y tế và Chất lượng Điều trị Quốc gia Anh (National Institute of Health and Care Excellence (NICE)), Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Hoa Kỳ (Centers for Disease Control and Prevention (CDC)), WHO và Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh châu Âu (European Centre for Disease Prevention and Control (ECDC)) duy trì khuyến nghị cho sử dụng oseltamivir.
Giai đoạn 2010-2012, Cochrane yêu cầu các báo cáo nghiên cứu lâm sàng đầy đủ của Roche về các thử nghiệm mà họ không cung cấp. Năm 2011, Cơ quan Dược phẩm Châu Âu (EMA) đã cung cấp cho Cochrane các báo cáo từ 16 thử nghiệm của Roche về oseltamivir. Năm 2012, nhóm nghiên cứu của Cochrane đã công bố đánh giá tạm thời dựa trên các báo cáo đó. Năm 2013, Roche đã công bố 77 báo cáo nghiên cứu lâm sàng đầy đủ về các thử nghiệm với oseltamivir sau khi GSK công bố dữ liệu của các nghiên cứu về zanamivir.
Roche đã được hưởng lợi từ oseltamivir hơn 18 tỷ USD kể từ khi ra mắt năm 1999. Doanh số của oseltamivir đã tăng 84% trong mùa cúm ở Hoa Kỳ năm 2013. Vương quốc Anh dự trữ 40 triệu liều oseltamivir trị giá 710 triệu USD. Hoa Kỳ đã chi 1.3 tỷ USD để dự trữ 65 triệu liều oseltamivir. Ấn Độ cũng tăng lượng thuốc dự trữ trong kho của mình lên 10 lần.
Năm 2016, bằng sáng chế về oseltamivir của Roche hết hạn.
Dược lực học
Oseltamivir là một thuốc kháng virus thuốc nhóm ức chế neurominidase.

Ảnh trên mô tả tóm tắt chu trình nhân lên của virus cúm A khi xâm nhập được vào tế bào chủ. Neuurominidase là một enzym chịu trách nhiệm cho việc cắt liên kết giữa carbohydrate và acid sialic, làm cho virus tách ra khỏi được tế bào vật chủ và đi lây nhiễm cho các tế bào khác. Nó là một enzym có bản chất là glycoprotein, là một kháng nguyên của virus và tên hệ thống là EC 3.2.1.18. Neuurominidase của virus cúm A có 9 phân nhóm nhỏ hơn đã được phát hiện.
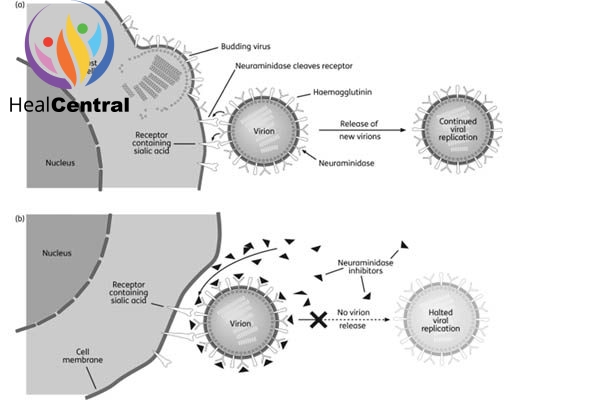
(b) Sự nhân lên của virus cúm A khi có mặt các chất ức chế neurominidase
Các chất ức chế neurominidase như oseltamivir ngăn không cho phản ứng cắt liên kết xảy ra, dẫn đến virus không thoát ra khỏi được tế bào chủ và như vậy sẽ làm hạn chế sự lây nhiễm virus cho các tế bào lành.
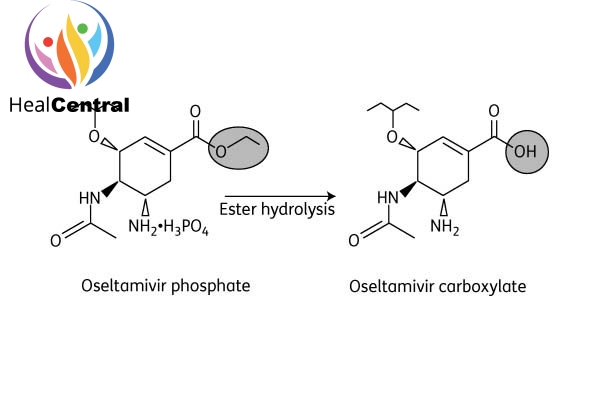
Oseltamivir thường dùng dưới dạng tiền thuốc là oseltamivir phosphate, sau đó vào cơ thể nó chuyển thành dạng hoạt động là oseltamivir carboxylate.
Một số thử nghiệm lâm sàng
Phân tích tổng hợp từ các thử nghiệm lâm sàng ngẫu nhiên của các tác giả Joanna Dobson, Richard J. Whitley, Stuart Pocock và Arnold S. Monto về điều trị bằng oseltamivir trên bệnh nhân trưởng thành bị cúm.

Phương pháp: Mặc dù được sử dụng rộng rãi, nhưng vẫn còn nhiều dấu hỏi hiệu quả của oseltamivir trong điều trị trong điều trị cúm. Các tác giả phân tích tổng hợp dữ liệu về bệnh nhân trong tất cả các thử nghiệm lâm sàng so sánh oseltamivir với giả dược điều trị cúm mùa ở người trưởng thành liên quan đến giảm triệu chứng, biến chứng và độ an toàn. Chúng bao gồm các thử nghiệm ngẫu nhiên, mù đôi và đối chứng giả dược do Roche tài trợ và chưa được công bố: 75 mg/lần x 2 lần/ngày ở người trưởng thành. Các tác giả đã tìm kiếm trên Medline, PubMed, Embase, Cochrane và ClinicalTrials.gov cho các thử nghiệm có liên quan được công bố trước ngày từ ngày 1 tháng 1 năm 2014 (tìm kiếm cập nhật lần cuối ngày 27 tháng 11 năm 2014). Họ sử dụng các tỉ lệ rủi ro và phương pháp Mantel-Haenszel.
Kết quả: Dữ liệu từ 9 thử nghiệm trên 4328 bệnh nhân. Trong nhóm người nhiễm trùng phải điều trị, các tác giả đã ghi nhận oseltamivir có thời gian giảm bớt tất cả các triệu chứng ngắn hơn so với giả dược là 21% (tỉ lệ thời gian 0.79, 95% CI 0.74-0.85; P < 0.0001). Thời gian trung bình để giảm bớt triệu chứng là 97.5 giờ đối với nhóm sử dụng oseltamivir và 122.7 giờ đối với nhóm sử dụng giả dược (chênh lệch -25.2 giờ, 95% CI -36.2 to -16.0). Các tác giả cũng ghi nhận ít biến chứng đường hô hấp dưới cần dùng kháng sinh hơn 48 giờ ở oseltamivir so với giả dược (tỉ lệ rủi ro [RR] 0.56, 95% CI 0.42-0.75; P = 0.0001; 4.9% ở oseltamivir vs 8.7% ở giả dược, chênh lệch rủi ro -3.8%, 95% CI -5.0 đến -2.2) và tỉ lệ nhập viện do mọi nguyên nhân cũng ít hơn (RR 0.37, 95% CI 0.17-0·81; P = 0.013; 0.6% với oseltamivir, 1.7% với giả dược, chênh lệch rủi ro -1.1%, 95% CI -1.4 đến -0.3). Liên quan đến độ an toàn thì oseltamivir làm tăng tỉ lệ buồn nôn (RR 1.60, 95% CI 1.29-1.99; P < 0.0001; 9.9% ở oseltamivir vs 6.2% với giả dược, chênh lệch rủi ro 3.7%, 95% CI 1.8-6.1) và nôn (RR 2.43, 95% CI 1.83-3.23; P < 0.0001; 8.0% ở oseltamivir vs 3.3% với giả dược, chênh lệch rủi ro 4.7%, 95% CI 2.7-7.3). Các tác giả không ghi nhận được rối loạn tâm – thần kinh hoặc phản ứng phụ nghiêm trọng.
Kết luận: Oseltamivir làm giảm bớt thời gian bị tất cả các triệu chứng, giảm nguy cơ biến chứng đường hô hấp dưới và nhập viện, nhưng làm tăng sự xuất hiện của buồn nôn và nôn.
Dược động học
Hấp thu: Thuốc hấp thu tốt qua đường tiêu hóa, sinh khả dụng (F) khoảng 75%. Thời gian đạt nồng độ đỉnh trong huyết tương (Tmax) từ 2.5 đến 6 giờ. Với liều 75 mg/lần x 2 lần/ngày: Nồng độ đỉnh trong huyết tương (Cmax) của oseltamivir và oseltamivir carboxylate lần lượt là 65 ng/mL và 348 ng/mL. Diện tích dưới đường cong AUC (0-12h) của oseltamivir và oseltamivir carboxylate lần lượt là 112 ng.h/mL và 2719 ng.h/mL.
Phân bố: Tỉ lệ gắn protein huyết tương là 3% với oseltamivir carboxylate và 42% với oseltamivir. Thể tích phân bố (Vd) của oseltamivir carboxylate là 23-26 L.
Chuyển hóa: Oseltamivir được chuyển hóa thành chất chuyển hóa hoạt động oseltamivir carboxylate bởi esterase ở gan. Oseltamivir carboxylate không được chuyển hóa thêm. Cả 2 chất này đều không phải cơ chất cũng không phải chất ức chế CYP450 ở gan.
Thải trừ: Thời gian bán thải (t1/2) từ 1 đến 3 giờ với oseltamivir và 6 đến 10 giờ với oseltamivir carboxylate. Thuốc được bài tiết qua phân và nước tiểu (90% dưới dạng oseltamivir carboxylate). Thanh thải thận (18.8 L/h) của thuốc vượt quá mức lọc cầu thận (7.5 L/h) cho thấy sự bài tiết ở ống thận xảy ra cùng với lọc ở cầu thận.
Chỉ định và liều dùng
Dự phòng cúm A và cúm B:
75 mg/ngày đường uống trong ít nhất 10 ngày.
Cần bắt đầu trong vòng 48 giờ sau khi tiếp xúc và trong vùng dịch, có thể sử dụng trong tối đa 6 tuần.
Điều trị cúm A và cúm B:
75 mg/lần x 2 lần/ngày x 5 ngày.
Cần bắt đầu trong vòng 48 giờ kể từ khi xuất hiện triệu chứng cúm.
Dự phòng cúm A/H1N1 (chỉ định ngoài nhãn):
75 mg/ngày đường uống trong ít nhất 10 ngày.
Cần bắt đầu trong vòng 7 ngày kể từ khi tiếp xúc.
Dự phòng trước phơi nhiễm: Bắt đầu trong thời gian phơi nhiễm tiềm tàng và tiếp tục sử dụng 10 ngày kể từ khi tiếp xúc lần cuối.
Cân nhắc thời gian sử dụng dài hơn (trên 5 ngày) ở những bệnh nhân ở những bệnh nhân vẫn còn ốm nặng sau 5 ngày điều trị.
Điều trị cúm A/H1N1 (chỉ định ngoài nhãn):
75 mg/lần x 2 lần/ngày x 5 ngày.
Cần bắt đầu trong vòng 48 giờ kể từ khi xuất hiện triệu chứng cúm.
Chỉnh liều ở bệnh nhân suy thận
Điều trị:
ü 60 < CrCl ≤ 90 mL/phút: Không cần chỉnh liều.
ü 30 < CrCl ≤ 60 mL/phút: 30 mg/lần x 2 lần/ngày.
ü 10 < CrCl ≤ 30 mL/phút: 30 mg/lần x 1 lần/ngày.
ü Bệnh thận giai đoạn cuối (ESRD), không được lọc máu: Không khuyến cáo.
ü ESRD CrCl ≤ 10 mL/phút, có lọc máu ngoài thận: 30 mg đường uống ngay lập tức và sau đó 30 mg đường uống mỗi chu kì lọc máu; thời gian điều trị không quá 5 ngày.
ü ESRD CrCl ≤ 10 mL/phút, thẩm phân phúc mạc liên tục di động: Liều đơn 30 mg dùng ngay lập tức.
Dự phòng:
ü CrCl > 60 mL/phút: Không cần chỉnh liều.
ü 30 < CrCl ≤ 60 mL/phút: 30 mg/lần x 1 lần/ngày.
ü 10 < CrCl ≤ 30 mL/phút: 30 mg 2 ngày 1 lần.
ü ESRD, không được lọc máu: Không khuyến cáo.
ü ESRD CrCl ≤ 10 mL/phút, có lọc máu ngoài thận: 30 mg đường uống ngay lập tức và sau đó 30 mg đường uống sau mỗi 2 chu kì lọc máu.
ü ESRD CrCl ≤ 10 mL/phút, thẩm phân phúc mạc liên tục di động: 30 mg đường uống ngay lập tức và sau đó 30 mg 1 lần/tuần.
Chỉnh liều ở bệnh nhân suy gan
Suy gan nhẹ đến trung bình: Không cần chỉnh liều.
Suy gan nặng: Không nghiên cứu.
Tác dụng phụ
Thường gặp (1-10%):
Rối loạn tiêu hóa: đau bụng, buồn nôn, nôn.
Viêm kết mạc.
Rối loạn thính giác.
Chảy máu cam.
Rối loạn thần kinh: mất ngủ, chóng mặt.
Tác dụng phụ < 1%:
Làm trầm trọng hơn bệnh đái tháo đường.
Thiếu máu.
Rối loạn nhịp tim, thấp tim, đau thắt ngực không ổn định.
Lú lẫn, mê sảng, động kinh.
Viêm đại tràng xuất huyết, viêm đại tràng giả mạc.
Gãy xương cánh tay.
Viêm phổi.
Sưng mặt hoặc lưỡi.
Viêm gan, tăng transaminase huyết thanh.
Hoại tử thượng bì nhiễm độc, phát ban.
Báo cáo hậu mãi (Postmarketing Reports):
Hạ thân nhiệt.
Hăm tã (trẻ từ 2 tuần đến dưới 1 tuổi).
Viêm da, nổi mày đay, eczema.
Hội chứng Stevens-Johnson.
Hồng ban đa dạng.
Xuất huyết dạ dày – ruột.
Xét nghiệm chức năng gan bất thường.
Lưu ý và thận trọng
Thuốc hiệu quả nhất khi dùng trong vòng 24-48 giờ kể từ khi xuất hiện triệu chứng cúm.
Thận trọng với trẻ dưới 1 tuổi do an toàn và hiệu quả trong điều trị và dự phòng cúm không được thiết lập.
Thận trọng với bệnh nhân suy giảm miễn dịch do an toàn và hiệu quả trong điều trị và dự phòng cúm không được thiết lập.
Thận trọng với bệnh nhân mắc bệnh tim mạn tính, suy gan nặng, suy thận, bệnh hô hấp.
Mê sảng và những hành vi bất thường dẫn đến chấn thương, bao gồm cả tử vong đã được báo cáo. Báo cáo chủ yếu ở bệnh nhân nhi, thường khởi phát đột ngột và cần giải quyết nhanh. Tuy nhiên chưa tìm thấy quan hệ nguyên nhân – kết quả giữa các phản ứng này với sử dụng oseltamivir. Theo dõi chặt chẽ bệnh nhân bệnh nhân được điều trị bằng oseltamivir khi thấy có dấu hiệu hành vi bất thường.
Thuốc không thay thế được cho vaccin.
Các phản ứng dị ứng nghiêm trọng như hội chứng Stevens-Johnson, hoại tử thượng bị nhiễm độc và hồng ban đa dạng; ngừng dùng thuốc và điều trị các phản ứng này thích hợp.
Thận trọng với nhiễm khuẩn thứ cấp.
Một liều 75 mg hỗn dịch uống chứa 2 g sorbitol. Đây là giới hạn trên tối đa với bệnh nhân không dung nạp fructose di truyền, có thể gây khó tiêu và tiêu chảy.
Phụ nữ mang thai: Thận trọng do mặc dù dữ liệu dịch tễ học cho thấy việc sử dụng oseltamivir không làm tăng nguy cơ dị tật bẩm sinh ở thai nhi ở bất kì tam cá nguyệt nào, tuy nhiên các nghiên cứu bị giới hạn ở cỡ mẫu nhỏ, sử dụng các nhóm so sánh khác nhau và thiếu một số thông tin về liều lượng, trong đó có loại trừ đánh giá chính xác về rủi ro.
Phụ nữ mang thai có nguy cơ cao bị biến chứng nặng do cúm, điều này có thể dẫn đến bất lợi khi mang thai như tử vong cả mẹ và con, hoặc vẫn có thể sinh con được nhưng thai bị dị tật bẩm sinh, sinh non, thai nhẹ cân…
Phụ nữ đang cho con bú: Thận trọng do dữ liệu được công bố hạn chế, đã cho thấy thuốc có mặt trong sữa mẹ ở nồng độ thấp. Tuy nhiên điều này được coi là không có khả năng gây độc tính cho trẻ bú mẹ. Sau khi đưa thuốc ra thị trường, không thấy báo cáo bất kỳ thông tin nào cho thấy tác dụng phụ nghiêm trọng đối với phơi nhiễm thuốc qua sữa mẹ ở trẻ sơ sinh.
Tương tác thuốc
Sử dụng đồng thời với các chất chống đông máu đường uống như wafarin hoặc chất ức chế kết tập tiểu cầu như aspirin, clopidogrel, ticagrelor…: Tăng nguy cơ xuất huyết.

Sử dụng đồng thời với các vaccin phòng cúm A: Làm giảm hiệu quả phòng bệnh của vaccin.
Sử dụng đồng thời với probenecid: Có thể làm giảm thải trừ oseltamivir.
Tương tác với các thuốc khác cần thận trọng: methotrexate, entacavir, pemetrexed, tafamidis.
Chống chỉ định
Quá mẫn cảm với oseltamivir hoặc bất cứ thành phần nào của thuốc.
Tài liệu tham khảo:
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(14)62449-1/fulltext
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2654582/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4942987/
https://www.ncbi.nlm.nih.gov/pubmed/24811411
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4375804/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4959743/
https://www.ncbi.nlm.nih.gov/pubmed/29186364
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5201449/