Bài viết Quá tải dịch truyền, lấy bỏ dịch hồi sức và kết cục ở những bệnh nhân bị bệnh nặng hoặc bị chấn thương: đánh giá có hệ thống với những gợi ý cho thực hành lâm sàng được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Fluid overload, de-resuscitation, and outcomes in critically ill or injured patients: A systematic review with suggestions for clinical practice
TÓM TẮT
Bối cảnh: Nhiễm trùng huyết có liên quan đến tổn thương nội mô và rò mao mạch toàn thân và theo truyền thống được điều trị bằng hồi sức dịch khối lượng lớn. Một số bệnh nhân bị nhiễm trùng huyết sẽ tích tụ dịch cơ thể. Mục đích của nghiên cứu này là xem xét một cách có hệ thống mối liên quan giữa cân bằng dịch truyền/quá tải dịch truyền và kết cục ở người lớn bị bệnh nghiêm trọng, và để xác định liệu các can thiệp nhằm giảm cân bằng dịch truyền có thể được liên kết với kết quả cải thiện hay không.
Phương pháp: Chúng tôi đã tìm kiếm MEDLINE, PubMed, EMBASE, Web of Science, Cơ bản dữ liệu của Cochrane, đăng ký thử nghiệm lâm sàng và thư mục của các bài báo. Hai tác giả đã xem xét độc lập các trích dẫn và các nghiên cứu được lựa chọn kiểm tra mối liên quan giữa cân bằng dịch truyền và kết cục hoặc trong đó can thiệp là bất kỳ chiến lược hoặc giao thức nào cố gắng đạt được sự cân bằng dịch truyền tích lũy âm tính hoặc trung tính sau ngày thứ ba so với chăm sóc thông thường. Các kết quả chính của mối quan tâm là tỷ lệ mắc IAH và tỷ lệ tử vong.
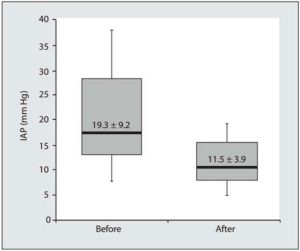
Kết quả: Trong số tất cả các trích dẫn được xác định, một phân tích tổng hợp, 11 thử nghiệm lâm sàng ngẫu nhiên có kiểm soát, bảy nghiên cứu can thiệp, 24 nghiên cứu quan sát và bốn loạt trường hợp đáp ứng các tiêu chí thu nhận. Tổng cộng, 19.902 bệnh nhân nguy kịch đã được nghiên cứu. Cân bằng dịch truyền tích lũy sau một tuần ở lại ICU dương tính nhiều hơn 4,4 L ở những người không sống sót so với những người sống sót. Chiến lược quản lý dịch truyền hạn chế dẫn đến cân bằng dịch truyền tích lũy ít dương tính hơn 5,6 L so với các biện pháp kiểm soát sau một tuần ở lại ICU. Quản lý dịch truyền hạn chế có liên quan đến tỷ lệ tử vong thấp hơn so với bệnh nhân được điều trị bằng chiến lược quản lý dịch truyền tự do hơn (24,7% so với 33,2%; OR, 0,42; KTC 95% 0,32−0,55; P <0,0001). Bệnh nhân tăng áp lực trong ổ bụng (IAH) có cân bằng dịch tích lũy dương tính hơn 3,4 L sau một tuần ở lại ICU. Can thiệp để giảm cân bằng dịch truyền dẫn đến giảm áp lực trong ổ bụng (IAP): loại bỏ toàn bộ dịch cơ thể trung bình 4,9 L dẫn đến giảm IAP từ 19,3 ± 9,1 mm Hg xuống 11,5 ± 3,9 mm Hg.
Kết luận: Cân bằng dịch truyền tích lũy dương có liên quan đến IAH và kết quả xấu hơn. Các can thiệp để hạn chế sự phát triển của cân bằng dịch truyền tích lũy dương tính có liên quan đến kết quả được cải thiện. Ở những bệnh nhân không tự phát chuyển từ giai đoạn “Ebb” sang giai đoạn “Flow” của sốc, nên xem xét quản lý dịch truyền bảo tồn muộn và loại bỏ dịch truyền theo mục tiêu muộn (khử dịch truyền hồi sức).
MỞ ĐẦU
Việc truyền dịch tĩnh mạch được coi là bước đầu tiên trong quá trình hồi sức cho những bệnh nhân bị bệnh nặng và bị chấn thương có bằng chứng tưới máu cơ quan bị suy yếu [1−3]. Surviving Sepsis Campaign khuyến nghị hồi sức tấn công trong suốt 24 giờ đầu tiên của quản lý dịch [4]. Mục đích của hồi sức dịch là để tăng hồi lưu tĩnh mạch (venous return) và thể tích nhát bóp (stroke volume) [5]. Quản lý dịch truyền làm tăng thể tích máu bị stress (stressed blood volume), tăng độ chênh lệch giữa áp lực làm đầy hệ thống trung bình (MSFP, mean systemic flling pressure) và áp lực nhĩ phải (CVP), do đó làm tăng hồi lưu tĩnh mạch [6-8]. Ở những bệnh nhân nằm trên nhánh tăng dần của đường cong Frank- Starling, sự hồi lưu tĩnh mạch tăng dẫn đến tăng thể tích nhát bóp và chỉ số tim [5].
Mặc dù vậy, các nghiên cứu lâm sàng đã chứng minh rằng ít hơn 50% bệnh nhân không ổn định huyết động là những người đáp ứng với dịch truyền, như được xác định bằng sự gia tăng thể tích nhát bóp 10-15% sau thử thách dịch truyền (fluid challenge) [5]. Sử dụng dịch truyền không có ích ở những bệnh nhân mà thể tích nhát bóp không tăng sau thử thách dịch truyền (không đáp ứng). Ở những bệnh nhân này, sử dụng dịch truyền thậm chí có thể có hại. Hơn nữa, do sự tái phân bố (redistribution) của dịch truyền, đáp ứng huyết động ở những người đáp ứng dịch truyền chỉ tồn tại trong thời gian ngắn với thể tích nhát bóp trở về đường cơ bản 30 đến 60 phút sau thử thách dịch truyền ban đầu [9]. Ở những người khỏe mạnh, 85% lượng bolus dung dịch tinh thể đã tái phân bố vào khoảng kẽ sau bốn giờ [10]. Ở những bệnh nhân nguy kịch với tổn thương nội mô và mao mạch bị rò rỉ, dưới 5% lượng dịch truyền vẫn còn trong mạch máu sau 90 phút [11]. Trong nghiên cứu Liệu pháp điều trị theo mục tiêu ban đầu của Rivers (EGDT, Early Goal Directed Therapy), 4,9 L dung dịch tinh thể đã được đưa ra trong sáu giờ đầu tiên và 13,4 L trong 72 giờ đầu tiên [12]. Surviving Sepsis Campaign khuyến nghị hồi sức tấn công trong suốt 24 giờ đầu tiên của quản lý [4].
Hồi sức dịch thể tích lớn dẫn đến phù nề nghiêm trọng và các dấu hiệu lâm sàng của tình trạng quá tải thể tích [13]. Phù nề làm suy yếu khuếch tán oxy và chất chuyển hóa, làm biến dạng kiến trúc mô, cản trở lưu lượng máu mao mạch và dẫn lưu bạch huyết, và làm xáo trộn các tương tác tế bào-tế bào [13]. Những ảnh hưởng này càng nặng nề thêm trong các cơ quan có vỏ bao, chẳng hạn như gan và thận, không có khả năng chứa thêm thể tích mà không làm tăng áp lực kẽ, dẫn đến lưu lượng máu của cơ quan bị tổn thương [14]. Hơn nữa, hồi sức dịch thể tích lớn làm tăng áp lực trong ổ bụng (IAP, intra-abdominal pressure), điều này làm tổn hại thêm đến tưới máu gan và thận. Như vậy, rò rỉ mao mạch góp phần đáng kể vào nguồn gốc của tăng áp lực trong ổ bụng (IAH, intra-abdominal hyper- tension) và hội chứng khoang bụng (ACS, abdominal compartment syndrome) (15−19). Kelm et al. [20] chứng minh rằng 67% bệnh nhân được cấp cứu bằng phương pháp giao thức EGDT có bằng chứng lâm sàng về tình trạng quá tải dịch truyền sau 24 giờ, với 48% bệnh nhân có các đặc điểm của tình trạng quá tải dịch truyền dai dẳng vào ngày thứ ba của bệnh viện.
Nhiều nghiên cứu đã chứng minh rằng sự cân bằng dịch truyền dương tính có liên quan độc lập với suy chức năng cơ quan và tăng nguy cơ tử vong [14, 15, 21−29]. Điều này gần đây đã được chứng minh trong một nghiên cứu của Murphy et al. [21]. Ngược lại, thành tựu của sự cân bằng dịch truyền âm tính có liên quan đến cải thiện chức năng cơ quan và tăng khả năng sống sót [30, 31]. Điều này đã được gọi là giai đoạn “Ebb” và “Flow” của sốc nhiễm trùng. Giai đoạn “Ebb” được mô tả bởi Cuthbertson vào năm 1932 như sau: khuôn mặt của Ashen, mạch nhẹ và tứ chi lạnh lẽo, trong khi trong giai đoạn Flow, bệnh nhân nóng lên, cung lượng tim tăng lên và nhóm phẫu thuật thư giãn … [25]. Dữ liệu gần đây cho thấy rằng nhiều bệnh nhân không bước vào giai đoạn “Flow” một cách tự nhiên và để tránh sự cân bằng dịch truyền tích lũy dương tính với phù cơ quan và rối loạn chức năng cơ quan, họ có thể cần phải can thiệp điều trị [32]. Tuy nhiên, phần lớn vẫn chưa biết liệu các chiến lược nhắm mục tiêu cân bằng dịch truyền trung tính hay thậm chí âm tính sau giai đoạn hồi sức ban đầu có liên quan đến kết quả lâm sàng được cải thiện ở người.
Liệu pháp hướng đến mục tiêu đã trở nên phổ biến, trong đó mục tiêu của hồi sức là sự đảo ngược nhanh chóng của sốc và giảm tưới máu trong vòng vài giờ. Surviving Sepsis Campaign Guidelines tập trung vào hồi sức ban đầu nhưng không cung cấp thông tin về đánh giá tình trạng quá tải thể tích hoặc khi nào và cách thực hiện khử dịch truyền hồi sức (de-resuscitation) [4]. Hơn nữa, áp lực tĩnh mạch trung tâm (CVP) cung cấp ít dữ liệu hữu ích về tình trạng thể tích chung của bệnh nhân và nhu cầu khử dịch truyền hồi sức. Các thiết bị EV1000/VolumeView (Edwards Lifescatics, Irvine, CA, USA) và PiCCO (Pulsion Medical Systems, Munich, Đức) cho phép, bên cạnh việc đo cung lượng tim, cũng như các thông số khác như chỉ số thể tích cuối tâm trương toàn cầu (GEDVI, global end-diastolic volume index) và chỉ số nước ngoài mạch máu phổi (EVLWI, extravascular lung water index) cung cấp thông tin hữu ích về tình trạng thể tích và phù mô [33- 35]. Những thiết bị này rất hữu ích khi phải đối mặt với xung đột trị liệu, tình huống mà mỗi quyết định điều trị có thể mang lại một số tác hại tiềm tàng, giúp cho bác sĩ lâm sàng có thể hỗ trợ cơ quan có nguy cơ gây hại cao nhất cho bệnh nhân [36, 37]. Do đó, ở những bệnh nhân có nguy cơ cao, các quyết định liên quan đến quản lý dịch truyền nên được thực hiện trong bối cảnh xung đột trị liệu.
Mục đích của nghiên cứu này là xem xét một cách có hệ thống mối liên quan giữa cân bằng dịch truyền/quá tải dịch truyền và kết quả ở người lớn bị bệnh nghiêm trọng và để xác định liệu các can thiệp nhằm giảm cân bằng dịch truyền có thể được liên kết với kết quả cải thiện hay không.
Trong cuộc thảo luận, chúng tôi sẽ tập trung vào các tài liệu có sẵn liên quan đến tình trạng quá tải dịch truyền và cân bằng dịch truyền tích lũy dương tính liên quan đến tỷ lệ mắc bệnh (ví dụ IAH) và tỷ lệ tử vong và cách đối phó với nó tại giường. Chúng tôi xem xét lại hồi sức: cái gì, tại sao, khi nào và như thế nào?
ĐỊNH NGHĨA
Trong phần này, chúng tôi sẽ định nghĩa “khử dịch truyền hồi sức” (de-resuscitation) và đề xuất một số định nghĩa liên quan đến quản lý dịch truyền và cân bằng dịch truyền [38-40]. Dịch truyền hồi sức.
Dịch truyền hồi sức (resuscitation fluids) được sử dụng để điều chỉnh thâm hụt thể tích nội mạch hoặc giảm thể tích máu cấp tính. Trong ba thập kỷ qua, đã có nhiều tranh luận về việc sử dụng dung dịch keo so với dung dịch tinh thể [41]. Tuy nhiên, các thử nghiệm lâm sàng gần đây cho thấy dung dịch keo có vai trò hạn chế trong hồi sức dịch [42−44]. Gần đây, vấn đề liên quan đến việc sử dụng dung dịch nước muối sinh lý (normal saline) so với dung dịch muối cân bằng (balanced salt solutions), với dữ liệu cho thấy kết quả được cải thiện với các dung dịch muối cân bằng [45, 46].
Dịch truyền duy trì. Các dịch truyền duy trì (maintenance fluids) được đưa ra một cách cụ thể để cung cấp cho bệnh nhân các nhu cầu cơ bản hàng ngày về nước và chất điện giải.
Dịch truyền thay thế. Các dịch truyền thay thế (replacement fluids) được chỉ định để khắc phục những thiếu hụt hiện có hoặc đang phát triển mà không thể bù đắp bằng đường uống, như đã thấy trong các tình huống mất nước qua ống dẫn lưu hoặc hậu môn tạm, rò đường tiêu hóa, sốt, tiểu nhiều và vết thương hở (kể cả bốc hơi trong khi phẫu thuật hoặc bỏng).
Hội chứng tăng tính thấm toàn cầu (GIPS, Global Increased Permeability Syndrome). GIPS được đặc trưng bởi chỉ số rò rỉ mao mạch cao (CLI, capillary leak index – được biểu thị bằng tỷ lệ CRP so với albumin), dịch mô kẽ dư thừa và chỉ số nước ngoài mạch máu phổi (EVLWI) cao, không đạt được quản lý dịch truyền bảo tồn muộn (LCFM, late conservative fluid manage- ment) và tiến triển thành suy cơ quan [32]. GIPS đại diện cho cú đánh thứ ba sau chấn thương cấp tính (cú đánh đầu tiên) với tiến triển thành hội chứng rối loạn chức năng đa cơ quan – MODS (multi-organ dysfunction syndrome) (cú đánh thứ hai) [47]. Cú đánh thứ ba có thể phát triển ở những bệnh nhân không chuyển vào giai đoạn “Flow” một cách tự nhiên. Đáp ứng thành công đối với tổn thương viêm cấp tính có xu hướng được đặc trưng bởi một bước ngoặt quan trọng vào ngày thứ ba. Sự phát triển của các cytokine và các chất trung gian gây viêm khác vào ngày thứ ba sau khi bắt đầu sốc cho phép chữa lành các rối loạn vi tuần hoàn và “đóng cửa” rò rỉ mao mạch. Giải thích này được hỗ trợ bởi các quan sát chứng minh bình thường hóa lưu lượng máu vi tuần hoàn vào ngày thứ ba ở bệnh nhân nhiễm trùng huyết từ ổ bụng [48]. Hơn nữa, EVLWI thấp hơn và các chỉ số tính thấm mạch máu phổi (PVPI, pulmonary vascular permeability indices) vào ngày thứ ba của sốc đã được chứng minh là có tương quan với khả năng sống sót tốt hơn [49]. Ở những bệnh nhân này, sử dụng dịch truyền dư thừa dẫn đến sự hình thành phù nề, tiến triển của suy cơ quan và kết quả tồi tệ hơn. Do đó, ngay khi huyết động học cho phép, việc chuyển đổi sớm sang quản lý dịch truyền bảo tồn và thậm chí loại bỏ dịch truyền trên cơ bản giao thức hướng dẫn từ EVLWI là bắt buộc (loại bỏ dịch truyền theo mục tiêu muộn) [21, 32, 47].
Hội chứng đa khoang (Polycompartment syndrome). Các định nghĩa đồng thuận gần đây của Hiệp hội Thế giới về Hội chứng khoang bụng (WSACS, www.wsacs.org) đã định nghĩa hội chứng đa khoang là một tình trạng trong đó hai hoặc nhiều khoang giải phẫu có áp lực trong khoang tăng cao [50]. Do rò rỉ mao mạch và giai đoạn “flow” bị suy yếu, việc sử dụng quá nhiều dịch truyền không cần thiết trong giai đoạn GIPS sẽ dẫn đến tình trạng quá tải dịch truyền và phù nề mô. Phù nề kẽ làm tăng áp lực ở cả bốn khoang cơ thể chính liên kết với nhau: đầu, ngực, bụng và tứ chi. Do đó, sức cản tĩnh mạch của các cơ quan trong các khoang tăng lên và áp lực tưới máu giảm góp phần vào sự tiến triển của suy cơ quan. Khi các khoang khác nhau tương tác và truyền áp lực khoang đối ứng, khái niệm hội chứng đa khoang được đề xuất [51-53]. Bụng đóng vai trò trung tâm trong GIPS và hội chứng đa khoang, vì cân bằng dịch truyền dương tính là yếu tố nguy cơ của IAH thứ phát, từ đó có liên quan đến các tác động xấu đến các khoang và chức năng cơ quan khác và cuối cùng có thể dẫn đến hội chứng khoang bụng (ACS) [15]. Với độ giãn nở (compliance) của bụng được định nghĩa là thước đo mức độ dễ mở rộng của bụng, được xác định bởi độ đàn hồi của thành bụng và cơ hoành, là yếu tố quyết định giải thích việc truyền áp lực khoang từ ngăn này sang ngăn khác.
Cân bằng dịch. Cân bằng dịch (fluid balance) hàng ngày là tổng hàng ngày của tất cả các dịch nhập và dịch xuất, và cân bằng dịch truyền tích lũy là tổng số tích lũy dịch truyền trong một khoảng thời gian định sẵn [38, 54].
Tình trạng quá tải dịch (fluid overload). Tỷ lệ tích lũy dịch truyền có thể được xác định bằng cách chia cân bằng dịch truyền tích lũy tính bằng lít cho trọng lượng cơ thể cơ bản của bệnh nhân và nhân với 100%. Quá tải dịch truyền được xác định bằng giá trị cut-off 10% tích lũy dịch truyền vì có liên quan đến kết quả tồi tệ hơn [38, 55].
Bolus dịch truyền. Một truyền dịch nhanh chóng (bolus) để điều chỉnh sốc hạ huyết áp và giảm thể tích (nhiễm trùng hoặc xuất huyết). Nó thường bao gồm truyền ít nhất 4 mL/kg trong tối đa 10 đến 15 phút.
Thử thách dịch truyền (fluid challenge). Một lượng 100-200 ml được cung cấp trong 5-10 phút với đánh giá lại tình trạng huyết động để tối ưu hóa tưới máu mô. Điều này cho phép xây dựng một đường cong được gọi là Frank-Starling để đánh giá loại đường cong và vị trí bệnh nhân nằm trên đường cong. CVP và áp lực bờ mao mạch phổi (PCWP, pulmonary capillary wedge pressure) có khả năng nguy hiểm và vô dụng để hướng dẫn một thách thức dịch truyền [5, 13, 56, 57]. Trước đây, những thay đổi động trong CVP (hoặc PCWP) đã được đề xuất nhưng những thay đổi này cũng có thể không hữu ích [58, 59]. Trong một thử thách lỏng lẻo, quy tắc 2-5 được tuân thủ một cách cổ điển đối với CVP và 3-7 cho PCWP. CVP cơ bản được đo lường và đánh giá lại sau mỗi bolus hoặc mỗi khoảng thời gian mười phút (như được minh họa trong Bảng 1).
| Bảng 1. Quy tắc 2−5 sử dụng các thay đổi động trong CVP để hướng dẫn thách thức dịch truyền |
1. Đo CVP cơ bản (mm Hg):
2. Đánh giá lại sự gia tăng CVP ở cuối bolus (tức là sau 10 phút kể từ khi bắt đầu tại điểm 1)
3. Đánh giá lại mức tăng CVP sau 10 phút nữa (tức là sau 20 phút kể từ khi bắt đầu tại điểm 1)
4. Lặp lại cho đến khi CVP 14 mm Hg hoặc phá vỡ quy tắc |
Quản lý dịch truyền định hướng mục tiêu sớm (EAFM, Early adequate goal directed fluid management). Hầu hết các nghiên cứu xem xét điều trị theo mục tiêu xác định đạt được sớm là cung cấp 25 đến 50 ml/kg dịch truyền trong vòng 6-8 giờ đầu tiên trong hồi sức trong trường hợp sốc nhiễm trùng hoặc giảm thể tích. Tuy nhiên, những người khác đã lập luận rằng khối lượng dịch truyền lớn như vậy dẫn đến chết đuối nước mặn do điều trị (iatrogenic salt water drowning) và đã đề xuất một chiến lược bảo tồn hơn [13, 60].
Quản lý dịch truyền bảo tồn muộn (LCFM, Late Conservative Fluid Management). Các nghiên cứu gần đây đã chỉ ra rằng quản lý dịch truyền bảo tồn muộn, được định nghĩa là hai ngày liên tiếp của sự cân bằng dịch truyền âm tính trong tuần đầu tiên ở ICU, là một yếu tố dự báo mạnh mẽ và độc lập về sự sống còn [21]. Ngược lại, bệnh nhân bị viêm toàn thân kéo dài duy trì rò rỉ albumin xuyên mao mạch và không đạt đến giai đoạn “flow” làm tăng cân bằng dịch truyền dương tính.
Loại bỏ dịch truyền có mục tiêu muộn (LGFR, Late Goal Directed Fluid Removal). Ở một số bệnh nhân, cần loại bỏ dịch truyền tích cực và tấn công hơn bằng thuốc lợi tiểu và điều trị thay thế thận bằng siêu lọc ròng là cần thiết. Điều này được gọi là “khử dịch truyền hồi sức”.
Phân loại động lực học dịch truyền (Classifcation of fluid dynamics). Kết hợp quản lý dịch truyền đầy đủ sớm (EA) hoặc bảo tồn sớm (EC) và bảo tồn muộn (LC) hoặc quản lý dịch truyền tự do muộn (LL), bốn nhóm riêng biệt có thể được xác định liên quan đến động lực của quản lý dịch truyền: EALC, EALL, ECLC và ECLL . Những điều này sẽ được thảo luận thêm.
PHƯƠNG PHÁP
CHIẾN LƯỢC TÌM KIẾM VÀ CÂU HỎI LÂM SÀNG
Chúng tôi đã tìm kiếm MEDLINE, PubMed, EMBASE, Web of Science, Cơ bản dữ liệu Cochrane, đăng ký thử nghiệm lâm sàng và thư mục của các bài báo để cập nhật một tổng quan hệ thống và phân tích tổng hợp đã được tiến hành trước đó [61]. Chúng tôi đã tìm cách xác định các nghiên cứu liên quan đến các bệnh nhân bị bệnh nghiêm trọng đã kiểm tra mối liên quan giữa cân bằng dịch truyền dương tính và kết quả sau ngày thứ 3 của ICU. Chúng tôi cũng đã tìm cách cập nhật một tổng quan hệ thống đã được tiến hành trước đó và phân tích tổng hợp các câu hỏi lâm sàng được xây dựng theo định dạng PICOD (Bệnh nhân, Can thiệp, So sánh, Kết quả, Thiết kế) [61]: Câu hỏi lâm sàng PICOD của chúng tôi là: chiến lược ở những bệnh nhân bị bệnh nghiêm trọng cố gắng đạt được sự cân bằng dịch truyền ở trạng thái cân bằng hoặc thậm chí âm tính (chiến lược dịch truyền bảo tồn) sau ngày thứ 3 (và trong tuần đầu tiên) dẫn đến IAP thấp hơn và kết quả bệnh nhân được cải thiện so với chiến lược dịch truyền tự do?
LỰA CHỌN BÀI BÁO VÀ TRÍCH XUẤT DỮ LIỆU
Hai tác giả đã độc lập xem xét tất cả các tiêu đề và tóm tắt và các bài báo toàn văn được chọn để đưa vào đánh giá. Hai tác giả này cũng trừu tượng hóa dữ liệu về thiết kế nghiên cứu, chất lượng phương pháp, đặc điểm bệnh nhân, cân bằng dịch truyền và kết quả quan tâm. Chúng tôi bao gồm các nghiên cứu trong đó: 1) bệnh nhân bị bệnh nặng hoặc người lớn bị chấn thương được điều trị tại phòng chăm sóc đặc biệt (một số trong số họ cũng được phẫu thuật); 2) Can thiệp là bất kỳ chiến lược hoặc giao thức nào cố gắng đạt được sự cân bằng dịch truyền tích lũy trung tính hoặc âm tính sau ngày thứ ba chăm sóc tích cực; 3) nhóm so sánh nhận được một chiến lược hoặc giao thức tương đương không cố gắng đạt được sự cân bằng hoặc cân bằng dịch truyền âm tính sau ngày thứ ba chăm sóc đặc biệt cho phép chiến lược quản lý dịch truyền tự do hơn; 4) các kết cục chính là tỷ lệ mắc IAH và tử vong; và 5) thiết kế nghiên cứu là một RCT hoặc nghiên cứu quan sát. Các kết quả thứ phát bao gồm chi phí, sử dụng ICU, thời gian nằm viện hoặc ICU, tỷ lệ suy thận cấp, ACS và yêu cầu phẫu thuật nội soi giải ép. Chúng tôi cũng bao gồm các đánh giá hệ thống được tiến hành trước đây và/hoặc phân tích tổng hợp.
RỦI RO CỦA ĐÁNH GIÁ BIAS
Chúng tôi đã áp dụng hệ thống Phân lớp của Khuyến nghị, Đánh giá, Phát triển và Đánh giá (GRADE, Grades of Recommendation, Assess- ment, Development, and Evaluation) để hướng dẫn đánh giá chất lượng bằng chứng nhằm giải quyết các câu hỏi quản lý lâm sàng. Ý kiến đồng thuận tốt nhất là LỚP từ cao (A) đến rất thấp (D) và để giúp xác định mức độ khuyến nghị từ các khuyến nghị mạnh mẽ cho thấy hội thảo cảm thấy các tác động mong muốn chung của can thiệp rõ ràng vượt xa các tác động không mong muốn tiềm tàng, cho các đề xuất yếu hơn rằng sự cân bằng giữa rủi ro và lợi ích ít rõ ràng hơn đối với bất kỳ sự can thiệp nào, để làm rõ sự không chắc chắn.
PHÂN TÍCH THỐNG KÊ
Các biến liên tục được biểu thị bằng trung bình ± SD (độ lệch chuẩn) hoặc là trung vị (với phần tư thứ nhất và thứ ba) tùy theo chúng có được phân bố bình thường hay không. Các biến liên tục được so sánh bằng cách sử dụng phép thử Student t-test cho các biến phân bố thông thường và Mann-Whitney U cho các biến không phân bố thông thường. Kết quả tóm tắt phân tích tổng hợp các hiệu ứng ngẫu nhiên được tính toán đưa ra mức trung bình từ phân bố (của các hiệu ứng điều trị) trong các nghiên cứu. Giá trị P dưới 0,05 được coi là có ý nghĩa thống kê. Phân tích thống kê được thực hiện với SAS (phiên bản 9.1, Học viện SAS, Cary, NC, Hoa Kỳ) và SPSS (phiên bản Windows 17.0, SPSS, Chicago, IL, Hoa Kỳ). Phân tích tổng hợp và các Forest plot (Forest plots) được tạo ra với Trình quản lý đánh giá 5 (Phiên bản 5.1. Copenhagen: Trung tâm Cochrane Bắc Âu, Hợp tác Cochrane, 2011).
CÁC KẾT QUẢ
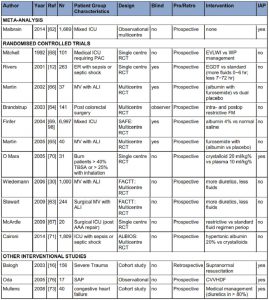
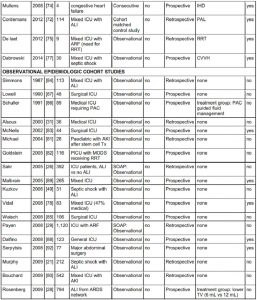
Tổng cộng, chúng tôi bao gồm 47 bài báo (bệnh nhân phẫu thuật được nghiên cứu trong 6, bỏng 3 và chấn thương 1, các nghiên cứu khác bao gồm bệnh nhân ICU hỗn hợp (chủ yếu là nội khoa). Chúng tôi cũng bao gồm một phân tích tổng hợp bệnh nhân riêng lẻ [62], 11 thử nghiệm lâm sàng ngẫu nhiên có kiểm soát (RCTs) (trong đó bốn nghiên cứu mù đôi) [12, 30, 63-71], bảy nghiên cứu can thiệp [16, 72−77], 24 nghiên cứu quan sát [21, 26, 28, 29, 31, 32, 49, 55, 78−93] và bốn loạt trường hợp [94−97]. Nhìn chung, tổng cộng 19902 bệnh nhân bị bệnh nặng đã được nghiên cứu và trong 20 nghiên cứu, IAP đã được đo (Bảng 2). Khi cập nhật phân tích tổng hợp được tiến hành trước đây, chúng tôi đã phân tích các câu hỏi phụ cụ thể sau:
Những người không sống sót có cân bằng dịch truyền dương tính hơn? Một tiếp cận phân tích tổng hợp đã được thông qua để phân tích dữ liệu tốt nhất được trừu tượng hóa từ một phân tích tổng hợp bệnh nhân riêng lẻ [62], chín nghiên cứu đoàn hệ tương lai không được kiểm soát [26, 28, 49, 77, 78, 82, 84, 89, 91], ba nghiên cứu đoàn hệ hồi cứu không kiểm soát [21, 31, 32], hai nghiên cứu đoàn hệ điều trị không ngẫu nhiên hồi cứu [72, 79] và đánh giá hồi cứu [86] về một thử nghiệm ngẫu nhiên về can thiệp riêng [68, 86] được coi là cân bằng dịch truyền trong liên quan đến sự sống còn trong bệnh hiểm nghèo. Khi được tổng hợp, dữ liệu từ tổng số 5.445 bệnh nhân từ 17 nghiên cứu cho thấy những người không sống sót (n = 2.609, tỷ lệ tử vong 47,9%) có cân bằng dịch truyền tích lũy dương tính hơn vào ngày thứ 7 ở lại ICU so với những người sống sót (6,982,6 ± 5,629 mL so với 2,449,1 ± 2,965,1 mL) (Hình 1). Cân bằng dịch truyền tích lũy trung bình 4,533,5 ± 3,626,7 mL dương tính hơn ở những người không sống sót so với những người sống sót (Hình 2). Kết quả đối chiếu của các nghiên cứu này được cung cấp trong Forest plot trong Hình 3.
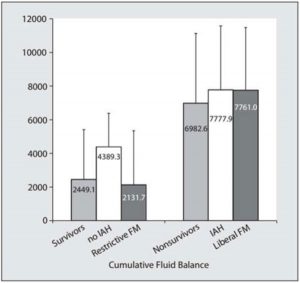
”Thanh màu xám nhạt cho thấy sự cân bằng dịch truyền tích lũy ở người sống sót (trái) so với người không sống sót (phải), thanh màu trắng hiển thị dữ liệu ở bệnh nhân không bị tăng áp lực trong ổ bụng, IAH (trái) so với có IAH (phải) và dữ liệu thanh màu xám đậm ở bệnh nhân có quản lý dịch truyền hạn chế (trái) vs quản lý dịch truyền tự do (phải)”
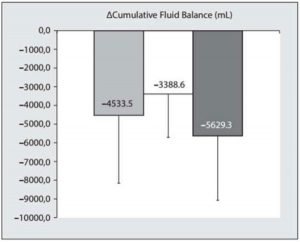
Liệu kết quả có cải thiện với sự can thiệp để hạn chế lượng dịch truyền hoặc cân bằng dịch truyền thấp hơn? Dữ liệu được tổng hợp từ 15.947 bệnh nhân tham gia vào 28 nghiên cứu [12, 16, 21, 28−32, 55, 63-68, 71, 72, 79−82, 84−87, 90, 91, 98] liên quan đến bệnh nặng và bệnh nhân phẫu thuật cho thấy kết quả đã được cải thiện đáng kể khi kết hợp với chế độ điều trị dịch truyền bảo tồn (OR 0,42 [95% CI 0,32 đến 0,55]), so với quản lý dịch truyền không bảo tồn. Điều này được minh họa trong Forest plot trong Hình 4.
![Hình 3. Forest plot nhìn vào cân bằng dịch truyền tích lũy sau một tuần * ở lại ICU những người sống sót so với những người không sống sót. Cập nhật và điều chỉnh từ Malbrain et al. [61]; FB - cân bằng dịch truyền.](https://www.healcentral.org/wp-content/uploads/2020/09/qua_tai_dich_truyen_6-300x141.jpg)
![Hình 4. Forest plot nhìn vào ảnh hưởng của chế độ dịch truyền hạn chế so với chế độ dịch truyền tự do đối với tỷ lệ tử vong. Cập nhật và điều chỉnh từ Malbrain et al. [61]](https://www.healcentral.org/wp-content/uploads/2020/09/qua_tai_dich_truyen_7-300x230.jpg)
Bệnh nhân IAH có cân bằng dịch truyền dương tính hơn? Dữ liệu có sẵn từ 1.517 bệnh nhân thu được từ một phân tích tổng hợp của từng bệnh nhân và bảy nghiên cứu đoàn hệ hoặc trường hợp kiểm soát [32, 62, 72, 78, 83, 88, 89, 100]. Phân tích tổng hợp các kết quả gộp cho thấy 597 bệnh nhân mắc IAH (tỷ lệ mắc là 39,4%) có cân bằng dịch dương tính hơn so với những người không có IAH (7.777,9 ± 3,804 mL so với 4,389,3 ± 1,996,4 mL) (Hình 1). Cân bằng dịch truyền tích lũy sau một tuần ở lại ICU trung bình là 3,388,6 ± 2,324,2 mL dương tính hơn (Hình 2). Một bản tóm tắt các kết quả của những nghiên cứu này được đưa ra trong Hình 6.
![Hình 5. Forest plot xem xét cân bằng dịch truyền tích lũy sau một tuần * ở lại ICU bệnh nhân có (quản lý dịch truyền hạn chế) và không có sự can thiệp (quản lý dịch truyền tự do). Cập nhật và điều chỉnh từ Malbrain et al. [61]; FM - quản lý dịch truyền; Điều trị PAL - PEEP, albumin và lasix (furosemide)](https://www.healcentral.org/wp-content/uploads/2020/09/qua_tai_dich_truyen_8-300x137.jpg)
![Hình 6. Forest plot xem xét cân bằng dịch truyền tích lũy sau một tuần ICU ở lại bệnh nhân có và không có tăng áp lực trong ổ bụng (IAH). Cập nhật và điều chỉnh từ Malbrain et al. [61]; IAH - tăng áp lực trong ổ bụng; FB - cân bằng dịch truyền](https://www.healcentral.org/wp-content/uploads/2020/09/qua_tai_dich_truyen_9-300x102.jpg)
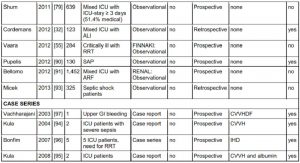
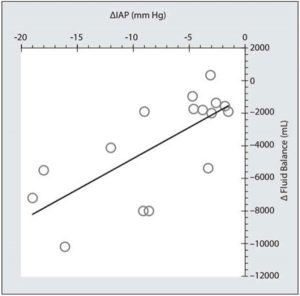
Đây là những nghiên cứu điển hình hoặc loạt nhỏ [70, 72−75, 77, 90, 92, 94−97]. Việc loại bỏ toàn bộ dịch truyền 4,876,3 ± 4,178,5 mL dẫn đến giảm IAP từ 19,3 ± 9,1 xuống 11,5 ± 3,9 mm Hg (Hình 8). Một hiệu ứng đã được quan sát: sự cân bằng dịch truyền hoặc loại bỏ dịch truyền càng âm thì mức giảm IAP càng lớn (Hình 9).
![Hình 7. Forest plot nhìn vào ảnh hưởng của việc loại bỏ dịch truyền đối với áp lực trong ổ bụng. Cập nhật và điều chỉnh từ Malbrain et al. [61]; PEEP - áp lực thở cuối dương tính; Điều trị PAL - PEEP, albumin và lasix (furosemide)](https://www.healcentral.org/wp-content/uploads/2020/09/qua_tai_dich_truyen_10-300x141.jpg)
GỢI Ý CHO THỰC HÀNH LÂM SÀNG
Mặc dù kết quả của phân tích tổng hợp này rất hấp dẫn, nhưng chúng bị hạn chế bởi tính gián tiếp và nguy cơ sai lệch do bao gồm các thiết kế nghiên cứu khác nhau và dân số bệnh nhân và sử dụng nhiều biện pháp can thiệp khác nhau. Sau khi xem xét nhiều bằng chứng ở trên, Hội chứng khoang bụng thế giới đã gợi ý sử dụng một giao thức để tránh sự cân bằng dịch truyền tích lũy dương tính ở những bệnh nhân bị bệnh nghiêm trọng, đặc biệt là những người có hoặc có nguy cơ IAH sau quá trình hồi sức cấp tính đã hoàn tất và các vấn đề thúc đẩy/kiểm soát nguồn đã được giải quyết (Grade 2C) [50].
Chúng tôi gợi ý mục tiêu cân bằng dịch truyền từ 0 đến âm vào ngày thứ 3 và để giữ cân bằng dịch truyền tích lũy vào ngày 7 càng thấp càng tốt (Grade 2B). Một vòng luẩn quẩn dẫn đến tải nhiều dịch truyền hơn và tăng IAP hơn nữa được minh họa trong Hình 10, và điều này phải tránh.
Sau khi xem xét các bằng chứng hạn chế, chúng tôi chỉ có thể đưa ra một gợi ý yếu về việc sử dụng thuốc lợi tiểu hoặc điều trị thay thế thận (kết hợp với albumin) so với không can thiệp để truyền dịch ở bệnh nhân ổn định huyết động với IAH và cân bằng dịch tích lũy dương tính sau khi hồi sức cấp tính đã được hoàn thành và các vấn đề thúc đẩy/kiểm soát nguồn đã được giải quyết (Grade 2D). Việc thiếu sự đồng thuận cho can thiệp này nhấn mạnh sự không chắc chắn về vai trò của nó trong việc quản lý cân bằng dịch truyền và sau đó là IAH, và sự cần thiết phải nghiên cứu thêm.
Để trả lời cho câu hỏi ‘Tại sao phải khử dịch hồi sức?”: “Vì quá tải dịch truyền có liên quan độc lập đến tỷ lệ mắc bệnh và tử vong”.
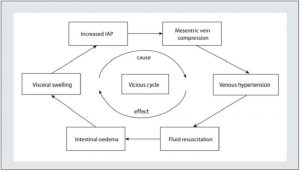
SINH LÝ BỆNH CỦA QUÁ TẢI DỊCH
Phần này sẽ giải quyết câu hỏi: ‘Khi nào cần KHỬ dịch hồi sức? (de-resuscitation) Lúc đầu năm 1942, khái niệm về đáp ứng chuyển hóa kép đối với tổn thương cơ thể đã được đưa ra. Để đáp ứng trực tiếp với các cytokine tiền viêm và hoocmon căng thẳng ban đầu, giai đoạn “Ebb” đại diện cho một cú sốc phân bố đặc trưng bởi giãn mạch máu và rò rỉ albumin xuyên mao mạch làm giảm áp lực keo huyết tương. Đổ đầy động mạch, rối loạn chức năng vi tuần hoàn và phù mô kẽ thứ phát dẫn đến giảm tưới máu toàn thân và sử dụng oxy trong mô bị suy yếu trong khu vực. Trong giai đoạn đầu của cú sốc này, liệu pháp dịch truyền đầy đủ bao gồm việc đổ đầy theo mục tiêu để ngăn ngừa tiến triển thành hội chứng rối loạn chức năng đa cơ quan (MODS, multiple organ dysfunction syndrome). Vì phản xạ thần kinh nội tiết bù trừ và rối loạn chức năng thận tiềm ẩn dẫn đến giữ nước và natri, cân bằng dịch truyền dương vốn có trong giai đoạn “Ebb”. Bệnh nhân bệnh nặng hơn cần nhiều dịch truyền hơn để đạt được tối ưu hóa tim mạch. Do đó, tại thời điểm này cân bằng dịch truyền có thể được coi là một dấu ấn sinh học của bệnh hiểm nghèo, theo đề xuất của Bagshaw et al. [101]. Bệnh nhân vượt qua sốc đạt được cân bằng nội môi của các chất trung gian tiền viêm và chống viêm một cách cổ điển trong vòng ba ngày. Sau đó, ổn định huyết động và phục hồi áp lực keo huyết tương đã tạo ra giai đoạn “Flow” với việc nối lại lợi tiểu và huy động dịch ngoại mạch dẫn đến cân bằng dịch âm.
Khi xem xét việc truyền dịch, điều quan trọng là phải biết khi nào nên bắt đầu truyền dịch (lợi ích của việc truyền dịch là gì), khi nào nên ngừng truyền dịch (những rủi ro của việc truyền dịch liên tục) là khi nào, bắt đầu lấy dịch truyền ra (những gì là lợi ích của việc lấy dịch truyền ra) và khi nào nên ngừng lấy dịch truyền ra (những rủi ro của việc lấy bỏ quá nhiều dịch truyền). Các tài liệu cho thấy sự cân bằng dịch truyền âm tính làm tăng tỷ lệ sống ở bệnh nhân bị sốc nhiễm trùng [31]. Bệnh nhân nhập viện ICU bị nhiễm trùng huyết, suy hô hấp, suy thận, ARDS, IAH hoặc ACS đều có cân bằng dịch tích lũy dương tính hơn so với những người không bị suy cơ quan [26, 27, 29, 102, 103]. Bệnh nhân được quản lý với một chiến lược dịch truyền bảo tồn dường như cũng đã cải thiện chức năng phổi, thời gian thở máy và thời gian ICU ngắn hơn mà không làm tăng suy cơ quan không do phổi [30]. Tuy nhiên, việc giám sát là rất cần thiết, vì bất kỳ phép đo nào trong ICU chỉ có giá trị khi nó chính xác và có thể tái tạo, và không có phép đo nào làm cải thiện khả năng sống sót, chỉ có một giao thức tốt có thể làm điều này. Ngược lại, một thuật toán điều trị kém có thể dẫn đến tác hại tiềm tàng cho bệnh nhân [104, 105]. Bệnh nhân đang trong giai đoạn sốc “Ebb” hoặc “Flow” có các biểu hiện lâm sàng khác nhau và do đó nhu cầu theo dõi (mục tiêu) khác nhau và các mục tiêu điều trị khác nhau [25, 61].
Chức năng thận đặc biệt bị ảnh hưởng mạnh mẽ do quá tải dịch truyền và IAH, và phù mô kẽ thận có thể làm suy giảm chức năng thận, ngay cả khi không có IAH [14, 23, 91, 101, 106]. Do đó, quá tải dịch truyền dẫn đến IAH và rối loạn chức năng thận liên quan có thể chống lại sự hồi phục của chính nó [107]. Các tác động bất lợi của quá tải dịch truyền và phù mô kẽ là rất nhiều và có ảnh hưởng đến tất cả các chức năng cơ quan cuối, mặc dù một số bác sĩ lâm sàng vẫn tin rằng phù ngoại biên chỉ là mối quan tâm sơ sài [108]. Do tác động bất lợi của tình trạng quá tải dịch truyền trong tình trạng rò rỉ mao mạch đặc biệt rõ rệt ở phổi, việc theo dõi EVLWI có thể cung cấp một công cụ có giá trị để hướng dẫn quản lý dịch truyền trong tình trạng nguy kịch. EVLWI cao cho thấy tình trạng rò rỉ mao mạch, liên quan đến mức độ nghiêm trọng của bệnh tật và tử vong cao hơn [32, 72, 109, 110]. Các nghiên cứu trước đây liên quan đến EVLWI với sự thoát mạch albumin ở bệnh nhân sau đa chấn thương [111]. Đáp ứng với LCFM vượt qua cú sốc phân bố và thực hiện chuyển đổi sang giai đoạn “Flow” [32]. Mặt khác, những người không đáp ứng nằm trong sự kìm kẹp của pha Ebb và tiến triển GIPS, dẫn đến cân bằng dịch truyền dương tính, suy cơ quan và tử vong.
Trong giả thuyết này, (thay đổi) EVLWI có giá trị tiên lượng là sự phản ánh mức độ rò rỉ mao mạch, thay vì định lượng suy giảm chức năng phổi bằng nước phổi [32, 47]. Các quan sát gần đây cũng có thể cho thấy hậu quả trực tiếp liên quan đến việc quản lý dịch truyền ở bệnh nhân bị bệnh nặng với IAH. Bệnh nhân có nguy cơ mắc GIPS được đánh giá bởi CLI, IAP, thay đổi EVLWI và cân bằng dịch truyền, yêu cầu chiến lược hạn chế dịch truyền và thậm chí loại bỏ dịch truyền được hướng dẫn bằng cách theo dõi huyết động kéo dài bao gồm đo nước phổi (loại bỏ dịch theo mục tiêu muộn) [22, 112]. Trước đây, việc áp dụng liệu pháp điều trị bằng dịch truyền có hướng dẫn EVLWI đã dẫn đến kết quả được cải thiện và cân bằng dịch truyền dương tính thấp hơn trong tình trạng rò rỉ mao mạch [68]. Để đạt được sự quản lý dịch truyền hạn chế có thể cần sử dụng nhiều hơn liệu pháp vận mạch, hồi sức bằng các dung dịch áp lực keo cao (ví dụ albumin 20%) và bắt đầu điều trị bằng thuốc lợi tiểu và thay thế thận, mặc dù trong thử nghiệm FACCT, nhóm bảo tồn có xu hướng lọc máu ít hơn [30].
“Khi nào nên bắt đầu khử dịch hồi sức?”: “Cần khử dịch hồi sức khi quá tải dịch truyền và tích tụ dịch truyền ảnh hưởng tiêu cực đến chức năng các cơ quan, vì vậy việc hồi sức là bắt buộc trong trường hợp cân bằng dịch tích lũy dương tính kết hợp với oxy hóa máu kém (tỷ lệ P/F < 200), tăng rò rỉ mao mạch (PVPI cao > 2,5 và EVLWI > 12 ml/kg PBW), tăng IAP ( > 15 mm Hg) và APP thấp (< 50 mm Hg), CLI cao, v.v. .
TIẾP CẬN THỰC TẾ
Làm thế nào để khử dịch hồi sức? Hiện tại: Đo tại giường của chỉ số nước ngoài mạch máu phổi (EVLWI) được thực hiện bằng phương pháp pha loãng nhiệt xuyên phổi cho phép ước tính mức độ rò rỉ mao mạch và quá tải dịch truyền. Theo đó, EVLWI tương quan tốt với chức năng cơ quan và khả năng sống sót [49, 102, 109, 113]. Hơn nữa, việc quản lý dịch truyền nhằm mục đích giảm EVLWI dẫn đến cân bằng dịch truyền âm tính hơn và kết quả được cải thiện [68]. Để đạt được sự cân bằng dịch truyền âm tính, các thử nghiệm tiền cứu trước đó đã loại trừ bệnh nhân bị tụt huyết áp và suy thận [30, 65, 68]. Gần đây trong một nghiên cứu trên 57 bệnh nhân được so sánh với 57 đối chứng phù hợp, tác dụng của chế độ điều trị hạn chế với cân bằng dịch âm tính bằng “Điều trị PAL” đã được kiểm tra ở những bệnh nhân thở máy có ALI bị thiếu oxy nặng, tăng EVLWI và IAP [72]. Điều trị PAL kết hợp mức độ PEEP cao, hồi sức thể tích nhỏ bằng albumin áp suất keo cao và loại bỏ dịch truyền bằng thuốc lợi tiểu (Lasix®) hoặc siêu lọc trong liệu pháp thay thế thận liên tục (CRRT). Đầu tiên, chuẩn độ PEEP trong 30 phút được thực hiện để đối trọng với các tác động của IAP tăng (PEEP tốt nhất tính bằng cm H2O = IAP tính bằng mm Hg). Tiếp theo, dung dịch albumin hyperoncotic (20%) được dùng 200 ml bolus trong hơn 60 phút hai lần vào ngày đầu tiên và sau đó được chuẩn độ theo mức albumin huyết thanh là 30 g/dL. Cuối cùng, 30 phút sau liều albumin đầu tiên, furosemide được bắt đầu với liều tải vào đường tĩnh mạch là 60 mg, sau đó là truyền liên tục ở mức 60 mg mỗi giờ trong bốn giờ đầu và 5−20 mg mỗi giờ sau đó, theo mực dung nạp của huyết động học (Hình 11).
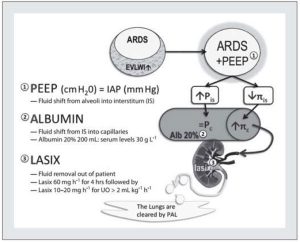
Ở những bệnh nhân vô niệu, CRRT có thể được thêm vào với tốc độ siêu lọc được thiết lập để có được sự cân bằng dịch truyền trung tính đến âm tính hàng ngày. Một tuần điều trị PAL có tác dụng có lợi đối với EVLWI, IAP, chức năng cơ quan và liệu pháp vận mạch, và điều này dẫn đến thời gian thở máy ngắn hơn (cai máy nhanh hơn) và cải thiện tỷ lệ tử vong trong 28 ngày (Hình 12).
Kết hợp các kết quả của hai nghiên cứu gần đây (n = 180), chúng tôi thấy rằng nhóm bệnh nhân được điều trị bằng quản lý dịch truyền bảo tồn ban đầu và muộn có kết quả tốt nhất, tiếp theo là những người được quản lý dịch truyền đầy đủ ban đầu và bảo tồn muộn [32, 72]. Tỷ lệ tử vong tăng đáng kể ở những bệnh nhân được điều trị bằng dịch truyền tự do muộn (Hình 14). Điều này phù hợp với kết quả trước đó của Murphy et al. [21].
![Hình 13. Biểu đồ dạng thanh cho thấy sự phân bố và kết quả của bệnh nhân trong các loại quản lý dịch truyền khác nhau so sánh dữ liệu từ Murphy (n = 212) [21] và dữ liệu tổng hợp từ hai nghiên cứu từ Cordemans (n = 180) [32, 72].](https://www.healcentral.org/wp-content/uploads/2020/09/qua_tai_dich_truyen_15-300x261.jpg)
THẢO LUẬN
Kết quả phân tích tổng hợp và tổng quan hệ thống các bằng chứng sẵn có hỗ trợ cho giả thuyết rằng quá tải dịch truyền gây bất lợi cho bệnh nhân và có liên quan đến tăng tỷ lệ mắc bệnh và tử vong.
Gần đây, chúng tôi đã đề xuất một mô hình ba cú sốc mà chúng tôi muốn mở rộng thành mô hình bốn cú sốc, trong đó chúng tôi có thể nhận ra năm giai đoạn động hoặc giai đoạn quản lý dịch truyền khác nhau [32]: Hồi sức, Tối ưu hóa, Ổn định và dẫn lưu (ROSE), theo sau là nguy cơ tiềm tàng của giảm tưới máu (Bảng 3, Hình 15).
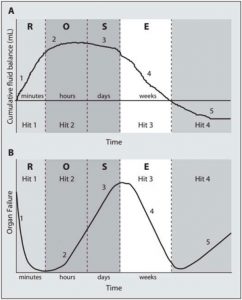
”Hình A: Biểu đồ cho thấy mô hình bốn cú sốc với sự tiến triển của tình trạng thể tích dịch tích lũy của bệnh nhân theo thời gian trong năm giai đoạn hồi sức riêng biệt: Hồi sức (1), Tối ưu hóa (2), Ổn định (3) và dẫn lưu (4) (ROSE), theo sau là nguy cơ giảm tưới máu (5) có thể xảy ra trong trường hợp khử dịch hồi sức quá tấn công. Xem văn bản để giải thích; Hình B – biểu đồ minh họa mô hình bốn cú sốc tương ứng với tác động lên chức năng cơ quan cuối liên quan đến tình trạng dịch truyền. Khi nhập viện, bệnh nhân bị giảm thể tích máu (1), sau đó là thể tích máu bình thường (2) sau khi hồi sức dịch, và quá tải dịch truyền (3), một lần nữa sau đó là giai đoạn chuyển sang thể tích máu bình thường với khử dịch hồi sức (4) và giảm thể tích máu có nguy cơ giảm tưới máu (5). Trong trường hợp giảm thể tích máu (giai đoạn 1 và 5), O2 không thể xâm nhập vào các mô vì các vấn đề đối lưu; trong trường hợp tăng thể tích máu (giai đoạn 3), O2 không thể xâm nhập vào các mô vì các vấn đề khuếch tán liên quan đến phù mô kẽ và phổi, phù ruột (hồi tràng) và tăng áp lực ổ bụng.”
Về mặt logic, những điều này mô tả năm giai đoạn lâm sàng khác nhau của liệu pháp điều trị bằng dịch truyền, xảy ra theo thời gian trong đó bệnh nhân trải qua một tác động khác nhau đối với chức năng của cơ quan cuối (Hình 15). Những nguyên tắc tương tự gần đây cũng được đề xuất bởi những người khác, xác nhận sự cần thiết của một thử nghiệm tiến cứu đa trung tâm với cách tiếp cận 2 mục tiêu sử dụng quản lý dịch truyền bảo tồn muộn sau khi điều trị theo mục tiêu ban đầu đầy đủ ở những bệnh nhân không tự phát chuyển từ giai đoạn “Ebb” sang giai đoạn “Flow” [22 , 24, 38, 40, 101, 114-116]. Chúng tôi sẽ thảo luận bên dưới mô hình bốn cú sốc, mỗi cú sốc tương ứng với một câu hỏi điều trị cụ thể.
1ST HIT: KHI NÀO TÔI BẮT ĐẦU CHO DỊCH? TẤT CẢ LỢI ÍCH CỦA DỊCH TRUYỀN LÀ GÌ?
Giai đoạn hồi sức. (Resuscitation phase) Sau cú đánh đầu tiên có thể là nhiễm trùng huyết, bỏng, viêm tụy hoặc chấn thương, bệnh nhân sẽ bước vào giai đoạn sốc “Ebb”. Giai đoạn sốc nặng này, có thể đe dọa đến tính mạng, xảy ra trong vòng vài phút và được đặc trưng bởi áp lực động mạch trung bình thấp, CO thấp và suy yếu vi tuần hoàn. Ở một số bệnh nhân, dịch truyền là bắt buộc vì oxy có thể gặp khó khăn đối lưu để đi vào các mô trong trường hợp giảm thể tích máu nặng [116].
![Hình 12. Ảnh hưởng của điều trị PAL (được điều chỉnh từ Cordemans và cộng sự [72]).](https://www.healcentral.org/wp-content/uploads/2020/09/qua_tai_dich_truyen_17-300x220.jpg)

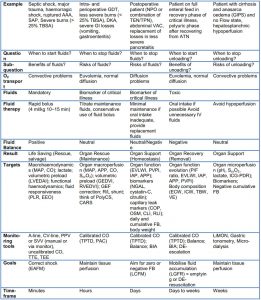
Dịch truyền duy trì nên được cung cấp với tỷ lệ 1 ml/kg/h kết hợp với dịch truyền thay thế khi được chỉ định. Trước khi truyền dịch, việc theo dõi chính xác cung lượng tim (CO) là bắt buộc và phải luôn luôn đánh giá mức độ đáp ứng của dịch truyền bằng xét nghiệm nâng chân thụ động hoặc xét nghiệm tắc nghẽn cuối thì thở ra trước khi truyền dịch. Nên sử dụng máy theo dõi cung lượng tim không xâm lấn hoặc xâm lấn tối thiểu để đánh giá khả năng đáp ứng của dịch truyền.
Giai đoạn này tương ứng với “R”, hoặc Hồi sức (Resuscitation) trong khái niệm ROSE. Trong giai đoạn đầu của giai đoạn hồi sức, nên truyền dịch nhanh chóng dưới dạng bolus (4 ml/kg trên 10 đến 15 phút) và chúng có thể cứu mạng, do đó điều trị trong giai đoạn này được gọi là cứu cánh hoặc điều trị cứu hộ. Mục tiêu là quản lý dịch truyền theo mục tiêu sớm (EAFM, early adequate goal directed fuid management), cân bằng dịch truyền phải dương tính và các mục tiêu hồi sức là: MAP > 65 mm Hg, CI > 2,5 L/min/m2, PPV < 12%, LVEDAI > 8 cm/m2.
2ND HIT: KHI NÀO NGƯNG CHO DỊCH? TẤT CẢ RỦI RO CỦA QUÁ TẢI DỊCH LÀ GÌ?
Giai đoạn tối ưu hóa. (Optimisation phase) Lần truy cập thứ hai xảy ra trong vài giờ và đề cập đến thiếu máu cục bộ và tái tưới máu. Sự tích tụ dịch truyền nên được xem như một dấu ấn sinh học cho mức độ nghiêm trọng của bệnh [24]. Nhu cầu dịch truyền càng lớn, bệnh nhân càng bệnh nặng. Việc sử dụng các kỹ thuật đo cung lượng tim bằng phương pháp pha loãng nhiệt xuyên phổi (PiCCO, Pulsion Medical Systems, Munich, Đức hoặc VolumeView/EV1000, Edwards Lifescatics, Irvine, CA, USA) cho phép theo dõi tiền tải thể tích bằng GEDVI và đo EVLWI được đề xuất trong giai đoạn này [34, 117]. Bác sĩ lâm sàng nên nhận thức được hội chứng đa khoang và khả năng CARS (cardio abdominal renal syndrome) [51, 118]. Trong bối cảnh IAP tăng, các ngưỡng khác có thể được áp dụng và bác sĩ lâm sàng phải biết rằng xét nghiệm PLR có thể âm tính giả [119, 120].
Trong giai đoạn Tối ưu hóa, tình hình vẫn không ổn định nhưng bệnh nhân không còn gặp nguy hiểm đe dọa đến tính mạng ngay lập tức mà thay vào đó là giai đoạn sốc bù – compensated shock (vẫn có nguy cơ mất bù cao) và nên điều trị bằng dịch truyền bổ sung một cách thận trọng hơn với mục đích tối ưu hóa chức năng tim để cải thiện tưới máu mô với mục đích cuối cùng là tránh rối loạn chức năng cơ quan hoặc suy cơ quan (giải cứu cơ quan – organ rescue) [38]. Do đó, mục tiêu là duy trì tưới máu mô và dịch truyền nên được coi là duy trì nhưng có thể an toàn cho cơ quan, cân bằng dịch truyền nên chuyển từ dương sang trung tính và các mục tiêu hồi sức là: MAP > 65 mm Hg, CI > 2,5 L/min/m2, PPV < 14%, LVEDAI 8−12 cm/m2. Trong giai đoạn này, IAP (< 15 mm Hg) được theo dõi và APP (> 55 mm Hg) được tính toán. Tiền tải phải được tối ưu hóa với GEDVI 640-800 mL/m2 và trong trường hợp có giá trị cao thông qua việc sử dụng công thức hiệu chỉnh GEF [33].
Giai đoạn ổn định. (Stabilisation phase) Sau giai đoạn Tối ưu hóa tiếp theo giai đoạn Ổn định phát triển trong những ngày tiếp theo. Giai đoạn cân bằng nội môi này tập trung vào hỗ trợ cơ quan và phản ánh điểm mà bệnh nhân ở trạng thái ổn định, điều trị bằng dịch truyền hiện chỉ được sử dụng để duy trì và thay thế liên tục trong tình trạng mất nước bình thường (ví dụ như thận, đường tiêu hóa, mất không nhận biết), nhưng đây cũng có thể là truyền dịch (bao gồm cả bù nước) nếu bệnh nhân bị mất nước liên tục vì các điều kiện bệnh lý chưa được giải quyết. Tuy nhiên, giai đoạn này được phân biệt với hai giai đoạn trước bởi sự vắng mặt của sốc (bù hoặc không bù) hoặc mối đe dọa sắp xảy ra của sốc. Trọng lượng cơ thể lý tưởng nên được đo hàng ngày và cân bằng dịch truyền tích lũy nên được tính toán để đánh giá nguy cơ quá tải dịch truyền. Phân tích trở kháng điện sinh học (BIA, Bio-electrical impedance analysis) với tính toán nước ngoại bào và nội bào (ECW, ICW), tổng lượng nước cơ thể (TBW) và lượng nước dư thừa (VE, volume excess) có thể cung cấp thêm thông tin. Theo dõi với TPTD hiệu chuẩn được tiếp tục và mục tiêu trong giai đoạn này là quản lý dịch truyền bảo tồn muộn (LCFM, late conservative fluid management), nhằm cân bằng dịch truyền hoặc âm, và dịch truyền nên được xem là duy trì và thay thế và để hỗ trợ chức năng cơ quan, và các mục tiêu hồi sức là chuyển sang chức năng cơ quan: EVLWI < 10−12 ml/kg PBW, PVPI < 2.5, IAP < 15 mm Hg, APP > 55 mm Hg, COP > 16−18 mm Hg và CLI < 60. NGAL, cystatin-C, citrullin, v.v.) có thể hữu ích để đánh giá chức năng cơ quan trong tình trạng quá tải dịch truyền tích lũy do quá trình khuếch tán oxy đến các mô có thể bị suy yếu.
3RD HIT: KHI NÀO TÔI BẮT ĐẦU DỠ TẢI DỊCH TRUYỀN? TẤT CẢ LỢI ÍCH CỦA LẤY BỎ DỊCH
Giai đoạn dẫn lưu. (Evacuation phase) Sau cú đánh thứ hai, hai điều có thể xảy ra: hoặc bệnh nhân hồi phục thêm và bước vào giai đoạn “Flow” một cách tự nhiên với việc dẫn lưu các dịch truyền dư thừa đã được truyền trước đó. Tuy nhiên, nhiều bệnh nhân ICU vẫn ở trạng thái không có “Flow”, sau đó là cú sốc thứ ba thường xảy ra do hội chứng tăng tính thấm toàn cầu (GIPS, global increased permeability syndrome) với sự tích tụ dịch truyền liên tục do rò rỉ mao mạch [47]. Dùng dịch truyền hơn nữa trong giai đoạn này trở nên có hại cho bệnh nhân. Phù ngoại biên và phù toàn thân không chỉ là mối quan tâm bên ngoài, như một số người tin rằng [108], nhưng có hại cho bệnh nhân vì nó dẫn đến rối loạn chức năng cơ quan. Hình 15 minh họa các tác động tiêu cực của quá tải dịch truyền lên chức năng cơ quan cuối. Mặc dù trong ba giai đoạn đầu (‘ROS’), dịch truyền thường được quản lý (ban đầu là cứu hộ, sau đó là duy trì và cuối cùng là thay thế), trong giai đoạn cuối, giai đoạn dẫn lưu (tương ứng với ‘E’ trong khái niệm ROSE) , dịch truyền sẽ cần phải được loại bỏ tích cực khỏi bệnh nhân trong những ngày tiếp theo đến vài tuần để hỗ trợ phục hồi cơ quan. Mục tiêu ở đây sẽ là thúc đẩy sự cân bằng dịch truyền âm tính bằng cách huy động các dịch truyền tích lũy với chiến lược loại bỏ dịch truyền theo mục tiêu muộn (LGFR, late goal directed fuid removal), còn được gọi là khử dịch hồi sức (de- resuscitation). Giám sát trong giai đoạn này nên tập trung vào đánh giá tình trạng quá tải dịch truyền và tác động của nó đến chức năng cơ quan với tỷ lệ TPTD và BIA: P/F, EVLWI, PVPI, IAP, APP, ECW, ICW, TBW và VE. Phương châm ở đây là “phổi khô là phổi hạnh phúc”.
4TH HIT: KHI NÀO TÔI DỪNG LẤY BỎ DỊCH RA? TẤT CẢ CÁC RỦI RO CỦA LẤY DỊCH RA?
Cú đánh cuối cùng cần phải tránh vì nó thường do điều trị sau khi loại bỏ dịch truyền quá nhiệt tình trong giai đoạn trước. Một sự cân bằng dịch truyền tích lũy âm tính và dẫn đến giảm thể tích máu có thể làm tăng trở lại các vấn đề đối lưu gây ra giảm tưới máu và thiếu oxy mô. Trong những tuần phục hồi, phải duy trì và theo dõi tưới máu mô bằng LiMON (Pulsion Medical Systems, Feldkirchen, Đức), đo pH dạ dày (Datex Ohmeda, Helsinki, Phần Lan), vi thẩm phân (micro- dialysis), v.v. phải khu trú vào vi tưới máu mô và tưới máu tạng (gan-lách) bằng cách theo dõi ScvO2, ICG-PDR, pHi và các dấu ấn sinh học. Phương châm ở đây là “gan khô có thể khiến bệnh nhân chết”.
KẾT LUẬN
Rò rỉ mao mạch là một tình trạng viêm với các yếu tố kích hoạt đa dạng xuất phát từ một con đường phổ biến bao gồm tái tưới máu thiếu máu, tạo ra chất chuyển hóa oxy hóa độc hại, tổn thương thành tế bào và enzyme dẫn đến mất chức năng hàng rào nội mô mao mạch.
Ở trạng thái như vậy, sự giãn nở thể tích huyết tương nhằm điều chỉnh quá trình giảm tưới máu có thể dự đoán được dẫn đến sự di chuyển ngoại mạch của nước, chất điện giải và protein. Phù mô ngoại biên, phù cơ quan và cổ trướng có thể được dự đoán theo tỷ lệ với thể tích dịch hồi sức theo quy định. Nhiều chiến lược cho bác sĩ lâm sàng để giảm thể tích dung dịch tinh thể được sử dụng trong khi khôi phục lưu lượng tuần hoàn vĩ mô và vi. Bất kể chiến lược hồi sức, bác sĩ lâm sàng phải duy trì nhận thức cao về mối quan hệ động giữa rò rỉ mao mạch, tải dịch truyền, phù ngoại biên, tăng áp lực trong ổ bụng và hội chứng khoang bụng.
Quản lý dịch truyền bảo tồn muộn và khử dịch hồi sức về lâu dài có thể quan trọng hơn những nỗ lực hồi sức ban đầu trong giai đoạn “Ebb” ở bệnh nhân bị sốc. EVLWI có thể được sử dụng tại giường như một hướng dẫn an toàn để bắt đầu chiến lược quản lý dịch truyền bảo tồn muộn hoặc loại bỏ dịch truyền theo mục tiêu muộn ở những bệnh nhân không tự phát từ giai đoạn Ebb sang giai đoạn Flow. Tuy nhiên, chúng ta phải nhớ rằng không có tham số đơn lẻ nào có thể thay đổi kết quả, điều này chỉ có thể đạt được bằng một giao thức tốt. Điều trị PAL có vẻ là một ví dụ tốt về giao thức như vậy, nhưng cần có các nghiên cứu trong tương lai.
Điều quan trọng là bác sĩ lâm sàng đầu giường phải biết và hiểu:
- Khi nào nên bắt đầu truyền dịch (MAP thấp, CO thấp, tăng lactate máu, LVEDAI thấp, GEF/GEDVI thấp, PPV cao và PLR hoặc EEO dương tính)
- Khi nào nên ngừng truyền dịch (GEF/GEDVI cao, PPV thấp, PLR âm tính, cân bằng dịch truyền hàng ngày dương tính, tăng cân)
- Khi nào bắt đầu loại bỏ dịch truyền (tỷ lệ P/F thấp, EVLWI cao, PVPI cao, IAP tăng, APP thấp được xác định là MAP trừ IAP, cân bằng dịch truyền tích lũy dương, tăng thông số BIA (ECW, TBW, VE), CLI cao hoặc cao RLI, chỉ số rò rỉ thận (albumin trong nước tiểu so với tỷ lệ creatinine)
- Khi nào nên ngừng loại bỏ dịch truyền (ICG- PDR thấp, APP thấp, ScvO2 thấp, cân bằng dịch truyền tích lũy trung tính hoặc âm tính)
Tuy nhiên, người ta phải nhận ra rằng các ngưỡng được đề cập ở trên là mục tiêu di chuyển mà còn với mục tiêu di chuyển (từ liệu pháp điều trị theo mục tiêu đầy đủ sớm, quản lý dịch truyền bảo tồn muộn với việc loại bỏ dịch truyền theo mục tiêu muộn). Và trên hết, người ta phải luôn nhớ rằng việc nạp dịch truyền không cần thiết có thể gây hại.
Nếu bệnh nhân không cần truyền dịch, thì không cho họ, và hãy nhớ rằng dịch truyền tốt nhất có thể là dịch truyền chưa được cung cấp cho bệnh nhân!
Điều cần thiết là phải cung cấp đúng dịch truyền vào đúng thời điểm, và sử dụng các biện pháp giám sát đúng.