Trên thị trường hiện nay có rất nhiều thuốc gerneric có hoạt chất là Codeine tuy nhiên lại rất ít thông tin liên quan đến hoạt chất này. Ở bài này HealCentral.org xin được chia sẻ các thông tin như: Cơ chế tác dụng của Codeine là gì? Codeine có tác dụng gì? Tác dụng phụ của Codeine là gì?… Dưới đây là thông tin chi tiết.
Lịch sử nghiên cứu và phát triển
Theo Tổ chức Y tế Thế giới WHO, codeine là opioid được sử dụng rộng rãi và phổ biến nhất trên thế giới. Nó thường được dùng bằng đường uống và được biết đến là loại an toàn nhất trong tất cả các thuốc giảm đau opioid.
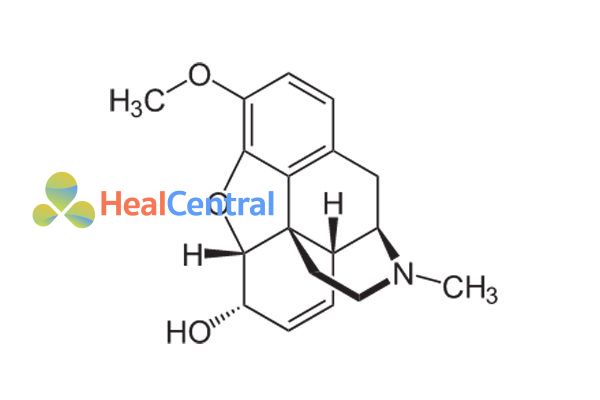
Codeine (hay 3-methylmorphin), là một alkaloid được tìm thấy trong cây thuốc phiện Papaver somniferum, thuộc họ Papaveraceae. Thuốc phiện đã được trồng và sử dụng trong suốt lịch sử loài người cho nhiều mục đích y tế khác nhau (giảm đau, giảm ho và chống tiêu chảy). Codein có nồng độ 1-3% trong thuốc phiện được điều chế bằng phương pháp latex từ vỏ quả chưa chín của Papaver somniferum.
Cho đến đầu thế kỷ XIX, thuốc phiện thô đã được sử dụng trong các chế phẩm đa dạng được gọi là laudanum và paregoric elixirs, một số trong đó đã phổ biến ở Anh kể từ đầu thế kỷ XVIII.

Chế phẩm đầu tiên dường như đã được tạo ra tại Leiden, Hà Lan vào khoảng năm 1715 bởi một nhà hóa học tên là Lemort. Năm 1721, Dược điển Luân Đôn đề cập đến Elixir Asthmaticum, sau này được thay thế bằng thuật ngữ Elixir Paregoricum (“giảm đau”) năm 1746. Sự tiến bộ trong cô lập một số thành phần hoạt động của thuốc phiện đã mở ra con đường cải thiện tính chọn lọc và an toàn của các opiate.
Morphin đã được phân lập ở Đức bởi Friedrich Sertürner năm 1804. Codeine được phân lập lần đầu năm 1832 tại Pháp bởi Pierre Robiquet, người nổi tiếng với việc phát hiện ra alizarin, thuốc nhuộm màu đỏ phổ biến nhất, khi đang nghiên cứu các quy trình tinh chế morphin. Robiquet cũng được ghi nhận là đã phát hiện ra caffein, độc lập với Pelletier, Caventou và Runge. Điều này đã mở đường cho việc xây dựng một thế hệ mới các thuốc chống tiêu chảy và chống ho cụ thể dựa trên codeine an toàn hơn.
Mặc dù codeine có thể được chiết xuất trực tiếp từ thuốc phiện (nguồn gốc của nó), hầu hết codeine được tổng hợp từ morphin thông qua quá trình methyl hóa nhóm –OH phenol, quá trình này lần đầu tiên được hoàn thành vào cuối thế kỷ XX bởi Robert C. Corcoran và Junning Ma.
Cuối năm 1973, các nhà nghiên cứu Hoa Kỳ được giao nhiệm vụ tìm cách tổng hợp codeine và các dẫn xuất của nó để ứng phó với tình trạng khan hiếm thuốc. Họ đã nhanh chóng thành công khi sử dụng dầu mỏ hoặc than đá và 1 quy trình được phát triển tại Viện Y tế Quốc gia Hoa Kỳ.
Nhiều muối của codeine đã được điều chế kể từ khi nó được phát hiện. Được sử dụng phổ biến nhất là muối hydrochloride (tỷ lệ chuyển đổi sang dạng base tự do 0.805), phosphste (0.736), sulfate (0.859) và citrate (0.842). Các loại khác bao gồm salicylate NSAID, codeine salicylate (0.686), muối bromide (codeine methylbromide, 0.759), và ít nhất 4 barbiturate dựa trên codeine, cyclohexenylethylbarbiturate (0.559), cyclopentenylallylbarbiturate (0.561), diallylbarbiturate (0.561) và diethylbarbiturate (0.619). Codeine methylbromide được coi là một loại thuốc riêng biệt dành cho các mục đích khác nhau.
Codeine và morphin, cũng như thuốc phiện, được sử dụng trong nỗ lực điều trị đái tháo đường vào những năm 1880 và gần đây là những năm 1950.
Codein được xếp vào nhóm thuốc gây nghiện tại Việt Nam, là thuốc được kiểm soát đặc biệt.
Dược lực học
Codeine là chất chủ vận chọn lọc receptor µ, nhưng ái lực với thụ thể này yếu hơn nhiều morphin. Trong cơ thể, codeine được chuyển một phần thành morphin có đặc tính giảm đau mạnh hơn. Khi liên kết với các receptor µ, dẫn truyền thần kinh cảm giác đau đến thần kinh trung ương bị cắt đứt, do đó bệnh nhân giảm cảm giác đau.
Cụ thể, khi hoạt hóa các receptor µ ở màng trước synap, Ca2+ vào tế bào giảm, giảm giải phóng các bọc dự trữ chứa chất dẫn truyền thần kinh. Còn ở màng sau synap, hoạt hóa các receptor µ làm tăng đẩy dòng ion K+ ra khỏi tế bào, làm tăng ưu phân cực màng sau synap. 2 tác dụng này hiệp đồng với nhau giảm dẫn truyền cảm giác đau đến thần kinh trung ương.
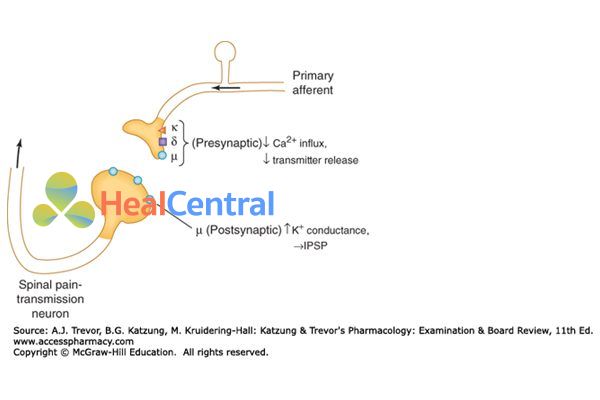
Chủ vận receptor µ ở ruột sẽ gây giảm nhu động ruột, gây táo bón.
Tác động lên các receptor µ trung ương gây an thần, ức chế trung tâm hô hấp.
Codeine cũng ức chế trung tâm ho ở hành não nên có tác dụng giảm ho.
Một số thử nghiệm lâm sàng
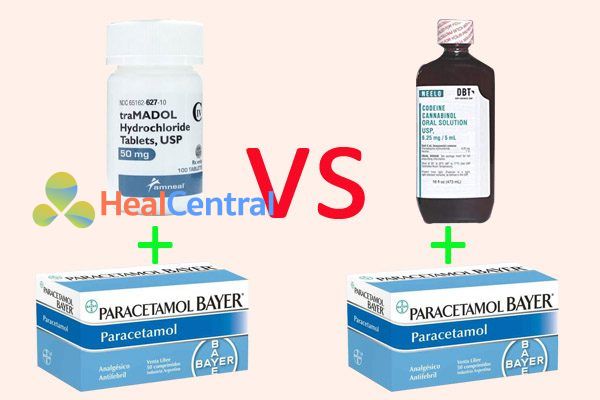
Thử nghiệm so sánh phối hợp tramadol / paracetamol với phối hợp codeine / paracetamol trên chứng mất ngủ ở các tình nguyện viên khỏe mạnh.
Các tác giả: Pickering G, Estrade M và Dubray C đến từ Khoa Dược lý lâm sàng, Bệnh viện Đại học, Khoa Y, 63009 Clermont-Ferrand, Pháp. gisele.pickering@u-clermont1.fr.
Phối hợp tramadol 37.5 mg / paracetamol 325 mg (a) hoặc codeine 30 mg / paracetamol 500 mg (b) hoặc 300 mg có hiệu quả giảm đau tương tự nhau nhưng một sự khác biệt đã được đề xuất liên quan đến các tác dụng phụ của chúng về chứng mất ngủ. Trong thực hành lâm sàng, các phối hợp này thường được dùng với liều như trên 3-4 lần/ngày.
Mục đích của nghiên cứu này là so sánh 1 liều duy nhất của 2 phối hợp (a) và (b) trên 24 tình nguyện viên trẻ khỏe mạnh về thời gian phản ứng lựa chọn thị giác (CRT, ms).
Kết quả cho thấy CRT dài hơn (P < 0.05) (tối đa 4% giá trị đối chứng 3 giờ sau khi dùng thuốc) và báo cáo cao hơn về tình trạng buồn ngủ ở nhóm codeine / paracetamol so với nhóm tramadol / paracetamol (50% so với 4% đối tượng).
Quan sát này rất quan trọng và chứng minh rằng ngay cả 1 liều duy nhất của những loại thuốc được sử dụng thường xuyên này cũng có thể có tác dụng đáng kể. Phát hiện này cần được nghiên cứu thêm ở những đối tượng cao tuổi, những người sử dụng phần lớn các loại thuốc này để giảm đau mạn tính và những người dễ bị loại tác dụng phụ này.
Dược động học
Hấp thu: Thời gian khởi phát tác dụng đưừng uống là 30-60 phút, đường tiêm bắp là 10-30 phút. Thời gian tác dụng 4-6 giờ. Thời gian đạt nồng độ đỉnh trong huyết tương (Tmax) 0.5-1 giờ.
Phân bố: Tỉ lệ liên kết protein huyết tương là 7-25%. Thể tích phân bố (Vd) 3-6 L/kg.
Chuyển hóa: Codeine được chuyển hóa thành morphin bởi CYP2D6, demethyl hóa hoặc liên hợp ở gan (O-demethyl hóa, N-demethyl hóa và liên hợp một phần với glucuronic). Các chất chuyển hóa chính trong hình dưới.
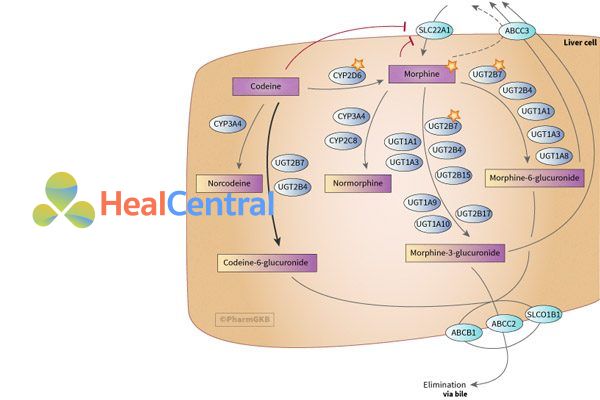
Thải trừ: Thời gian bán thải (t1/2) 3-4 giờ. Bài xuất qua nước tiểu 90% (10% dưới dạng không đổi) và phân. Thanh thải thận là 183 +/- 59 mL/phút.
Hệ gen dược lí:
10% codein được chuyển hóa thành morphin bởi CYP2D6. Chất chuyển hóa morphin có ái lực cao với các thụ thể opioid hơn codeine.
Chuyển hóa kém ở CYP2D6 có thể không đạt được sự giảm đau đầy đủ.
Các chất chuyển hóa cực nhanh (7% người da trắng và lên đến 30% dân số châu Á và châu Phi) có thể làm tăng độc tính.
Chỉ định và liều dùng
Đau:
15-60 mg PO mỗi 4-6 giờ khi cần thiết. Không quá 360 mg/ngày ở bệnh nhân điều trị lần đầu.
Bệnh nhân đã dùng opioid trước đó có thể cần liều ban đầu cao hơn.
Chuẩn độ liều để giảm đau. Sử dụng liều thấp nhất có hiệu quả trong thời gian điều trị ngắn nhất.
Ho:
7.5-30 mg PO mỗi 4-6 giờ khi cần thiết.

Chú thích: PO: đường uống.
Tác dụng phụ
Rất thường gặp (> 10%):
- Táo bón.
- Buồn ngủ.
Thường gặp (1-10%):
- Rối loạn tim mạch: Huyết áp thấp, nhịp tim nhanh hoặc chậm.
- Rối loạn thần kinh trung ương: Lú lẫn, chóng mặt, đau đầu, xây xẩm, khó chịu, sự kích thích nghịch lý hệ thần kinh trung ương, bồn chồn.
- Phản ứng dị ứng: Phát ban, nổi mày đay.
- Rối loạn tiêu hóa: Chán ăn, buồn nôn, nôn, khô miệng.
- Rối loạn tiết niệu: Co thắt niệu quản, tiểu tiện giảm.
- Các xét nghiệm chức năng gan bất thường.
- Nóng tại vị trí tiêm.
- Yếu, nhìn mờ.
- Khó thở, tăng giải phóng histamine.
Tác dụng phụ < 1%:
- Hạ huyết áp với đường tĩnh mạch.
- Phản ứng phản vệ (hiếm).
- Co giật với liều quá cao.
- Suy hô hấp.
Báo cáo hậu mãi:
- Hạ huyết áp nặng.
- Suy hô hấp đe dọa tính mạng.
- Hội chứng cai opioid ở trẻ sơ sinh.
- Tử vong liên quan đến các chất chuyển hóa quá nhanh của codeine.
- Thiểu năng thượng thận.
- Phản ứng có hại trên đường tiêu hóa, đau bụng.
- Động kinh, hưng phấn.
- Khó phát âm.
- Ngứa, đổ mồ hôi.
- Hội chứng serotonin.
- Sốc phản vệ.
- Thiếu hụt androgen.
Lưu ý và thận trọng
Cảnh báo hộp đen:
Chiến lược đánh giá và giảm thiểu rủi ro thuốc giảm đau opioid (REMS):
- Để đảm bảo lợi ích của thuốc giảm đau opioid lớn hơn nguy cơ nghiện và lạm dụng, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã yêu cầu REMS cho các sản phẩm này. Theo yêu cầu của REMS, các công ty dược phẩm với các sản phẩm giảm đau opioid được phê duyệt phải cung cấp các chương trình giáo dục tuân thủ REMS cho các nhà cung cấp dịch vụ chăm sóc sức khỏe.
- Các nhà cung cấp chăm sóc sức khỏe được khuyến khích mạnh mẽ để:
ü Hoàn thành chương trình giáo dục tuân thủ REMS.
ü Tư vấn cho bệnh nhân và / hoặc người chăm sóc của họ với mỗi đơn thuốc về cách sử dụng an toàn, những rủi ro nghiêm trọng, cách lưu trữ và loại bỏ các sản phẩm này.
ü Nhấn mạnh cho bệnh nhân và người chăm sóc của họ tầm quan trọng của việc đọc hướng dẫn sử dụng thuốc được dược sĩ cung cấp.
ü Xem xét các công cụ khác để cải thiện sự an toàn của bệnh nhân, hộ gia đình và cộng đồng.
Nghiện và lạm dụng thuốc:
- Nguy cơ nghiện và lạm dụng opioid có thể dẫn đến quá liều và tử vong. Đánh giá rủi ro của từng bệnh nhân trước khi kê đơn và theo dõi tất cả các bệnh nhân thường xuyên.

Suy hô hấp đe dọa tính mạng:
- Có thể xảy ra nghiêm trọng, đe dọa tính mạng hoặc tử vong.
- Theo dõi tình trạng suy hô hấp, đặc biệt là khi bắt đầu sử dụng hoặc khi tăng liều.
Vô tình nuốt phải:
- Vô tình nuôt phải 1 liều, đặc biệt là trẻ em, có thể dẫn đến quá liều gây tử vong.
Hội chứng cai opioid ở trẻ sơ sinh:
- Sử dụng kéo dài trong thai kỳ có thể dẫn đến hội chứng cai opioid ở trẻ sơ sinh, có thể đe dọa đến tính mạng nếu không được nhận biết sớm và điều trị kịp thời.
- Nếu việc sử dụng opioid trong thời gian dài ở phụ nữ mang thai là cần thiết, hãy thông báo cho bệnh nhân về nguy cơ mắc hội chứng cai opioid ở trẻ sơ sinh và đảm bảo sẽ có phương pháp điều trị thích hợp.
Chuyển hóa quá nhanh codeine và các yếu tố nguy cơ khác gây ức chế hô hấp đe dọa tính mạng ở trẻ em:
- Suy hô hấp và tử vong được báo cáo ở những trẻ được nhận codeine sau phẫu thuật cắt amidan và / hoặc cắt VA do đa hình di truyền CYP2D6.
- Chống chỉ định ở trẻ dưới 12 tuổi và trẻ dưới 18 tuổi sau phẫu thuật cắt amidan và / hoặc cắt VA. Tránh sử dụng ở trẻ 12-18 tuổi có yếu tố nguy cơ có thể làm tăng độ nhạy cảm với tác dụng ức chế hô hấp của codeine.
Tương tác với các thuốc ảnh hưởng đến isoenzyme cytochrom P450:
- Sử dụng các chất gây cảm ứng CYP3A4, chất ức chế CYP3A4 hoặc chất ức chế CYP2D6 cần phải xem xét cẩn thận các tác dụng đối với thuốc mẹ codeine và chất chuyển hóa hoạt động morphin.
Rủi ro từ việc sử dụng đồng thời với các benzodiazepine hoặc thuốc ức chế thần kinh trung ương khác:
- Sử dụng đồng thời opioid với các benzodiazepine hoặc thuốc ức chế hệ thần kinh trung ương khác (bao gồm cả rượu) có thể dẫn đến an thần sâu sắc, suy hô hấp, hôn mê và tử vong.
- Dự trữ đồng thời codeine và benzodiazepine hoặc thuốc ức chế thần kinh trung ương khác để sử dụng cho những bệnh nhân không đủ lựa chọn điều trị thay thế.
- Liều lượng và thời gian điều trị tối thiểu.
- Theo dõi bệnh nhân các dấu hiệu và triệu chứng của suy hô hấp và an thần.
Thận trọng:
Nguy cơ nghiện và lạm dụng thuốc. Nghiện có thể xảy ra ở liều khuyến cáo. Đánh giá nguy cơ nghiện opioid hoặc lạm dụng của từng bệnh nhân trước khi kê đơn. Thận trọng ở những bệnh nhân có tiền sử cá nhân hoặc gia đình lạm dụng chất gây nghiện hoặc bệnh tâm thần. Kê đơn với liều nhỏ nhất trong thời gian ngắn nhất có thể.
Có thể gây hạ huyết áp nặng bao gồm hạ huyết áp thế đứng và ngất ở bệnh nhân cấp cứu. Có nguy cơ gia tăng ở những bệnh nhân mà khả năng duy trì huyết áp đã bị tổn hại do giảm thể tích máu hoặc sử dụng đồng thời một số loại thuốc ức chế thần kinh trung ương (ví dụ: phenothiazin hoặc thuốc gây mê nói chung). Theo dõi bệnh nhân các dấu hiệu hạ huyết áp sau khi bắt đầu hoặc chuẩn độ liều. Nên tránh ở những bệnh nhân bị sốc tuần hoàn, liệu pháp có thể gây giãn mạch, làm giảm thêm cung lượng tim và huyết áp.
Ở những bệnh nhân dễ bị ảnh hưởng nội sọ do giữ CO2 (ví dụ: tăng áp lực nội sọ hoặc u não), liệu pháp có thể làm giảm tình trạng hô hấp và giữ CO2, làm tăng thêm áp lực nội sọ. Theo dõi các dấu hiệu an thần và suy hô hấp, đặc biệt khi bắt đầu điều trị. Các opioid có thể che khuất triệu chứng lâm sàng ở bệnh nhân bị chấn thương đầu. Tránh sử dụng trên những bệnh nhân bị suy giảm ý thức hoặc hôn mê.
Chống chỉ định ở những bệnh nhân đã biết hoặc nghi ngờ tắc nghẽn tiêu hóa, bao gồm cả tắc do liệt ruột, có thể gây co thắt cơ vòng Oddi. Các opioid có thể gây tăng amylase huyết thanh. Theo dõi bệnh nhân mắc bệnh đường mật, bao gồm cả viêm tụy cấp.
Điều trị có thể làm tăng tần suất động kinh. Theo dõi bệnh nhân có tiền sử rối loạn co giật để kiểm soát cơn động kinh.
Tránh sử dụng thuốc chủ vận / đối kháng hỗn hợp (ví dụ: pentazocine, nalbuphine và butoranol) hoặc thuốc chủ vận một phần (ví dụ: buprenorphin) để giảm đau ở những bệnh nhân đang dùng opioid đầy đủ. Thuốc chủ vận / đối kháng hỗn hợp và thuốc chủ vận một phần có thể làm giảm tác dụng giảm đau và / hoặc xuất hiện các triệu chứng cai. Khi ngừng điều trị ở những bệnh nhân này, giảm dần liều dùng, không ngừng điều trị đột ngột.
Cảnh báo bệnh nhân không lái xe hoặc vận hành máy móc nguy hiểm trừ khi họ chịu được tác dụng của thuốc và biết sẽ phản ứng với thuốc như thế nào.
Suy hô hấp nghiêm trọng, đe dọa tính mạng hoặc tử vong có thể xảy ra bất cứ khi nào trong khi điều trị, nguy cơ lớn nhất khi bắt đầu điều trị hoặc sau khi tăng liều. Theo dõi bệnh nhân chặt chẽ về suy hô hấp, đặc biệt là trong vòng 24-72 giờ đầu tiên bắt đầu điều trị và sau khi tăng liều. Vô tình uống phải 1 liều, đặc biệt là trẻ em, có thể dẫn đến suy hô hấp và tử vong do quá liều codeine.
Tử vong đã xảy ra ở trẻ bú mẹ tiếp xúc với lượng morphin cao trong sữa mẹ vì phụ nữ đang cho con bú là chuyển hóa rất nhanh của codeine.
Sử dụng ở những bệnh nhân hen phế quản cấp hoặc nghiêm trọng trong môi trường không được giám sát hoặc không có thiết bị hồi sức bị chống chỉ định. Bệnh nhân mắc bệnh phổi tắc nghẽn mạn tính đáng kể hoặc bệnh tim phổi, với dự trữ hô hấp giảm đáng kể, thiếu oxy, tăng carbonic huyết, hoặc suy hô hấp trước đó tăng nguy cơ giảm hô hấp, bao gồm cả ngưng thở, ngay cả ở liều khuyến cáo.
Suy hô hấp đe dọa tính mạng có khả năng xảy ra cao ở bệnh nhân cao tuổi, suy kiệt hoặc suy nhược vì dược động học thay đổi so với bệnh nhân trẻ và khỏe mạnh hơn. Cần giám sát chặt chẽ.
Các chất ức chế monoamin oxydase (IMAO) có thể làm tăng tác dụng của morphin (chất chuyển hóa hoạt động của codeine), bao gồm ức chế hô hấp, hôn mê và lú lẫn. Không nên dùng codeine trong vòng 14 ngày sau khi uống IMAO.
Các trường hợp thiểu năng thượng thận đã được báo cáo khi sử dụng opioid, thường sau hơn 1 tháng sử dụng. Các triệu chứng có thể bao gồm buồn nôn, nôn, chán ăn, mệt mỏi, yếu, chóng mặt và huyết áp thấp. Nếu chẩn đoán thiểu năng thượng thận, điều trị bằng corticoid, cai nghiện opioid để chức năng tuyến thượng thận phục hồi và tiếp tục điều trị bằng corticoid cho đến khi chức năng phục hồi hoàn toàn. Opioid khác có thể được thử vì một số trường hợp báo cáo sử dụng opioid khác không gây tái phát thiểu năng thượng thận.
Sử dụng opioid mạn tính có thể làm giảm khả năng sinh sản ở nữ và nam giới. Không rõ liệu những ảnh hưởng này có thể đảo ngược hay không.
Thận trọng khi chọn liều cho bệnh nhân cao tuổi, thường bắt đầu ở mức thấp nhất. Người cao tuổi có nhiều khả năng bị suy giảm chức năng thận.
Dược động học của codeine thay đổi ở bệnh nhân suy thận. Độ thanh thải có thể giảm và các chất chuyển hóa có thể tích lũy trong huyết tương với nồng độ cao hơn nhiều so với bệnh nhân chức năng thận bình thường. Bắt đầu ở liều thấp hơn bình thường hoặc khoảng thời gian dùng thuốc dài hơn và chuẩn độ từ từ, theo dõi các dấu hiệu suy hô hấp, an thần và hạ huyết áp.
Thận trọng trong rối loạn nhịp tim, lạm dụng / phụ thuộc thuốc, rối loạn cảm xúc, bệnh túi mật, chấn thương đầu, suy gan, suy giáp, tăng ICP, phì đại tiền liệt tuyến, suy thận, co giật do động kinh, hẹp niệu đạo, phẫu thuật đường tiết niệu, suy hô hấp đe dọa tính mạng và tử vong được báo cáo ở những trẻ dùng codeine. Dựa trên các báo cáo hậu mãi, trẻ dưới 12 tuổi dường như dễ chịu tác động ức chế hô hấp của codeine, đặc biệt nếu có các yếu tố nguy cơ gây suy hô hấp. Trẻ em bị ngưng thở khi ngủ do tắc nghẽn được điều trị bằng codeine sau cắt amidan và / hoặc cắt VA có thể đặc biệt nhạy cảm với tác dụng ức chế hô hấp.
Khi kê đơn codeine cho thanh thiếu niên, các nhà cung cấp dịch vụ chăm sóc sức khỏe nên chọn liều thấp nhất, có hiệu quả trong thời gian ngắn nhất và thông báo cho bệnh nhân và người chăm sóc về nguy cơ và dấu hiệu của quá liều morphin.
Phụ nữ có thai: Sử dụng opioid kéo dài trong thai kỳ có thể dẫn đến hội chứng cai opioid ở trẻ sơ sinh ngay sau sinh. Quan sát các triệu chứng của hội chứng cai opioid ở trẻ sơ sinh và xử trí phù hợp. Các opioid có thể qua nhau thai và gây ức chế hô hấp, ảnh hưởng tâm sinh lý ở trẻ sơ sinh. 1 chất đối kháng opioid như naloxone phải có sẵn để đảo ngược tình trạng suy hô hấp do opioid gây ra ở trẻ sơ sinh. Codeine không được khuyến cáo sử dụng cho phụ nữ mang thai trong thai kỳ hoặc ngay trước khi chuyển dạ, khi có các cách giảm đau khác phù hợp hơn. Opioid có thể kéo dài thời gian chuyển dạ thông qua làm giảm tạm thời cường độ, thời gian và tần suất co bóp tử cung.

Phụ nữ đang cho con bú: Codeine được bài tiết vào sữa mẹ. Ở những phụ nữ có chuyển hóa codeine bình thường (hoạt động CYP2D6 bình thường), lượng codeine được tiết vào sữa mẹ thấp và phụ thuộc liều dùng. Một số phụ nữ chuyển hóa quá nhanh codeine, đạt nồng độ chất chuyển hóa hoạt động morphin trong máu cao hơn dự kiến, dẫn đến nồng độ morphin trong sữa mẹ cao hơn bình thường và có khả năng gây ra nồng độ morphin huyết thanh nguy hiểm ở trẻ sơ sinh, có thể dẫn đến các phản ứng bất lợi nghiêm trọng, bao gồm tử vong. Không có thông tin về tác dụng của codeine trong sản xuất sữa.
Lợi ích phát triển và sức khỏe của việc cho con bú nên được xem xét cùng với nhu cầu điều trị lâm sàng của người mẹ và bất kì tác dụng phụ tiềm ẩn nào với trẻ bú mẹ hoặc người mẹ.
Tương tác thuốc
Dùng cùng alvimopan: Cạnh tranh gắn trên thụ thể. Alvimopan chống chỉ định ở những bệnh nhân dung nạp opioid (nghĩa là những người đã dùng opioid điều trị trong hơn 7 ngày liên tiếp ngay trước khi dùng alvimopan). Bệnh nhân gần đây có tiếp xúc với opioid dự kiến sẽ nhạy cảm hơn với tác dụng của alvimopan và do đó có thể bị đau bụng, buồn nôn và nôn, tiêu chảy.
Dùng cùng benzhydrocodone/paracetamol, clonidine: Tránh sử dụng do tăng độc tính của mỗi thuốc.
Dùng cùng fentanyl, hydrocodone, natri oxybate, sufentanil: Có thể gây ức chế hô hấp, hạ huyết áp, an thần sâu sắc, hôn mê và / hoặc tử vong.
Dùng cùng bremelanotide: Giảm nồng độ hoặc tác dụng của codeine.
Dùng cùng isocaroxazid, linezolid, phenelzine, procarbazine, rasagiline, tranylcypromine: Tăng độc tính của codeine theo cơ chế không rõ.
Dùng cùng xanh methylene: Hiệp đồng tác dụng tăng nồng độ serotonin.
Dùng cùng prasugrel, ticagrelor: Codeine làm giảm nồng độ và tác dụng của prasugrel và ticagrelor bằng cách ức chế hấp thu qua đường tiêu hóa. Xem xét sử dụng 1 thuốc ức chế kết tập tiểu cầu đường tiêm ở bệnh nhân mắc hội chứng vành cấp cần dùng đồng thời với thuốc chủ vận thụ thể opioid.
Dùng cùng valerian: Tăng tác dụng an thần.
Dùng cùng các thuốc cảm ứng CYP2D6: Tăng nồng độ morphin và nguy cơ gặp tác dụng phụ tăng lên.
Dùng cùng các thuốc ức chế CYP2D6: Giảm nồng độ morphin và giảm hiệu quả giảm đau của thuốc.
Chống chỉ định
Quá mẫn cảm với codeine hoặc bất cứ thành phần nào của thuốc.
Suy hô hấp đáng kể.
Trẻ em dưới 12 tuổi.
Quản lí đau hậu phẫu ở trẻ em (<18 tuổi) đã trải qua phẫu thuật cắt amidan và / hoặc cắt VA.
Hen phế quản cấp tính hoặc nghiêm trọng trong môi trường không được giám sát hoặc trong trường hợp không có thiết bị hồi sức.
Sử dụng đồng thời các chất ức chế monoamin oxydase (IMAO) hoặc dừng IMAO chưa đủ 14 ngày.
Đã biết hoặc nghi ngờ tắc nghẽn đường tiêu hóa, bao gồm cả tắc ruột do liệt ruột.
Tài liệu tham khảo:
https://www.ncbi.nlm.nih.gov/books/NBK526029/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3658028/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3789666/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2351742/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2921574/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1427610/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1368573/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1368322/