Bài viết Dự đoán đáp ứng dịch truyền: Đánh giá tài liệu và hướng dẫn cho bác sĩ lâm sàng được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Predicting fluid responsiveness: A review of literature and a guide for the clinician
Tóm tắt
Hồi sức thể tích là vô cùng quan trọng trong điều trị sốc. Điều bắt buộc là việc hồi sức này phải được hướng dẫn bằng cách sử dụng một phương pháp đáng tin cậy để xác định tình trạng thể tích để tránh các tác động xấu của giảm thể tích máu trong khi cũng tránh các phương pháp hồi sức quá mức. Có rất nhiều công cụ và phương pháp có sẵn trong thời đại này để hỗ trợ bác sĩ tại giường trong việc hướng dẫn hồi sức thể tích, sẽ được mô tả trong tổng quan tài liệu này.
Các phương pháp để đánh giá mức độ đáp ứng của tiền tải được chia thành các phép đo tĩnh và động. Các phép đo tĩnh liên quan đến các “ảnh chụp nhanh” của tiền tải. Các phép đo động dựa trên các ứng dụng trong tương tác giữa tim hoặc phổi hoặc thử thách thể tích mô phỏng để dự đoán liệu việc tăng tiền tải bằng cách truyền dịch tăng thể tích sẽ có lợi hay không. Các phép đo động được ưa chuộng hơn các phép đo tĩnh, tuy nhiên, các điều kiện cần đáp ứng cho hầu hết các phép đo động là hợp lệ để các phương pháp này được sử dụng một cách đáng tin cậy trong một quần thể bệnh nặng riêng biệt. Vấn đề này được khắc phục bằng cách sử dụng các thao tác đã được phát triển để đánh giá khả năng đáp ứng của nó nhằm tự do hóa các điều kiện cần thiết cho hầu hết các phép đo động, chẳng hạn như ra nâng chân thụ động, tắc nghẽn thì thở ra và liều dịch bơm TM nhỏ.
Tổng quan tài liệu này nhấn mạnh sự khác biệt giữa các phép đo tĩnh và động của khả năng đáp ứng và đưa ra hướng dẫn để lựa chọn các phương pháp đáng tin cậy nhất để xác định mức độ đáp ứng thể tích riêng biệt cho từng bệnh nhân.
1. Giới thiệu
Sốc tuần hoàn về cơ bản là tình trạng giảm tưới máu và được coi là một dạng suy tuần hoàn cấp tính, đe dọa tính mạng, liên quan đến việc sử dụng oxy không đủ bởi các tế bào [1]. Nó chủ yếu được phân loại thành giảm thể tích, phân bố, tim mạch và tắc nghẽn. Nguyên nhân của sốc được xác định bằng sự tương tác giữa tiền tải, sức cản mạch máu hệ thống (SVR, systemic vascular resistance) và cung lượng tim. Sự khác biệt về huyết áp và huyết động ở các trạng thái sốc được tóm tắt trong Bảng 1.
| Bảng 1. Một bảng cho thấy các loại sốc phổ biến nhất, nguyên nhân và nguyên nhân huyết động. | ||||
| Loại sốc | Bệnh nguyên | Tiền tải | Cung lượng tim | SVR |
| Hypovolemic | Mất nước, xuất huyết | ↓ | ↓ | ↑ |
| Cardiogenic | Nhồi máu cơ tim, ngộ độc, viêm cơ tim do siêu vi | ↑ | ↓ | ↑ |
| Obstructive | Thuyên tắc phổi, tràn dịch màng ngoài tim, tràn khí màng phổi có áp lực | ↔ or ↓ | ↓ | ↑ |
| Distributive | Nhiễm trùng huyết, phản vệ, Suy thượng thận | ↔ or ↓ | ↔ or ↑ | ↓ |
| Neurogenic | Chấn thương não, tủy sống | ↓ | ↔ or ↑ | ↓ |
Một trong những mục tiêu của việc hồi sức sốc là cải thiện việc cung cấp oxy, điều này có thể đạt được bằng cách tăng cung lượng tim bằng cách truyền dịch. Thật không may, không phải lúc nào sự thay đổi của giảm tưới máu cũng như ý muốn, và cân bằng dịch dương thì có liên quan đến việc tăng thời gian điều trị ICU và thời gian nằm viện và tỷ lệ tử vong [2,3]. Do đó, trước khi sử dụng bolus, điều quan trọng là phải xác định xem liệu truyền dịch tăng thể tích có cải thiện tình trạng giảm tưới máu của bệnh nhân hay không. Như vậy, khái niệm về khả năng đáp ứng đã được thiết lập để hướng dẫn xử trí [4].
Khả năng đáp ứng của dịch truyền đã được thay đổi thường xuyên, điều phổ biến nhất là tăng thể tích nhát bóp từ 10 đến 15% sau 500 ml truyền dung dịch tinh thể trong 10 đến 15 phút [5]. Chỉ có khoảng một nửa số bệnh nhân huyết động không ổn định là đáp ứng dịch truyền (fluid- responsive) [6]. Các dấu hiệu lâm sàng bao gồm nhịp tim nhanh và lượng nước tiểu không phải là yếu tố dự đoán nhạy cảm hay đáng tin cậy về khả năng đáp ứng của bệnh nhân [7-10]. Vì những lý do này, cần phải nhấn mạnh đến việc dự đoán đáp ứng và điều trị bằng liệu pháp có hướng dẫn.
Lý do đằng sau dự đoán khả năng đáp ứng của bệnh nhân là xác định bệnh nhân ở phần tăng dần của đường cong Frank-Starling, những người có khả năng sẽ đáp ứng dịch truyền. Các bệnh nhân ở phần tăng dần của đường cong này có dự trữ tiền tải (preload reserve) và có thể tăng cung lượng tim để đáp ứng với thử thách dịch truyền (fluid challenge). Các phép đo đáp ứng thể tích được phân loại thành các phép đo tĩnh và động, tùy thuộc vào cách thức và mức độ thay thế được đo. Hướng dẫn Surviving Sepsis Campaign đã khuyến nghị các phép đo tim tĩnh cho đến khi cập nhật năm 2016 hiện khuyến nghị các phép đo tim động để hướng dẫn hồi sức [11]. Điều cần thiết là các bác sĩ lâm sàng chăm sóc bệnh nhân nguy kịch phải biết sự khác biệt giữa các phương pháp tĩnh và động, và hiểu ứng dụng của nó ở những bệnh nhân nguy kịch.
Hầu hết các nghiên cứu được thực hiện về khả năng đáp ứng của bệnh nhân đã kết hợp cả bệnh nhân bị bệnh nặng trong phẫu thuật và nội khoa. Tổng quan tài liệu này tập trung chủ yếu vào các bệnh nhân bị bệnh nặng ở người lớn mà không có sự phân biệt giữa bệnh nhân phẫu thuật và bệnh nhân nội khoa. Một số phương pháp đánh giá đáp ứng dịch truyền mà không được sử dụng thường xuyên trong khoa cấp cứu (ED) và ICU (như những phương pháp được đánh giá bằng siêu âm tim qua thực quản) không được thảo luận trong tổng quan này.
2. Các chỉ số tĩnh của đáp ứng dịch
Đo áp lực tim tĩnh đề cập đến ước tính tiền tải bằng cách sử dụng các chỉ số thay thế khác nhau. Tiền tải trong môi trường lâm sàng thường được sử dụng đồng bộ với hồi lưu tĩnh mạch, là lưu lượng máu hệ thống trở lại tim phải. Do hệ tuần hoàn cấu thành tuần hoàn phổi và hệ thống, nên hồi lưu tĩnh mạch phải bằng cung lượng tim trong điều kiện ổn định khi lấy trung bình theo thời gian [12]. Cần lưu ý rằng hồi lưu tĩnh mạch không được đo trực tiếp trong thực hành lâm sàng. Nó được mô tả một cách toán học như sau: (áp lực đổ đầy hệ thống trung bình – áp lực nhĩ phải)/kháng lực tĩnh mạch. Nhưng công thức này không mô tả đầy đủ các yếu tố quyết định của sự quay hồi lưu tĩnh mạch bởi vì nó không bao gồm dung lượng tĩnh mạch (venous capacitance), mà ảnh hưởng lớn nhất là áp lực tĩnh mạch trung tâm (CVP) [13].
Mặc dù cung lượng tim và hồi lưu tĩnh mạch là phụ thuộc lẫn nhau, mỗi loại có thể được điều chỉnh độc lập. Nếu tất cả các yếu tố khác là không đổi, mối quan hệ giữa thể tích nhát bóp và đổ đầy tâm trương thất được điều chỉnh bởi cơ chế Frank-Starling trong đó sự gia tăng tiền tải đến tâm thất phải chuyển thành tăng thể tích nhát bóp từ tâm thất trái [14] [15]. Tuy nhiên, khi đã đạt được dung lượng đổ đầy tim, áp lực đổ đầy tâm trương tăng mà không tăng đồng thời thể tích tâm trương thất [16]. Khi sự cân bằng giữa hồi lưu tĩnh mạch và cung lượng tim bị xáo trộn, tình trạng dư thừa tĩnh mạch (venous excess) xảy ra. Khi tim không thể đối phó với sự gia tăng tiền tải, việc ứ máu tĩnh mạch và sau đó phù nề xảy ra [13].
Các biện pháp tĩnh về khả năng đáp ứng dịch của bạn liên quan đến việc sử dụng “ảnh chụp nhanh” các phép đo để ước tính tiền tải và đã được sử dụng rộng rãi trong 5 thập kỷ qua. Các biện pháp tim tĩnh cổ điển là CVP. Các biện pháp tĩnh được nghiên cứu kỹ lưỡng khác bao gồm áp lực động mạch phổi bít, diện tích khu vực cuối tâm trương thất trái, tĩnh mạch chủ dưới (IVC) và thể tích cuối tâm trương toàn cầu.
2.1. Áp lực tĩnh mạch trung tâm (Central venous pressure)
Kể từ khi được mô tả vào năm 1959, việc theo dõi CVP đã được sử dụng thường xuyên để hướng dẫn hồi sức thể tích và được khuyến nghị trong các hướng dẫn Surviving Sepsis Campaign nhiều lần [11,17,18]. Các nghiên cứu hiện đại đã chứng minh CVP là một yếu tố dự đoán không chính xác và không đáng tin cậy về đáp ứng dịch [10,19].
CVP có thể hoán đổi cho nhau với áp lực nhĩ phải (RAP), một đóng góp chính cho tiền tải tâm thất phải. Giả sử đặt tâm thất phải tỷ lệ thuận với thất trái, RAP được coi là sự thay thế của tiền tải tâm thất trái. Do đó, RAP thấp sẽ gợi ý một bệnh nhân nằm trên phần tăng dần của đường cong Frank- Starling, trong khi giá trị cao sẽ cho thấy bệnh nhân nằm trên phần cao nguyên của đường cong này. Giả định này có những hạn chế. Đầu tiên, RAP là thước đo áp lực chứ không phải thể tích, giả sử mối quan hệ áp lực – thể tích tuyến tính. Thứ hai, sự thay đổi về trương lực mạch máu, áp lực trong lồng ngực hoặc chức năng tim ảnh hưởng trực tiếp đến RAP, mà không có sự thay đổi trong tiền tải [19]. Các bệnh nhân có độ dốc khác nhau của các đường cong Frank-Starling, khiến cho việc dự đoán liệu RAP thấp hay cao là mô tả đúng về tiền tải của bệnh nhân.
Trong một tổng quan hệ thống bao gồm 24 nghiên cứu và 803 bệnh nhân, sự khác biệt về CVP cơ bản (8,7 ± 2,32 mm Hg) ở những người đáp ứng so với (9,7 ± 2,2 mm Hg) những người không đáp ứng không có ý nghĩa thống kê (p = 0,3). Các tác giả không tìm thấy mối liên quan giữa CVP cơ bản cũng như ΔCVP và đáp ứng dịch truyền. Hãy ghi nhớ các kết quả của phân tích tổng hợp này, bản thân CVP không phải là một yếu tố dự báo tốt về khả năng đáp ứng tiền tải [6].
2.2. Áp lực động mạch phổi bít (Pulmonary artery occlusion pressure)
Khi được giới thiệu ban đầu, ống thông động mạch phổi (PAC, pulmonary artery catheters) được cho là các biện pháp chính xác của tiền tải tâm thất trái. PAC đo áp lực động mạch phổi bít (PAOP) tương đương với áp lực cuối tâm trương thất trái (LVEDP, left-ventricular end-diastolic pressure) giả định sức cản mạch máu phổi bình thường và không có hẹp van hai lá. Vì đây cũng là một phép đo áp lực, một giả định áp lực – thể tích liền quan tuyến tính, trong thực tế, mối liên hệ này là đường cong.
Cũng như CVP, PAOP cũng chịu vô số biến số gây nhầm lẫn: thay đổi độ giãn nở cơ tim (nhiễm trùng huyết, thiếu máu cơ tim, tiểu đường và lão hóa), quá tải tâm thất phải, bệnh màng ngoài tim và tăng áp lực nội tâm mạc do thông khí áp lực dương có thể ảnh hưởng đến các phép đo [20]. Những yếu tố này gây khó khăn cho việc xác định rằng PAOP là sự mô tả chân thực về tiền tải của bệnh nhân. Ngoài ra, đặt và rút bỏ PAC mang lại những rủi ro nghiêm trọng bao gồm rối loạn nhịp tim, nhồi máu phổi, thắt nút/vướng ống thông và vỡ động mạch phổi (PA) [21].
Osman và cộng sự. đã nghiên cứu mối tương quan giữa đáp ứng dịch truyền và PAOP ở 96 bệnh nhân [22]. PAOP trước truyền dịch có ý nghĩa thấp hơn ở những người đáp ứng so với những người không đáp ứng (10 ± 4 so với 11 ± 4 mm Hg, p < 0,05), nhưng có sự chồng chéo của các giá trị cá nhân giữa các nhóm. AUROC là 0,63 (95% CI, 0,55-0,70) và không lớn hơn về mặt thống kê so với CVP, với sự khác biệt giữa AUROC là 0,053 (95% CI, 0,01-0,12; p = 0,12).
Trong một đánh giá, Michard et al. so sánh PAOP trước và sau truyền dịch tăng thể tích ở người đáp ứng thể tích và người không đáp ứng và lưu ý rằng PAOP không có ý nghĩa thấp hơn ở người đáp ứng trong 7 trên 9 nghiên cứu [10].
Việc áp dụng PAC để theo dõi huyết động thường quy của bệnh nhân bị bệnh nặng đã dần bị loại bỏ do những hạn chế nêu trên và sự sẵn có của các thiết bị theo dõi ít xâm lấn và chính xác hơn.
2.3. Thể tích cuối tâm trương toàn cầu
Thể tích cuối tâm trương toàn cầu (GEDV, global end-diastolic volume) và chỉ số thể tích cuối tâm trương toàn cầu (GEDI, global end-diastolic volume index) là ước tính của tổng lượng máu trong các buồng tim, được đo bằng phương pháp pha loãng nhiệt xuyên phổi (transpulmonary thermodilution method). Có thể sử dụng máy theo dõi PiCCO (Pulsion Medical Systems, Munich, Đức) hoặc EV1000 (Edwards Lifescatics, Irvine CA, USA) để thu thập dữ liệu. Hệ thống PiCCO sử dụng phương pháp pha loãng nhiệt xuyên phổi thông qua một ống thông động mạch và một ống thông tĩnh mạch trung tâm, thông qua đó sử dụng một lượng nhỏ nước muối ấm/lạnh để đo. Nhiều biến số được đo bằng máy theo dõi PiCCO, trong đó GEDV/GEDI đo lượng máu trong các buồng tim, một biện pháp trực tiếp của tiền tải tim. GEDV/GEDI chia sẻ mối quan hệ sinh lý với thể tích nhát bóp, mặc dù có dữ liệu liên quan đến mối quan hệ giữa GEDV và khả năng đáp ứng của nó. Khả năng phát hiện sự thay đổi trong tiền tải bởi GEDV được xác định bởi dung lượng tĩnh mạch và độ giãn nở của buồng tim [10].
Michard và cộng sự đã nghiên cứu 36 bệnh nhân bị bệnh nặng so sánh chỉ số GEDV với chỉ số thể tích nhát bóp (SVI) trước và sau thử thách dịch truyền hoặc tăng tỷ lệ dobutamine [23]. Họ đã tìm thấy một mối tương quan có ý nghĩa thống kê với SVI (r = 0,72, p < 0,001), và cũng tìm thấy chỉ số GEDV trước truyền dịch thấp hơn về đáp ứng thể tích so với người không đáp ứng (637 ± 134 mL/m2 so với 781 ± 161 mL/m2, p < 0,001). Endo et al. đã nghiên cứu khả năng đáp ứng của 93 bệnh nhân thở máy bằng GEDV và thấy GEDV không nhất quán trong việc dự đoán khả năng đáp ứng dịch của bệnh nhân [24]. Sự khan hiếm dữ liệu về GEDV và sự không nhất quán của kết quả [25-28] cần thiết điều tra thêm về tiện ích của GEDV/GEDI như một công cụ để dự đoán khả năng đáp ứng dịch.
2.4. Đường kính tĩnh mạch chủ dưới
Đường kính của tĩnh mạch chủ dưới (IVCd) được giả định là thay đổi khi tiền tải. Về mặt lý thuyết, sự gia tăng của IVCd có nghĩa là sự gia tăng tiền tải và tâm nhĩ phải. IVC được hiển thị bằng cách sử dụng phương pháp siêu âm tại giường trong mặt phẳng dưới sườn như trong Hình 1.
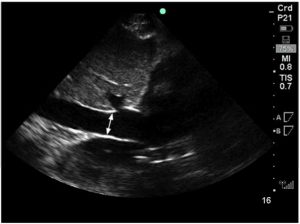
Nó được đo ở khoảng cách từ lổ tâm nhĩ phải trong giai đoạn thở ra [29]. Như với hầu hết các phương pháp siêu âm, độ chính xác của nó phụ thuộc vào người siêu âm và cần phải đào tạo trước. Nhiều yếu tố liên quan đến bệnh nhân như béo phì, tăng căng phồng phổi do bệnh phổi tắc nghẽn, hiện diện tràn khí màng phổi và chướng khí ở bụng có thể khiến cửa sổ siêu âm không đầy đủ khiến phương pháp này không thể sử dụng được.
Đường kính của IVC đã được chứng minh là tương quan với RAP [30, 31]. Điều này cũng chịu những hạn chế tương tự gặp phải với các phép đo RAP bao gồm giả định về mối liên hệ thể tích – áp lực tuyến tính và sự thay đổi áp lực bên trong truyền đến IVC. Hiệp hội Siêu âm Tim Hoa Kỳ hiện khuyến nghị sử dụng cả đường kính IVC và chỉ số TM chủ dưới để ước tính RAP bằng cách sử dụng siêu âm [32]. Chỉ số Caval hoặc biến thiên IVC sẽ được thảo luận riêng như một biện pháp động.
2.5. Khu vực cuối tâm trương thất trái
Khu vực cuối tâm trương thất trái (LVEDA, Left ventricular end-diastolic area) có thể được đo bằng siêu âm tim tại giường hoặc siêu âm qua thực quản (TEE).
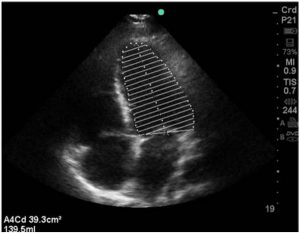
Sử dụng siêu âm tim tại giường, nó được đo ở góc nhìn 4 buồng như hình 2. Về mặt lý thuyết, LVEDA sẽ tăng khi truyền dịch tăng thể tích ở bệnh nhân bị giảm thể tích máu. Feissel et al. đã nghiên cứu LVEDA cuối thì thở ra trước và sau khi truyền dịch tăng thể tích. Họ báo cáo không có mối tương quan đáng kể nào (r2 = 0.11, p = 0,17) giữa chỉ số LVEDA cơ bản và tỷ lệ phần trăm tăng của chỉ số tim để đáp ứng với truyền dịch tăng thể tích [33]. Tavernier et al. trong một nghiên cứu khác đã so sánh hiệu suất của các biến thiên huyết động khác nhau và thấy LVEDA có AUROC thấp hơn so với biến thiên áp lực tâm thu (0.77, 95% CI 0.59–0.92 vs 0.94 95% CI 0.81–0.99) [34].
Như với tất cả các phương pháp siêu âm, cần có năng lực siêu âm và việc thu nhận hình ảnh phụ thuộc vào cửa sổ siêu âm. Nó cũng đòi hỏi sự hiện diện của người siêu âm tại giường khi cần đánh giá lặp lại chức năng huyết động ở bệnh nhân bị bệnh nặng.
3. Các trị số động của đáp ứng tiền tải
Ở những bệnh nhân thở tự nhiên khỏe mạnh, một sự thay đổi nhỏ về huyết áp (< 10 mm Hg) xảy ra do thay đổi áp lực trong lồng ngực trong quá trình hô hấp. Thì hít vào làm cho áp lực trong lồng ngực trở nên âm hơn, làm tăng hồi lưu tĩnh mạch cho tim phải. Tăng đổ đầy tâm thất phải làm tăng thể tích tâm thất phải và làm tăng máu tĩnh mạch phổi quay trở lại tâm thất trái. Sự giãn nở mạch máu phổi đồng thời gây ra sự tích tụ máu tĩnh mạch trong mạch máu phổi làm giảm hồi lưu tĩnh mạch phổi. Trong sự phối hợp, các cơ chế này làm giảm đổ đầy thất trái gây ra sự giảm về thể tích nhát bóp, biểu hiện là giảm huyết áp tâm thu. Một sự khác biệt về áp lực tâm thu >10 mm Hg trong chu kỳ hô hấp, cái gọi là mạch nghịch, có thể xảy ra trong một loạt các quá trình bệnh như tràn dịch màng ngoài tim, viêm màng ngoài tim co thắt, giảm thể tích máu và tắc mạch phổi [35,36].
Một hiện tượng mạch nghịch ngược xảy ra với thông khí áp lực dương. Theo hít vào với thông khí áp lực dương, có sự gia tăng áp lực trong lồng ngực, được truyền đến tâm nhĩ phải, từ đó làm giảm tiền tải. Do đó, một sự thay đổi theo chu kỳ của tiền tải được tạo ra với thông khí áp lực dương [37]. Mức độ giảm tiền tải này càng cao, bệnh nhân càng có nhiều khả năng nằm trên phần tăng dần của đường cong Frank-Starling và do đó sẽ đáp ứng dịch truyền.
Trong thập kỷ qua, các nhà điều tra đã tận dụng các tương tác giữa tim và phổi này để dự đoán khả năng đáp ứng dịch. Các phép đo tim động như biến thiên áp lực xung (PPV, pulse pressure variation), biến thiên áp lực tâm thu (SPV, systolic pressure variation) và biến thiên thể tích nhát bóp (SVV, stroke volume variation) đã được nghiên cứu để dự đoán khả năng đáp ứng của bệnh, và sẽ được thảo luận chi tiết. Tổng số các công thức được sử dụng để tính toán các biến này và các điều kiện cần có được bao gồm trong Bảng 2. Các ngưỡng và độ chính xác của các phép đo động khác nhau được cung cấp trong Bảng 3.
3.1. Biến thiên áp lực xung (PPV)
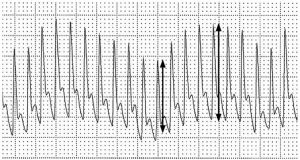
Sự thay đổi áp lực xung là sự khác biệt được tính toán giữa các áp lực xung trong một chu kỳ hô hấp. Áp lực xung là sự khác biệt được tính toán giữa huyết áp tâm thu và huyết áp tâm trương và sự thay đổi của nó có thể được tính bằng cách sử dụng các dạng sóng động mạch được lấy từ đường cong biểu diễn huyết áp động mạch như trong Hình 3 và sử dụng công thức được hiển thị trong Bảng 2. Hầu hết dữ liệu được công bố trên PPV liên quan đến các bệnh nhân thở máy với thể tích khí lưu thông cao mà không có nỗ lực thở tự phát [38-42]. Nếu bệnh nhân thở tự nhiên, ngay cả khi đang hỗ trợ kiểm soát thông khí, họ có thể thay đổi áp lực trong lồng ngực và do đó gây ra phản ứng phóng đại hoặc tù xuống đối với nhịp thở áp lực dương [43]. Monnet và cộng sự chứng minh rằng nếu độ giãn nở của hệ hô hấp là <30 mL/cmH2O, giá trị của PPV để dự đoán khả năng đáp ứng dịch đã giảm đáng kể [44].
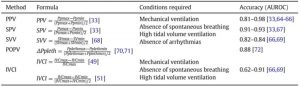
”(PPV = pulse pressure variation; Ppmax = pulse pressure maximum; Ppmin = pulse pressure minimum; SPV = systolic pressure variation; Psmax = systolic pressure maximum; Psmin = systolic pressure minimum; SVV = stroke volume variation; SVmax = stroke volume maximum; SVmin = stroke volume minimum; POPV = pulse-oximetry plethysmographic var- iation; Ppleth = pulse-oximetry plethysmography; Pplethmax = pulse-oximetry plethysmography maximum; Pplethmin = pulse-oximetry plethysmography minimum; IVCI = inferior venacaval index; IVCmax = inferior venacaval maximum diameter; IVCmin = inferior venacaval minimum diameter).”
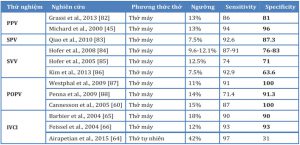
Một phân tích tổng hợp gần đây cho thấy PPV ở bệnh nhân thở máy có kiểm soát với thể tích khí lưu thông > 8 mL/kg là một yếu tố dự báo chính xác về khả năng đáp ứng của bệnh nhân ở bệnh nhân bị bệnh nặng, với độ nhạy 0,88 (KTC 95% = 0,81 đến 0,92), độ đặc hiệu là 0,89 (95% CI = 0,84 đến 0,92) và AUROC là 0,94 (95% CI = 0,91 đến 0,95) [43]. Trên thực tế, các nghiên cứu so sánh PPV với SVV phân tích bằng pulse contour và SPV cho thấy PPV đáng tin cậy hơn [45,46].
Mặc dù độ chính xác và độ tin cậy của nó, nó chỉ giới hạn ở những bệnh nhân thở máy mà không có thở tự nhiên chủ động, với thể tích khí lưu thông cao (> 8 mL/kg). Nó cũng cần truy cập động mạch và không có rối loạn nhịp tim.
Một khái niệm về thách thức thể tích khí lưu thông (TVC, tidal volume challenge) đã được mô tả như là một thao tác mới lạ để khơi gợi khả năng đáp ứng dịch. Thủ thuật này thực hiện bằng cách tăng tạm thời thể tích khí lưu thông từ 6 mL/kg lên 8 mL/kg trong 1 phút và lưu ý những thay đổi trong các phép đo. ΔPPV > 3,5% dự đoán khả năng đáp ứng dịch với độ chính xác cao [47].
Myatra et al. đã mô tả 30 TVC và tắc nghẽn cuối thì thở ra (EEO, end-expiratory occlusion) ở 20 bệnh nhân và ghi lại sự thay đổi PPV (ΔPPV) và SVV (ΔSVV) trước và sau TVC [48]. Họ đã báo cáo AUROC là 0,96 (0,89-1,00, p < 0,001) cho SVV và 0,97 (0,92-1.00, p < 0,001) cho TVC.
3.2. Biến thiên áp lực tâm thu (SPV)
Huyết áp tâm thu dao động với nhịp thở tự nhiên cũng như khi thở máy tương tự như mô tả ở đầu phần này [36]. Sử dụng dạng sóng động mạch, áp lực tâm thu cơ bản được thiết lập sau 7 đến 12 giây tạm dừng thở ra. Biến thiên hô hấp ở trên và dưới đường cơ bản này được đo là delta Up (dUp) và delta Down (dDown) như trong Hình 4 [34]. Tổng của dUp và dDown (chênh lệch giữa áp lực tâm thu tối đa và tối thiểu) được gọi là SPV. Mặc dù thiếu các nghiên cứu lớn xung quanh SPV và đáp ứng dịch truyền nhạy, dDown đã được quan sát là một yếu tố dự báo đáng tin cậy về đáp ứng dịch truyền [34,49]. Tavernier et al. được mô tả bằng SPV trong 35 bước truyền dịch tăng thể tích được thực hiện ở 15 bệnh nhân. Họ báo cáo rằng thành phần dDown >5 mm Hg có PPV là 95% và NPV là 93% [34].
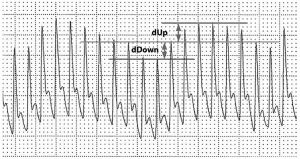
Phương pháp này dựa vào thở máy mà không có thở tự phát chủ động, tương tự như các phương pháp khác dựa vào các hoạt động của tim-phổi. Nó cũng sẽ không đáng tin cậy trong rối loạn nhịp tim do áp lực tâm thu sẽ thay đổi không đáng tin cậy với thời gian kéo dài tâm trương không đều. Nó có lợi thế là không liên quan đến các thiết bị đắt tiền, và nó có thể được sử dụng trong hầu hết các ED và ICU ngày nay.
3.3. Biến thiên thể tích nhát bóp (SVV)
Một phép đo thường được sử dụng dựa trên các tương tác giữa tim và phổi là biến thiên thể tích nhát bóp (SVV) có được nhờ phân tích đường viền xung động mạch (arterial pulse contour analysis). SVV là một hiện tượng xảy ra tự nhiên, trong đó thể tích nhát bóp tăng trong khi hít vào và giảm trong khi thở ra do thay đổi áp lực trong lồng ngực liên quan đến thông khí áp lực dương. Nó được tính toán bằng thiết bị theo dõi huyết động (FloTrac hoặc PiCCO) bằng phân tích đường viền xung. SVV càng lớn, bệnh nhân càng có nhiều khả năng đáp ứng. Theo truyền thống, SVV > 13% đã được coi là ngưỡng cho khả năng đáp ứng dịch [48,50-53]. Một phân tích tổng hợp của Zhang et al. bao gồm 23 nghiên cứu và đưa ra tỷ lệ chênh lệch chẩn đoán là 18,4 cho SVV để dự đoán khả năng đáp ứng của bệnh nhân ở độ nhạy 0,81 và độ đặc hiệu là 0,80 [53].
Có những hạn chế đối với phương pháp này để xác định khả năng đáp ứng. Phương pháp này chỉ được xác nhận ở những bệnh nhân thở máy mà không có hoạt động thở tự nhiên [54]. Hoạt động hô hấp tự phát đặc biệt ở những bệnh nhân bị suy hô hấp tạo ra những thay đổi bất thường về áp lực trong lồng ngực do đó làm cho SVV không chính xác. Bệnh nhân cũng cần có thể tích khí lưu thông cao trong khoảng từ 8 đến 10 mL/kg. Các nghiên cứu đã chỉ ra rằng SVV mất khả năng đoán trước ở mức khí lưu thông thấp hơn [55,56]. Rối loạn nhịp tim là một tình huống khác trong đó SVV là một yếu tố dự báo không đáng tin cậy về đáp ứng thể tích [36,38,50,52].
3.4. CO2 cuối thể tích khí lưu thông
Capnography được sử dụng để đo mức carbon dioxide cuối thể tích khí lưu thông (EtCO2) biểu thị áp lực riêng phần của CO2 khi kết thúc quá trình thở ra. Vì EtCO2 được xác định bởi cả lưu lượng máu phổi (hoặc cung lượng tim) và áp lực riêng phần của CO2 động mạch, nên có thể phát hiện tăng hoặc giảm cung lượng tim không xâm lấn bằng phương pháp capnography. ΔEtCO2 được tính là chênh lệch giữa EtCO2 trước và sau một bolus hoặc một thao tác truyền dịch tăng thể tích mô phỏng.
Chỉ có một số ít các nghiên cứu đã khám phá phương pháp không xâm lấn này để dự đoán khả năng đáp ứng thể tích và hai kỹ thuật khác nhau đã được sử dụng. Trong một nghiên cứu của Toupin và cộng sự, EtCO2 đã được đo trước, trong và sau khi thực hiện động tác nâng chân và so sánh với cung lượng tim bằng phương pháp pha loãng nhiệt ở bệnh nhân phẫu thuật tim có dùng thuốc liệt cơ [57]. Các tác giả lưu ý rằng sự gia tăng EtCO2 ≥ 2 mm Hg bằng thao tác nâng chân có liên quan đến khả năng đáp ứng thể tích (tỷ lệ chênh 7,3; 95% CI 2,7 đến 20,2; p< 0,01; độ nhạy 75%) và có giá trị dự đoán âm tính cao là 86%. Trong một nghiên cứu tương tự, Monnet et al. so sánh biến thiên EtCO2 ở 40 bệnh nhân thở máy, trải qua các động tác nâng chân với đo đạc chỉ số tim (cardiac index) bằng thiết bị PiCCO [58]. Họ báo cáo rằng sự gia tăng EtCO2 5% dự đoán mức tăng CI ≥ 15% khi truyền dịch tăng thể tích với độ nhạy 71% (95% CI 48-89%) và độ đặc hiệu là 100% (95% CI 82-100%) Young và cộng sự. so sánh EtCO2 và EtCO2 đo bằng phương pháp thể tích (volumetric EtCO2) với phản ứng sinh học theo kiểu hơi khác nhau [59]. Bệnh nhân (n = 44) đã trải qua các thao tác nâng chân hoặc truyền dịch tăng thể tích và sự thanh thải EtCO2 trong 5 phút sau khi thực hiện thao tác nâng chân hoặc tăng thể tích. Các tác giả đã báo cáo rằng EtCO2 tăng 5,9 ± 7,6% về đáp ứng thể tích so với 1,4 ± 4,4% ở những người không đáp ứng (p = 0,02) và AUROC là 0,67 (KTC 95% 0,63 -0,89).
Những nghiên cứu này bị giới hạn bởi kích thước mẫu nhỏ và tính nhất quán trong dấu hiệu. Tuy nhiên, phương thức này là một phương thức không xâm lấn đầy hứa hẹn thường được tìm thấy trong các ED và ICU.
3.5. Biến thiên plethysmographic của pulse oximetry
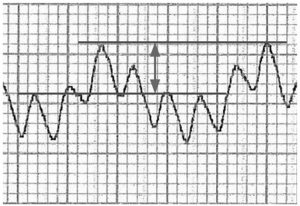
Pulse oximetry được sử dụng phổ biến để theo dõi độ bão hòa oxy của máu động mạch. Nó có sẵn, không xâm lấn và dễ sử dụng, và có thể theo dõi những thay đổi trong thể tích nhát bóp. Dạng sóng pulse oximetry được hiển thị trong Hình 5 gần giống với dạng sóng áp lực động mạch và theo kiểu tương tự như PPV, có thể sử dụng biến thiên dang sóng (plethmysmograph) của máy đo độ bão hòa oxy (pulse oximetry) (POPV, pulse oximetry plethysmographic variation) để dự đoán khả năng đáp ứng của nó. Tương tự như PPV và SVV, biên độ của phép đo POPV sẽ cao nhất trong khi hít vào và thấp nhất khi thở ra ở các các bệnh nhân đang được thông khí cơ học. Sự khác biệt giữa biên độ của plethmysmograph của pulse oximetry được gọi là POPV. Cannesson et al. so sánh PPV với POPV và tìm thấy mối tương quan mạnh mẽ (r² = 0,83; p < 0,001) với một sự đồng thuận tốt [60].
Có một số hạn chế trong việc sử dụng POPV để dự đoán khả năng đáp ứng. Tín hiệu dạng sóng pulse oximetry kém thường gặp ở bệnh nhân nguy kịch. Các tín hiệu plethysmography dựa vào lưu lượng máu đầy đủ, có thể bị ảnh hưởng ở những bệnh nhân có SVR cao hoặc những người đang được truyền thuốc vận mạch. Xử lý tín hiệu đáng kể cũng có thể làm giảm theo tỷ lệ giữa các biến thiên hô hấp trong thể tích nhát bóp và POPV [61].
3.6. Chỉ số Caval
Siêu âm tại giường đã trở nên phổ biến rộng rãi và thường xuyên được dạy cho hầu hết các thực tập sinh cấp cứu và chăm sóc y tế khẩn cấp tại Hoa Kỳ [62,63]. Ước tính tại giường về khả năng đáp ứng thể tích bằng hình ảnh của tĩnh mạch chủ dưới (IVC, inferior vena cava) thường được sử dụng, chủ yếu là do tính dễ sử dụng của nó. IVC cũng chịu sự biến thiên hô hấp gây ra sự dao động trong đường kính của nó. Biến thiên này được gọi là chỉ số caval. IVC được hiển thị bằng siêu âm cửa số vùng dưới sườn (subcostal view) và chế độ M được sử dụng để đo sự thay đổi đường kính IVC này như trong Hình 6. Sự thay đổi phần trăm trong đường kính IVC được gọi là chỉ số caval. Ngưỡng để thiết lập khả năng đáp ứng dịch thay đổi từ nghiên cứu này sang nghiên cứu khác nhưng thường được chấp nhận là 12- 18% ở bệnh nhân thở máy và lên đến 50% ở bệnh nhân thở tự nhiên [64-66].
Phân tích tổng hợp lớn nhất về biến thiên IVC bao gồm 17 nghiên cứu với 533 bệnh nhân và báo cáo AUROC gộp là 0,79, độ nhạy 0,63 và độ đặc hiệu là 0,73 [67]. Các tác giả kết luận rằng biến thiên hô hấp của IVC có khả năng dự đoán vừa phải về khả năng đáp ứng dịch, và xét nghiệm âm tính có thể không loại trừ khả năng đáp ứng. Ngoài ra còn có dữ liệu liên quan đến độ tin cậy của các phép đo IVC ở bệnh nhân thở tự nhiên [8,64,68].
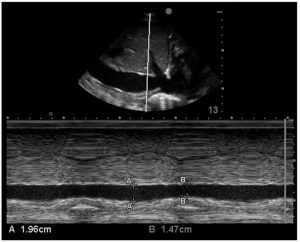
Phương pháp này đòi hỏi đào tạo trước về siêu âm, và nó thực sự được dạy phổ biến ở hầu hết các bệnh viện đại học. Nó dễ bị các cửa sổ siêu âm kém ngăn cản nhìn IVC cũng như lỗi vận hành liên quan đến hình ảnh động mạch chủ liền kề thay vì IVC. Áp lực cuối thì thở ra cao (PEEP), thông khí thể tích khí lưu thông thấp, nỗ lực thở tự nhiên, hen suyễn/COPD gây ra PEEP tự động, rối loạn chức năng thất phải mãn tính, chèn ép tim, tăng áp lực trong ổ bụng và tăng áp lực cục bộ khác ảnh hưởng đến hồi lưu tĩnh mạch qua IVC tất cả làm cho phương pháp này kém chính xác hơn [67,69].
Ở những bệnh nhân thở máy với thể tích khí lưu thông cao và sự ngừng hoạt động của hơi thở tự nhiên, chỉ số caval là một công cụ hữu ích để dự đoán khả năng đáp ứng dịch.
3.7. Đo Doppler động mạch cảnh
Thời gian động mạch cảnh (FTc, carotid flow time) và tích phân thời gian vận tốc (VTI, velocity time integral) là hai phép đo riêng biệt có thể được thực hiện bằng cách sử dụng Doppler sóng xung trên siêu âm. Đây là những kỹ thuật mới xuất phát từ cùng một khái niệm như thời gian động mạch chủ và VTI động mạch chủ (được đo bằng Doppler qua siêu âm thực quản) [70,71], và đang trở nên phổ biến để sử dụng cho bệnh nhân bị bệnh nặng.
Sử dụng Doppler sóng xung trên động mạch cảnh, VTI tính toán lượng máu thông qua động mạch cảnh trong tâm thu. Khi nhân với diện tích mặt cắt ngang của động mạch cảnh, phép tính này ước tính tỷ lệ thể tích nhát bóp mà động mạch cảnh nhận được. Sử dụng một kỹ thuật tương tự, FTc đo tỷ lệ thời gian dành cho hệ thống tim trên mỗi chu kỳ tim như trong Hình 7. Các nghiên cứu tương tự cũng được thực hiện bằng cách sử dụng Doppler động mạch cánh tay mặc dù tài liệu về các phương pháp này khan hiếm với cỡ mẫu nhỏ, chúng đã được sử dụng cùng với các thao tác tải trọng như nâng cao chân thụ động hoặc các thử thách dịch truyền nhỏ.
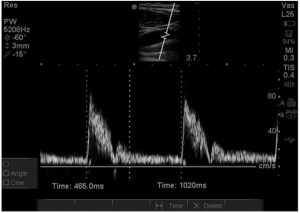
Marik et al. tìm thấy một mối tương quan mạnh mẽ giữa sự thay đổi chỉ số SV (bằng phản ứng sinh học) với sự nâng chân thụ động (PLR) và sự thay đổi đồng thời về carotid VTI (r = 0,59, p = 0,0003) với độ nhạy 94% và độ đặc hiệu là 86 % [72]. Trong một nghiên cứu khác ở những bệnh nhân bị bệnh nặng sử dụng PLR để gợi ra sự thay đổi FTc so với thay đổi SV trên FloTrac, ROC là 0,75 với độ nhạy 60% và độ đặc hiệu là 92% để dự đoán khả năng đáp ứng của bệnh nhân đã được quan sát [73].
Trong một môi trường không có sẵn máy theo dõi nhịp tim, các phép đo động mạch cảnh bằng siêu âm Doppler có thể được sử dụng như là một thay thế cho cung lượng tim hoặc thể tích nhát bóp. Các nghiên cứu lớn hơn áp dụng VTI và thời gian để dự đoán khả năng đáp ứng thể tích là cần thiết để hiểu được tiện ích của chúng trong một thiết lập.
4. Các thủ thuật huyết động học động
Một cách tiếp cận phổ biến để đánh giá khả năng đáp ứng dịch là đo lường sự thay đổi rõ rệt trong thông số huyết động (SV, SVI, CO, CI) bằng thao tác thay đổi tiền tải. Một sự thay đổi trong phép đo huyết động trên một ngưỡng nhất định có nghĩa là bệnh nhân sẽ đáp ứng dịch truyền. Nhiều chỉ số cung lượng tim đã được đánh giá trong việc đánh giá sự thay đổi cảm ứng này trong bao gồm cung lượng tim (CO, cardiac output) đo bằng phương pháp Vigileo/FloTrac, PiCCO và bioreactance [74-78]. Các phép đo Doppler siêu âm cũng đã được nghiên cứu bao gồm cả thời gian động mạch cảnh [79].
4.1. Nâng cao chân thụ động (PLR)
Nâng cao chân thụ động (PRL, passive leg raise) là một động tác huy động lượng máu từ phần dưới cơ thể vào các buồng tim. Sự gia tăng tiền tải này được coi là sự gia tăng cung lượng tim. Khả năng đáp ứng của dịch truyền có thể được xác định mà không cần truyền dịch [80]. Nó có thể được sử dụng ở những bệnh nhân thở tự nhiên, rối loạn nhịp tim và không được đặt nội khí quản [78,81].
Bệnh nhân được đặt nửa nằm ngửa tại giường ở 45°. Sau khi ghi lại các phép đo cơ bản, đầu giường được hạ xuống và chân được nâng lên 45° trong 2 phút. Tốt nhất là sử dụng giường để thay đổi vị trí vì kích thích bằng tay có thể làm tăng trương lực giao cảm dẫn đến đọc sai. Nâng chân thụ động đã được nghiên cứu và tương quan với việc tăng thể tích gây ra tăng cung lượng tim [75]. Trong một phân tích tổng hợp của Monnet và cộng sự, AUROC gộp 0,95 ± 0,01 đã được báo cáo với độ nhạy 0,85 (0,81-0,88) và độ đặc hiệu là 0,91 (0,88-0,93). Hầu hết các nghiên cứu loại trừ bệnh nhân bị đoạn chi do giảm thể tích máu và gãy xương chi dưới cấp tính do nguy cơ chấn thương nặng hơn.
Mặc dù đây là một phương pháp đầy hứa hẹn để đánh giá khả năng đáp ứng và có thể được áp dụng cho hầu hết tất cả các bệnh nhân bị bệnh nặng, không được thở máy, nỗ lực thở tự nhiên hoặc rối loạn nhịp tim, vẫn có một số hạn chế. Những thao tác này không thể được thực hiện chính xác khi giường bệnh không được trang bị khả năng nâng cao chân. Họ cũng có thể không áp dụng cho bệnh nhân chấn thương và những người nằm sấp.
Vì phương pháp này đạt được độ nhạy, độ đặc hiệu và AUROC cao, nên tài liệu hỗ trợ phương pháp này xác định mức độ đáp ứng thể tích. Tuy nhiên, có thể không thực tế khi được sử dụng thường xuyên trong môi trường chăm sóc quan trọng do thời gian thực hiện nhiều phép đo, không có giường cơ có khả năng thực hiện nâng chân và dân số bệnh nhân mà các thao tác này bị chống chỉ định (bệnh nhân chấn thương, đoạn chi chi dưới và bệnh nhân nằm sấp).
4.2. Thử nghiệm tắc nghẽn cuối thì thở ra
Ở những bệnh nhân thở máy, tình trạng tiền tải tim bên trái tăng lên theo hít vào do tăng áp lực trong lồng ngực. Về mặt lý thuyết, EEO (End- expiratory occlusion test) ngăn chặn sự giảm tải này do hít vào gây ra và hoạt động như một thách thức dịch. Thao tác này được thực hiện thông qua việc giữ ngưng thì thở ra trong 15 giây đối với bệnh nhân thở máy. Monnet và cộng sự. nghiên cứu 34 bệnh nhân và so sánh EEO, PLR và thử thách 500 ml [78]. Họ đã báo cáo sự gia tăng áp lực xung động mạch 5% trong EEO dự đoán đáp ứng dịch truyền với độ nhạy 87% (95% CI, 66-97%) và độ đặc hiệu là 100% (95% CI , 71% – 100%).
Đây lại là một thao tác không giới hạn ở những bệnh nhân không bị rối loạn nhịp tim, nhưng đòi hỏi bệnh nhân phải thở máy. Việc ngưng thở ra trong 15 giây sẽ chỉ thực tế ở những bệnh nhân bị an thần sâu hoặc dùng thuốc liệt cơ.
4.3. Thử thách dịch nhỏ (Mini fluid challenge)
Phương pháp này liên quan đến việc truyền nhanh một lượng nhỏ dịch với ước tính cung lượng tim trước và sau. Vì huyết áp phụ thuộc vào cả cung lượng tim và độ đàn hồi, nên thao tác này không thể được thực hiện bằng cách chỉ đo một sự thay đổi của huyết áp. Việc sử dụng máy theo dõi nhịp tim (phân tích đường viền xung, phản ứng sinh học, pha loãng nhiệt xuyên phổi) là cần thiết để đo lường sự thay đổi của cung lượng tim hoặc thể tích nhát bóp. Lần đầu tiên được mô tả bởi Muller et al. với truyền dung dịch keo 100 ml trong hơn 1 phút và cung lượng tim được ước tính bằng tích phân tích thời gian vận tốc ở đường ra động mạch chủ, trước và sau [56]. Ở những bệnh nhân an thần sâu khi thở máy mà không bị rối loạn nhịp tim, phương pháp này có độ chính xác tuyệt vời (AUROC = 0,92, KTC 95%: 0,78, 0,98, r = 0,81, p < 0,0001). Tích phân thời gian vận tốc được giải thích trước đây trong phần đo Doppler động mạch cảnh. Các nghiên cứu này nhấn mạnh tầm quan trọng của việc giảm thiểu thể tích tải để xác định mức độ đáp ứng của PLR, EOO và TVC đều liên quan đến cùng một nguyên tắc mà không cần sử dụng bất kỳ dịch ngoại sinh nào. Khi các phương pháp khác không thể được sử dụng, một thể tích nhỏ có thể được sử dụng với sự chú ý chặt chẽ đến các chỉ số tưới máu để xem tình trạng giảm tưới máu của bệnh nhân có cải thiện không.
5. Kết luận
Trong quá trình hồi sức sốc, điều cần thiết là xác định sự đáp ứng dịch để ngăn chặn truyền dịch không cần thiết và các rủi ro liên quan. Các phép đo tĩnh không phải là yếu tố đáng tin cậy của khả năng đáp ứng dịch, trong khi các phép đo động và thủ thuật có vẻ hữu dụng hơn. Hầu hết các phương pháp có sẵn đòi hỏi phải có các điều kiện tiên quyết, thông khí cơ học với thể tích khí lưu thông cao hơn là phổ biến nhất, nhưng ít có phương pháp đáng tin cậy hơn cho bệnh nhân thở tự nhiên. Trong số các phương pháp được xem xét, nâng cao chân thụ động kết hợp với theo dõi cung lượng tim xâm lấn tối thiểu có ít điều kiện tiên quyết nhất và có thể được sử dụng ở nhiều bệnh nhân nguy kịch.
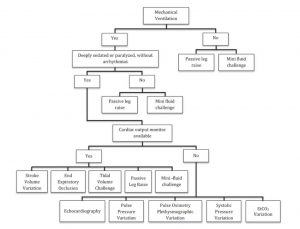
Điều quan trọng cần lưu ý là khả năng đáp ứng dịch chỉ là một đánh giá về vị trí của bệnh nhân trên đường cong Frank-Starling. Việc tích hợp đánh giá khả năng đáp ứng dịch với các thông số đánh giá tình trạng quá tải là rất quan trọng. Chúng bao gồm khám lâm sàng, cân bằng dịch, cân nặng và siêu âm phổi rất quan trọng. Siêu âm đang được sử dụng ngày càng nhiều và khả năng dự đoán đáp ứng tiền tải của nó rất hứa hẹn và là chủ đề của các nghiên cứu đang diễn ra.
Chúng tôi thừa nhận rằng hầu hết các nghiên cứu đánh giá đáp ứng dịch là những nghiên cứu trung tâm nhỏ, đơn lẻ thiếu đánh giá về khả năng tái thực hiện. Không rõ các phép đo động nào là vượt trội và không thể kết luận thứ tự ưu tiên nào. Chúng tôi đề xuất một cách tiếp cận cá nhân để tích hợp các phương thức khác nhau để đánh giá khả năng đáp ứng và hướng dẫn hồi sức ở bệnh nhân bị bệnh nặng, như trong Hình 8. Ở tại giường, các bác sĩ lâm sàng nên biết về những cạm bẫy và giới hạn của các phương thức có sẵn xác định đáp ứng dịch.