Tác giả: Bác sĩ Đặng Thanh Tuấn
Tóm tắt
Những bệnh nhân nặng có suy hô hấp cấp nằm khoa Cấp cứu (ED) khi chờ đợi giường nằm trong phòng chăm sóc đặc biệt (ICU). Các bác sĩ cấp cứu thường được gọi để cài đặt máy thở ban đầu, khắc phục sự cố báo động mày thở, và đánh giá và điều trị bệnh nhân bị mất bù. Vấn đề này xem xét các khái niệm cơ bản về độ giãn nở hệ thống hô hấp, sức đề kháng đường thở, và các rối loạn trao đổi khí. Các bước để đánh giá và xử lý các áp lực cao, sự trao đổi khí xấu đi hơn, và căng phổi động được phác thảo. Các phương pháp xác định kháng lực đường thở và auto-PEEP được hướng dẫn. Cơ sở bằng chứng về thông khí bảo vệ phổi và các liệu pháp cứu hộ được xem xét lại. Mặc dù có nhiều phương pháp cứu hộ và phương thức thông khí, chỉ có thông khí bảo vệ phổi với thể tích khí lưu thông thấp đã được chứng minh cải thiện khả năng sống sót do suy hô hấp cấp. Các kỹ thuật xử trí thông khí, bao gồm thông khí bảo vệ phổi cho hội chứng suy hô hấp cấp và điều trị căng phổi động ở bệnh nhân bị bệnh phổi tắc nghẽn, được thảo luận.
MỞ ĐẦU
Quản lý đường thở thường được coi là kỹ năng quan trọng nhất mà một bác sĩ cấp cứu cần phải có. Các bác sĩ cấp cứu thường được yêu cầu đặt nội khí quản cho những bệnh nhân nặng nhất trong khoa cấp cứu (ED), và đôi khi ở trong bệnh viện. Nhiều bác sĩ cấp cứu đã đi tiên phong trong việc sử dụng các công cụ và kỹ thuật mới để đảm bảo đường thở trong các tình huống lâm sàng khác nhau, nhưng việc quản lý thông khí thường là vấn đề quan trọng thứ hai sau việc quản lý đường thở trong ED. Các cài đặt thông khí ban đầu thường được hoãn lại cho chuyên viên trị liệu hô hấp, với sự quản lý tiếp theo do đội chăm sóc tích cực (ICU) thực hiện. Lý tưởng nhất là bác sĩ cấp cứu sẽ đảm bảo đường thở và thực hiện việc hồi sức ban đầu, và sau đó bệnh nhân sẽ được đưa đến ICU để tiếp tục điều trị. Tuy nhiên, thường thì các bệnh nhân bị bệnh nặng sẽ nằm ED hàng giờ, thậm chí cả ngày. Trong khi đội ICU có thể sắp xếp cho nhập khoa, bác sĩ cấp cứu là bác sĩ điều trị thay cho các chuyên viên trị liệu về hô hấp khi có vấn đề về hô hấp xảy ra trong ED. Xử lý sự cố của máy thở có thể là khác biệt, vì vậy cần phải hiểu những vấn đề thường gặp mà bệnh nhân đặt nội khí quản phải đối mặt và cách điều chỉnh máy thở phù hợp.
Những khuyến cáo trong tổng quan này áp dụng cho các bệnh nhân trong ED với suy hô hấp cấp cần thông khí cơ học. Các chế độ thông khí thông thường sẽ được thảo luận. Chúng bao gồm hệ thống thông khí hỗ trợ – kiểm soát thể tích (VCV), nơi bác sĩ điều chỉnh thể tích khí lưu thông và thông khí hỗ trợ – kiểm soát áp lực (PCV), nơi bác sĩ cải đặt áp lực hít vào. Cần lưu ý rằng VCV và PCV là những thuật ngữ chung, và các nhà sản xuất các máy thở khác nhau đều có chế độ “thương hiệu” riêng. Dräger CMV, Puritan BennettTM VC+, và Maquet PRVC đều là các chế độ VCV cho những thương hiệu đó. Trong bài này, tên chung sẽ được sử dụng. Ngoài ra, trong khi các bài trình bày trong trường hợp mô tả bệnh nhân người lớn, các khái niệm cũng có liên quan đến bệnh nhân nhi đang được thông khí trong ED.
BỆNH NGUYÊN VÀ SINH LÝ BỆNH
Độ giãn nở hệ thống hô hấp
Hiểu được độ giãn nở của hệ thống hô hấp là cần thiết để khắc phục sự thông khí cơ học. Nhớ lại rằng độ giãn nở là sự thay đổi thể tích (ΔV) chia cho sự thay đổi áp lực (ΔP):
C = ΔV / ΔP
Đối với hệ hô hấp, ΔV là thể tích khí lưu thông được tạo ra bằng cách sử dụng thông khí áp lực dương. ΔP là áp lực cần thiết để đạt được thể tích khí lưu thông đó. Độ giãn nở hô hấp bình thường khoảng 100 mL/cm H2O. Trong quá trình thông khí cơ học, độ giãn nở có thể được tính bằng cách chia thể tích khí lưu thông cho hiệu số giữa áp lực đường thở cao điểm (PAP, peak airway pressure) và PEEP. Do đó, nếu một bệnh nhân đang thở máy với thể tích khí lưu thông là 450 mL, PAP 25 cm H2O, và PEEP 10 cm H2O, độ giãn nở là 30 mL/cm H2O.
C = thể tích khí lưu thông / (PAP-PEEP) ⇒ C = 450 / (25-10) = 450/15 = 30
Các bệnh về phổi và thành ngực có thể ảnh hưởng đến độ giãn nở. Các yếu tố làm giảm độ giãn nở của phổi bao gồm đặt ống nội khí quản vào phế quản gốc, tắc nghẽn NKQ, viêm phổi, co thắt phế quản, phù phổi, hội chứng suy hô hấp cấp (ARDS) và xơ hóa phổi. (Xem Bảng 1). Các rối loạn giảm độ giãn nở của thành ngực và giới hạn sự nâng lên của lồng ngực khi hít vào bao gồm chứng béo phì, bỏng quanh ngực, và hội chứng tăng áp lực ổ bụng. Trong VCV, khi bác sĩ đặt một thể tích khí lưu thông, việc độ giãn nở ngày càng tồi tệ sẽ làm PAP cao hơn. Trong PCV, khi bác sĩ đặt áp lực hít vào, độ giãn nở nặng hơn sẽ làm giảm thể tích khí lưu thông và giảm thông khí phút. Nói chung, độ giãn nở ngày càng tồi tệ có nghĩa là tình trạng bệnh nhân ngày càng tồi tệ.

Sức cản đường thở
Các câu hỏi đầu tiên các bác sĩ cấp cứu nên hỏi là, “là vấn đề của đường thở, hoặc tại phổi?” Điều này có thể được trả lời bằng cách ước tính mức độ sức cản đường thở. Khi máy thở vận hành trong VCV, nó sẽ cung cấp áp lực dương cho đến khi đạt được thể tích khí lưu thông mục tiêu. Lượng áp lực cần thiết cung cấp nhịp thở lần lượt giảm dần qua ống NKQ, khí quản, đường dẫn khí lớn, tiểu phế quản, và phế nang được ghi nhận là PAP. Nếu bác sĩ ấn một nút giữ vào cuối thì hít vào (giống như để giữ hơi thở của bạn) thì lưu lượng sẽ dừng lại. Điều này gây ra cân bằng áp lực trong hệ thống, có nghĩa là áp lực trong phế nang bằng áp lực trong đường thở lớn và trong ống NKQ. Áp lực này, được ghi lại vào cuối đoạn hít vào khoảng từ 0,5 đến 1 giây, được gọi là PPLAT.
PPLAT đại diện cho áp lực (và do đó là độ giãn nở) của phổi trong thời gian hít vào. Khi PPLAT tăng lên, độ giãn nở của phổi giảm. Giảm độ giãn nở của ngực cũng sẽ làm tăng PPLAT. Hãy suy nghĩ về nó như là một chất kết dính làm hạn chế khả năng căng phồng lên của phổi trong thì hít vào. PAP đại diện cho cả độ giãn nở của phổi và sức cản của đường thở (bao gồm cả ống NKQ). Sự khác biệt giữa PAP và PPLAT thường là < 5 cm H2O. Sự gia tăng đáng kể trong PAP mà không tăng PPLAT là tăng sức cản đường thở và không nhất thiết là có vấn đề với phổi hoặc thành ngực. Điều này được thấy trong bệnh hen suyễn, bệnh phổi tắc nghẽn mãn tính (COPD), nút nhầy trong khí phế quản, và nghẹt ống NKQ.
Sự gián đoạn trong trao đổi khí thông thường
Thông khí cơ học thường sẽ cải thiện việc trao đổi khí, nhưng thỉnh thoảng những vấn đề vẫn còn tồn tại sau khi đặt ống NKQ đòi hỏi sự điều chỉnh của máy thở. Hai cơ chế chính để gây ra sự gián đoạn đáng kể trong trao đổi khí (ngay cả sau khi bắt đầu thông khí áp lực dương) là shunt và thông khí khoảng chết.
Shunt rất dễ hình dung: máu chảy từ phía bên phải tim sang bên trái tim thông qua các khu vực không thông khí. Một shunt có thể là trong tim (bệnh tim bẩm sinh có shunt phải- trái), hầu hết đó là shunt trong phổi. Shunt trong phổi là do ngăn cản khí hít vào đến các phế nang. Các ví dụ bao gồm atelectasis, ARDS, phù phổi, và đông đặc phổi trong viêm phổi. Với tỷ lệ shunt 50%, ngay cả việc sử dụng oxy 100% sẽ không làm tăng PaO2 đến > 60 mmHg. [3] Do đó, điều trị suy hô hấp giảm oxy máu do shunt đòi hỏi phải có thông khí áp lực dương để huy động và ổn định các đơn vị phổi bị xẹp. Điều này được thực hiện bằng cách sử dụng PEEP. Theo một nguyên tắc chung, việc khống chế các phần đông đặc trong phổi của bệnh nhân càng nhiều, PEEP càng cần nhiều hơn.
Các phương pháp xác định lượng PEEP tối ưu được thảo luận rộng rãi. Các nghiên cứu do nhóm nghiên cứu ARDSNet thực hiện dựa trên yêu cầu FiO2 (xem Bảng 2), với việc chuẩn độ FiO2 và PEEP để duy trì độ bão hòa oxy (SpO2) từ 88% đến 95%. [4,5] Một số nhà nghiên cứu đã chứng minh rằng việc đo điểm uốn thấp (LIP, lower inflection point) trên đường cong áp lực-thể tích có thể được sử dụng để cài đặt PEEP ban đầu. [6,7,8] LIP là điểm mà tại đó các phế nang được huy động và độ giãn nở phổi cải thiện. (Xem Hình 1) Một số máy thở thương mại có thể đo đường cong áp lực – thể tích trong một khoảng thời gian lưu lượng hằng định. Việc thiết lập PEEP ở ngay hoặc phía trên LIP có thể ngăn ngừa sự xẹp phổi và tái xẹp phổi. [9] Một tổng quan hệ thống gần đây về việc sử dụng đường cong áp lực – thể tích để cài đặt PEEP gợi ý rằng mặc dù có thể có mối liên quan giữa phương pháp này và sự cải thiện sống còn của ARDS, chỉ có 3 thử nghiệm ngẫu nhiên đã nghiên cứu điều này, và cần thêm nhiều bằng chứng. [10] Các nghiên cứu khác đã đề xuất sử dụng cách chuẩn độ PEEP giảm dần, nơi PEEP ban đầu được đặt ở 20 cm H2O và sau đó giảm đi 2 cm mỗi 20 phút. PEEP tối ưu là mức thấp nhất mà ở đó duy trì tốt tình trạng oxy hóa. [11] Một chuẩn độ PEEP giảm dần sẽ tốn thời gian và cần nhân lực, tuy nhiên, và có thể không thực tế trong ED. Sử dụng bảng PEEP-FiO2 hoặc đường cong áp lực-thể tích có thể là một phương pháp thuận tiện hơn.
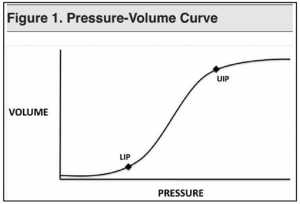
Thông khí khoảng chết là sự đối nghịch của shunt. Mô hình thông khí khoảng chết được mô tả tốt nhất trong thời gian ngừng tim (không ép ngực) – các phế nang thông khí, nhưng không có tưới máu. Thông khí khoảng chết gặp trong với thuyên tắc phổi, thuyên tắc khí tĩnh mạch, và trong giai đoạn cung lượng tim rất thấp. Nó cũng có thể gặp với sự căng quá mức của phế nang (overdistention) trong quá trình thông khí áp lực dương và căng phế nang động (dynamic hyperinflation) ở bệnh nhân COPD. Sự bất thường khi trao đổi khí trong thông khí khoảng chết là cả thiếu oxy máu và tăng CO2 máu. Carbon dioxide không được làm sạch vì máu tĩnh mạch không tiếp xúc với phế nang.

Thông khí bảo vệ phổi
Về mặt lịch sử, thông khí cơ học nhằm khôi phục lại sự trao đổi khí thông thường. Tuy nhiên, trong 15 – 20 năm qua, một số nghiên cứu đang phát triển đã giúp chuyển mục tiêu từ việc điều chỉnh giảm oxy máu và tăng CO2 máu sang mục tiêu tránh tình trạng tổn thương phổi do thở máy gây ra. [4,10] Trong số đó có một nghiên cứu cổ điển từ nghiên cứu nhóm nghiên cứu ARDSNet kiểm tra việc sử dụng thông khí thể tích khí lưu thông thấp ARDS. [5] Trong nghiên cứu này, những người được thông khí sử dụng thể tích khí lưu thông 6 mL/kg trọng lượng cơ thể dự đoán (PBW) có tỉ lệ sống sót cao hơn rõ rệt khi so sánh với những bệnh nhân nhận được 12 mL/kg PBW. Giảm tỷ lệ tử vong tuyệt đối là 8,8%, mặc dù nhóm thể tích khí lưu thông thấp cũng có oxy hóa tồi tệ hơn có ý nghĩa thống kê. Các nghiên cứu tiếp theo đã xác nhận các kết quả này. [13,14] Hệ thống thông khí gọi là thể tích khí lưu thông thấp là một sự nhầm lẫn. Thể tích khí lưu thông sinh lý bình thường đối với người khỏe mạnh là 5 đến 7 mL/kg PBW. Nó chỉ được coi là thấp khi nó được so sánh với thể tích khí lưu thông sử dụng trong quá khứ, trong khoảng từ 10 đến 15 mL/kg và được giữ ở mức cao hơn để tránh sự xẹp phổi và bình thường hóa trao đổi khí. [15] Một thuật ngữ tốt hơn sẽ là hệ thống thông khí khí lưu thông bình thường. Thể tích khí lưu thông cao bất thường khi bắt đầu thở máy đã liên quan đến sự phát triển thương tích phổi cấp tính, thậm chí ở những bệnh nhân không bị tổn thương phổi tại thời điểm đặt nội khí quản. [16,17]
PEEP được sử dụng để mở các phế nang sụp đổ và giữ chúng mở trong khi thông khí cơ học. Lợi ích là hai lần: đầu tiên, bằng cách tuyển dụng các phế nang sụp đổ, shunt fraction được giảm và giảm oxy máu sẽ cải thiện. Thứ hai, phòng ngừa việc mở và đóng các phế nang lặp đi lặp lại trong quá trình thông khí giảm thiểu sự căng thẳng trên các phế nang. [18] Tránh atelectrauma được coi là một phần quan trọng trong việc làm giảm tổn thương phổi do thở máy gây ra. [19]
CÁC CÔNG CỤ VÀ KỸ THUẬT KHẮC PHỤC SỰ CỐ CỦA MÁY THỞ
Sự suy giảm tình trạng hô hấp của bệnh nhân thở máy thường sẽ được chú ý bởi các báo động trên máy thở. Đối với VCV, một chế độ thông thường được sử dụng ở Hoa Kỳ, báo động áp lực cao sẽ thường báo động. Đối với PCV, âm báo động thường gặp là thể tích khí lưu thông thấp hoặc báo động về thông khí phút thấp. Vì hầu hết các ED và ICU sử dụng VCV, bài đánh giá này sẽ tập trung vào báo động áp lực cao (mặc dù các bước để khắc phục sự cố là giống hệt nhau nếu PCV đang được sử dụng).
Có 4 kỹ năng tại giường mà bác sĩ cấp cứu có thể thực hiện trên máy thở. Mỗi thương hiệu của máy thở khác nhau một chút, và điều quan trọng là phải học những điều này trên các máy trong mỗi ED.
Đo áp lực phế nang (áp lực bình nguyên) – plateau pressure
Trong khi máy thở đang cung cấp nhịp thở, nhấn và giữ nút “inspiratory hold” trên máy trong thời gian từ 0.5 đến 1.0 giây. (Xem hình 2.) Sóng áp lực ban đầu sẽ giảm và sau đó dạng sóng sẽ trở thành nằm ngang. Áp lực tại thời điểm này được gọi là PPLAT, và nó phản ánh sự cân bằng của áp lực đường thở trong một khoảng thời gian không có lưu lượng không khí ở cuối của thì hít vào. Do sự cân bằng này, áp lực trong NKQ bằng với áp lực trong phế nang. Nhả nút. Hầu hết các máy thở hiện đại sẽ hiển thị PPLAT trên màn hình. Một PPLAT > 30 cm H2O được cho là có khả năng gây tổn thương cho phổi, mặc dù không xác định được ngưỡng an toàn cho áp lực này. [5,12-14]
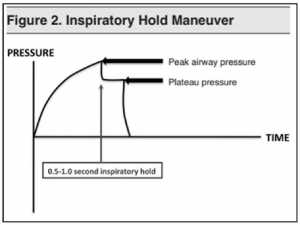
Xác định sức cản đường thở (airway resistance)
Thực hiện việc ngưng thì hít vào, như mô tả ở trên. Xem dạng sóng áp lực trên máy thở, và ghi cả PAP và PPLAT. Một sự chênh lệch lớn (> 5 cm H2O) giữa PAP và PPLAT cho thấy sự gia tăng sức cản đường thở. (Xem trong hình 3.) Điều này có thể xảy ra ở co thắt phế quản (như hen), đường thở dẫn khí lớn hơn (như trong tắc nút nhày), hoặc trong ống NKQ (quá hẹp, gập ống, hoặc tắc nghẽn).
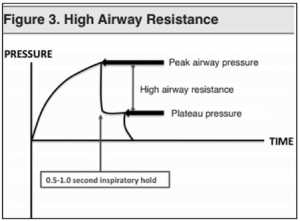
Xác định căng phổi động (dynamic hyperinflation)
Thông thường, khi thở ra, luồng khí ra khỏi phổi đạt đến đường cơ bản, hoặc bằng không. Trong các bệnh như COPD và hen suyễn, bệnh nhân có thể không thể thở ra hoàn toàn trước khi máy thở cung cấp nhịp thở kế tiếp. Làm trống không khí trong phế nang không đủ để dẫn đến sự căng phổi động (còn gọi là autoPEEP hoặc breath stacking). Sự căng phổi động có thể gây ra một số hậu quả:
(1) kích hoạt máy thở do bệnh nhân trở nên khó khăn hơn, có thể làm tăng sự không đồng bộ của bệnh nhân – máy thở;
(2) thông khí khoảng chết tăng lên, dẫn đến tình trạng tăng CO2 và giảm ôxy máu xấu đi; và
(3) áp lực phế nang tăng có thể cao đến mức mà hồi lưu tĩnh mạch trở về tim bị ảnh hưởng.
Điều này dẫn đến hạ huyết áp và thậm chí là suy tuần hoàn. Trên dạng sóng thời gian, hãy đảm bảo rằng lưu lượng thở ra sẽ quay trở lại đường cơ bản vào cuối mỗi nhịp thở. Nếu không, có một số mức độ tắc nghẽn của khí thở ra (xem Hình 4) Giảm tần số hô hấp, và do đó cho phép thở ra có nhiều thời gian hơn, là cách dễ nhất để giải quyết vấn đề. Các giải pháp khác bao gồm rút ngắn thời gian hít vào hoặc gia tăng lưu lượng đỉnh khí hít vào. Điều này cũng sẽ cho phép nhiều thời gian hơn trong giai đoạn thở ra.
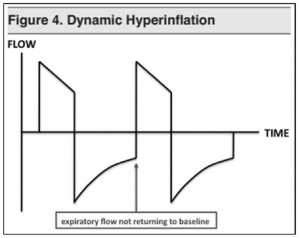
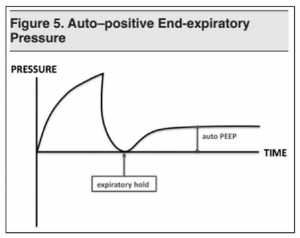
Đo lường mức độ căng phổi động – Đo auto-PEEP
Nếu nghi ngờ căng phổi động, số lượng của autoPEEP có thể được đo bằng cách sử dụng thủ thuật giữ cuối kỳ thở ra. Điều này rất giống với giữ thì hít vào dùng để đo PPLAT. Nhấn và giữ nút “expiratory hold” ở cuối khi thở ra. (Xem Hình 5) Dòng sẽ dừng lại, cho phép áp lực phế nang và áp lực đường thở cân bằng. Nhả nút sau từ 0.5 đến 1.0 giây. PEEP tổng được hiển thị trên máy thở là áp lực phế nang tại thời điểm thở ra. Trừ PEEP được cài đặt (PEEP mà bác sĩ cấp cứu đặt trên máy thở) để tính toán autoPEEP của bệnh nhân.
THỰC TẾ LÂM SÀNG TẠI KHOA CẤP CỨU
Xác định sự ổn định
Ổn định bệnh nhân bị suy hô hấp cấp tính trong ED nên tập trung vào 2 câu hỏi:
(1) Liệu việc trao đổi khí có đáp ứng nhu cầu trao đổi chất của bệnh nhân không? và
(2) Máy thở có được điều chỉnh theo cách để ngăn ngừa thương tích hoặc mất bù lại không?
Đối với trao đổi khí, các bác sĩ cấp cứu nên ghi nhớ rằng oxy hóa là ưu tiên một. PaO2 bình thường là 90 đến 100 mm Hg trong khi thở không khí trong phòng, với SaO2 từ 98% đến 100%. Tuy nhiên, ở những bệnh nhân nặng, có thể chấp nhận được trong hầu hết các trường hợp để duy trì PaO2 từ 55 đến 80 mmHg và một SpO2 từ 88% đến 95%. [5,13] Đã xác định rằng thở oxy 100% có thể gây ra chứng viêm khí phế quản cấp. [20] Chưa thấy rõ ràng rằng nồng độ oxy hít vào cao hơn có liên quan đến kết cục lâm sàng tồi tệ hơn, tuy nhiên vẫn có khả năng xảy ra các tác dụng bất lợi. [21] Nghiên cứu đoàn hệ đa trung tâm của bệnh nhân hồi sức vì ngừng tim thấy rằng PaO2 ban đầu> 300 mmHg đã được kết hợp độc lập với tỷ lệ tử vong trong bệnh viện cao hơn. [22] Dường như thận trọng khi điều trị oxy như bất kỳ loại thuốc nào khác và chỉ sử dụng nồng độ cần thiết để đáp ứng nhu cầu của bệnh nhân.
Thông khí nên được tập trung vào việc duy trì độ pH ít nhất là 7,15. Thông thường, tần số trên máy thở có thể được điều chỉnh an toàn để giữ cho PaCO2 trong phạm vi bình thường từ 35 đến 45 mm Hg và độ pH trong khoảng 7,35 đến 7,45. Trong trường hợp nhất định, tuy nhiên, không thể có được sự thanh thải CO2 bình thường. Ví dụ, ở trạng thái hen, mức tần số thở cao hơn có thể dẫn đến căng phổi động nhiều hơn, và thể tích khí lưu thông cao có thể gây căng phế nang quá mức và dẫn đến tổn thương phổi. [23] Trong nhiều trường hợp, tốt hơn là chấp nhận một mức độ nhiễm toan hô hấp hơn là có nguy cơ bị tổn thương thêm cho phổi bệnh nhân. Tuy nhiên, tăng CO2 máu có thể làm tăng áp lực nội sọ, và nên tránh nhiễm toan hô hấp ở bệnh nhân chấn thương sọ não, chảy máu trong sọ, hoặc các điều kiện khác liên quan đến tăng áp lực nội sọ. Kiềm hóa máu nhanh (pH > 7.60) cũng có thể có tác dụng phụ. Sự co thắt động mạch não và cơ tim có thể xảy ra. Ngoài ra, alkalemia có thể dẫn đến hạ canxi ion hóa, co giật, tetany, và rối loạn tri giác. [24] Kiềm hô hấp cũng nên tránh.
Lấy khí máu động mạch sau khi cài đặt máy thở ban đầu được áp dụng, và sau khi có bất kỳ thay đổi lớn trong cài đặt là biện pháp thận trọng. Theo dõi tim liên tục và đo SpO2 cũng được khuyến cáo cho tất cả các bệnh nhân thông khí trong ED. Theo dõi CO2 liên tục (capnography), mặc dù không phổ biến, rất hữu ích trong việc theo dõi vị trí NKQ thích hợp và trong việc thông khí sau đó. PetCO2 không tương quan chính xác với PaCO2, nhưng những thay đổi có ý nghĩa ở PetCO2 nhắc nhở bác sĩ cấp cứu đánh giá lại bệnh nhân. Cuộc thảo luận chuyên sâu về việc sử dụng biểu đồ dạng sóng capnography nằm ngoài phạm vi của tổng quan này, nhưng các độc giả quan tâm được đề nghị xem xét lại tuyệt vời bởi Kodali, [25] hoặc tham khảo Bài tập về Thực hành Y khoa Cấp cứu Nhi khoa có tiêu đề “Capnography In The Emergency Emergency Department: Ứng dụng lâm sàng”, có tại www.ebmedicine.net/capnography.
Xác định và xử trí diễn tiến xấu
Bất cứ khi nào bệnh nhân diễn tiến xấu trong ED, bác sĩ cấp cứu phải thực hiện một cuộc khảo sát sơ bộ nhanh chóng. Ở những bệnh nhân thông khí, điều này bao gồm việc đảm bảo rằng NKQ vẫn còn trong khí quản (kết hợp cả hai phổi) và đánh giá sự tưới máu của bệnh nhân.
Bác sĩ cấp cứu nên luôn luôn quay trở lại cuộc khảo sát chính khi có điều gì đó không ổn. Một bệnh nhân bị kích động trên máy thở không bao giờ được chích thuốc an thần trước khi bác sĩ kiểm tra ống NKQ, âm thở và SpO2. Sau đây là một số mục tiêu cụ thể để xem xét, dựa trên báo động hoặc kiểm tra chẩn đoán, một khi cuộc khảo sát chính hoàn tất.
Vấn đề: Áp lực đường thở cao
Đây là báo động trong VCV. Nếu PCV đang được sử dụng, báo động sẽ cho thấy thể tích khí lưu thông thấp; tuy nhiên, cách tiếp cận là như nhau. Báo động này chỉ ra rằng có sự giảm độ giãn nở của hệ thống hô hấp. Bước đầu là để xác định xem đây là vấn đề về phổi hay vấn đề về đường thở (xem Bảng 3):
- Thực hiện động tác giữ thì hít vào để xác định PPLAT. Nếu có PAP cao và PPLAT thấp, thì vấn đề là sức cản đường thở cao. Nếu có PAP cao và PPLAT cao, thì vấn đề là ở giảm độ giãn nở của phổi (hoặc thành ngực).
- Siêu âm tại giường là một cách hiệu quả để đánh giá tràn khí màng phổi, tràn dịch màng phổi và phù phổi.
- X-quang ngực có thể xác định vị trí thích hợp của ống NKQ và sẽ cho thấy sự xẹp phổi, tràn dịch, tràn khí màng phổi, hoặc phù phổi.

Vấn đề: Thiếu oxy máu
Tình trạng thiếu oxy máu mới hoặc xấu đi luôn luôn nghiêm trọng. Bước đầu là loại trừ các vấn đề cơ học hoặc di lệch ống NKQ. Ngắt kết nối bệnh nhân khỏi máy thở, và bóp bóng bằng tay với oxy 100%. Định vị vị trí NKQ với capnography và nghe phổi. Xem trực quan trực tiếp bệnh nhân và máy thở. Một khi xác nhận rằng các cài đặt thông khí trên máy thở và NKQ đang đúng vị trí, hãy xem xét các công việc sau cho thiếu oxy máu:
- Siêu âm phổi tại giường là một cách nhanh chóng để chẩn đoán tràn khí màng phổi, tràn dịch màng phổi, hoặc phù phổi. [26]
- Chụp X-quang ngực cũng sẽ chứng minh sự gia tăng thâm nhiễm phổi trầm trọng hơn, tràn khí màng phổi, phù phổi, xẹp phổi, hoặc tràn dịch. Tăng PEEP nếu vấn đề ở trong nhu mô phổi.
- Luôn xem xét thuyên tắc phổi như một nguyên nhân gây thiếu oxy máu mới ở một bệnh nhân nặng. Siêu âm tại giường để đánh giá chức năng thất phải hoặc tĩnh mạch đùi không ép xuống được có thể giúp chẩn đoán. Chụp CT mạch máu phổi được xem là tiêu chuẩn vàng để chẩn đoán thuyên tắc phổi.
- Nếu có phế âm giảm ở một bên, kéo NKQ ra 1 vài cm nếu nó đang vào phế quản gốc trên phim X quang ngực. Với soi phế quản bằng ống nội soi mềm để nhìn trực quan hình ảnh của vị trí ống là một thay thế khác.
- Nếu có phế âm giảm ở một bên, ngay cả với ống đúng vị trí, hãy xem xét pneumothorax hoặc tắc do nút nhầy làm xẹp 1 thùy hoặc toàn bộ 1 bên phổi.
- Cần nghi ngờ tràn khí màng phổi nếu thấy phế âm giảm ở một bên và nếu bệnh nhân hạ huyết áp, nhịp tim nhanh và thiếu oxy. Không nghe phế âm 1 bên không nhạy cảm với chẩn đoán tình trạng này, và khí quản lệch là dấu hiệu muộn.
Vấn đề: căng phổi động (dynamic hyperinflation)
Sự căng phổi động thường do thời gian thở ra không đủ. Sức cản đường thở cao chỉ làm cho nó tồi tệ hơn. Trên máy thở, lưu lượng thở ra sẽ không trở lại đường cơ bản trước khi hơi thở tiếp theo bắt đầu và sẽ có thể đo được autoPEEP. Khi thăm khám, bệnh nhân sẽ thấy không thoải mái. Cơ bụng của bệnh nhân sẽ co thắt trong quá trình thở ra chủ động, và có thể có giãn tĩnh mạch cổ. Do tăng khoảng chết, PaCO2 sẽ thực sự tăng lên khi tần số thở máy thở được tăng lên. Dưới đây là một số bước để sửa đổi căng phổi động:
- Nếu bệnh nhân không ổn định về huyết động học, ngắt kết nối máy thở là cách nhanh nhất để cho phép không khí bị bẫy thoát ra. Thông khí với mặt nạ túi có thể được thực hiện cho đến khi bệnh nhân ổn định, sau đó có thể điều chỉnh máy thở.
- Giảm tần số thở máy, thường là từ 10 đến 14 lần/phút. Đây là cách đơn giản và nhanh nhất để cải thiện lưu lượng thở ra.
- Rút ngắn thời gian hít vào để giữ tỷ lệ thời gian hít vào:thời gian thở ra (I: E) trong khoảng từ 1:3 đến 1:5.
- Giữ thể tích khí lưu thông trong phạm vi từ 6 đến 8 mL/kg. Thể tích khí lưu thông cao hơn thường làm chậm sự hô hấp tự nhiên của bệnh nhân, nhưng thể tích khí lưu thông > 8 mL/kg PBW có thể gây tổn thương phổi. [16,17]
- Tăng luồng thở ra từ 60 đến 80 L/phút để cho phép thở ra nhiều thời gian hơn.
- Sự an thần thích hợp với opioids sẽ giúp giảm thở nhanh, nhưng cũng có thể dẫn đến tình trạng giữ CO2 và nhiễm toan hô hấp. Điều này có thể gây hại cho bệnh nhân tăng áp lực nội sọ.
- Điều trị chứng co thắt phế quản bằng thuốc giãn phế quản dạng hít và steroid hệ thống.
TRƯỜNG HỢP ĐẶC BIỆT
Trong một số trường hợp, bác sĩ cấp cứu có thể muốn duy trì PaO2 cao hơn và tránh tình trạng tăng CO2 máu cho phép. Ở những bệnh nhân bị tổn thương cấp tính của não, cho phép PaCO2 tăng lên và độ pH giảm xuống có thể làm tăng áp lực nội sọ bằng cách giãn mạch não. Có thể là cần thiết tăng thể tích khí lưu thông vượt ra ngoài những gì được coi là phổi bảo vệ phổi để ngăn ngừa biến chứng này, mặc dù tăng tần số thở thường là đủ để duy trì PaCO2 trong phạm vi bình thường. Ở những bệnh nhân bị tổn thương não, cũng cần phải duy trì một PaO2 gần với những gì được coi là bình thường, tức là ít nhất 90 mm Hg. [27]
NHỮNG ĐIỀU CÒN BÀN CÃI
Bằng chứng mạnh mẽ nhất về thông khí bảo vệ phổi là do các nghiên cứu do nhóm ARDSNet tiến hành. [4,5] Một số đã đưa ra những lời chỉ trích, cho rằng 6 mL/kg PBW là quá thấp và ≥ 8 mL/kg PBW nên được sử dụng. Tuy nhiên, một thử nghiệm đối chứng ngẫu nhiên đa trung tâm trong tương lai thử nghiệm các chiến lược bảo vệ phổi khác sẽ cần thiết để biện minh cho yêu cầu này.
Cũng có bằng chứng cho thấy việc sử dụng thể tích khí lưu thông vượt quá 8 mL/kg PBW ở bệnh nhân không bị tổn thương phổi nguyên phát có thể gây căng phồng phổi quá mức và gây nguy hiểm. [16,28,29] Giữ thể tích khí lưu thông ở ≤ 8 mL/kg PBW có thể là cách tốt nhất.
PPLAT đã được đề xuất như một cách khác để hướng dẫn điều trị, với đề xuất rằng nếu PPLAT được giữ < 30 cm H2O, nó không quan trọng thể tích khí lưu thông là bao nhiêu. Có 3 vấn đề với cách tiếp cận này. Thứ nhất, không có thử nghiệm lâm sàng ngẫu nhiên so sánh phương pháp này với phương pháp ARDSNet để cho thấy sự ưu việt (hoặc thậm chí tương đương). Thứ hai, trong phân tích nghiên cứu của ARDSNet, tỷ lệ tử vong gia tăng cùng với mỗi nhóm của việc tăng PPLAT. [5] Không có ngưỡng an toàn nào được xác định. Thứ ba, các nghiên cứu trên động vật đã chứng minh rằng sự quá căng của phế nang (và không phải là áp lực căng) là nguyên nhân của phần lớn các tổn thương phổi do thở máy gây ra. Dreyfuss và cộng sự đã sử dụng cả hai kết hợp phổi sắt và băng quấn ngực bụng ở chuột để chứng minh rằng khối thể tích khí lưu thông cao làm tăng tính thấm và tổn thương phổi, bất kể áp lực cần thiết để tạo ra một thể tích như thế nào. [30]
CÁC BIỆN PHÁP CỨU HỘ
Nhiều phương pháp thay thế khác của thông khí và các liệu pháp cứu hộ khác đã được đề xuất cho giảm oxy máu kháng trị. Chúng bao gồm thủ thuật huy động phổi, thông khí tần số cao, thông khí xả áp, hít nitric oxit, thuốc phong tỏa thần kinh cơ, và tư thế nằm sấp.
Thủ thuật huy động phổi
Các thủ thuật huy động phổi đã được chứng minh là cải thiện oxy hóa ở những bệnh nhân thông khí [31,32] và họ có thể dễ dàng thực hiện trong ED để giảm thiếu oxy. Việc đặt bệnh nhân lên áp lực dương tính liên tục (CPAP) từ 35 đến 40 cm H2O trong 30 đến 40 giây có thể giúp cho việc huy động phế nang và cải thiện oxy hóa ngắn hạn, mặc dù sự ổn định lâu dài của những thủ thuật này không rõ ràng. [33]
Việc huy động phế nang cho thử nghiệm ARDS là một thử nghiệm đối chứng ngẫu nhiên tiền cứu được thiết kế để so sánh thông khí phổi thông thường với một phác đồ được thiết kế để tối đa hóa việc huy động phế nang. [34] Thử nghiệm này hiện đang được tiến hành.
Thông khí rung tần số cao
Thông khí rung tần số cao (HFOV) hoạt động trên khái niệm sử dụng thể tích khí lưu thông nhỏ hơn khoảng chết giải phẫu và sinh lý của bệnh nhân, với dao động của màng ngăn trong máy thở từ 3 đến 15 Hz (180-900 dao động/phút). Về mặt lý thuyết, cho phép trao đổi khí mà không làm giãn các đơn vị phổi dễ bị tổn thương và không gây áp lực lên phổi cao. Trong dịch cúm H1N1 năm 2009, HFOV đã được báo cáo là đã xem như chế độ cứu hộ thông khí thành công ở những người lớn bệnh nặng. [35,36]
HFOV cần một máy thở đặc biệt có thể không có trong ED, và các thử nghiệm lâm sàng gần đây không cho thấy một hiệu quả với chế độ thông khí này. Các nghiên cứu ngẫu nhiên (OSCAR) của được công bố năm 2013 đã không chứng minh được sự sống còn ở bệnh nhân ARDS, ngay cả khi được sử dụng sớm trong bệnh của bệnh nhân. [37,38] Không có sự khác biệt về thống kê về tử vong ở OSCAR, và thử nghiệm OSCILLATE đã ngừng sớm do tăng nguy cơ tử vong ở nhóm HFOV (47% so với 35%).
Airway Pressure Release Ventilation
Thông khí xả áp (APRV) sử dụng thời gian kéo dài của áp lực thở cao và giảm áp lực trong khoảng thời gian ngắn (thường là < 1 giây) để CO2 thoát ra khỏi phổi. Không giống như HFOV, APRV có thể được thực hiện với hầu hết các máy thở có sẵn thương mại, làm cho điều này hữu ích hơn như là một chế độ cứu hộ. Ngoài ra, APRV không đòi hỏi phải có thuốc an thần hoặc phong bế thần kinh cơ, cả hai đều rất cần thiết với HFOV. [39] Bằng cách duy trì áp lực đường thở trung bình cao hơn, sự oxy hóa có thể cải thiện so với thông khí thông thường. [40] Mặc dù việc cải thiện oxy hóa rất hấp dẫn và có thể là nguyên nhân chính đằng sau sự phổ biến của APRV, điều này, tự nó đã không được chứng minh để cải thiện sự sống còn ở bệnh nhân suy hô hấp cấp. Một nghiên cứu đơn lẻ gồm 63 bệnh nhân chấn thương so sánh APRV với thông khí thể tích khí lưu thông thấp không có sự khác biệt về tỷ lệ tử vong, số ngày thở máy, viêm phổi hoặc tràn khí màng phổi. [41] Đến nay, không có nghiên cứu lâm sàng nào cho thấy khả năng sống sót với APRV khi so sánh với thông khí bảo vệ phổi.
Inhaled Nitric Oxide
Hít nitric oxit (iNO) là chất làm giãn mạch phổi chọn lọc giúp cải thiện sự thông khí/tưới máu bằng cách làm giãn các mao mạch phổi ở các phế nang thông khí tốt. Điều này cải thiện oxy hóa ở bệnh nhân ARDS; tuy nhiên, iNO đã không được chuyển thành một hiệu quả sống còn ở người lớn. Một phân tích gộp gần đây cho thấy rằng iNO không liên quan với kết quả cải thiện, bất kể mức độ nghiêm trọng của ARDS. [42] Không nên sử dụng iNO trong ED.
Thuốc chẹn thần kinh cơ
Việc điều trị bằng thuốc chẹn thần kinh cơ, cùng với thuốc an thần thích hợp, cũng đã được nghiên cứu ở bệnh nhân ARDS. Có lẽ, thư giãn của thành ngực cải thiện độ giãn nở hệ thống hô hấp và cải thiện thông khí. Cũng có thể có một lợi ích từ giảm tiêu thụ oxy hệ thống. Một thử nghiệm gần đây so sánh việc sử dụng cisatracurium besylate với giả dược đã cho thấy tăng tỷ lệ sống sót. [43] Tỷ lệ nguy cơ tử vong (hazard ratio for death) ở 90 ngày tốt hơn ở nhóm cisatracurium besylate (0,68, 95% CI, 0,48-0,98), nhưng tỷ lệ tử vong 90 ngày tổng thể giữa 2 nhóm không đạt được ý nghĩa thống kê. Một cách giải thích điều này là nhóm cisatracurium besylate sống lâu hơn trong ICU và bệnh viện, nhưng không có sự khác biệt về tỷ lệ sống sót lâu dài. Ngoài ra, 56% bệnh nhân ở nhóm giả dược đã nhận được nhãn cisatracurium besylate trong thời gian ở lại ICU, điều này làm cho nó khó xác định được một điểm chính xác của liệu pháp này.
Tư thế nằm sấp
Tư thế nằm sấp trong quá trình thở máy làm ảnh hưởng đến sự thông khí/tưới máu bằng cách tái phân phối lưu lượng máu phổi sang vùng phổi trước ngực (do đó tăng cường huy động phế nang) và cải thiện sự thanh thải dịch tiết từ đường thở. Các nghiên cứu ban đầu về cơ chế này cho thấy sự cải thiện trong trao đổi khí, nhưng nó không chứng minh được làm giảm tỷ lệ tử vong. [44,45] Tuy nhiên, một nghiên cứu đa trung tâm gần đây đã cho thấy sự cải thiện tỷ lệ sống sót với tư thế nằm sấp kéo dài (16 giờ/ngày) ở bệnh nhân với ARDS nặng. [46] Sự kéo dài thời gian nằm sấp cũng làm giảm tỷ lệ tử vong trong một phân tích gộp 2246 bệnh nhân trong 11 nghiên cứu. [47] Trong số 11 nghiên cứu được đưa vào phân tích, có 10 nghiên cứu có 95% CI vượt qua 1, chỉ có nghiên cứu của Guérin và cs có một CI 95% < 1, và báo cáo của nó giảm nguy cơ tử vong có vẻ chiếm một phần lớn các hiệu quả điều trị được thấy trong phân tích gộp này. [46] Khó khăn đó làm cho đề nghị tư thế nằm sấp như một điều trị cứu hộ dựa trên bằng chứng, cho rằng chỉ có 1 thử nghiệm lâm sàng trong số 11 phân tích cho thấy một lợi ích sống còn. Ngoài ra, tư thế nằm sấp có thể không thực tế trong ED. Việc đặt các đường tĩnh mạch và động mạch trung tâm là rất khó khăn trong việc điều trị bệnh nhân bình thường, và xoay bệnh nhân một cách an toàn đòi hỏi nhiều nhân viên. Giường đặc biệt cho nằm sấp có sẵn, nhưng nó không có khả năng là sẽ có sẵn cho các bác sĩ cấp cứu. Đây có thể là một động cơ giải cứu phù hợp hơn với ICU so với ED.
NÂNG CAO CHẤT LƯỢNG CHĂM SÓC
1. Đảm bảo rằng trao đổi khí là phù hợp để đáp ứng nhu cầu của bệnh nhân. Điều này không có nghĩa là nó phải là bình thường. Một PaO2 55 mm Hg (SpO2 88% -95%) được chấp nhận trong hầu hết các trường hợp, và như vậy là tăng CO2 máu cho phép. Những trường hợp ngoại lệ đáng lưu ý là bệnh nhân bị bệnh lý hoặc chấn thương thần kinh.
2. Thông qua phương pháp tiếp cận bảo vệ phổi để thở máy. Mở phổi và giữ chúng mở bằng PEEP (càng thâm nhiễm nhiều hơn, càng cần PEEP cao hơn). Nhiều bác sĩ sử dụng PEEP tối thiểu là 5 cm H2O, được chứng minh là làm giảm công thở ở bệnh nhân có chức năng của phổi bình thường và ở những bệnh nhân COPD. [48] Sử dụng bảng PEEP-FiO2 (xem Bảng 2) là phương pháp thuận tiện nhất trong ED, nhưng sử dụng LIP trên đường cong áp lực thể tích cũng được chấp nhận. Không nên cho bệnh nhân thể tích khí lưu thông quá cao (6-8 mL/kg PBW ở hầu hết các bệnh nhân, bệnh nhân ARDS nên có khối thể tích khí lưu thông thấp hơn 4-6 mL/kg PBW).
3. Khắc phục sự cố PAP cao với thủ thuật giữ thì hít vào để đo PPLAT. Nếu PAP và PPLAT đều cao, thì có vấn đề về phổi. Nếu PAP cao hơn đáng kể so với PPLAT, vấn đề là sức cản đường thở. Cần kiểm tra ống NKQ, và nghe tiếng khò khè.
4. Căng phổi động là phổ biến ở bệnh nhân COPD và hen. Tần số thở máy nhanh không cho phép đủ thời gian để thở ra và có thể làm trầm trọng thêm vấn đề. Cho phép nhiều thời gian thở ra để bệnh nhân thở ra được hoàn toàn.
5. Quan trọng nhất, luôn luôn quay trở lại cuộc khảo sát chính nếu có điều gì sai. Một bệnh nhân bị kích động trên máy thở không bao giờ được làm yên trước khi bạn kiểm tra ống NKQ, âm thở và SpO2.
Bố trí
Bệnh nhân suy hô hấp cấp cần thông khí cơ học phải được nhận vào ICU. Có thể cần phải tư vấn với một chuyên gia ICU hoặc chuyên về phổi học để giải quyết sự cố của máy thở. Việc giới thiệu và chuyển đến bệnh viện chuyên khoa cao hơn bởi một đội vận chuyển được đào tạo đặc biệt nếu bác sĩ cấp cứu cảm thấy mức độ suy hô hấp là nghiêm trọng đủ để đảm bảo cho các thủ thuật cứu hộ mà không có trong cơ sở của mình.
Tóm lược
Khắc phục sự cố báo động của máy thở và điều chỉnh các cài đặt này là một phần công việc của một bác sĩ cấp cứu cho bệnh nhân nặng. Việc chăm sóc lâu dài của các bệnh nhân thở máy là một vấn đề thường gặp, và các bác sĩ cấp cứu phải hiểu rõ những dấu hiệu báo hiệu và cách giải quyết các vấn đề về áp lực đường thở cao, sự căng phổi động và sự trao đổi khí nặng hơn.





