Bài viết Thở máy tại khoa Chăm sóc đặc biệt Tim mạch Nhi: Những điều chủ yếu được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Mechanical ventilation in the pediatric cardiac intensive care unit: the essentials
Tóm tắt
Thông khí cho trẻ em hoặc trẻ sơ sinh trong quá trình hậu phẫu sau khi sửa chữa bệnh tim bẩm sinh đòi hỏi sự hiểu biết cơ bản về cơ học hệ thống hô hấp (mối tương quan áp lực – thể tích của hệ thống hô hấp và khái niệm về hằng số thời gian) và sinh lý tim phổi. Hơn nữa, phải chú ý cẩn thận để tránh làm hư hại phổi bằng cách thông khí cơ học gây tổn hại. Tối ưu hóa các cài đặt thông khí trong quá trình thông khí kiểm soát và hỗ trợ, cho phép thông khí tự phát càng sớm càng tốt bằng cách vẫn hỗ trợ cho các nỗ lực hô hấp của bệnh nhân, là tính năng quan trọng để bảo vệ phổi, giảm thiểu tác dụng phụ huyết động học của thông khí áp lực dương, và để cai máy sớm. Với cách nhẹ nhàng hơn, việc sử dụng thông khí không xâm lấn trong môi trường hồi sức tim tăng nhanh mặc dù vẫn còn thiếu bằng chứng về tính ưu việt, và đòi hỏi có kiến thức tốt về các kỹ thuật và thiết bị cụ thể của phương pháp này. Bài đánh giá này sẽ giải quyết nhiều khía cạnh và nêu bật các yếu tố cần thiết cần biết khi thông khí cho trẻ trong Đơn vị Chăm sóc Đặc biệt Tim mạch (CICU).
Giới thiệu
Bất kỳ thủ thuật thở máy thụ động hoặc chủ động nào, không chỉ ảnh hưởng đến thông khí và trao đổi khí, mà còn có thể ảnh hưởng đến chức năng tim mạch bằng cách thay đổi thể tích phổi và các áp lực trong lồng ngực (ITP, intrathoracic pressure). Vì những lý do này, việc sử dụng áp lực đường thở thấp, đặc biệt là PEEP thấp thường được đề xuất và ngày càng rút ống NKQ sớm sau phẫu thuật tim. Tuy nhiên, một số bệnh nhân có thể cần hỗ trợ hô hấp trong một thời gian dài sau phẫu thuật tim và đôi khi việc sử dụng áp lực tương đối cao có thể chứng minh là có lợi cho một số bệnh nhân. Một sự hiểu biết thấu đáo về cơ học hô hấp, tương tác bệnh nhân – máy thở, cơ chế trao đổi khí trong phổi, và tương tác tim – phổi trong điều kiện sinh lý và bệnh lý do đó được yêu cầu khi cung cấp thông khí cơ học cho bệnh nhân trong Đơn vị chăm sóc tim chuyên sâu (CICU).[1,2]
Cơ sở của cơ học hô hấp quan trọng trong thông khí cơ học
Tính chất tĩnh của phổi và thành ngực
Thể tích thư giãn (do sự cân bằng của sự đàn hồi ra phía bên ngoài của thành ngực và sự đàn hồi vào phía trong của phổi) của trẻ nhỏ ít hơn ở người lớn, dẫn đến dung tích cặn chức năng (FRC, functional residual capacity) thấp hơn ở trẻ em (khoảng 15% dung tích sống so với 35% ở người lớn). Điều này gây ra một bất lợi rõ ràng về sự ổn định của phế nang với xu hướng giảm, đặc biệt là ở trẻ được an thần trong khi thở máy liên tục.
Hằng số thời gian (Time Constant)
Hằng số thời gian của hệ thống hô hấp (T = Compliance x Resistance) rất quan trọng khi thông khí cho trẻ em. Trong các bệnh lý hạn chế (bệnh lý phổi hoặc thành ngực) T sẽ ngắn hơn, trong khi các bệnh lý tắc nghẽn (bệnh đường hô hấp trên hoặc dưới) T sẽ dài hơn so với phổi khỏe mạnh. Khoảng 5 lần T được yêu cầu cho cân bằng áp lực giữa đường hô hấp gần và khoảng phế nang.
Do đó, tần số hô hấp cao với thời gian hút vào (TI) và thở ra (TE) ngắn có thể thích hợp cho bệnh lý phổi hạn chế hoặc thành ngực mức độ cao nhất nhưng có thể trở nên không phù hợp trong quá trình phục hồi (tăng độ giãn nở) hoặc trong phổi chỉ bị tổn thương nhẹ. Do đó, sử dụng tần số cố định kết hợp với TI và TE cố định trong suốt thời gian nằm CICU có thể không phù hợp, vì bệnh đang tiến triển và do đó cơ học hệ thống hô hấp thay đổi theo thời gian. Hơn nữa, cài đặt thời gian cố định và tần số thông khí theo tuổi bệnh nhân, mặc dù bình thường, nhưng có thể không phù hợp. Hai vấn đề lớn có thể xảy ra với các cài đặt TI hoặc TE không phù hợp:
Thời gian hít vào (TI) không đủ có thể giới hạn thể tích khí lưu thông tại một cài đặt áp lực đường thở cụ thể và cần sử dụng áp lực đường thở cao và nguy hiểm để đạt thể tích khí lưu thông ”vừa đủ”.[3,4] Vấn đề này có thể dễ dàng phát hiện bằng cách quan sát đường cong lưu lượng – thời gian trên máy thở (tức là không kết thúc dòng khí hít vào trước khi máy thở chuyển sang thở ra; Hình 1A) hoặc bằng quan sát lâm sàng (ví dụ, không có tạm dừng ngắn trong chuyển động của ngực của bệnh nhân ở cuối thì hít vào)
Thời gian thở ra (TE) quá ngắn sẽ không cho phép làm rỗng hoàn toàn khoảng khí ngoại vi ở cuối thì thở ra (không chấm dứt lưu lượng thở ra trước khí hít vào tiếp theo; Hình 1B), với nguy cơ tạo ra PEEP nội tại (intrinsic PEEP), còn được gọi là PEEP tự động (auto-PEEP). Trên lâm sàng nên có tạm dừng ngắn trong chuyển động thành ngực của bệnh nhân khi cuối thì thở ra.

Sinh lý tim phổi và bệnh tim mạch
Thông khí áp lực dương (PPV, positive pressure ventilation) ảnh hưởng đến chức năng tim mạch bằng cách thay đổi ITP, thể tích phổi và trao đổi khí/pH. Trong điều kiện bình thường, những ảnh hưởng này là không quan trọng. Tuy nhiên khi có rối loạn chức năng tim mạch, thay đổi ít trong hô hấp có thể tác động đáng kể đến chức năng tim phổi.
Hồi lưu tĩnh mạch (Venous Return)
Thông khí áp lực dương ảnh hưởng đến chức năng tim mạch bằng cách thay đổi gradient áp lực giữa các cấu trúc mạch máu trong và ngoài lồng ngực, và khi làm như vậy PPV ảnh hưởng đến sự trở lại của tĩnh mạch hệ thống và cung lượng tim (CO, cardiac output).[5] Động lực (driving force) cho hồi lưu tĩnh mạch là sự khác biệt về áp lực giữa hệ thống dự trữ tĩnh mạch (venous reservoirs) (chủ yếu là của mạch máu mạc treo, lách và gan) cũng được gọi là áp lực hệ thống trung bình (PMS, mean systemic pressure) và tâm nhĩ phải (RA, right atrium). PMS tùy thuộc vào dung lượng mạch máu (vascular capacitance) và thể tích nội mạch, cả hai là yếu tố chủ yếu của hồ chứa tĩnh mạch này. Sự gia tăng áp lực RA phải được bù đắp bằng sự gia tăng PMS, nếu không, sự trở về tĩnh mạch sẽ giảm. Sự co mạch qua trung gian adrenergic ngay lập tức làm giảm dung lượng mạch máu và do đó làm tăng PMS trong khi huy động máu từ ngoại vi. Phản ứng này được bổ sung theo thời gian bằng cách kích thích hệ thống RAA: renin– angiotensin-aldosterone và tăng thể tích nội mạch máu. Sự sụt giảm của PMS sẽ dẫn đến sự sụt giảm hồi lưu tĩnh mạch.
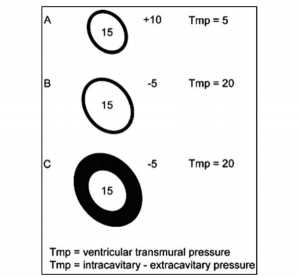
Áp lực tâm nhĩ phải bị ảnh hưởng bởi sự thay đổi trong ITP. Mức độ mà một cấu trúc trong lồng ngực có thể căng phồng lên được trải qua biến dạng phụ thuộc vào áp lực xuyên thành (Ptm, transmural pressure) của nó (áp lực xuyên thành = áp lực trong khoang – áp lực ngoài khoang) và độ giãn nở; và tăng một trong hai tham số này làm tăng kích thước buồng và kết quả là áp lực buồng giảm. Mức độ gia tăng ITP ảnh hưởng đến hồi lưu tĩnh mạch phụ thuộc vào mức phản xạ tuần hoàn (circulatory reflexes) đầy đủ để duy trì PMS (như đã thảo luận) và mức độ ITP được truyền đến RA. Sự lan truyền ITP đến RA tùy thuộc vào cơ học hô hấp, trong đó áp lực đường thở truyền vào hố tim (cardiac fossa) giảm khi sức cản đường thở tăng lên và độ giãn nở phổi giảm.
Đổ đầy tâm thất (ventricular filling) nguyên phát tùy thuộc vào hồi lưu tĩnh mạch hệ thống hoặc tĩnh mạch phổi, độ giãn nở tâm thất (ventricular compliance), và Ptm tâm trương tâm thất (Hình 2). Nó không phải là áp lực làm đầy tâm thất mà nó chỉ ra hoặc xác định mức độ làm đầy tâm thất, mà đúng hơn là Ptm tâm trương tâm thất, bị ảnh hưởng bởi ITP.[6] Sự gia tăng ITP làm giảm Ptm tâm trương tâm thất. Kết quả là, kích thước tâm thất giảm trong khi áp lực của nó tăng lên. Mặc dù tăng áp lực đổ đầy tâm thất, nhưng thể tích tâm thất giảm. Mối tương quan dường như nghịch lý này giữa áp lực và thể tích làm đầy thất xảy ra với những thay đổi trong ITP.[7]
Hậu tải tâm thất hệ thống (Systemic Ventricular Afterload)
Những thay đổi của ITP tạo ra một gradient áp lực giữa các mạch máu trong và ngoài lồng ngực. Khi ITP tăng, Ptm và mặt cắt ngang mạch máu trong lồng ngực giảm, và kết quả là áp lực của chúng tăng lên so với các mạch máu ngoài lồng ngực, tạo ra hiệu ứng giống như thác nước (waterfall-like effect).[8]
Nếu tăng ITP xảy ra trong kỳ tâm thu, tống máu của LV (LV ejection) được hỗ trợ. Nếu tăng ITP xảy ra trong kỳ tâm trương, tống máu tâm thất vào hệ thống động mạch trong lồng ngực tương đối giảm đi.
Thể tích phổi và trao đổi khí
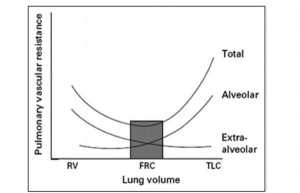
Hô hấp cũng ảnh hưởng đến chức năng tim mạch bằng cách thay đổi thể tích phổi, pH và trao đổi khí. Khi thể tích phổi tăng lên trên mức bình thường (FRC), sức cản mạch máu phổi (PVR) tăng lên do sự nén của các mạch máu giữa các phế nang.
Khi thể tích phổi giảm xuống dưới mức FRC bình thường, PVR tăng chủ yếu do xẹp phổi và ức chế quá trình sản xuất NO của nội mạc phổi do thiếu oxy, làm tăng sức đề kháng của các mạch máu ngoài phế nang (Hình 3). Một yếu tố quyết định quan trọng khác của PVR là pH máu (không phải là PaCO2), tương quan nghịch với pH.
Tối ưu hóa hỗ trợ hô hấp ở bệnh nhân bị bệnh tim
Các khái niệm về thông khí bảo vệ
Trong CICU, thường là cần thiết phải can thiệp sớm và chọn lọc phương pháp hỗ trợ hô hấp. Bất kỳ giảm trương lực cơ hoặc kiểm soát trung khu hô hấp kém, như còn tác dụng của thuốc mê, hoặc giảm độ giãn nở phổi, do gia tăng nước ngoài mạch máu phổi (ví dụ, thứ phát sau chạy tuần hoàn ngoài cơ thể gây ra phản ứng viêm và/hoặc phù phổi do tim) có thể gây giảm FRC và giảm trao đổi khí. Trong các tình huống như vậy, có 3 mục tiêu điều trị chính cần hướng dẫn các chiến lược thông khí:
1. khôi phục FRC (ví dụ, huy động đơn vị phổi xẹp),
2. bình thường hóa thông khí phế nang (duy trì PaCO2 trong phạm vi chấp nhận được) nhưng tránh tạo ra khoảng chết (ví dụ, tránh quá căng phế nang), và
3. ”stent” đường thở xẹp bằng cách áp dụng đủ PEEP hoặc áp lực dương liên tục (CPAP).
Để đạt được những mục tiêu này cùng với các khái niệm thực tế về bảo vệ phổi (thể tích khí lưu thông thấp, hạn chế áp lực hít vào và sử dụng PEEP đầy đủ), điều quan trọng là xác định ‘cài đặt bảo vệ’ cho từng bệnh nhân. Thông khí thể tích khí lưu thông thấp [9] (tức là 6 mL/kg) thường được đề xuất trong nhiều hướng dẫn lâm sàng, mặc dù nó chỉ được bảo vệ tốt hơn về tỷ lệ tử vong của bệnh nhân hơn 12 ml/kg ở bệnh nhân người lớn mắc hội chứng suy hô hấp cấp tính. Tuy nhiên, vẫn còn tranh cãi là thể tích khí lưu thông 6 mL/kg có tốt nhất cho tất cả bệnh nhân hay không vì mức độ và loại bệnh lý phổi thay đổi đáng kể từ bệnh nhân đến bệnh nhân. Một nghiên cứu hồi cứu gần đây cho thấy thể tích khí lưu thông có liên quan nghịch, trong khi áp lực đường thở liên quan trực tiếp đến kết quả kém (tức là tử vong) ở trẻ bị tổn thương phổi cấp tính.[10] Tương tự, phân tích bổ sung từ xử trí hô hấp trong tổn thương phổi cấp tính /ARDS (ARMA) thử nghiệm (6 vs 12 mL/kg) cho thấy ở những bệnh nhân có độ giãn nở phổi thấp trước khi ngẫu nhiên hóa (tức là phổi ít giãn nở hơn và do đó thể tích phổi nhỏ hơn), tử vong (42% so với 29%) so với hạ khí lưu thông xuống 6 mL/kg. Ngược lại, ở những bệnh nhân có độ giãn nở phổi cao hơn trước khi ngẫu nhiên (tức là phổi giãn nở hơn và do đó thể tích phổi lớn hơn), tăng thể tích khí lưu thông lên 12 mL/kg giảm tỷ lệ tử vong (21% so với 37%) so với hạ khí lưu thông xuống 6 mL/kg.[11] Những quan sát này đặt câu hỏi về khuyến nghị chung để giảm thể tích khí lưu thông xuống 6 mL/kg ở mỗi bệnh nhân không phụ thuộc vào loại và mức độ bệnh phổi tiềm ẩn. Hơn nữa, các nghiên cứu đã hạn chế áp lực đường thở trong cả hai nhóm nghiên cứu với áp lực đường thở < 30 cm H2O và không tìm thấy sự khác biệt về kết quả giữa các nhóm. Dựa trên những quan sát này và lưu ý rằng thể tích khí lưu thông sinh lý ở người là 6 đến 7 mL/kg, các nguyên tắc sau có thể được áp dụng trong môi trường lâm sàng:
Thể tích phổi cặn nhỏ hơn (ví dụ, độ giãn nở phổi kém) thì thể tích khí lưu thông cho phép càng nhỏ; thể tích phổi cặn lớn hơn (tức là, độ giãn nở phổi tốt hơn), thể tích khí lưu thông cho phép càng lớn.
Giới hạn áp lực cho phép khắc phục một phần khó khăn trong việc ước tính thể tích khí lưu thông cho phép ở một bệnh nhân (tức là phổi kém giãn nở sẽ nhận được lượng khí lưu thông thấp; phổi giãn nở hơn sẽ nhận được thể tích khí lưu thông lớn hơn).
Trong những trường hợp độ giãn nở của thành ngực giảm, áp lực đường thở cần thiết để bơm phồng phổi đầy đủ sẽ cao hơn do sự gia tăng ITP, mà ITP đối nghịch lại tác động của áp lực đường thở áp dụng (Paw), với áp lực đẩy (driving pressure) làm bơm phồng phổi là áp lực xuyên phổi (TPP, transpulmonary pressure) (TPP = Paw – ITP). Trong những tình huống như vậy yêu cầu áp lực đường thở để cung cấp một lượng khí lưu thông chấp nhận được sẽ tương đối cao, với hậu quả ITP có thể làm giảm hồi lưu tĩnh mạch.
Cách thứ hai để bảo vệ phổi là một cài đặt PEEP đầy đủ. PEEP có tác dụng duy trì thể tích phổi tại thời điểm cuối thì thở ra của chu kỳ hô hấp, lúc thể tích phổi nhỏ nhất và là lúc phổi có nguy cơ sụp đổ cao nhất. PEEP đơn thuần không cản trở hồi lưu tĩnh mạch, nhưng khi PEEP tăng lên ngoài việc sử dụng thể tích khí lưu thông lớn, áp lực hít vào sẽ cao, làm tăng nguy cơ hạn chế hồi lưu tĩnh mạch và do đó tương tác tim phổi không mong muốn. Với sự ra đời của thông khí thể tích khí lưu thông thấp, nguy cơ này đã trở nên thấp hơn, nhưng mặt khác thể tích khí lưu thông thấp có thể không cho phép đủ thể tích khí lưu thông huy động trong phổi bị tổn thương nhiều hơn, vì vậy có xu hướng xẹp xuống nhiều hơn. Việc sử dụng mức PEEP cao hơn một chút, thay vì tăng áp lực đường thở đỉnh và do đó tăng thể tích khí lưu thông, có thể là một lựa chọn tốt hơn để bảo vệ phổi. Nếu PEEP cho phép khôi phục FRC bình thường, PVR sẽ là thấp nhất (Hình 3) và có thể giảm thiểu nguy cơ tương tác tim – phổi không mong muốn.
Duy trì đồng bộ hóa bệnh nhân – máy thở trong quá trình thông khí tự phát
Các mục tiêu trong quá trình thở máy là giảm công hô hấp, hỗ trợ trao đổi khí và cho phép bệnh nhân hồi phục sau những gì cần thiết phải thở máy. Sau phẫu thuật tim, các mục tiêu tương tự ngoại trừ việc thở máy áp lực dương có thể có tác động bất lợi đến tình trạng tim mạch của bệnh nhân, đặc biệt ở bệnh nhân thể tích máu bình thường và giảm thể tích.[12] Do đó, các ưu tiên điều trị trong thở máy là để giảm thiểu tác dụng phụ của PPV cho chức năng tim mạch do tăng công hô hấp, ITP dao động âm và căng phế nang quá mức.
Đối với bệnh nhân nhi và trẻ sơ sinh thở tự nhiên khi thở máy có sự kết hợp của 2 bộ điều khiển riêng biệt: bơm cơ học do bác sĩ kiểm soát (máy thở) và bơm cơ hô hấp của bệnh nhân. Sự tương tác này là phức tạp và liên quan đến nhiều con đường phản hồi. Do đó, máy thở trở thành một phần mở rộng của cơ hô hấp bệnh nhân, gây ra giảm tải một phần cơ hô hấp và chia sẻ tải giữa cơ hô hấp và máy thở. Những tương tác này tạo ra một vòng phản ứng bị ảnh hưởng bởi sự tương tác này giữa máy thở (bộ điều khiển nhịp thở, bao gồm kích hoạt, cung cấp khí và cách kết thúc nhịp thở) và các yếu tố bệnh nhân (cơ học của hệ thống hô hấp và đáp ứng cơ hô hấp), nguyên nhân sự thay đổi thể tích theo thời gian, ảnh hưởng đến phản ứng cơ hô hấp của bệnh nhân, do đó bị ảnh hưởng bởi mối tương quan lực – cơ và lực – vận tốc của cơ hô hấp.
Không đồng bộ bệnh nhân – máy thở là sự thất bại của 2 bộ điều khiển để hoạt động hài hòa. Công hô hấp và nỗ lực của bệnh nhân bị ảnh hưởng bởi khả năng của máy thở để đáp ứng nhu cầu hít vào tối đa của bệnh nhân.[13] Kết quả không đồng bộ dẫn đến trao đổi khí không hiệu quả và có liên quan đến bẫy khí, rò rỉ khí lồng ngực, tăng công thở và cung cấp thể tích không hằng định. Bởi vì thông khí là hoạt động luyện tập, bất kỳ sự giảm thiểu tải chuyển hóa nào trên cơ hô hấp sẽ cho phép dòng máu được chuyển đến các hệ cơ quan khác cần oxy. Các yếu tố ảnh hưởng đến sự không đồng bộ bệnh nhân – máy thở được liệt kê trong Bảng 1 và có thể được chia thành các yếu tố thiết bị, yếu tố bệnh nhân và yếu tố lâm sàng ra quyết định. Hình thức phổ biến nhất của mất đồng bộ kích hoạt là kích hoạt trễ. Kích hoạt trễ là một độ trễ trong thời gian từ khi bắt đầu hoạt động cơ hô hấp đến khi bắt đầu bơm phồng phổi cơ học. Nguyên nhân gây kích hoạt trễ được liệt kê trong Bảng 2. Các kỹ thuật cần thiết để giảm thiểu công thở trong khi thở tự nhiên là cải thiện sự đồng bộ bệnh nhân – máy thở, giảm sức cản đường thở và huy động các đơn vị phế nang. Các can thiệp lâm sàng có thể khuyến khích thở tự nhiên và giảm sự không đồng bộ được nêu trong Bảng 3.
Thông khí không xâm lấn ở bệnh nhân tim sau phẫu thuật
Thông khí không xâm lấn (NIV), giả sử rằng CPAP được bao gồm trong thuật ngữ này, đã được chứng minh là có lợi trong một số nghiên cứu sau phẫu thuật tim.[24-35] Một nghiên cứu ngẫu nhiên (trình bày tại Hội nghị Thông khí nhi khoa và sơ sinh châu Âu lần thứ 10, Montreux 2010, chưa công bố) không cho thấy lợi thế của CPAP chọn lọc so với CPAP cứu mạng ở bệnh nhân tim sau phẫu thuật.[36] Theo đó, NIV chọn lọc chưa thể được khuyến cáo như một cách tiếp cận thông thường.
| Bảng 1: Nguyên nhân mất đồng bộ bệnh nhân – máy thở | |
| Yếu tố bệnh nhân |
|
| Yếu tố máy thở |
|
| Yếu tố quyết định lâm sàng |
|
| Bảng 2: Kích hoạt trễ (Trigger delay) | |
| Đặc trưng máy thở và cài đặt |
|
| Đặc trưng của bệnh nhân |
|
| Đặc trưng bộ dây và giao diện |
|
Mặc dù bất kỳ máy thở thông thường nào có tùy chọn NIV đều có thể được sử dụng để cung cấp PPV không xâm lấn, việc sử dụng chúng bị hạn chế ở trẻ nhỏ và đặc biệt là ở trẻ dưới 6 tháng tuổi vì nhiều lý do, bao gồm hệ thống kích hoạt không chính xác và bù đắp rò rỉ không đủ.[37] Tuy nhiên, các thế hệ mới hơn máy thở được hứa hẹn vì những máy thở này cung cấp các hệ thống tinh vi hơn để khắc phục một số hạn chế được mô tả cũng như các hệ thống kích hoạt thay thế, chẳng hạn như kích hoạt dựa trên tín hiệu hoạt động của cơ hoành (hỗ trợ thông khí điều chỉnh theo tự nhiên [NAVA]). Hầu hết các máy thở chuyên dụng cho NIV sử dụng một tuabin tạo ra 2 mức áp lực đặt trước: gọi là áp lực đường thở hai mức dương (BiPAP, bi-level positive airway pressure). Nói chung, máy thở dành riêng cho NIV cho phép áp lực tăng lên mặc dù mức độ rò rỉ cao và cho phép điều chỉnh chính xác hơn độ nhạy kích hoạt và tiêu chí chuyển chu kỳ. Tuy nhiên, máy thở dành riêng cho NIV không thể sử dụng được cho trẻ em dưới một trọng lượng cơ thể nhất định, thứ phát do các hạn chế về quy định các phép đo thể tích không chính xác. Kinh nghiệm lâm sàng với NIV ở bệnh nhân sau phẫu thuật rất ít do đó các khuyến nghị thực tế sau đây phản ánh kinh nghiệm lâm sàng cá nhân và không dựa trên bằng chứng được ghi chép rõ ràng.
Chọn giao diện. Mặt nạ mũi miệng (oronasal masks) có thể được khuyên dùng cho bệnh nhân suy hô hấp thiếu oxy cấp tính, nhưng mặt nạ mũi (nasal masks) lớn che cả mũi và miệng có thể sử dụng thay thế.[38,39]
Chọn thiết bị. BiPAP Vision (Respironics) đã được chứng minh là an toàn và hiệu quả trong việc cung cấp NIV ở bệnh nhân nhỏ (cân nặng trung bình 9 kg) do suy hô hấp và ở bệnh nhân tim sau phẫu thuật.[31,33,40]
Chọn chế độ. CPAP có thể được lựa chọn cho những bệnh nhân không bị tăng PaCO2 máu hoặc suy hô hấp đáng kể. Nên chọn chế độ BiPAP cho các bệnh nhân còn lại và đã được áp dụng thành công cho bệnh nhân lớn tuổi (trung bình 5 tuổi).[41] Đối với chế độ BiPAP, phương thức thở spont của NIV có thể là lựa chọn tốt nhất ngoại trừ trẻ dưới 6 tháng tuổi do không thể hoạt hóa các yếu tố kích hoạt hô hấp.[37] Đối với những bệnh nhân này, nên sử dụng chế độ chu kỳ theo thời gian.[31,41] Có thể quan sát thấy sự không đồng bộ khi sử dụng máy thở thông thường ở chế độ hỗ trợ áp lực (chu kỳ lưu lượng) bởi vì thời gian hít vào có thể thay đổi từ nhịp thở tới nhịp thở do rò rỉ khí là thường gặp. Do đó, điều quan trọng là phải điều chỉnh kích hoạt thở ra (nghĩa là tiêu chí chấm dứt lưu lượng) và theo mức độ quan trọng của rò rỉ hoặc cài đặt thời gian hít vào tối đa nếu có, sẽ tránh được tình huống thời gian hít vào dài không phù hợp khi rò rỉ tăng đột ngột.[42] Ngoài ra, có thể sử dụng thông khí kiểm soát áp lực (mặc dù vẫn cho phép bệnh nhân kích hoạt nhưng chu kỳ theo thời gian) (khởi phát nhịp thở trên bộ kích hoạt hít vào, chấm dứt chu kỳ theo TI) và cũng có thể cho phép đồng bộ hóa hợp lý.
Giảm thiểu tác dụng phụ trên hệ tuần hoàn của thông khí cơ học
Sự liên quan lâm sàng của tương tác tim phổi tăng đáng kể trong thở máy bệnh nhân có rối loạn chức năng tim mạch. Tác dụng chủ yếu của các tương tác này phụ thuộc vào một số yếu tố bao gồm dung lượng tĩnh mạch, sức cản mạch máu động mạch, chức năng mạch máu phổi và chức năng tâm trương và tâm thu của thất phải và trái (LV).
Rối loạn chức năng tâm trương. Với suy tâm trương thất, thể tích nhát bóp (SV, stroke volume) thấp do thể tích thất không đủ. Kết quả là, tác dụng chủ yếu của hô hấp là hồi lưu tĩnh mạch và làm đầy thất và không phải trên hậu tải thất hệ thống. Trong bệnh cơ tim phì đại, giảm tiền tải tâm thất và hậu tải thất hệ thống do PPV làm tăng tắc nghẽn đường ra LV động.[43,44] Sau thủ thuật Fontan, tình trạng cung lượng tim thấp có nhiều khả năng là do thể tích thất không đủ hơn là rối loạn chức năng tâm trương luôn luôn có mặt. Ngoài ra, trái ngược với Glenn hai chiều (bidirectional Glenn), tất cả hồi lưu tĩnh mạch hệ thống phải vượt qua sức cản của tuần hoàn phổi mà không cần sự hỗ trợ của buồng bơm dưới phổi (subpulmonic pumping chamber), điều này làm tổn hại thêm đến việc làm đầy thất. Thực tế này cũng làm cho tuần hoàn Fontan đặc biệt nhạy cảm với sự gia tăng của PVR. Williams và các đồng nghiệp đã chứng minh sự gia tăng đáng kể của PVR với mức PEEP khiêm tốn ở những bệnh nhân sau làm thủ thuật Fontan, điều này dẫn đến việc giảm đáng kể CO.[45] Tách biệt với những thay đổi về thể tích phổi, Shekerdescent và các đồng nghiệp đã chứng minh tầm quan trọng của ITP đối với CO ở các bệnh nhân này, vì họ đã chứng minh sự gia tăng đáng kể lưu lượng máu phổi khi chuyển từ PPV sang thở áp lực âm (sử dụng curaiss) ở bệnh nhân sau thủ thuật Fontan.[46] Sau khi sửa chữa tứ chứng Fallot, luôn có một số mức độ rối loạn chức năng tâm trương RV, với khoảng 20% đến 25% bệnh nhân bị CO thấp. Thông khí áp lực âm đã được chứng minh là cải thiện đáng kể SV và CO ở những bệnh nhân này.[47,48]
| Bảng 3. Can thiệp lâm sàng | |
| Can thiệp | Bàn luận |
| Chọn phương thức thở thích hợp | Người ta đã chứng minh rằng thở tự nhiên cung cấp thông khí cho các vùng phổi phụ thuộc có lưu lượng máu tốt nhất, trái ngược với PPV với bệnh nhân bị dùng thuốc liệt cơ.[14] Người ta đã đề xuất rằng hiệu quả này có thể được tối ưu hóa bằng cách sử dụng thông khí giải phóng áp lực đường thở (APRV hoặc tương đương của nó, ví dụ, bivent …). Ưu điểm của chế độ này là cho phép thở tự nhiên trong tất cả các giai đoạn, oxygen hóa và thông khí có thể được duy trì ở áp suất thấp hơn, cải thiện các thông số huyết động, giảm nhu cầu an thần và phong tỏa thần kinh cơ. Về mặt lý thuyết có thể thu được kết quả tương tự với chế độ điều khiển kép với mức PEEP phù hợp để tối ưu hóa FRC. Chìa khóa trong cả hai kịch bản là huy động phổi đầy đủ. |
| Giảm sự không đồng bộ bệnh nhân – máy thở | Giảm sự không đồng bộ bệnh nhân – máy thở đòi hỏi phải nhận biết trước tiên sau đó xác định các yếu tố liên quan đến sự không đồng bộ trong Bảng 1 và 2. Để nhận biết, vui lòng tham khảo các đánh giá của Kondii et al [16] và Nilseestuen et al.[17] Gần đây, người ta đã đề xuất rằng không đồng bộ và hoạt động của nhịp thở có thể được giảm bớt bằng cách sử dụng nhịp thở được kích hoạt tự nhiên (NAVA) so với hơi thở được kích hoạt bằng khí nén.[18,19] Tuy nhiên, cần nghiên cứu thêm trước khi đề xuất chế độ thông khí này. |
| Sử dụng phương pháp bổ trợ để giảm thời gian PPV | Việc sử dụng áp lực dương xâm lấn có thể được giảm bớt bằng cách sử dụng thở lưu lượng cao qua ống thông mũi (HFNC) [20] và hỗ trợ máy thở không xâm lấn (NIV).[21-23] |
Rối loạn chức năng tâm thu. Trong suy tim tâm thu, tâm thất giãn nằm trên phần phẳng của đường cong áp lực-thể tích nhát bóp (Starling curve), do đó giảm hồi lưu tĩnh mạch sẽ ít ảnh hưởng đến SV. Ảnh hưởng chủ yếu của những thay đổi trong ITP ở bệnh nhân suy tim sung huyết là giảm hậu tải thất hệ thống và tăng SV/CO. Tầm quan trọng của những thay đổi trong ITP trên CO tăng lên khi chức năng tâm thu thất của hệ thống suy yếu và khi mức độ thay đổi của ITP tăng lên. Khác với những thay đổi trong ITP, thông khí cơ học sẽ dỡ tải bơm hô hấp. Khi làm như vậy, tiêu thụ oxy cơ hô hấp giảm, cho phép phân phối lại CO hạn chế để duy trì tưới máu cho các cơ quan quan trọng khác. Tác dụng có lợi của việc tăng ITP và dỡ tải bơm hô hấp lên CO và cân bằng vận chuyển oxy toàn phần và cơ tim là có ý nghĩa. Rasanen và các đồng nghiệp nhận thấy rằng tiến triển từ hỗ trợ máy thở đầy đủ đến thở tự nhiên đã ảnh hưởng xấu đến cân bằng và vận chuyển oxy của cơ tim ở 5 trong số 12 bệnh nhân bị nhồi máu cơ tim cấp tính phức tạp do suy hô hấp.[50] Ở 5 bệnh nhân này, tăng dấu hiệu thiếu máu trên điện tim và tăng đáng kể áp lực làm đầy LV xảy ra khi loại bỏ PPV. Scharf và các đồng nghiệp đã chứng minh sự mất vận động (akinesis) ở ít nhất một vùng của LV ở 9 trong số 14 bệnh nhân bị rối loạn chức năng LV và không có người nào trong 12 bệnh nhân kiểm soát, khi thực hiện thao tác Mueller (giảm áp lực đường thở chống lại thanh môn đóng kín).[51] Tầm quan trọng của tương tác tim phổi cũng được thể hiện trong chứng ngưng thở khi ngủ do tắc nghẽn trong khi hai thất tăng hậu tải có thể làm thúc đẩy thiếu máu cơ tim.[52]
Theo dõi bệnh nhân thở máy
Giám sát trao đổi khí
Oxygen hóa. Bước đầu tiên trong phân tầng oxygen hóa là thông khí. Do đó thông khí là yếu tố chính quyết định PO2. Một khi oxy đến được phế nang, khuếch tán oxy đến giường mao mạch là bước tiếp theo. Tình trạng sinh lý bệnh trong đó máu tĩnh mạch khử oxy đi vào tuần hoàn động mạch mà không đi qua các vùng thông khí được gọi là shunt trong phổi từ phải sang trái. Một shunt trong phổi sẽ dẫn đến giảm PaO2 và mất độ bão hòa hệ thống. Pulse oximeter là một công cụ thiết yếu trong ICU. Công nghệ này ước tính độ bão hòa oxy động mạch (SpO2) bằng cách đo sự hấp thụ ánh sáng trong máu mạch đập. Sự khác biệt giữa SpO2 (độ bão hòa oxy động mạch ước tính) và SaO2 (độ bão hòa oxy động mạch thực) có thể có ý nghĩa đặc biệt khi độ bão hòa oxy động mạch giảm.
Loại bỏ CO2. Loại bỏ CO2 theo một mô hình tương tự như việc cung cấp oxy. Sự khác biệt chính có liên quan đến thực tế là CO2 và O2 có đường cong phân ly khác nhau và ảnh hưởng khác nhau đến phản xạ thông khí. Đo CO2 có thể thông qua đánh giá CO2 end-tidal (EtCO2) hoặc đánh giá qua da. EtCO2 là giá trị CO2 cao nhất khi thở ra và có thể được đo bằng phương pháp quang phổ hồng ngoại. Ở những người tham gia bình thường, sự khác biệt giữa động mạch và EtCO2 là < 2 mm Hg. Độ chênh CO2 từ động mạch đến end-tidal tăng kết quả của thông khí lãng phí và khoảng chết, thể tích phổi quá mức và tưới máu phổi thấp.[53]
Đo CO2 qua da (TCO2). Cách tiếp cận này có thể cung cấp giám sát không xâm lấn tuyệt vời PaCO2 khi EtCO2 không có sẵn như trong thông khí tần số cao. Mặc dù có thể quan sát được độ lệch nhất định giữa PaCO2 và TCO2 (tùy thuộc vào tưới máu da và khả năng làm nóng của cảm biến), theo dõi TCO2 thường cho phép thấy xu hướng PaCO2 tuyệt vời theo thời gian.
Biểu đồ dạng sóng. Việc sử dụng biểu đồ dạng sóng hiện đã trở thành một thành phần thiết yếu trong việc quản lý bệnh nhân được thở máy. Hầu hết các máy thở cho phép theo dõi liên tục đồ họa đường thở bao gồm hiển thị đồ họa về lưu lượng, áp lực đường thở và thể tích. Một số ví dụ về cách đồ họa được sử dụng để tối ưu hóa các chiến lược thông khí sẽ được thảo luận dưới đây.
Căng phổi quá mức (overdistention). Căng phổi quá mức xảy ra khi giới hạn thể tích của một số thành phần của phổi được tiếp cận. Nó sẽ được biểu hiện như một sự giảm đáng kể sự độ giãn nở ở đầu cuối của nhịp thở (Hình 4). Điều này thường được gọi là mỏ chim (beaking). Căng phổi quá mức nên tránh vì nó có một số tác dụng xấu trên hệ thống tim mạch và phổi. Đầu tiên, căng phổi quá mức khiến bệnh nhân có nguy cơ bị chấn thương liên quan đến áp lực (barotrauma) và chấn thương liên quan đến thể tích (volutrauma). Thứ hai, căng phổi quá mức có thể làm tăng khoảng chết và do đó làm cho thông khí kém hiệu quả hơn. Thứ ba, căng phổi quá mức sẽ dẫn đến sự gia tăng mạnh mẽ của PVR (Hình 3). Những hiệu ứng này sẽ còn ấn tượng hơn nữa ở mức PEEP cao hơn trong khi duy trì thể tích khí lưu thông hoặc áp lực lái xe như cũ (ΔP = PIP – PEEP). Khi quan sát thấy hình mỏ chim (Hình 4), bác sĩ lâm sàng nên giảm PIP đã cài đặt hoặc thể tích khí lưu thông để giảm nguy cơ căng phổi quá mức.
Căng phổi động (Dynamic hyperexpansion). Khi sức cản đường thở cao và/hoặc nhịp hô hấp nhanh được sử dụng, bệnh nhân có nguy cơ bị căng phổi động. Điều này xảy ra khi thì thở ra không hoàn thành (Hình 1B). Kết quả là, có giữ khí lại trong hệ thống hô hấp của bệnh nhân (tức là bẫy khí) dẫn đến PEEP nội tại, khó kiểm soát và nên tránh. Căng phổi động có thể làm giảm hồi lưu tĩnh mạch và do đó tiền tải và cuối cùng là CO. Để hạn chế rủi ro của căng phổi động, người ta nên giảm TI, nếu nó trở nên quá ngắn có thể làm giảm thể tích khí lưu thông (xem ở trên) hoặc giảm tần số máy thở để cho phép một TE dài hơn.
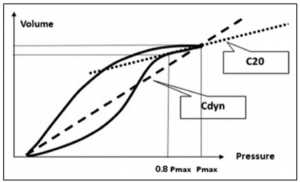
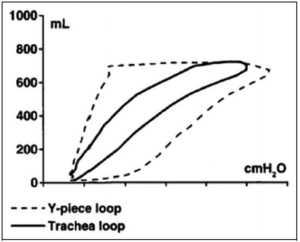
Tối ưu hóa PEEP bằng phân tích dạng sóng. Biểu đồ dạng sóng đặc biệt hữu ích ở những bệnh nhân mắc hội chứng suy hô hấp cấp tính. Thường thì những bệnh nhân này đòi hỏi nhiều thao tác trong cài đặt máy thở để tối ưu hóa oxy. Một chiến lược là sử dụng biểu đồ dạng sóng để xác định PEEP ”tốt nhất” để tránh sự sụp đổ đường thở cuối thì thở ra, như được mô tả bởi đường cong áp lực – thể tích động nằm ngang dẹt (mức thể tích đạt trị số zero giữa PEEP cài đặt và mức áp lực cao hơn ở đó bắt đầu mở đường thở). Trong khi phần đầu của đường cong thể tích áp lực từ PEEP được cài đặt cho thấy mức tăng chậm và phần thứ hai tăng nhanh về thể tích (Hình 5), điều này sẽ không cho thấy cài đặt PEEP quá thấp. Hiện tượng như vậy là kết quả của lưu lượng nhanh ban đầu trong một hệ thống sức cản cao (ống nội khí quản) trong khi áp lực đường thở tăng nhanh, bởi vì áp lực được đo trong mạch hô hấp ở kết nối ETT chứ không phải ở mức khí quản (Hình 5).
Cai máy từ thông khí cơ học
Theo truyền thống, hỗ trợ thông khí cơ học là một sự pha trộn giữa khoa học và nghệ thuật. Mặc dù có một sự đồng thuận tương đối về việc khi nào nên bắt đầu thở máy, việc ngừng máy thở trong những trường hợp phức tạp có thể khó khăn. Bệnh nhân cai máy thành công từ thở máy là vô cùng quan trọng, bởi vì có nhiều nguy cơ cho bệnh nhân liên quan đến một can thiệp y tế xâm lấn như vậy. Phục hồi bệnh nhân về trạng thái sinh lý của thông khí tự nhiên bình thường là rất quan trọng đối với tiên lượng lâu dài của họ. Có nhiều ý kiến khác nhau về cách thích hợp để bệnh nhân cai máy khi thở máy.[55-57] Sự chậm trễ cai máy ở bệnh nhân từ hỗ trợ thở máy có liên quan đến sự kết hợp của các yếu tố thiết bị, tình trạng bệnh nhân và quyết định của người chăm sóc về tiêu chí cai máy và rút ống.
Thông khí cơ học là cần thiết miễn là tải trên bơm hô hấp còn vượt quá khả năng. Dự đoán sự thành công của bệnh nhân cai máy từ thở máy là một thách thức và chủ yếu dựa trên các dấu hiệu và triệu chứng lâm sàng. Mặc dù một bác sĩ lâm sàng sắc sảo có thể dự đoán thời gian bệnh nhân sẵn sàng bắt đầu cai máy, thất bại rút ống vẫn xảy ra ở 24% trường hợp.
Các nỗ lực đã được thực hiện để đưa ra một số chỉ số dự đoán khách quan có thể giúp xác định thời gian tối ưu để rút ống. Các chỉ số hoặc thông số này đánh giá các chức năng sinh lý khác nhau của hệ thống hô hấp, bao gồm sự khác biệt giữa thành phần đàn hồi và sức cản của rối loạn chức năng phổi; xác định những thay đổi hoặc hạn chế trong lưu lượng khí hít vào và thở ra; xác định cường độ của áp lực đẩy, công và nỗ lực để duy trì thể tích khí lưu thông; và xác định các thay đổi liên tiếp để theo dõi sự tiến triển và giải quyết của quá trình bệnh tiềm ẩn.
Cai máy là một quá trình động thường bắt đầu trong quá trình phục hồi bệnh nhân tại thời điểm được xác định bởi bác sĩ tại giường. Ra quyết định bởi các chuyên gia chăm sóc hô hấp từ lâu đã cho thấy có khả năng làm giảm thời gian thở máy do sự đánh giá bệnh nhân thường xuyên. Quá trình ngừng thở máy phải cân bằng nguy cơ biến chứng do chậm trễ rút ống với nguy cơ biến chứng do ngừng thở máy sớm. Việc sử dụng PPV không xâm lấn là một liệu pháp đầy hứa hẹn sau khi thất bại rút ống, nhưng vẫn được chứng minh là làm giảm nhu cầu đặt NKQ lại hoặc giảm tỷ lệ mắc bệnh và tử vong sau tái đặt NKQ.[58] Về nguyên tắc, hầu hết bệnh nhân nhi đều cần đặt NKQ lại do gắng sức qua nhiều hoặc kiệt sức, việc hỗ trợ thông khí không xâm lấn sau rút NKQ có thể cho phép bệnh nhân được tự chủ trong hô hấp tự phát. Tuy nhiên, việc sử dụng hỗ trợ thông khí không xâm lấn ở bệnh nhân nhi có những thách thức của nó, chẳng hạn như cần đảm bảo kín và hợp tác với bệnh nhân.
Nếu chức năng tim mạch đã hồi phục, việc thất bại sau cai máy có thể được phân loại theo quá tải hô hấp hoặc giảm khả năng hô hấp. Tăng tải hô hấp được đặc trưng bởi tăng tải đàn hồi (bệnh phổi nhu mô, phổi tăng căng phồng và bệnh lý thành ngực hoặc bụng), tăng tải sức cản (chất bài tiết đường thở và tắc nghẽn đường thở), hoặc tăng thông khí phút (phản ứng viêm toàn thân và tăng thân nhiệt và nhiễm toan chuyển hóa). Giảm khả năng hô hấp được đặc trưng bởi giảm hô hấp, rối loạn chức năng cơ hô hấp và suy yếu thần kinh cơ. Những định hướng trong tương lai sẽ đòi hỏi sự phát triển trong thực hành cai máy dựa trên dữ liệu lâm sàng có được từ các thử nghiệm lâm sàng lớn hiện đang xử lý một số lượng đáng kể bệnh nhân nhi.
Phần kết luận
Khi cung cấp thở máy cho bệnh nhân mắc bệnh tim mạch, cần phải hiểu thấu đáo không chỉ sinh lý hô hấp và cơ học mà còn nắm vững huyết động và tương tác tim phổi. Việc sử dụng các thông số máy thở tối ưu trong cài đặt thông khí xâm lấn hoặc NIV là điều cần thiết để cải thiện kết quả của bệnh nhân trong CICU.





