Giới thiệu
Các trường hợp cấp cứu tim mạch cấp tính đòi hỏi sự chăm sóc tích cực nhanh chóng, phức tạp, và tốn nhiều nguồn lực và có nguy cơ tử vong cao, với khoảng bốn triệu lượt khám tại phòng cấp cứu (ER) hàng năm tại Hoa Kỳ [1]. Các dấu ấn sinh học (biomarkers) tim đã nổi lên như một công cụ đáng tin cậy không thể thiếu trong chẩn đoán và điều trị bệnh nhân với bệnh tim cấp tính và là một trong những tiến bộ quan trọng nhất trong y học, cho phép xác định nhanh tình trạng thiếu máu cục bộ, vi hoại tử hoặc hoại tử, rối loạn chức năng tâm thất, và hoạt hóa tan huyết khối nội sinh, phân tầng nguy cơ trong bệnh viện và theo dõi [2]. Mặt khác, mặc dù đã có những tiến bộ to lớn trong việc cải thiện các đặc điểm về phân tích và lâm sàng của chúng, hiện vẫn còn cách xa dấu ấn sinh học lý tưởng, vì tất cả các xét nghiệm đều cho kết quả dương giả và âm giả. Sự nguy hiểm của các kết quả tiềm ẩn này liên quan đến xét nghiệm được thực hiện, mức độ khác biệt giữa kết quả được báo cáo và kết quả thực sự, cũng như khả năng của bác sĩ lâm sàng và nhân viên phòng xét nghiệm để nhận ra những trở ngại này [3].
Mặc dù các dấu ấn sinh học đang được sử dụng để làm tăng kỹ năng và phán đoán của bác sĩ, nhưng việc sử dụng nó phải được hỗ trợ bởi sự nhạy cảm thường gặp và bối cảnh lâm sàng của mỗi bệnh nhân. Ngoài ra, dấu ấn sinh học không nên được sử dụng như các xét nghiệm độc lập để chẩn đoán lâm sàng mà là các công cụ bổ sung để ra quyết định lâm sàng [4]. Lý luận Bayes là một phương pháp heuristic (để tự khám phá) cho phép các bác sĩ lâm sàng kết hợp suy nghĩ ban đầu của họ về tình trạng của bệnh nhân với kết quả xét nghiệm để xác định xác suất nghi ngờ chẩn đoán sau xét nghiệm (giữ và điều chỉnh) [4]. Điều cần thiết là các bác sĩ lâm sàng biết về các đặc điểm hoạt động phân tích và lâm sàng của dấu ấn sinh học và cách tích hợp chúng với lý luận Bayes để hỗ trợ và tối ưu hóa việc ra quyết định lâm sàng hàng ngày. Do đó, với nhiều dấu ấn sinh học hiện có hoặc sắp có, sự hiểu biết về cơ sở của dấu ấn sinh học và vai trò của chúng trong chăm sóc tim mạch là quyết định. Theo đó, trong chương này, chúng tôi sẽ thảo luận về các nguyên tắc cơ bản để sử dụng hợp lý các dấu ấn sinh học tim tập trung vào các đặc điểm tiền-phân tích và phân tích của chúng, cũng như các đặc điểm về việc sử dụng trên lâm sàng. Chủ yếu, chúng tôi sẽ tập trung vào các troponin tim (cTn), natriuretic peptide (NP), và D-dimer (DD) và tiện ích của chúng tại ER. Ngoài ra, chúng tôi sẽ giải quyết các khái niệm về giá trị tiên đoán và tỷ số khả dĩ là các thành tố thiết yếu của lý luận Bayes và ứng dụng của nó trong ER.
Phạm vi vấn đề
Trong các ER quá đông, nhu cầu về thời gian quay vòng nhanh chóng làm cho thực hành không phù hợp về các bộ xét nghiệm ban đầu để loại bỏ các quá trình tuần tự tốn thời gian (đánh giá lâm sàng sau đó là xét nghiệm) [4]. Do đó, dấu ấn sinh học tim thường được chỉ định trước khi bác sĩ có mặt thậm chí đánh giá bệnh nhân thông qua khám lâm sàng tỉ mỉ và bệnh sử chi tiết [4]. Việc sử dụng bừa bãi các dấu ấn sinh học ở nhiều bệnh nhân mang lại một số lượng lớn kết quả dương tính giả [5]. Do đó, các bác sĩ lâm sàng phải làm quen với các đặc điểm tiền-phân tích và phân tích của dấu ấn sinh học, cũng như các đặc điểm ứng dụng trên lâm sàng của chúng và phải luôn luôn sử dụng chúng kết hợp với các vũ khí chẩn đoán có sẵn, đặc biệt là phán đoán lâm sàng. Tuy nhiên, những yếu tố này ảnh hưởng đến suy nghĩ của chúng ta về một bệnh nhân nào đó như thế nào [4].
Đặc điểm hoạt động tiền-phân tích (tiền kiểm)
| Bảng 4.1 Các yếu tố quyết định đặc điểm tiền-phân tích của dấu ấn sinh học | |
| Thông số | Ví dụ |
| Thu thập và chất lượng. | Đường lấy mẫu là động hoặc tĩnh mạch, tán huyết, máu cục, mỡ trong máu. |
| Quá trình. | Không đủ thể tích, ống chứa không chính xác, chất bảo quản hết hạn. |
| Lưu trữ. | Không đủ hoặc đông lạnh kéo dài. |
Làm thế nào các mẫu (xét nghiệm) được lấy là rất quan trọng đối với đo lường mọi chất phân tích [6]. Khái niệm “giai đoạn tiền-phân tích” mô tả tất cả các hành động và khía cạnh của quy trình chẩn đoán trong phòng xét nghiệm y khoa và được công nhận là phần dễ gây ảnh hưởng nhất trong toàn bộ quá trình xét nghiệm [7, 8]. Các yếu tố quyết định của giai đoạn tiền-phân tích được liệt kê trong Bảng 4.1. Các vấn đề tiền-phân tích có thể phát sinh tại bất kỳ thời điểm nào trước khi làm xét nghiệm, bao gồm (nhưng không giới hạn ở) việc thu thập và chất lượng, xử lý, vận chuyển, phân tách, và lưu trữ mẫu [3], can thiệp vào kết quả của xét nghiệm. Vấn đề này có thể không quan trọng đối với các khảo sát có độ nhạy thấp; tuy nhiên, trong ER, nơi mà việc đánh giá sự thay đổi biểu hiện của dấu ấn sinh học tim là rất quan trọng, thì vấn đề này trở nên có liên quan [6].
Đặc điểm của hoạt động phân tích (quá trình phân tích mẫu thử)
Bác sĩ lâm sàng cần phải làm quen với các khái niệm độ nhạy và độ đặc hiệu khi phân tích một xét nghiệm. Độ nhạy phân tích biểu thị cho lượng chất nhỏ nhất trong mẫu có thể được đo chính xác bằng một xét nghiệm và được biểu thị bằng nồng độ (a.k.a giới hạn phát hiện (LoD)). Độ đặc hiệu phân tích đề cập đến khả năng của một xét nghiệm để đo trên sinh vật hoặc chất cụ thể, chứ không phải là các sinh vật hoặc chất khác, trong một mẫu [9]. Cả hai đều phụ thuộc vào đặc điểm của thiết bị và phương pháp được sử dụng. Bảng 4.2 cho thấy các đặc điểm phân tích của dấu ấn sinh học.
| Bảng 4.2 Đặc điểm phân tích của các dấu ấn sinh học [9] | |
| Đặc điểm | Định nghĩa |
| Độ nhạy. | Khả năng phát hiện nồng độ thấp của một chất nhất định trong mẫu sinh học. Còn được gọi là “khả năng của xét nghiệm” để phát hiện sự thay đổi về nồng độ. Nồng độ có thể phát hiện càng thấp thì độ nhạy phân tích càng lớn. Thay đổi có thể phát hiện càng nhỏ thì độ nhạy phân tích càng lớn. |
| Độ đặc hiệu. | Khả năng xác định duy nhất một chất hoặc sinh vật đích chứ không phải các chất hoặc sinh vật tương tự nhưng khác nhau chẳng hạn natriuretic peptide loại B (BNP) chứ không phải N-terminal proBNP (NT-proBNP) trong mẫu máu hoặc mẫu dịch tiết. Phân tích không đặc hiệu tạo ra kết quả dương tính khi mẫu thử thực sự âm tính với dấu ấn sinh học chính xác. Trong các xét nghiệm phân tích có độ nhạy cao, sự thay đổi nhỏ nhất gây ra kết quả xét nghiệm dương tính giả trong một xét nghiệm mà “độ đặc hiệu rất cao”. |
Đặc điểm hoạt động lâm sàng (khả năng ứng dụng của kết quả)
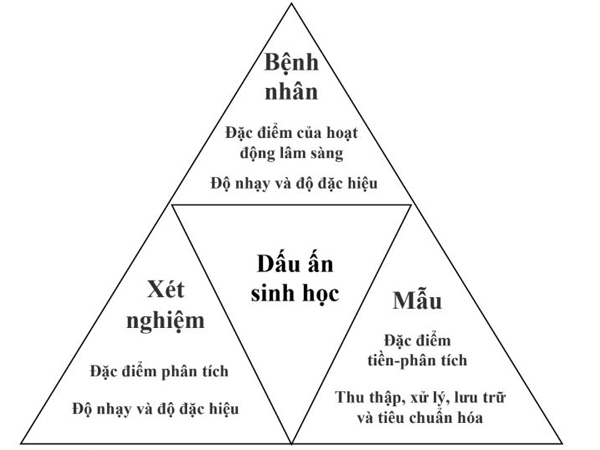
Độ nhạy và độ đặc hiệu là đặc điểm hoạt động lâm sàng của bất kỳ xét nghiệm nào. Độ nhạy đề cập đến tỷ lệ xác định chính xác một đối tượng mắc bệnh (tỷ lệ dương tính thật (TPR)); tương tự như vậy, độ đặc hiệu đề cập đến tỷ lệ xác định chính xác một đối tượng không có bệnh (tỷ lệ âm tính thật (TNR)). Độ nhạy và độ đặc hiệu thay đổi theo giá trị ngưỡng được chọn cho xét nghiệm chẩn đoán và không phải là bản thân xét nghiệm đã như thế mà phụ thuộc rất nhiều vào bối cảnh lâm sàng [10]. Dấu ấn sinh học lý tưởng xác định chính xác tất cả các đối tượng mắc bệnh và xác định chính xác tất cả các đối tượng không mắc bệnh [11] (Bảng 4.3). Các bác sĩ lâm sàng trong ER nên quen thuộc với các đặc điểm thể hiện trong Bảng 4.3, vì họ đang dẫn đầu một nhóm đa chuyên khoa có nhịp độ nhanh trong các tình huống quan trọng mà mỗi giây đều có giá trị (Hình 4.1).
| Bảng 4.3 Đặc điểm hoạt động xét nghiệm lâm sàng. | |||
| Đặc điểm | Định nghĩa | Giải quyết câu hỏi | Công thức |
| Độ nhạy hoặc TPR. | Khả năng xác định chính xác những người mắc bệnh. | Khả năng xét nghiệm phát hiện những đối tượng thật sự có bệnh là bao nhiêu? | TP:(TP+FN). |
| Độ đặc hiệu hoặc TNR. | Khả năng xác định chính xác những người không mắc bệnh. | Khả năng xét nghiệm phát hiện những đối tượng thật sự không bệnh là bao nhiêu? | TN:(TN+FP). |
TPR=tỷ lệ dương tính thật; TNR=tỷ lệ âm tính thật; dương tính thật (TP), bệnh nhân mắc bệnh và xét nghiệm dương tính; dương tính giả (FP), bệnh nhân không bệnh và xét nghiệm dương tính; âm tính thật (TN), bệnh nhân không bệnh và xét nghiệm âm tính; âm tính giả (FN), bệnh nhân có bệnh nhưng xét nghiệm âm tính.
sinh học
Nguyên tắc sử dụng dấu ấn sinh học tim thích hợp tại ER
- Các dấu ấn sinh học tim không phải là dấu hiệu của bệnh mà là quá trình sinh lý bệnh liên quan đến các thực thể lâm sàng khác nhau; do đó, chúng phải được sử dụng cùng với phán đoán lâm sàng đầy đủ và các công cụ chẩn đoán khác hiện có [12].
- Để tối đa hóa khả năng chẩn đoán và tiên lượng của dấu ấn sinh học, chúng phải được phân tích như là các biến định lượng. Ví dụ, một biểu hiện cTn gấp 50 lần giới hạn trên bình thường có PPV cao hơn nhiều về sự xuất hiện của nhồi máu cơ tim (MI) so với mức ngay trên giới hạn trên [6].
- Cách tiếp cận có hệ thống trước tiên xem xét một xét nghiệm có độ nhạy cao/độ đặc hiệu thấp và sau đó sử dụng xét nghiệm có độ nhạy thấp/độ đặc hiệu cao. Cách này gần như tất cả các dương tính giả có thể được xác định chính xác là không bệnh.
Các troponin tim
Do độ đặc hiệu và độ nhạy lâm sàng vượt trội so với các dấu ấn sinh học khác (như creatine kinase, lactate dehydrogenase, và myoglobin) nên các troponin tim đã được sử dụng thường quy trong thực hành lâm sàng [17], những dấu ấn sinh học này được ESC và AHA/ACC xem là tiêu chuẩn vàng để phát hiện thiếu máu cục bộ, vi hoại tử, hoặc hoại tử, với ít nhất một giá trị bách phân vị thứ 99 trên giới hạn tham chiếu trên [13-16]. Khuyến cáo này cho biết thực tế rằng các phương pháp xét nghiệm để kiểm tra các troponin tim (cTn) đã được cải thiện rõ rệt trong hai thập kỷ qua, dẫn đến LoD thấp hơn và độ chính xác của xét nghiệm được cải thiện [4] (Hình 4.2). Tuy nhiên, những tiến bộ này nên được các bác sĩ tích hợp với lý luận lâm sàng tốt để biết khi nào cần đến, cũng như giải thích kết quả chính xác, đặc biệt vì các xét nghiệm có độ nhạy cao cho phép chúng tôi xác định nhiều lý do của sự gia tăng cTn và do đó làm giảm tính đặc hiệu của bất kỳ sự gia tăng nào đối với bệnh tim thiếu máu cục bộ không ổn định [6].
Sinh lý học
cTn là một phức hợp gồm ba protein là troponin C, T và I, điều hòa sự kích thích và co cơ vân. cTnI và cTnT có các chuỗi acid amin đặc trưng cho mô tim, mặc dù đôi khi cTnT cũng được tìm thấy trong cơ xương có bệnh lý [4, 17]. Sau khi các tế bào cơ tim bị tổn thương (nghĩa là thiếu máu cục bộ), nồng độ các protein này tăng lên trong máu, làm cho chúng trở thành các chỉ dấu hữu ích của thiếu máu cục bộ, vi hoại tử, hoặc hoại tử mà không phụ thuộc vào nguyên nhân gây tổn thương [17] (Hình 4.3).
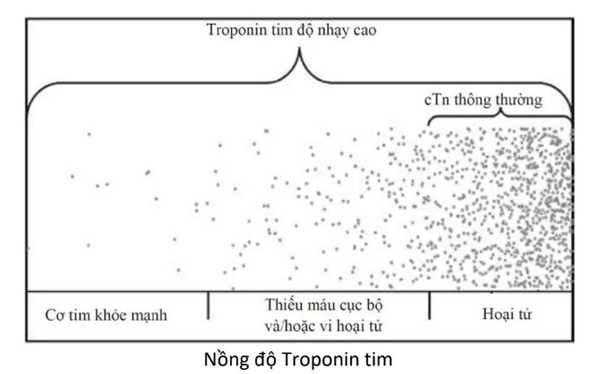
![Hình 4.3 Biểu hiện troponin và bối cảnh sinh lý bệnh. Xét mô hình gia tăng và khả năng MI dựa trên biểu hiện cTn. (Chuyển thể từ Westermann và cộng sự [17]).](https://www.healcentral.org/wp-content/uploads/2020/06/dau_an_sinh_hoc_2.jpg)
Xem xét tiền-phân tích
Các yếu tố tiền-phân tích ảnh hưởng đến cTn bao gồm tán huyết và heparin, làm kết quả dương tính giả [18]. Ngoài ra, có thể có sự khác biệt giữa các mẫu huyết thanh và huyết tương, độc lập với heparin [6]. Mặt khác, việc hiệu chuẩn sai số, trục trặc máy phân tích, thuốc thử hư hỏng, vận chuyển dụng cụ, và pha loãng mẫu không phù hợp, tất cả đều liên quan đến phòng xét nghiệm hóa sinh, cũng có thể ảnh hưởng trực tiếp đến năng lực của bác sĩ lâm sàng và chăm sóc bệnh nhân [18]. Bảng 4.4 mô tả thêm các yếu tố tiền-phân tích ảnh hưởng đến cTn.
| Bảng 4.4 Các yếu tố tiền-phân tích ảnh hưởng đến cTn [6, 18, 19] | |
| Yếu tố | |
| Lưu trữ. | HS-cTnT: ổn định trong ít nhất 24 giờ trong máu toàn phần ở nhiệt độ phòng. Hiện tại không có loại ống chứa lý tưởng để giảm thiểu sự không đồng nhất, nhưng ống chứa có chất bất hoạt kháng thể dị thể có thể hữu ích nhưng làm tăng chi phí xét nghiệm. |
| Mẫu xét nghiệm. | Tán huyết, mẫu huyết thanh hoặc huyết tương, mẫu có heparin hoặc không heparin hóa. |
| Tiêu chuẩn hóa. | Hiệu chuẩn sai lệch, trục trặc máy phân tích, thuốc thử hư hỏng, vận chuyển dụng cụ, và pha loãng mẫu không phù hợp. |
Đặc điểm phân tích
Thuật ngữ “xét nghiệm độ nhạy cao” đề cập đến việc tăng khả năng phát hiện nồng độ thấp hơn so với các xét nghiệm thông thường có hệ số biến thiên (CV) ≤10%, tùy thuộc từng xét nghiệm, tăng khả năng xác định sự khác biệt nhỏ về cTn theo thời gian [4, 20] (Hình 4.2). Một tổng quan về các xét nghiệm chọn lọc hiện có, LoD cụ thể của chúng, và giá trị phân vị thứ 99 được đưa ra bởi Westermann và cộng sự [17]. Mặt khác, mặc dù các xét nghiệm tại giường có tầm quan trọng lâm sàng lớn, vì việc hoàn thành phân loại các bệnh nhân đau ngực trong ER sẽ khả thi trong vòng vài phút [17], không nên sử dụng xét nghiệm tại giường cho các phép đo cTn nối tiếp vì sự không chính xác trong số các xét nghiệm này có thể làm xuất hiện sự sai lệch tăng hoặc giảm nồng độ cTn [4, 20]. Tuy nhiên, mỗi trung tâm nên xác định giá trị phân vị thứ 99 cho xét nghiệm đã sử dụng, từ hướng dẫn của nhà sản xuất thử nghiệm hoặc tài liệu tham khảo của phòng xét nghiệm.
Mặt khác, ở những bệnh nhân mắc hội chứng mạch vành cấp tính (ACS), tỷ lệ tự kháng thể cTnI là ~ 20%. Những điều này ảnh hưởng đến hiệu năng của xét nghiệm với kết quả âm tính giả và dương tính giả, làm trì hoãn chẩn đoán và điều trị bệnh nhân ACS. Mặc dù các nghiên cứu điều tra sự ảnh hưởng của tự kháng thể đã bị giới hạn về cỡ mẫu và không thể xác định được ý nghĩa lâm sàng, nhưng các bác sĩ lâm sàng trong ER nên xem xét khả năng này khi kết quả xét nghiệm không phù hợp với biểu hiện lâm sàng [17]. Trong trường hợp của cTn, tỷ lệ xét nghiệm dương tính giả được ước tính là 3% dân số nói chung [18]. Khuyến cáo của FDA hiện tại thiết lập ngưỡng cụ thể theo giới tính là 14 ng/L đối với nữ, 22 ng/L đối với nam và 19 ng/L cho cả hai giới đối với cTnT độ nhạy cao [17, 21].
Liên quan lâm sàng
Khái niệm MI nên được sử dụng khi có bằng chứng về vi hoại tử hoặc hoại tử (một giá trị vượt quá phân vị thứ 99 giới hạn tham chiếu trên) trong bối cảnh lâm sàng phù hợp với thiếu máu cục bộ cơ tim [14, 16]. Tuy nhiên, các xét nghiệm có độ nhạy cao có thể phát hiện troponin trong máu của bệnh nhân không bị vi hoại tử hoặc hoại tử, có lẽ do sự thay đổi tế bào cơ tim bình thường hoặc hình thành các exosome giải phóng một lượng nhỏ troponin tự do vào máu [4]. Giống như bệnh nhân bị rối loạn chức năng thận, tăng HS-cTn nhẹ thường thấy ở những bệnh nhân cao tuổi không MI, COPD, mất trí nhớ, bệnh mạch máu ngoại biên, cũng như ở những bệnh nhân phẫu thuật (không phải tim) mà kết cục xấu đi được quan sát so với những người mắc bệnh không có biểu hiện HS-cTn [22-25]. Mặc dù các cơ chế không được biết rõ, nhưng chúng có thể gợi ý về tổn thương tế bào cơ tim mãn tính thứ phát sau các biến cố dưới lâm sàng của bệnh động mạch vành [26]. Một cách để phân biệt biểu hiện HS-cTn ở bệnh nhân ổn định và không ổn định là phân tích kiểu gia tăng các giá trị. Một số bệnh nhân bị đau thắt ngực ổn định và HF có tăng troponin mạn tính như là biểu hiện dưới lâm sàng của một biến cố tim mạch [6, 17]. Một sự thay đổi troponin đáng kể, phù hợp với ACS, có thể được biểu thị bằng sự thay đổi (Δ, %) tuyệt đối (Δ, ng/L) hoặc tương đối (%), trong đó sự thay đổi tuyệt đối cho thấy lợi thế chẩn đoán [27]. Hình 4.3 cho thấy biểu hiện troponin trong bối cảnh sinh lý bệnh của vi hoại tử hoặc hoại tử cơ tim.
Một số tác giả cho rằng sự thay đổi 20% với một số xét nghiệm và một sự thay đổi 30% vớ những xét nghiệm khác là rất đáng kể [6]. Từ góc độ chẩn đoán, có khuyến cáo sử dụng cTn như một công cụ định lượng và tránh diễn giải kết quả theo kiểu nhị phân, tức là sử dụng thuật ngữ “cTn dương tính”. Ở nồng độ cTn cao hơn, khả năng MI cao hơn; ở nồng độ thấp hơn, khả năng là thấp hơn [28]. Mặc dù mối quan hệ mạnh mẽ này giữa nồng độ và khả năng xảy ra biến cố, nhưng các bác sĩ lâm sàng phải xem xét khả năng phân tích “dương giả”, đặc biệt khi có sự không phù hợp đáng chú ý giữa các phép đo cTn và biểu hiện lâm sàng. Đối với kịch bản này, Twerenbold và cộng sự đề xuất lưu đồ sau [28].
Bác sĩ nên xét nghiệm lại với cùng một xét nghiệm, nếu có thay đổi đáng kể, và MI phải được loại trừ bằng hình ảnh hoặc chiến lược xâm lấn.
- Không có bằng chứng về MI và các phép đo cTn nối tiếp vẫn nằm dưới phân vị thứ 99 của giới hạn tham chiếu trên: dương tính giả do không thể lặp lại ngoại lệ.
- Nếu không có thay đổi sau khi xét nghiệm lại, nên đo cTn bằng cách sử dụng xét nghiệm thay thế (nếu có). Trong trường hợp cTn không phù hợp, hãy đánh giá khả năng ảnh hưởng của quá trình phân tích.
- Nếu phù hợp, hoại tử mạn tính hoặc vi hoại tử phải được nghi ngờ và nên được đánh giá bằng các kỹ thuật hình ảnh.
Tình trạng lâm sàng liên quan đến tăng biểu hiện của cTn
Bất kể nguyên nhân, sự gia tăng các giá trị cTn có liên quan đến kết cục lâm sàng xấu trong hầu hết các tình trạng lâm sàng như ở bệnh nhân MI, suy tim mạn, thuyên tắc phổi (PE), hoặc tăng áp động mạch phổi [12]. Các phép đo cTn bất thường ở bệnh nhân đau thắt ngực ổn định gợi ý các biến cố cấp tính dưới lâm sàng [29]. Bảng 4.5 cho thấy chẩn đoán phân biệt đối với việc cTn tăng.
| Bảng 4.5 Các tình trạng lâm sàng liên quan đến tăng troponin tim [20, 30] | |
| Hệ thống | Tình trạng lâm sàng |
| Tim mạch. | ACS, PE, PAH nặng, đụng giập cơ tim do chấn thương, cắt đốt, đặt tạo nhịp, cấy máy chuyển nhịp, máy phá rung, CS, chuyển nhịp tim, sinh thiết nội tâm mạc, HF cấp và mãn, bóc tách động mạch chủ, bệnh van động mạch chủ, bệnh cơ tim phì đại, rối loạn nhịp tim nhanh và chậm, hội chứng Takotsubo, sau PCI, hủy cơ vân, viêm cơ tim hoặc viêm nội/ngoại tâm mạc, bệnh Kawasaki, can thiệp đóng thông liên nhĩ. |
| CNS | CVA cấp, xuất huyết dưới nhện. |
| Phổi | Suy hô hấp |
| Thận | Suy thận |
| Chuyển hóa/ viêm | Bỏng, đặc biệt khi tổng BSA ≥30%, nhiễm khuẩn huyết, DM, độc tính của thuốc (tức là, adriamycin, 5-fluorouracil, Herceptin, nọc rắn). Suy giáp, các bệnh thâm nhiễm bao gồm amyloidosis, hemochromatosis, sarcoidosis, và xơ cứng bì, kiệt sức/tập thể dục nặng, các bệnh lý viêm, parvovirus B19, sarcoid, tiêm phòng bệnh đậu mùa, sau phẫu thuật lớn không phải tim. |
ACS, hội chứng mạch vành cấp; PE, thuyên tắc phổi; PAH, tăng áp phổi; CS, phẫu thuật tim; HF, suy tim; PCI, can thiệp vành qua da; CNS, hệ thần kinh trung ương; CVA, tai biến mạch máu não; BSA, diện tích bề mặt cơ thể; DM, đái tháo đường.
| Bảng 4.6 Lưu đồ ESC 0/1 h và 0/3 h để phân loại bệnh nhân nghi ngờ ACS [28] | ||
| HS-cTnT | HS-cTnI | |
| 0/1 h | ||
| Loại trừ | 0 h <12 ng/L VÀ 1 h thay đổi <3 ng/L | 0 h <5 ng/L VÀ 1 h thay đổi <2 ng/L |
| Xác nhận | 0 h ≥52 ng/L HOẶC 1 h thay đổi ≥5 ng/L | 0 h ≥52 ng/L HOẶC 1 h thay đổi ≥6 ng/L |
| 0/3 h | ||
| Loại trừ | 0 h và 3 h <14 ng/L | 0 h và 3 h <26 ng/L |
HS-cTnT troponin T tim độ nhạy cao, HS-cTnI troponin I tim độ nhạy cao.
Lưu đồ chẩn đoán và thang điểm tiên đoán
Một số chiến lược dựa trên HS-cTn với các xét nghiệm nối tiếp. Hai trong số đó, lưu đồ 0/1 h và lưu đồ 0/3 h, được ESC khuyến nghị với khuyến cáo Loại I với giá trị tiên đoán âm (NPV) từ 99.1% đến 100% và 99.6% đến 100%, tương ứng [28]. Tuy nhiên, các chiến lược này nên được xem là chiến lược phân loại thay vì chiến lược chẩn đoán xác định, bởi vì các xét nghiệm hình ảnh bổ sung, chẳng hạn như chụp mạch vành xâm lấn, nghiệm pháp gắng sức, siêu âm tim, hoặc chụp cắt lớp vi tính mạch vành, là bắt buộc để chẩn đoán xác định [28]. Bảng 4.6 cho thấy các tiêu chí xác nhận và loại trừ của ESC để đánh giá nhanh bệnh nhân có tiềm năng ACS tại ER.
Thang điểm nguy cơ lâm sàng cung cấp một cách tiếp cận khác để xác định bệnh nhân có nguy cơ MI thấp có thể phù hợp để xuất viện sớm. Việc bổ sung các thang điểm GRACE, TIMI, HEART và EDACS vào lưu đồ ESC 3 h cho thấy có lợi trong phân tầng nguy cơ. Tuy nhiên, thang điểm lâm sàng không cải thiện khả năng của các lưu đồ áp dụng nồng độ cTn thấp vào phân tầng nguy cơ, chẳng hạn như thang điểm STEACS cao hoặc lưu đồ ESC 0/1 h [31].
Khó khăn, thách thức, và hạn chế tại ER
Các xét nghiệm HS-cTn cải thiện và làm tăng tốc độ quản lý sớm các bệnh nhân nhập ER với nghi ngờ ACS. Trong thực hành hàng ngày, các tiêu chí để chỉ định xét nghiệm cTn trong ER ít nghiêm ngặt hơn so với trong nghiên cứu lâm sàng; do đó, các bác sĩ lâm sàng phải xem xét bối cảnh lâm sàng của từng bệnh nhân [4]. Xét nghiệm cTn bừa bãi có thể khiến các bác sĩ lâm sàng đi đến kết luận và điều trị đặc hiệu cho những bệnh nhân mà họ không được hưởng lợi ích và có thể bị tổn hại [19, 26]. Nhiều yếu tố khác ngoài MI có thể gây thiếu máu cục bộ, hoại tử, hoặc vi hoại tử, và do đó, tăng HS-cTn nhẹ có thể được quan sát thấy ở bệnh suy tim và suy thận, ngộ độc thuốc, COPD, bệnh động mạch ngoại biên, bệnh mất trí nhớ, bệnh nhân phẫu thuật không phải tim, v.v. Trong những trường hợp này, các phép đo nối tiếp là chìa khóa để phân biệt những thay đổi động của các biến cố dưới lâm sàng hoặc cấp tính. Ngoài ra, các bác sĩ lâm sàng nên chú ý đến nhiều yếu tố có thể ảnh hưởng đến kết quả xét nghiệm, vì vậy lý luận lâm sàng và quy trình chuẩn hóa là nền tảng để tối đa hóa khả năng của dấu ấn sinh học, giúp tăng độ an toàn cho bệnh nhân và giảm đáng kể thời gian nằm trong ER.
Natriuretic peptide, căng thẳng tim, và suy tim
Natriuretic peptide (NP) có giá trị lâm sàng rất lớn trong chẩn đoán HF không chỉ ở bệnh nhân khó thở không rõ nguyên nhân; bệnh nhân với bệnh tim mà không có biểu hiện lâm sàng, mà còn ở những người có nguy cơ HF; và ở những bệnh nhân khỏe mạnh nhưng có nguy cơ cao HF. Mặc dù NP nhĩ là NP đầu tiên được sàng lọc từ sự kéo căng mô tim đã được xác định và nghiên cứu ở bệnh nhân HF, nhưng do tính không ổn định và các vấn đề về phân tích khác, nên nó đã sớm được thay thế bằng BNP và đoạn prohormone của BNP, NT-proBNP, cả hai peptide đều có nguồn gốc chủ yếu từ tâm thất [32]. Các NP đã được đánh giá thành công trong việc tiên đoán các biến chứng, khả năng sống sót, và tái nhập viện trong HF, và đặc biệt là MR-proANP (mid-regional pro-atrial natriuretic peptide) để tiên đoán kết cục lâu dài [33]. Tuy nhiên, phần này chỉ tập trung vào NT-proBNP và BNP.
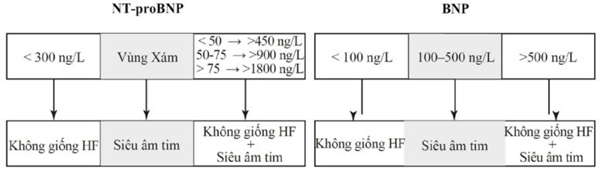
Ở bệnh nhân người lớn, nồng độ BNP >100 ng/L được coi là bất thường; bằng chứng gần đây cho thấy rằng một khoảng tham chiếu <50 ng/L sẽ làm tăng độ nhạy lâm sàng và giá trị tiên đoán âm. Ví dụ, ở phụ nữ không mang thai và phụ nữ mang thai, cũng như ở trẻ sơ sinh khỏe mạnh, khoảng tham chiếu lần lượt là <20 và <34 ng/L [34]. Do đó, vẫn còn những câu hỏi chưa được trả lời, chẳng hạn như nếu nồng độ từ 50 đến 100 ng/L là phản ánh của suy thất dưới lâm sàng. Mặt khác, khoảng tham chiếu của NT-proBNP là 300 ng/L, với giá trị tiên đoán âm là 90-98% (trong một phân tích gộp) để loại trừ HF [35].
Sinh lý học
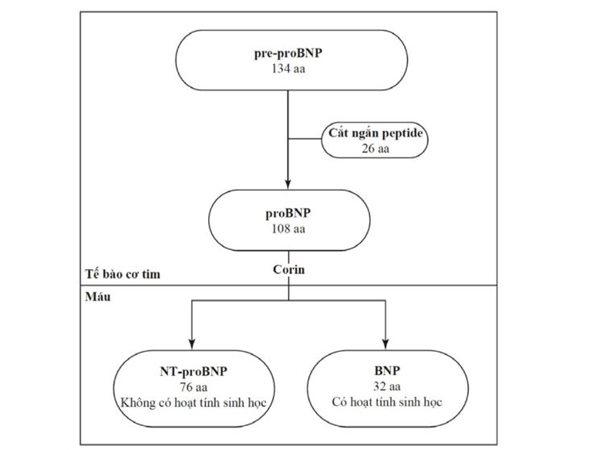
Các cơ chế chính của việc tăng BNP là sự gia tăng căng thẳng thành cơ tim thứ phát do tình trạng quá tải thể tích hoặc áp lực [36]. BNP có nguồn gốc từ pre- proBNP, chứa chuỗi peptide tín hiệu ở đầu N-terminal. Sau khi peptide tín hiệu bị cắt đi, proBNP tiếp tục được tách protein thành một đoạn N-terminal không hoạt tính (NT-proBNP) và một hormone peptide có hoạt tính sinh học là BNP [37]. Thời gian bán hủy của BNP là 20 phút, trong khi NT-proBNP là 120 phút, điều này giải thích tại sao giá trị NT-proBNP huyết thanh cao hơn khoảng sáu lần so với giá trị BNP, mặc dù cả hai phân tử đều được giải phóng theo tỷ lệ tương đương [38] (Hình 4.4). Quá trình này đòi hỏi sự tổng hợp mới phải được phóng thích ra với số lượng đáng kể và có hoạt tính sinh học trong việc kích thích bài niệu do natri và lợi tiểu, ức chế hệ thống renin-angiotensin-aldosterone và hệ thần kinh giao cảm, làm giãn cơ trơn mạch máu và phổi, gây giãn mạch. Tăng tính thấm nội mô, làm tăng ly giải lipid trong mô mỡ, và ức chế tái cấu trúc tim và mạch máu và tác dụng bảo vệ tế bào [2].
Xem xét tiền-phân tích
Bác sĩ lâm sàng phải biết cách chuẩn bị lấy mẫu máu, cách lấy mẫu, và một số nguyên tắc cơ bản của phân tích để diễn giải xét nghiệm thích hợp [2]. Sự thoái hóa ly giải protein của phân tử BNP dường như xảy ra ngay khi máu được rút vào bơm tiêm. Sự ổn định của mẫu máu dường như phụ thuộc vào phương pháp lấy, rõ ràng là do sự ổn định khác nhau của các epitope là đích các xét nghiệm khác nhau. Hơn nữa, BNP được báo cáo là không ổn định khi được thu thập trong ống thủy tinh do kích hoạt kallikrein của con đường đông máu ngoại sinh, nhưng hiện tượng này có thể phụ thuộc vào đặc tính của kháng thể được sử dụng trong phương pháp xét nghiệm. NT-proBNP dường như tương đối ổn định trong quá trình lưu trữ mẫu máu. Đối với các xét nghiệm BNP, EDTA huyết tương là mẫu thử phù hợp duy nhất [37]. Bảng 4.7 tóm tắt các yếu tố có thể ảnh hưởng đến kết quả xét nghiệm.
| Bảng 4.7 Các yếu tố tiền-phân tích ảnh hưởng đến NT-proBNP và BNP [2] | |
| Yếu tố | |
| Mẫu máu | NT-pro-BNP: Ổn định ở nhiệt độ phòng trong ít nhất 2 ngày. Độ ổn định lâu dài là ít nhất 4 tháng ở -20°C và ít nhất 1 năm ở -80°C. BNP: Sự thoái hóa ly giải protein của phân tử BNP xảy ra ngay khi máu được thu thập. Xét nghiệm phụ thuộc. Ổn định trong ít nhất 4 giờ ở nhiệt độ phòng. Về lâu dài, các giá trị giảm dần, thậm chí ở -80°C. Sự không ổn định của mẫu huyết tương EDTA với nồng độ BNP cao đã được báo cáo ngay cả ở -80°C. Để an toàn, nên thêm một loại cocktail chất ức chế protease bao gồm các chất ức chế protease đặc hiệu kallikrein và serine. |
| Lưu trữ | NT-pro-BNP: Huyết thanh hoặc huyết tương heparin là sự lựa chọn, thu thập trong ống thủy tinh hoặc nhựa đều được chấp nhận. Huyết tương EDTA cho độ lệch âm 8-10% so với huyết thanh. |
| Tiêu chuẩn hoá | Các xét nghiệm hiện có không được chuẩn hóa, điều đó có nghĩa là kết quả không thể so sánh ở từng bệnh nhân. Hơn nữa, giá trị BNP và NT-proBNP trong mỗi mẫu có thể khác nhau giữa các xét nghiệm sử dụng cùng một kháng thể do hiệu ứng ma trận. |
Đặc điểm phân tích
Trong bối cảnh cấp tính, các điều kiện lấy mẫu máu của NP không cần phải xem xét đặc biệt. Các xét nghiệm hiện có không được chuẩn hóa, điều đó có nghĩa là kết quả không thể so sánh ở từng bệnh nhân. Hơn nữa, giá trị BNP và NT-proBNP trong mỗi mẫu có thể khác nhau giữa các xét nghiệm sử dụng cùng một kháng thể do hiệu ứng ma trận [2]. Các đặc điểm của từng kiểu xét nghiệm phụ thuộc vào nhà sản xuất, và các khuyến cáo chi tiết đã được ban hành bởi International Federation of Clinical Chemistry and Laboratory Medicine (IFCC) Committee on the Standardization of Markers of Cardiac Damage (C-SMCD) và the National Academy of Biochemistry (NACB) [37, 39]. Liên quan đến sự khác biệt giới tính, dữ liệu cho thấy việc sản xuất và phóng thích NT-proBNP bị giảm bởi testosterone và tăng bởi estrogen [40]. Mặc dù có một số tình trạng lâm sàng liên quan đến tăng peptide như tuổi cao, suy thận, tai biến mạch máu não, bệnh nguy kịch, tình trạng cung lượng cao, v.v., điều quan trọng là phải cân nhắc việc rối loạn chức năng tâm thất thứ phát là cơ chế chính [41]. Ngoài ra, việc sử dụng các chất ức chế neprilysin mới, chẳng hạn như sacubitril-valsartan, dẫn đến gia tăng giá trị BNP do thuốc bằng cách làm giảm sự thanh thải và ức chế hệ thống renin- angiotensin-aldosterone bằng cách ức chế thụ thể angiotensin II [35]. Đáng chú ý, các loại thuốc này không ảnh hưởng đến nồng độ NT-proBNP.
Mặt khác, một số tình trạng có liên quan đến nồng độ NP thấp hơn dự kiến: HF phân suất tống máu bảo tồn (HFpEF) so với HF phân suất tống máu giảm, béo phì (với độ nhạy thấp hơn) [41], người da đen có liên quan với nồng độ thấp hơn, mà không liên quan đến lâm sàng, có khả năng do sự ức chế tổng hợp hoặc giải phóng natriuretic peptide. Hơn nữa, các tình trạng khác liên quan đến biểu hiện NP thấp hơn dự kiến bao gồm phù phổi chớp nhoáng (<1 h), phù phổi cấp thứ phát do đứt cơ nhú kèm hở van hai lá (khởi phát <2 h), và viêm cơ tim thất phải thứ phát do lupus ban đỏ hệ thống. Ngoài ra, ở PE với rối loạn chức năng thất phải nghiêm trọng (khởi phát triệu chứng <1 h), biểu hiện BNP có thể giảm, điều này nhấn mạnh rằng thời gian từ lúc xuất hiện triệu chứng đến khi làm xét nghiệm (<2 h) cũng có thể ảnh hưởng đến kết quả, vì đó có thể là biểu hiện về mặt di truyền của BNP đã không đủ thời gian, giữa yếu tố kích hoạt ban đầu của sự gia tăng căng thành tâm thất và đo nồng độ BNP, vì thời gian bán hủy của BNP là 23 phút, và do đó, cần khoảng 2 giờ để phản ánh đầy đủ các thay đổi do rối loạn chức năng RV [42].
Liên quan lâm sàng
Việc bổ sung xét nghiệm BNP hoặc NT-proBNP vào đánh giá lâm sàng tiêu chuẩn đã được chứng minh là có giá trị trong bối cảnh ER để chẩn đoán và tiên lượng HF được chính xác và hiệu quả, cải thiện kết cục lâm sàng [36]. Các bác sĩ lâm sàng phải xem xét bối cảnh lâm sàng và thậm chí là thời điểm khởi đầu các triệu chứng đến khi xét nghiệm. NT-proBNP có độ nhạy, độ đặc hiệu tuyệt vời, và diện tích dưới ROC (receiver operating curve) để chẩn đoán HF cấp và ngưỡng cắt điều chỉnh theo tuổi có OR >10 để chẩn đoán HF, mạnh hơn nhiều so với các biến truyền thống từ bệnh sử, khám lâm sàng, hoặc xét nghiệm khác [43]. Hơn nữa, khả năng chẩn đoán và loại trừ của NT-proBNP vẫn chính xác với các tác động nhất quán của giới tính và chủng tộc, chức năng thận bất thường, béo phì, và rung nhĩ về độ nhạy hoặc độ đặc hiệu của NT-proBNP [43], nhưng việc phát hiện và/hoặc loại trừ HF ít chính xác hơn ở những bệnh nhân có GFR = 30 mL/phút/1.73m2 [2]. Mặt khác, năng lực chẩn đoán của NP được tối đa hóa dưới dạng các biến liên tục ở bệnh nhân có khả năng trung gian trước xét nghiệm. Do đó, việc sử dụng thường quy trong các nhóm nguy cơ thấp và cao đang gây tranh cãi. Sức mạnh của NP trong HF là NPV cao của nó, mặc dù không thể sử dụng để phân biệt HF tâm trương với tâm thu [2].
Tình trạng lâm sàng liên quan đến tăng biểu hiện NP
NP cũng tăng lên trong tất cả các rối loạn phù nề với quá tải muối và dịch, và tăng sức căng thành tâm nhĩ hoặc tâm thất [2]. Yếu tố kích thích chính để giải phóng BNP là thiếu máu cục bộ cơ tim do sự căng thành cuối tâm trương gợi lên sự bài tiết BNP và các yếu tố paracrine, như angiotensin II, endothelin và cytokine [2]. Bảng 4.8 tóm tắt chẩn đoán phân biệt liên quan đến tăng NT-proBNP và BNP.
| Bảng 4.8 Chẩn đoán phân biệt theo hệ thống dành cho NT-proBNP và BNP tăng cao [2, 44-46]. | |
| Hệ thống | Tình trạng lâm sàng |
| Tim mạch | Bệnh động mạch vành, bệnh cơ tim phì đại, bệnh cơ tim thâm nhiễm (tức là amyloidosis), hội chứng Takotsubo, viêm cơ tim, nhiễm độc tim do hóa trị liệu, bệnh van tim (hẹp động mạch chủ hoặc hẹp và hở van hai lá), rối loạn nhịp tim (rung và cuồng nhĩ), thuyên tắc phổi, tăng áp phổi, bệnh tim bẩm sinh. |
| CNS | Bệnh mạch máu não cấp tính. |
| Huyết học | Thiếu máu. |
| Thận | Suy thận. |
| Phổi | Suy hô hấp nguy kịch người lớn, bệnh phổi tắc nghẽn mạn tính, ngưng thở khi ngủ. |
| Chuyển hóa/ viêm. | Nhiễm khuẩn huyết, bỏng, quá tải tuần hoàn liên quan đến truyền máu, nọc rắn, xơ gan, cường aldosterone, cường giáp. |
Lưu đồ chẩn đoán và thang điểm tiên đoán
Các NP hỗ trợ chẩn đoán HF cấp và được đưa vào là khuyến cáo Loại I, Cấp độ bằng chứng A trong hướng dẫn thực hành lâm sàng [43]. Không có sự khác biệt về việc dùng BNP và NT-proBNP để chẩn đoán, ngoại trừ khi sử dụng các chất ức chế nesiritide và neprilysin [2, 35]. Như đã thảo luận với cTn, nồng độ NP càng cao thì khả năng HF càng cao. Tuy nhiên, áp dụng giới hạn duy nhất cho tất cả các tình huống là không đúng, và nồng độ tuyệt đối không thể thay thế cho nhau giữa các xét nghiệm. Trong ER, việc xác định HF ở bệnh nhân chỉ có biểu hiện lâm sàng khó thở là một thách thức; nghiên cứu lâm sàng trong bối cảnh cấp cứu đã xác nhận NP có độ chính xác cao về chẩn đoán. Ngoài ra, NT-proBNP và BNP là tương đương nhau, với độ nhạy ~ 90% và độ đặc hiệu ~ 70%, nâng cao độ chính xác chẩn đoán của phán đoán lâm sàng từ 74% lên 81% [2]. Hình 4.5 minh họa giới hạn quyết định của NT-proBNP và BNP cho bệnh nhân khó thở cấp tính mà không bị suy thận [43].
Khó khăn, thách thức và hạn chế tại ER
Các NP được tiết ra từ tế bào cơ tim để đáp ứng với căng thẳng huyết động qua trung gian của việc quá tải thể tích và/hoặc áp lực và do đó liên quan đến mức độ rối loạn chức năng tâm nhĩ, tâm thất, và van tim nhưng không phải là HF cũng không phải bệnh đặc hiệu về tim [2]. Việc phóng thích các phân tử này kích hoạt các cơ chế bù trừ khác nhau, như là một công cụ hữu ích để xác định sớm và phân tầng nguy cơ. NP cũng là công cụ có giá trị để ước tính tiên lượng của bệnh nhân. Thận thải bỏ cả hai NP đến một mức độ tương đương nhau; cả hai đều tăng khi bịsuy thận, nhưng giá trị NT-proBNP cao hơn giá trị BNP do thời gian bán hủy sinh học dài hơn [2]. Cả hai đều là yếu tố tiên đoán về tỷ lệ mắc bệnh và tử vong trong HF cấp; do đó, nó là một công cụ hữu ích và mang tính quyết định trong bối cảnh bệnh nhân ở ER. Ngoài những cân nhắc này, thời điểm khởi đầu các triệu chứng khi đến ER cũng cần được xem xét nếu có sự không phù hợp giữa biểu hiện lâm sàng và phép đo NP.
D-Dimer và sự kích hoạt tiêu sợi huyết nội sinh
D-Dimer (DD) là một sản phẩm được tạo ra trong quá trình tiêu sợi huyết. Nó là một dấu hiệu của hoạt động thrombin và thu lại fibrin, và do đó phản ánh cả sự cầm máu và tiêu sợi huyết, hiện được coi là tiêu chuẩn vàng về sinh hóa để loại trừ nghi ngờ lâm sàng thấp của VTE, bao gồm huyết khối tĩnh mạch sâu (DVT) và PE [47]. Các phân tử DD là sản phẩm thoái hóa liên kết chéo nhỏ nhất của fibrin liên kết chéo và nồng độ cũng tăng trong huyết tương của bệnh nhân bị huyết khối động mạch (bao gồm MI và đột quỵ), nguy cơ huyết khối tái phát sau khi điều trị chống đông, và đông máu nội mạch lan tỏa [48] . Ngoài ra, nó có liên quan đến thai kỳ khỏe mạnh, hoặc trong tình trạng sau phẫu thuật, và ở những bệnh nhân mắc bệnh gan nặng, ác tính, và nhiễm khuẩn huyết [49], nêu bật mối quan hệ với huyết khối và viêm, còn được gọi là huyết khối miễn dịch [50]. Trong ER, vai trò của nó để loại trừ một biến cố huyết khối là rất quan trọng. Các bác sĩ lâm sàng phải biết ứng dụng và những hạn chế của nó, cũng như các yếu tố có thể ảnh hưởng đến việc giải thích kết quả thích hợp, dẫn đến kết cục lâm sàng bất lợi.
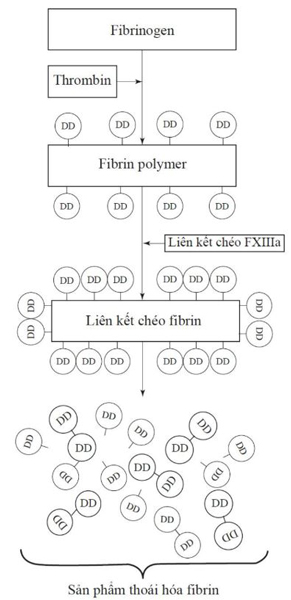
Sinh lý học
Sự hình thành các cục máu đông bởi hệ thống đông máu để phản ứng lại tổn thương mạch máu và việc bộc lộ yếu tố mô nội mạch được cân bằng bởi sự phân hủy của cục máu đông bởi hệ thống tiêu sợi huyết. DD là một trong một số mảnh được giải phóng khi plasmin, một enzyme được kích hoạt thông qua con đường tiêu sợi huyết, cắt fibrin để phá vỡ cục máu đông. Nó bao gồm hai miền fibrin D liên kết cộng hóa trị được liên kết chéo bởi yếu tố XIII khi cục máu đông được hình thành. Mảnh này tạo thành các epitope duy nhất có thể làm mục tiêu cho các kháng thể đơn dòng trong các xét nghiệm DD để xác nhận rằng dòng thác đông máu đang tạo ra thrombin [51]. Sau khi hình thành huyết khối, thời gian để phát hiện DD trong máu là khoảng 2 giờ, với thời gian bán hủy là 4-6 giờ, và có thể tăng kéo dài ít nhất 1 tuần sau khi giải quyết biến cố VTE, trở lại giá trị bình thường sau 3 tháng xảy ra biến cố cấp tính [47, 52].
Xem xét tiền-phân tích
Các mẫu máu để xét nghiệm DD phải được thu thập trước khi các mẫu xét nghiệm khác được rút, hoặc bất kỳ quy trình nào được thực hiện, ngay cả những mẫu xâm lấn tối thiểu, chẳng hạn như đặt kim luồn. Ngoài ra, nó nên được xử lý nhanh nhất có thể (lý tưởng là trong vòng 1 giờ sau khi thu thập) và xét nghiệm được thực hiện trong vòng 4 giờ sau khi thu mẫu (hoặc nếu không, có thể được xử lý bằng cách ly tâm và đông lạnh huyết tương) [8]. Bảng 4.9 chỉ ra các yếu tố tiền-phân tích ảnh hưởng đến xét nghiệm DD.
| Bảng 4.9 Các yếu tố tiền-phân tích ảnh hưởng đến D-dimer [3]. | |
| Yếu tố | |
| Mẫu máu. | Việc lấy máu nên làm trước bất kỳ thủ thuật hoặc xét nghiệm nào và nên được xử lý càng nhanh càng tốt (lý tưởng là trong vòng 1 giờ sau khi rút máu). Xét nghiệm được thực hiện trong vòng 4 giờ thu mẫu (hoặc nếu không, nên được xử lý bằng cách ly tâm và đông lạnh huyết tương). DD có thể được đo trong máu toàn phần, có heparin, hoặc huyết tương có citrate (tùy chọn mẫu thử). Huyết tương EDTA ảnh hưởng kết quả. Các mẫu có nguồn gốc từ các đường tĩnh mạch trung tâm, dẫn đến các mẫu bị vón cục, bị tán huyết, hoặc bị kích hoạt hoặc các mẫu được pha loãng bởi nước muối hoặc bị nhiễm heparin. |
| Lưu trữ. | Việc đổ gần đầy ống chứa có thể gây ra pha loãng mẫu đáng kể và cũng sẽ dẫn đến việc đánh giá thấp kết quả xét nghiệm định lượng. Các mẫu phải được trộn kỹ (nhưng nhẹ nhàng) từ 3 đến 6 lần đảo ngược đầu ống để đảm bảo trộn đầy đủ mẫu thử với thuốc chống đông máu và để tránh tạo cục máu đông trong mẫu. |
| Tiêu chuẩn hoá. | Mặc dù hiện có nhiều loại xét nghiệm DD dựa trên kháng thể, nhưng không có tiêu chuẩn nào có thể hiệu chuẩn tất cả các xét nghiệm; do đó, sự khác biệt đáng kể có thể được quan sát trong ngưỡng quan trọng lâm sàng và giá trị khoảng tham chiếu giữa các hệ thống. Sự biến thiên này góp phần vào tính không đồng nhất giữa các xét nghiệm được thực hiện bằng các phương pháp khác nhau trong các phòng xét nghiệm khác nhau, cũng như sự đa dạng về tính đặc hiệu của các kháng thể được sử dụng. |
EDTA=ethylenediaminetetraacetic acid; FEU=đơn vị đương lượng fibrinogen; DDU=đơn vị DD.
Đặc điểm phân tích
DD là một trong những sản phẩm của tiêu sợi huyết nội sinh. Tùy thuộc vào mức độ ly giải của fibrin liên kết chéo, một hỗn hợp không đồng nhất của các sản phẩm thoái hóa fibrin có chứa hợp chất DD sẽ được hình thành [52]. Do hiện nay có nhiều loại xét nghiệm DD, nên không có tiêu chuẩn nào có thể hiệu chuẩn tất cả các xét nghiệm; do đó, sự khác biệt đáng kể có thể được quan sát ở ngưỡng có ý nghĩa lâm sàng và giá trị khoảng tham chiếu giữa các hệ thống, dẫn đến sự không đồng nhất giữa các xét nghiệm. Ngoài ra, các bộ xét nghiệm khác nhau có thể báo cáo DD trong FEU hoặc DDU, sử dụng các đơn vị đo khác nhau (nghĩa là, ng/mL, g/mL, g/L). Những bất cập này đã dẫn đến sự nhầm lẫn ở một số cơ quan, đặc biệt đối với các trường hợp mà ngưỡng loại trừ VTE phải được xác định [8, 52].
Liên quan lâm sàng
DD là một dấu hiệu của huyết khối với sự kích hoạt tiêu sợi huyết nội sinh sau đó, và trên lâm sàng việc sử dụng xét nghiệm DD chủ yếu để sàng lọc VTE [47, 52]. Tuy nhiên, nồng độ DD có thể tăng lên trong bất kỳ tình trạng nào liên quan đến kích hoạt tiêu sợi huyết nội sinh, chẳng hạn như VTE, thuyên tắc phổi, nhiễm trùng, ung thư, phẫu thuật, suy tim hoặc suy thận, hội chứng mạch vành cấp, đột quỵ cấp không phải lỗ khuyết, mang thai, và đợt cấp của bệnh hồng cầu hình liềm [53]. Mặt khác, việc sử dụng xét nghiệm DD kết hợp với lưu đồ lâm sàng dựa trên bằng chứng ở bệnh nhân ngoại trú chưa trải qua các liệu pháp chống đông máu nhưng nghi ngờ có DVT hoặc PE có thể loại trừ chính xác sự hiện diện của bệnh lý mà không cần sử dụng các kỹ thuật hình ảnh [54]. Mặc dù độ nhạy và NPV của DD liên quan đến DVT và PE khác nhau đôi chút, nhưng về mặt logic là chúng giống nhau, vì các bệnh thường chồng chéo ở dạng cục huyết khối hoặc bệnh do huyết khối [52]. Trong hội chứng động mạch chủ cấp, DD có thể có giá trị chẩn đoán cũng như tiên lượng. Hơn nữa, nồng độ DD tương quan với độ lớn giải phẫu của bóc tách [49]. DD đã được chứng minh là một dấu hiệu tiên lượng trong nhồi máu cơ tim ST chênh lên được PCI, cũng như trong AF, đặc biệt ở bệnh nhân có nhiều yếu tố nguy cơ thuyên tắc, những bệnh nhân được loại trừ huyết khối trong tâm nhĩ và cắt đốt qua catheter trước đó. Hơn nữa, nó có NPV cao trong bệnh huyết khối xoang tĩnh mạch não [53, 55-57]. Độ nhạy và độ đặc hiệu lâm sàng của các phép đo DD giảm rõ rệt ở bệnh nhân nằm viện, vì hầu hết bệnh nhân có nhiều bệnh đi kèm, do đó họ cũng là những bệnh nhân có nguy cơ cao, điều này cho thấy thách thức trong chẩn đoán biến cố huyết khối [54. Tuổi là một yếu tố cần được xem xét khi diễn giải kết quả xét nghiệm, vì tỷ lệ xuất hiện các tình trạng tăng đông và viêm mãn tính như ung thư có thể tăng theo tuổi [47]. Trên thực tế, ở những bệnh nhân trên 80 tuổi, độ đặc hiệu lâm sàng có thể giảm tới 15%, làm tăng số lượng bệnh nhân có kết quả dương tính giả [49]. Do đó, ngưỡng DD cho bệnh nhân trên 50 tuổi có thể được tăng lên một cách an toàn bằng cách nhân tuổi được tính bằng năm với 10 (tức là ngưỡng DD cho bệnh nhân 60 tuổi sẽ là 600 μg/L thay vì ngưỡng của nhà sản xuất là 500 μg/L), có sự tăng nhẹ độ nhạy của xét nghiệm [47, 49, 58]. Ở những bệnh nhân mang thai, kết quả xét nghiệm DD có nhiều khả năng dương tính do nồng độ tăng dần trong suốt thai kỳ, đặc biệt là trong tam cá nguyệt thứ ba cho đến 45 ngày đầu sau sinh. Kết quả này là thách thức do PE; nó là nguyên nhân hàng đầu gây tử vong mẹ liên quan đến thai kỳ ở các nước phát triển [59, 60]. Do đó, bác sĩ lâm sàng phải xem xét rằng, như trong các dấu ấn sinh học đã thảo luận ở trên, nồng độ DD càng cao thì khả năng xuất hiện biến cố liên quan đến huyết khối càng cao, và ngược lại.
Tình trạng lâm sàng liên quan đến tăng biểu hiện DD
Các trạng thái tăng đông
Do mối quan hệ giữa bệnh huyết khối và quá trình viêm, nên các trạng thái tăng đông liên quan đến kết quả xét nghiệm DD bất thường bao gồm MI, bệnh động mạch ngoại biên, chảy máu cấp, hội chứng động mạch chủ cấp, rung nhĩ, biến cố não cấp, và bệnh Alzheimer, hội chứng đáp ứng viêm nặng, cũng như nhiễm trùng hoặc ác tính. Bảng 4.10 tóm tắt các chẩn đoán phân biệt DD.
| Bảng 4.10 Các trạng thái tăng đông cho D-dimer cao [47, 61, 62]. | |
| Tình trạng lâm sàng. | |
| Tim mạch. | Nhồi máu cơ tim, bệnh động mạch ngoại biên, chảu máy cấp, hội chứng động mạch chủ cấp, thuyên tắc huyết khối động mạch hoặc tĩnh mạch, điều trị tiêu sợi huyết cho huyết khối nội mạch (catheter, máy tạo nhịp tim, van nhân tạo), ly giải fibrin bất thường, rung nhĩ. |
| CNS | Bệnh Alzheimer, bệnh mạch máu não cấp, huyết khối xoang tĩnh mạch não. |
| Huyết học | Bệnh đông máu nội mạch lan tỏa, bệnh hồng cầu hình liềm, tán huyết, viêm tắc huyết khối tĩnh mạch nông. |
| Thận | Suy thận cấp hoặc mãn tính, hội chứng thận hư. |
| Sản khoa | Mang thai, hội chứng HELLP, tiền sản giật, và sản giật. |
| Phổi | Hội chứng suy hô hấp cấp nguy kịch. |
| Toàn thân/ viêm | Hội chứng đáp ứng viêm nặng, nhiễm trùng, ác tính, tuổi già, thời kỳ sơ sinh, khuyết tật, nằm viện, phẫu thuật, chấn thương, bỏng. |
Lưu đồ chẩn đoán và thang điểm tiên đoán
Đo DD không được khuyến cáo là xét nghiệm độc lập để loại trừ hoặc chẩn đoán VTE khi nhập ER, vì nếu không có sự tiền chọn lọc lâm sàng thích hợp, kết quả DD có thể là âm tính giả. Như đã nêu ở trên, nồng độ DD tăng cao là không đặc hiệu; do đó, kết quả DD dương tính ở bệnh nhân nghi ngờ mắc VTE nên được thực hiện tiếp theo hình ảnh học để xác định chẩn đoán [51].
Kết quả DD âm tính có thể loại trừ chẩn đoán VTE mà không cần xét nghiệm thêm nhưng chỉ khi độ nhạy của xét nghiệm cao (>98%). Mặc dù, độ nhạy cao đi kèm với chi phí cụ thể [51]. Do đó, để cải thiện tiện ích của xét nghiệm DD ở bệnh nhân nghi ngờ VTE, cần đánh giá xác suất lâm sàng của bệnh nhân đối với VTE và thường kết hợp với hình ảnh học như một phần của lưu đồ chẩn đoán [51, 61].
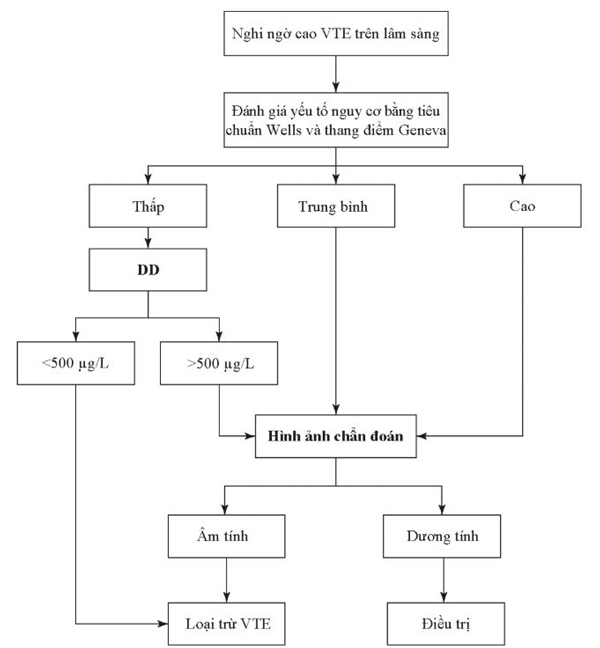
Một số quy tắc quyết định lâm sàng để chẩn đoán DVT và PE đã được phát triển, nhưng được chấp nhận nhiều nhất bao gồm thang điểm Wells và Geneva [51]. Thang điểm Wells có hai cấp độ, không có khả năng hoặc có khả năng, và sự hiện diện của từng đặc điểm lâm sàng được cho điểm dương +1. Điểm số −2 được đưa ra nếu chẩn đoán thay thế rất có khả năng, điều này chủ yếu phụ thuộc vào đánh giá của từng bác sĩ [47, 61]. Những bệnh nhân được xem là “thấp” hay “không có khả năng” bị VTE mà được xét nghiệm DD, nếu kết quả DD âm tính, VTE được xem bị loại trừ, và không nên thực hiện thêm xét nghiệm nào nữa [51]. Hình 4.7 thể hiện lưu đồ chẩn đoán VTE bằng cách sử dụng DD và hình ảnh học.
Khó khăn, thách thức và hạn chế tại ER
Việc sử dụng DD trong ER cho phép loại trừ nhanh chóng ở những bệnh nhân VTE nghi ngờ lâm sàng thấp (giá trị tiên đoán âm tính cao). Ngoài ra, DD có giá trị tiên đoán âm tính cao để loại trừ huyết khối xoang tĩnh mạch ở bệnh nhân nữ trẻ [57]. Hiện tại không có giá trị tiên đoán dương trong thuyên tắc phổi; tuy nhiên, các kết quả DD rất cao là ổn định ở bệnh nhân PE lớn hoặc trung bình. Độ chính xác của xét nghiệm DD bị ảnh hưởng thêm bởi sự không đồng nhất DD của từng bệnh nhân do tuổi cao, ảnh hưởng di truyền, yếu tố bệnh lý, thiếu hụt đông máu di truyền và mắc phải, kích thước cục máu đông, và thời điểm lấy mẫu bệnh phẩm về biến cố huyết khối [54]. Mục đích là để loại trừ bất kỳ khả năng biến cố huyết khối nào có thể có kết cục bất lợi.
Lý luận Bayes và việc ra quyết định lâm sàng
Trong việc ra quyết định y khoa, ước tính xác suất lâm sàng ảnh hưởng mạnh đến niềm tin của bác sĩ về việc bệnh nhân có mắc bệnh hay không, và chính niềm tin này quyết định các hành động: loại trừ, điều trị, hoặc làm thêm xét nghiệm [63]. Lý luận Bayes là một phương pháp cho phép kết hợp suy nghĩ ban đầu về một bệnh nhân với kết quả xét nghiệm để xác định xác suất chẩn đoán sau khi làm xét nghiệm [5]. Đầu tiên, nó yêu cầu ước tính xác suất cơ sở của bệnh trước khi bất kỳ xét nghiệm nào được đề ra. Xác suất cơ sở này đi theo các từ đồng nghĩa “xác suất trước” và “xác suất trước xét nghiệm” [63]. Theo đó, các bác sĩ phải chỉnh sửa xác suất cơ sở dựa trên mức độ của độ lệch được đưa vào bởi độ nhạy chẩn đoán của xét nghiệm (tỷ lệ bệnh nhân mắc bệnh có xét nghiệm dương tính – TPR) và độ đặc hiệu (tỷ lệ bệnh nhân không mắc bệnh có xét nghiệm âm tính – TNR). Công cụ số tóm tắt độ lệch này là tỷ lệ khả dĩ (LR) [63]. LR có thể là một cách dễ hiểu hơn để truyền đạt các thuộc tính của xét nghiệm chẩn đoán cho bác sĩ lâm sàng và có thể áp dụng thêm vào thực hành. Một LR được định nghĩa là tỷ lệ phần trăm bệnh nhân mắc bệnh với một kết quả xét nghiệm nhất định chia cho tỷ lệ phần trăm những người khỏe mạnh có cùng kết quả xét nghiệm [4]. Trong lý luận Bayes, người ta tiếp tục điều chỉnh xác suất ban đầu bằng cách thu thập thông tin mới đến điểm mà người ta hài lòng với giá trị xác suất có thể được sử dụng để đưa ra quyết định cuối cùng (ngưỡng chẩn đoán) [63].
Quy tắc ra quyết định dựa trên xác suất
Xét nghiệm nên được đề ra nếu chúng chỉ ảnh hưởng đến quyết định quản lý.
Giá trị ngưỡng phải được thiết lập trước khi bất kỳ thử nghiệm nào được đề ra.
Ngưỡng nên được cá nhân hóa cho từng bệnh lý.
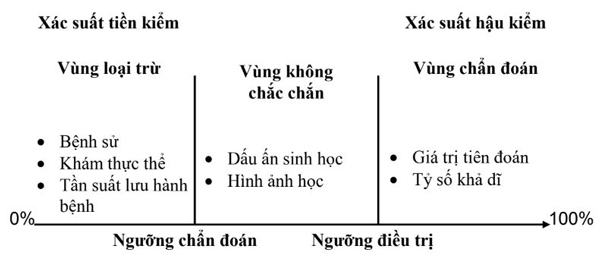
Xác suất trước xét nghiệm (xác suất tiền kiểm)
Xác suất trước xét nghiệm là điểm khởi đầu cho tất cả các quyết định lâm sàng [64]. Hỏi bệnh và khám thực thể thành thạo cho phép các bác sĩ đưa ra chẩn đoán tạm thời có thể giải thích tình trạng của một đối tượng [4]. Các giá trị tiên đoán đánh giá xác suất mà một đối tượng thực sự có hoặc không mắc bệnh trước khi thực hiện một xét nghiệm. Tuy nhiên, kết quả phụ thuộc vào tỷ lệ lưu hành của bệnh; do đó, giá trị tiên đoán dương (PPV) sẽ cao bằng tỷ lệ lưu hành của bệnh với NPV thấp [10]. Nếu xác suất bệnh là rất không có khả năng (dưới ngưỡng xét nghiệm), có thể loại trừ được từ chẩn đoán phân biệt tiềm năng. Ngược lại, nếu xác suất đủ cao để bắt đầu điều trị (trên ngưỡng điều trị), thì xét nghiệm tiếp theo là không cần thiết. Khi xác suất nằm giữa hai ngưỡng, thì xét nghiệm chẩn đoán thêm được chỉ định. Bảng 4.11 tóm tắt các đặc điểm của PPV và NPV.
Xác suất sau xét nghiệm (xác suất hậu kiểm)
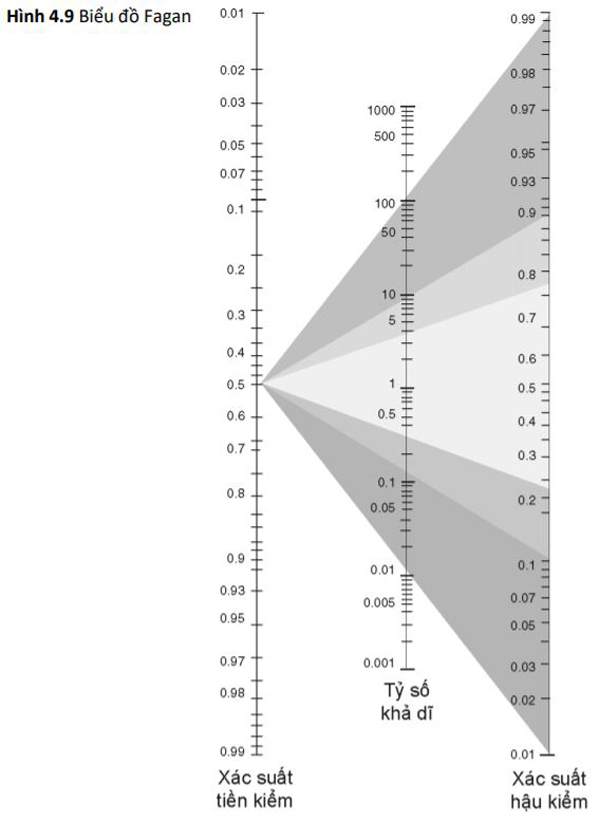
Chúng tôi cũng có thể thể hiện khả năng của một xét nghiệm bằng cách sử dụng LR xuất phát từ độ nhạy và độ đặc hiệu và mang đến khái niệm về sức mạnh của kết quả xét nghiệm dương tính hoặc âm tính. LR có thể là một cách dễ hiểu hơn để truyền đạt các thuộc tính của xét nghiệm chẩn đoán cho bác sĩ lâm sàng và có thể áp dụng thêm vào thực hành. Một LR được định nghĩa là tỷ lệ phần trăm bệnh nhân mắc bệnh với một kết quả xét nghiệm nhất định chia cho tỷ lệ phần trăm những người khỏe mạnh có cùng kết quả xét nghiệm. Kết hợp các kết quả xét nghiệm với chẩn đoán ban đầu để điều chỉnh xác suất mà đối tượng mắc bệnh được gọi là xác suất sau xét nghiệm. LR là lợi thế trong vấn đề này bởi vì chúng là thước đo sức mạnh của kết quả xét nghiệm. Nó có thể giúp điều chỉnh ước tính xác suất ban đầu như thế nào khi cố gắng xác định ước tính xác suất cuối cùng [3]. Với mục đích này, biểu đồ Fagan là một công cụ đồ họa để ước tính kết quả của một xét nghiệm chẩn đoán thay đổi xác suất bệnh nhân mắc bệnh ra sao [65] (Hình 4.9). Bảng 4.12 tóm tắt các đặc điểm của LR.
| Bảng 4.11 Giá trị tiên đoán của các xét nghiệm lâm sàng. | ||||
| Đặc điểm | Định nghĩa | Xác xuất | Giải quyết câu hỏi | Công thức |
| Giá trị tiên đoán dương (PPV). | Xác suất đối tượng có kết quả xét nghiệm dương tính sẽ thật sự có bệnh. | Trước xét nghiệm. | Khả năng mà đối tượng có bệnh cho kết quả xét nghiệm dương tính là bao nhiêu? | TP:(TP+FP) |
| Giá trị tiên đoán âm (NPV). | Xác suất đối tượng có kết quả xét nghiệm âm tính sẽ thật sự không có bệnh. | Khả năng mà đối tượng không có bệnh cho kết quả xét nghiệm âm tính là bao nhiêu? | TN:(TN+FN) | |
Dương tính thật (TP), đối tượng có bệnh và xét nghiệm dương tính; dương tính giả (FP), đối tượng không có bệnh và xét nghiệm dương tính; âm tính thật (TN), đối tượng không có bệnh và xét nghiệm âm tính; âm tính giả (FN), đối tượng có bệnh nhưng xét nghiệm âm tính; TPR, tỷ lệ dương tính thật; TNR, tỷ lệ âm tính thật.
| Bảng 4.12 Tỷ số khả dĩ của xét nghiệm chẩn đoán. | |||
| Đặc điểm | Định nghĩa | Giải quyết câu hỏi | Công thức |
| Tỷ số khả dĩ (+) | Xác suất đối tượng mắc bệnh với một kết quả xét nghiệm nhất định chia cho tỷ lệ phần trăm những người khỏe mạnh có cùng kết quả xét nghiệm. | Khả năng hậu kiểm thay đổi thế nào sau một kết quả xét nghiệm dương tính? | Sensitivity:(1-specificity) hoặc TPR:(1-specificity) |
| Tỷ số khả dĩ (−) | Khả năng hậu kiểm thay đổi thế nào sau một kết quả xét nghiệm âm tính? | (1-sensitivity): Specificity hoặc (1-Sensitivity) : TNR | |
Dương tính thật, đối tượng có bệnh và xét nghiệm dương tính; dương tính giả, đối tượng không có bệnh và xét nghiệm dương tính; âm tính thật, đối tượng không có bệnh và xét nghiệm âm tính; âm tính giả, đối tượng có bệnh nhưng xét nghiệm âm tính; TPR, tỷ lệ dương tính thật; TNR, tỷ lệ âm tính thật.
Những điểm chính
Dấu ấn sinh học được sử dụng để tăng cường kỹ năng và phán đoán của bác sĩ nhưng phụ thuộc vào bối cảnh lâm sàng.
Lý luận lâm sàng tốt là điều cần thiết để yêu cầu và giải thích chính xác kết quả.
Dấu ấn sinh học không nên được sử dụng như là các xét nghiệm độc lập để chẩn đoán bệnh tim mạch và nên được phân tích như các biến định lượng.
Các đặc điểm tiền-phân tích và phân tích phải được xem xét khi giải thích kết quả.
Đặc điểm hoạt động lâm sàng và giá trị tiên đoán phụ thuộc vào giá trị ngưỡng và tỷ lệ lưu hành của bệnh, tương ứng.
Tỷ số khả dĩ là một cách dễ hiểu hơn để truyền đạt các thuộc tính của xét nghiệm chẩn đoán cho bác sĩ lâm sàng.
HS-cTn là dấu hiệu của thiếu máu cục bộ, vi hoại tử, hoặc hoại tử, trong khi độc lập với nguyên nhân gây tổn thương, do đó, sẽ xác định các nguyên nhân mới gây tăng cTn và do đó làm giảm độ đặc hiệu của bất kỳ sự gia tăng nào đối với bệnh tim thiếu máu cục bộ.
Các NP không phải là HF cũng không phải là bệnh tim vì chúng có các giá trị tiêu chuẩn của các giá trị ngưỡng cho phép loại bỏ khả năng của HF. Đối với giá trị tiên đoán mà các phân tử này thêm vào sự tích hợp của việc ra quyết định, thì việc sử dụng chúng là rất quan trọng trong ER.
DD là các dấu hiệu của biến cố liên quan đến bệnh do huyết khối; tuy nhiên, nó không phải là một công cụ được tiêu chuẩn hóa và mỗi xét nghiệm có giá trị ngưỡng của nó. Do tính đặc hiệu thấp, cần xác định xác suất trước xét nghiệm để tăng khả năng chẩn đoán của xét nghiệm này, cũng như sử dụng cùng với các công cụ hình ảnh cho phép loại trừ khả năng biến cố với kết quả không thuận lợi. Nó rất hữu dụng trong khu vực cấp cứu.
Công cụ được đề xuất
MdCalc+: MDCalc là tài liệu tham khảo y khoa số 1 cho các công cụ quyết định lâm sàng và nội dung được sử dụng bởi hơn một triệu chuyên gia y tế trên toàn cầu, bao gồm hơn 50% bác sĩ Hoa Kỳ, mỗi tháng. https://www.mdcalc.com.
DocNomo®: DocNomo là một công cụ đồ họa thuận tiện để tăng cường việc giải thích đầu giường về kết quả xét nghiệm chẩn đoán. Từ độ nhạy và độ đặc hiệu của xét nghiệm chẩn đoán đến xác suất bệnh nhân bị rối loạn mục tiêu trước khi chạy xét nghiệm. DocNomo tính toán xác suất hậu kiểm. https://itunes.apple.com/us/app/docnomo/id901279945?mt=8.
Nhóm NNT® Một nhóm các bác sĩ lâm sàng đa chuyên khoa đã xây dựng một khung và hệ thống xếp hạng để đánh giá các liệu pháp dựa trên lợi ích và tác hại mà quan trọng là bệnh nhân cũng như một hệ thống để đánh giá chẩn đoán bằng dấu hiệu, triệu chứng, xét nghiệm, hoặc cận lâm sàng của bệnh nhân. http://www.thennt.com/
Tài liệu tham khảo
1. Graham KJ, Strauss CE, Boland LL, Mooney MR, Harris KM, Unger BT, et al. Has the time come for a National Cardiovascular Emergency Care System? Circulation. 2012;125: 2035–44.
2. Thygesen K, Mair J, Mueller C, Huber K, Weber M, Plebani M, et al. Recommendations for the use of natriuretic peptides in acute cardiac care: a position statement from the Study Group on Biomarkers in Cardiology of the ESC Working Group on Acute Cardiac Care. Eur Heart J. 2012;33:2001–6.
3. Favaloro EJ, Adcock Funk DM, Lippi G. Pre-analytical variables in coagulation testing associated with diagnostic errors in hemostasis. Lab Med. 2012;43:1.2–10.
4. Brush JE, Kaul S, Krumholz HM. Troponin testing for clinicians. J Am Coll Cardiol. 2016;68:2365–75.
5. Brush JE, Krumholz HM. The science of the art of medicine: a guide to medical reasoning. 1st ed: Manakin-Sabot, VA: Dementi Milestone Publishing; 2015.
6. Jaffe A. The use of biomarkers for acute cardiovascular disease. In: Tubaro M, Vranckx P, editors. The ESC textbook of Acute and Intensive Cardiosvacular Care. 2nd ed. Oxford, England, UK: Oxford University Press; 2014.
7. Magnette A, Chatelain M, Chatelain B, Ten Cate H, Mullier F. Pre-analytical issues in the haemostasis laboratory: guidance for the clinical laboratories. Thromb J [Internet]. 2016. [cited 2018 Sep 2];14:49. Available from: https://doi.org/10.1186/s12959-016- 0123-z.
8. Simundic A-M, Lippi G. Preanalytical phase–a continuous challenge for laboratory professionals. Biochem Med. 2012;22:145–9.
9. Saah AJ, Hoover DR. “Sensitivity” and “specificity” reconsidered: the meaning of these terms in analytical and diagnostic settings. Ann Intern Med. 1997;126:91–4.
10. Florkowski CM. Sensitivity, specificity, receiver-operating characteristic (ROC) curves and likelihood ratios: communicating the performance of diagnostic tests. Clin Biochem Rev. 2008;29( Suppl 1):S83– 7.
11. Lalkhen AG, McCluskey A. Clinical tests: sensitivity and specificity. Contin Educ Anaesth Crit Care Pain. 2008;8:221–3.
12. Thygesen K, Mair J, Giannitsis E, Mueller C, Lindahl B, Blankenberg S, et al. How to use high-sensitivity cardiac troponins in acute cardiac care. Eur Heart J. 2012;33:2252–7.
13. Thygesen K, Alpert JS, Jaffe AS, Simoons ML, Chaitman BR, White HD, et al. Third universal definition of myocardial infarction. Circulation. 2012;126:2020–35.
14. Amsterdam EA, Wenger NK, Brindis RG, Casey DE, Ganiats TG, Holmes DR, et al. 2014 AHA/ACC guideline for the management of patients with non–ST-elevation acute coronary syndromes. J Am Coll Cardiol. 2014;64:e139–228.
15. Ibanez B, James S, Agewall S, Antunes MJ, Bucciarelli-Ducci C, Bueno H, et al. 2017 ESC guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation. Eur Heart J. 2018;39:119–77.
16. Thygesen K, Alpert JS, Jaffe AS, Chaitman BR, Bax JJ, Morrow DA, et al. Fourth universal definition of myocardial infarction. Eur Heart J. 2018;00:1–33.
17. Westermann D, Neumann JT, Sörensen NA, Blankenberg S. High-sensitivity assays for troponin in patients with cardiac disease. Nat Rev Cardiol. 2017;14:472–83.
18. Okyay K, Yildirir A. The preanalytical and analytical factors responsible for false-positive cardiac troponins. Anadolu Kardiyol Derg Anatol J Cardiol. 2015;15:264–5.
19. Herman DS, Kavsak PA, Greene DN. Variability and error in cardiac troponin testing. Am J Clin Pathol. 2017;148:281–95.
20. Mahajan VS, Jarolim P. How to interpret elevated cardiac troponin levels. Circulation. 2011;124:2350–4.
21. Wu AHB, Christenson R. The era for high-sensitivity cardiac troponin has begun in the US ( finally). J Appl Lab Med AACC Publ. 2017;2:1– 3.
22. Adamson PD, Anderson JA, Brook RD, Calverley PMA, Celli BR, Cowans NJ, et al. Cardiac troponin I and cardiovascular risk in patients with chronic obstructive pulmonary disease. J Am Coll Cardiol. 2018;72:1126–37.
23. Schneider ALC, Rawlings AM, Sharrett AR, Alonso A, Mosley TH, Hoogeveen RC, et al. High-sensitivity cardiac troponin T and cognitive function and dementia risk: the atherosclerosis risk in communities study. Eur Heart J. 2014;35:1817–24.
24. Matsushita K, Kwak L, Yang C, Pang Y, Ballew SH, Sang Y, et al. High-sensitivity cardiac troponin and natriuretic peptide with risk of lower-extremity peripheral artery disease: the Atherosclerosis Risk in Communities (ARIC) Study. Eur Heart J. 2018;39:2412–9.
25. Devereaux PJ, Duceppe E, Guyatt G, Tandon V, Rodseth R, Biccard BM, et al. Dabigatran in patients with myocardial injury after non-cardiac surgery (MANAGE): an international, randomised, placebo-controlled trial. Lancet. 2018;391:2325–34.
26. Twerenbold R, Boeddinghaus J, Mueller C. Update on high-sensitivity cardiac troponin in patients with suspected myocardial infarction. Eur Heart J Suppl. 2018;20:G2–10.
27. Lee GR, Browne TC, Guest B, Khan I, Murphy E, McGorrian C, et al. Transitioning high sensitivity cardiac troponin I (hs-cTnI) into routine diagnostic use: more than just a s ensitivity issue. Pract Lab Med. 2016;4:62–75.
28. Twerenbold R, Boeddinghaus J, Nestelberger T, Wildi K, Rubini Gimenez M, Badertscher P, et al. Clinical use of high-sensitivity cardiac troponin in patients with suspected myocardial infarction. J Am Coll Cardiol. 2017;70:996–1012.
29. Eikelboom JW, Connolly SJ, Bosch J, Dagenais GR, Hart RG, Shestakovska O, et al. Rivaroxaban with or without aspirin in stable cardiovascular disease. N Engl J Med. 2017;377:1319–30.
30. Sherwood MW, Kristin Newby L. High-sensitivity troponin assays: evidence, indications, and reasonable use. J Am Heart Assoc. 2014;3:e000403.
31. Chapman AR, Hesse K, Andrews JPM, Lee KK, Anand A, Ferry A, et al. High-sensitivity cardiac troponin I and clinical risk scores in patients with suspected acute coronary syndrome. Eur Heart J [Internet]. 2018 [cited 2018 Sep 12];39. Available from: https://doi.org/10.1093/ eurheartj/ehy565.1085/5079282
32. Braunwald E. Heart failure. JACC Heart Fail. 2013;1:1–20.
33. Hollinger A, Cerlinskaite K, Bastian K, Mebazaa A. Biomarkers of increased intraventricular pressure: are we ready? Eur Heart J Suppl. 2018;20:G21–7.
34. Rodriguez D, Garcia-Rivas G, Laresgoiti-Servitje E, Yañez J, Torre-Amione G, Jerjes- Sanchez C. B-type natriuretic peptide reference interval of newborns from healthy and pre-eclamptic women: a prospective, multicentre, cross-sectional study. BMJ Open. 2018;8:e022562.
35. Mair J, Lindahl B, Giannitsis E, Huber K, Thygesen K, Plebani M, et al. Will sacubitril- valsartan diminish the clinical utility of B-type natriuretic peptide testing in acute cardiac care? Eur Heart J Acute Cardiovasc Care. 2017;6:321–8.
36. Kim H-N, Januzzi JL. Natriuretic peptide testing in heart failure. Circulation. 2011;123:2015–9.
37. Apple FS. Quality specifications for B-type natriuretic peptide assays. Clin Chem. 2005;51:486–93.
38. Weber M. Role of B-type natriuretic peptide (BNP) and NT-proBNP in clinical routine. Heart. 2005;92:843–9.
39. Apple FS, Wu AHB, Jaffe AS, Panteghini M, Christenson RH, Christenson RH, et al. National Academy of Clinical Biochemistry and IFCC Committee for standardization of markers of cardiac damage laboratory medicine practice guidelines: analytical issues for biomarkers of heart failure. Circulation. 2007;116:e95–8.
40. Kim H-L, Kim M-A, Choi D-J, Han S, Jeon E-S, Cho M-C, et al. Gender difference in the prognostic value of N-terminal pro-B type natriuretic peptide in patients with Heart Failure — a report from the Korean Heart Failure registry (KorHF) —. Circ J. 2017;81:1329–36.
41. Gaggin H, Januzzi J Jr. Cardiac Biomarkers and Heart Failure [Internet]. Am Coll Cardiol. 2015;. [cited 2018 Sep 12]. Available from: https://www.acc.org/latest-in-cardiology/ articles/2015/02/09/13/00/cardiac-biomarkers-and-heart-failure
42. Quintanilla J, Jerjes-Sanchez C, Perez L, Valdes F, Jimenez V, Trevino AR, et al. Intermediate- to high-risk pulmonary embolism with normal B-type natriuretic peptide. Am J Emerg Med. 2016;34:2463.e1–3.
43. Januzzi JL, Chen-Tournoux AA, Christenson RH, Doros G, Hollander JE, Levy PD, et al. N- terminal pro–B-type natriuretic peptide in the emergency department. J Am Coll Cardiol. 2018;71:1191–200.
44. Baggish AL, van Kimmenade RRJ, Januzzi JL. The differential diagnosis of an elevated amino-terminal pro–B-type natriuretic peptide level. Am J Cardiol. 2008;101:S43–8.
45. Jespersen CM, Fischer Hansen J. Myocardial stress in patients with acute cerebrovascular events. Cardiology. 2008;110:123–8.
46. Chen H, Colucci W. Natriuretic peptide measurement in non-heart failure settings – UpToDate [Internet]. 2017 [cited 2018 Sep 5]. Available from: https://0-www.uptodate. com.millenium.itesm.mx/contents/natriuretic-peptide- measurement-in-non-heart-failure- settings?search=Natriuretic%20peptide%20measurement%20in%20non- heart%20failure%20 settings&source=search_result&selectedTitle=1~150&usage_type=default&display_ra nk=1.
47. Giannitsis E, Mair J, Christersson C, Siegbahn A, Huber K, Jaffe AS, et al. How to use D- dimer in acute cardiovascular care. Eur Heart J Acute Cardiovasc Care. 2017;6:69–80.
48. Zucker M. D-dimer for the exclusion of venous thromboembolism. Lab Med. 2011;42:503–4.
49. Hahne K, Lebiedz P, Breuckmann F. Impact of D-Dimers on the differential diagnosis of acute chest pain: current aspects besides the widely known. Clin Med Insights Cardiol [Internet]. 2014 [cited 2018 Sep 13];8s2. Available from: https://doi.org/10.4137/CMC.S15948
50. Vazquez-Garza E, Jerjes-Sanchez C, Navarrete A, Joya-Harrison J, Rodriguez D. Venous thromboembolism: thrombosis, inflammation, and immunothrombosis for clinicians. J Thromb Thrombolysis. 2017;44:377–85.
51. Linkins L-A, Takach Lapner S. Review of D-dimer testing: good, bad, and ugly. Int J Lab Hematol. 2017;39:98–103.
52. Sadosty AT, Goyal DG, Boie ET, Chiu CK. Emergency department D-dimer testing. J Emerg Med. 2001;21:423–9.
53. Cohen A, Ederhy S, Meuleman C, Di Angelantonio E, Dufaitre G, Boccara F. D-dimers in atrial fibrillation: a further step in risk stratification of thrombo-embolism? Eur Heart J. 2007;28:2179–80.
54. Riley RS, Gilbert AR, Dalton JB, Pai S, McPherson RA. Widely used types and clinical applications of D-dimer assay. Lab Med. 2016;47:90–102.
55. Akgul O, Uyarel H, Pusuroglu H, Gul M, Isiksacan N, Turen S, et al. Predictive value of elevated D-dimer in patients undergoing primary angioplasty for ST elevation myocardial infarction. Blood Coagul Fibrinolysis. 2013;24:704–10.
56. Milhem A, Ingrand P, Tréguer F, Cesari O, Da Costa A, Pavin D, et al. Exclusion of Intra- Atrial Thrombus Diagnosis Using D-Dimer Assay Before Catheter Ablation of Atrial Fibrillation. JACC Clin Electrophysiol [Internet]. 2018 [cited 2018 Nov 12]; Available from: https://linkinghub.elsevier.com/retrieve/pii/S2405500X18307904.
57. Alons IME, Jellema K, Wermer MJH, Algra A. D-dimer for the exclusion of cerebral venous thrombosis: a meta-analysis of low risk patients with isolated headache. BMC Neurol [Internet]. 2015 [cited 2018 Nov 12];15:118. Available from: https://doi.org/10.1186/s12883-015-0389-y.
58. Takach Lapner S, Stevens SM, Woller SC, Snow G, Kearon C. Age-adjusted versus clinical probability-adjusted D-dimer to exclude pulmonary embolism. Thromb Res. 2018;167:15–9.
59. Jerjes-Sanchez C, Rodriguez D, Navarrete A, Parra-Cantu C, Joya-Harrison J, Vazquez E, et al. Inferior vena cava filters in pulmonary embolism: a historic controversy. Arch Cardiol México. 2017;87:155–66.
60. Marik PE, Plante LA. Venous thromboembolic disease and pregnancy. N Engl J Med. 2008;359:2025–33.
61. Pulivarthi S, Gurram MK. Effectiveness of D-dimer as a screening test for venous thromboembolism: an update. North Am J Med Sci. 2014;6:491.
62. Thompson B, Kabrhel C, Pena C. Clinical presentation, evaluation, and diagnosis of the nonpregnant adult with suspected acute pulmonary embolism – UpToDate [Internet]. 2018 [cited 2018 Sep 13]. Available from: https://www.uptodate.com/contents/clinicalpresentation-evaluation-and-diagnosis- of-the-nonpregnant-adult-with-suspected-acutepulmonary-embolism?search=d- dimer&source=search_result&selectedTitle=2~150&usa ge_type=default&display_rank=2#H746822394.
63. Zehtabchi S, Kline JA. The art and science of probabilistic decision-making in emergency medicine. Acad Emerg Med. 2010;17:521–3.
64. McGee S. Chapter 2 – diagnostic accuracy of physical findings. In: McGee S, editor. Evidence- based physical diagnosis [Internet]. 3rd ed. Philadelphia: W.B. Saunders; 2012. p. 9–21. Available from: http://www.sciencedirect.com/science/article/pii/B9781437722079000021.
65. Fagan T. Nomogram for Bayes’s theorem. N Engl J Med 1975;293:257.
Đăng tải bởi: Heal Central





