Bài viết Áp dụng hỗ trợ hô hấp cho bệnh nhân COVID-19 được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Position Paper for the State-of-the-Art Application of Respiratory Support in Patients with COVID-19
TÓM TẮT
Trong bối cảnh đại dịch do nhiễm virut SARS-CoV-2, Hiệp hội Hô hấp Đức đã chỉ định các chuyên gia xây dựng chiến lược trị liệu cho bệnh nhân COVID-19 bị suy hô hấp cấp tính (ARF). Ở đây chúng tôi trình bày các tuyên bố quan trọng bao gồm các quan sát về sinh lý bệnh học của (ARF). Về mặt sinh lý bệnh của nhiễm trùng phổi với SARS-CoV-2, COVID-19 có thể được chia thành 3 giai đoạn. Tổn thương phổi ở COVID-19 tiên tiến thường khác với những thay đổi đã biết trong hội chứng suy hô hấp cấp tính (ARDS). Hai loại (loại L và loại H) được phân biệt, tương ứng với tổn thương phổi giai đoạn đầu và giai đoạn cuối. Sự khác biệt này cần được xem xét trong hỗ trợ hô hấp của ARF. Việc đánh giá mức độ của ARF nên dựa trên phân tích khí máu động mạch hoặc mao mạch trong điều kiện thở không khí phòng, và nó cần bao gồm việc tính toán lượng oxy cung cấp (được đo từ các biến số của độ bão hòa oxy, mức độ hemoglobin, giá trị hiệu chỉnh của yếu tố Hüfner và cung lượng tim). Hạt khí dung có thể gây lây truyền virut. Các hệ thống mở hoặc hệ thống thông khí có thể làm tăng sự giải phóng các hạt có thể đi vào đường hô hấp. Các thủ thuật trong đó hệ thống thông khí xâm lấn và đặt nội khí quản có liên quan đến tăng nguy cơ nhiễm trùng. Thiết bị bảo vệ cá nhân (PPE) nên được ưu tiên hàng đầu vì việc sợ lây nhiễm chính là lý do để không đặt nội khí quản. Dựa trên kiến thức hiện tại, liệu pháp hít, điều trị lưu lượng cao qua mũi (NHF, nasal high-flow therapy), áp lực đường thở dương liên tục (CPAP) hoặc thông khí không xâm lấn (NIV) có thể được thực hiện mà không làm tăng nguy cơ nhiễm trùng cho nhân viên nếu được cung cấp PPE. Một tỷ lệ đáng kể bệnh nhân mắc ARF có tình trạng thiếu oxy liên quan, thường không thể điều chỉnh hoàn toàn, ngay cả với FiO2 trong NHF. Trong tình huống này, liệu pháp oxy có thể được nâng lên thành CPAP hoặc NIV khi các tiêu chí đặt nội khí quản không được đáp ứng. Trong ARF, NIV nên được thực hiện trong một đơn vị chăm sóc đặc biệt hoặc một cơ sở tương đương bởi các nhân viên có kinh nghiệm. Với hỗ trợ của CPAP/NIV, một bệnh nhân có thể xấu đi nhanh chóng. Vì lý do này, việc theo dõi liên tục và sẵn sàng đặt nội khí quản phải được đảm bảo mọi lúc. Nếu ARF tiến triển theo CPAP/NIV, nên đặt nội khí quản không chậm trễ ở những bệnh nhân không có chống chỉ định đặt nội khí quản.
GIỚI THIỆU
Trong bối cảnh đại dịch do nhiễm virut SARS-CoV-2, Hiệp hội hô hấp Đức đã hợp tác với các hiệp hội khác, đã chỉ định một nhóm chuyên gia trả lời các câu hỏi về cách thức để đối phó với bệnh nhân COVID-19 ở giai đoạn mà, theo như dự đoán hiện tại, các bệnh viện sẽ không bị quá tải (cập nhật lần cuối: 15/12/2020). Do hiệu quả của các biện pháp dịch tễ học như giãn cách xã hội do lệnh giới nghiêm một phần, đại dịch ở Đức hiện có thể được dự kiến sẽ chậm lại và giảm bớt mức độ nặng [1].
Vì lý do này, tầm quan trọng lớn đã được gắn liền với tính chính xác của các tuyên bố ngay cả bên ngoài tình huống dịch bệnh và các tuyên bố quan trọng đã được các tác giả phối hợp trong một quy trình đồng thuận công phu. Bài viết này nhằm mục đích bổ sung, tiếp tục và thúc đẩy sự phát triển của sự đồng thuận liên ngành dựa trên các hướng dẫn hiện hành [2-5].
Các ấn phẩm trước đây về COVID-19 cho thấy sự không đồng nhất đáng chú ý của các triệu chứng kèm theo của nhiễm SARS-CoV-2. Điều này là do các định nghĩa khác nhau về các trạng thái bệnh nhất định (ví dụ: sốc), mức độ nặng khác nhau nhưng không xác định, các giai đoạn bệnh khác nhau và dân số khác nhau. Điều này làm cho việc so sánh trở nên khó khăn. Ngoài ra, thông tin hiện đang được công bố khá nhanh chóng và các nhóm bệnh nhân được mô tả đôi khi chỉ bao gồm một vài cá nhân. Bài viết này đã được chuẩn bị trong một quy trình tuân thủ các yêu cầu của Hiệp hội y khoa khoa học ở Đức và được chia thành 5 tuyên bố chủ đề. Các điểm chính được nêu bật dưới dạng các tuyên bố và phát hiện quan trọng.
Bài viết này dựa trên tình trạng kiến thức hiện tại về COVID-19, sẽ cải thiện trong thời gian ngắn do số lượng bệnh nhân ở Đức ngày càng tăng. Do đó, bản thảo đã được lên kế hoạch cập nhật tại thời điểm xuất bản.
PHƯƠNG PHÁP
Đề xuất này dựa trên sự đồng thuận của một nhóm các chuyên gia. Các chuyên gia này đã được Hội đồng DGP bổ nhiệm dựa trên chuyên môn của họ về vấn đề và kinh nghiệm của họ trong việc xây dựng sự đồng thuận có cấu trúc theo tiêu chí AWMF.
Các chương khác nhau đã được xác định trước và phát triển bởi các nhóm tác giả. Các nhóm này (mỗi nhóm 2-3 tác giả) được giao nhiệm vụ chuẩn bị một phiên bản dự thảo và phát triển các tuyên bố quan trọng để mức độ xây dựng đồng thuận đầu tiên sẽ nằm trong một nhóm nhỏ. Có thể thực hiện tối đa 3 tuyên bố quan trọng trên mỗi khu vực chủ đề. Các tác giả không được phân công làm việc trên các chương được yêu cầu tránh bình luận trước khi đạt được sự đồng thuận.
Các tài liệu, dựa trên các báo cáo quan trọng, được đánh giá theo các hướng dẫn của Trung tâm Y học dựa trên bằng chứng dựa trên dữ liệu hiện có. Theo yêu cầu của việc phát triển hướng dẫn tuân thủ AWMF, các tuyên bố quan trọng được diễn đạt theo một mức khuyến nghị (GOR), theo đó, Grade A là “should/should not,”, Grade B là “ought to/ought not to”, Grade 0 là “may be considered/no specific recommenda- tion”. Ngoài ra, những phát hiện không được chấm điểm nhưng được thống nhất đã được nêu bật.
Tất cả các khuyến nghị đã được tóm tắt trong một bản thảo chung đã được chỉnh sửa trong 4 vòng trực tuyến bằng kỹ thuật Delphi (vào các ngày 04/13/2020, 04/14/2020, 04/15/2020 và 04/16/2020). Một bản tóm tắt về các khuyến nghị và phát hiện khác nhau, cũng như sự chấp thuận của nhóm chuyên gia về bản thảo, đã được tổng hợp vào cuối vòng Delphi cuối cùng.
Tuyên bố 1: Sinh lý bệnh của suy hô hấp cấp tính ở bệnh nhân SARS-CoV-2 không có miễn dịch
M. Pfeifer, S. Ewig và T. Voshaar.
1.1 Tổng quát
Sự bùng phát COVID-19, do nhiễm mầm bệnh virus coronavirus SARS-CoV2 gây ra ở người và được mô tả lần đầu tiên ở Trung Quốc vào cuối tháng 12 năm 2019, đã trở thành một đại dịch toàn cầu [6-8]. Theo các nghiên cứu hiện tại, căn bệnh này nhẹ ở khoảng 80% trong số những người có kết quả xét nghiệm dương tính, nặng hơn ở 20% với các dấu hiệu suy hô hấp do thiếu oxy và cần phải điều trị nội khoa tích cực. 5% trường hợp [9]. Tỷ lệ tử vong được báo cáo là từ 1 đến 10% [9]. Tuy nhiên, những số liệu này liên quan đến số người được xét nghiệm dương tính và đánh giá thấp tình hình do số lượng người mắc bệnh không được báo cáo cao hơn đáng kể có thể được giả định.
SARS-CoV-2 chủ yếu được truyền qua các giọt bắn (lây truyền qua giọt bắn, droplet transmission); đến mức độ hạt nhân giọt nhỏ (droplet nuclei) (lây truyền trong không khí, airborne transmission) hoặc truyền bằng cách chạm vào các vật thể bị ô nhiễm (truyền dựa trên vật tiếp xúc, fomite-based transmission) có thể đóng một vai trò bổ sung chưa được thiết lập một cách thuyết phục.
Virus liên kết với thụ thể angiotensin – enzyme chuyển hóa 2 (ACE2) trong phổi, một aminopeptidase gắn màng của các tế bào biểu mô phế nang [10, 11]. Điều này làm cho phổi là cơ quan mục tiêu chính của virus. Virus chủ yếu nhân lên trong biểu mô phế quản của đường hô hấp trên, ở vùng mũi họng, với sự nhân lên thêm ở đường hô hấp dưới và niêm mạc đường tiêu hóa [12, 13]. Ở giai đoạn này, một số bệnh nhiễm trùng được kiểm soát bởi phản ứng miễn dịch và bệnh nhân có thể vẫn không có triệu chứng.
COVID-19 có 3 giai đoạn, được mô tả như sau: nhiễm trùng sớm, liên quan đến phổi và viêm quá mức nặng [14, 15] (Hình 1). Trong giai đoạn đầu của nhiễm trùng, virus xâm nhập vào nhu mô phổi và bắt đầu sao chép; điều này gây ra một phản ứng viêm liên quan đến giãn mạch cục bộ, tăng tính thấm nội mô và huy động bạch cầu [16]. Viêm phổi khu trú này dẫn đến thiếu oxy và phản ứng căng thẳng tim mạch. Dữ liệu hiện tại chỉ ra rằng tình trạng tim mạch từ trước và tăng huyết áp động mạch là những yếu tố rủi ro chính dẫn đến kết cục gây tử vong của COVID-19 [6].
![Hình 1. Ý nghĩa của phòng thủ miễn dịch và phản ứng viêm toàn thân đối với các triệu chứng của bệnh nhân COVID-19. Tiến triển lâm sàng của COVID-19 (nhẹ, xanh lá cây, nặng, xám; nguy kịch, đỏ) theo thời gian [14, 15].](https://www.healcentral.org/wp-content/uploads/2020/09/ap_dung_ho_tro_ho_hap_cho_benh_nhan_covid_19_1-300x178.jpg)
Viêm hệ thống rõ rệt được đặc trưng bởi một cơn bão cytokine, với sự gia tăng interleukin (IL) -6, IL-2, IL-7, yếu tố hoại tử khối u (TNF) -α, interferon-, protein cảm ứng (IP) -10 , protein hóa trị đơn chất (MCP) -1, protein viêm đại thực bào (MIP) -1α, yếu tố kích thích bạch cầu hạt (G- CSF), protein phản ứng C (CRP), procalcitonin và ferritin [6, 20-22].
Liên quan đến tiên lượng là nồng độ IL-6 và ferritin tăng hoặc tăng [21, 22]. Trong các nghiên cứu lâm sàng hồi cứu, bệnh nhân COVID- 19 đã chết có nồng độ IL-6, ferritin và CRP tăng đáng kể [22]. Các dấu hiệu tiên lượng bổ sung là D-dimers và troponin [21, 22].
Viêm cục bộ nguyên phát, nặng, là có thể dẫn đến tổn thương nặng đến nhu mô phổi, dẫn đến suy hô hấp tiến triển. Hơn nữa trong quá trình của bệnh, phản ứng viêm toàn thân có thể dẫn đến suy đa cơ quan. Trong các nghiên cứu bệnh lý giải phẫu, viêm mạch và huyết khối của các mạch nhỏ cũng có thể được nhìn thấy, ví dụ, trong SARS [23]. Ở mức độ nào những hiện tượng này có thể đóng vai trò trong việc nhiễm SARS-CoV2 vẫn chưa được thiết lập.
1.2 COVID-19 và suy hô hấp
Mức độ nặng của suy hô hấp được xác định bởi sự tương tác của 3 yếu tố: (1) mức độ nặng của nhiễm trùng, phản ứng miễn dịch và chức năng và bệnh đi kèm, (2) phản ứng thông khí của bệnh nhân đối với tình trạng thiếu oxy (tăng hoạt trung khu hô hấp do thiếu oxy – hypoxic drive) và (3) thời gian giữa khi bắt đầu các triệu chứng ban đầu và bắt đầu điều trị lâm sàng.
Trong các hình ảnh chụp cắt lớp vi tính (CT) của phổi, tình trạng viêm của mô phổi khi bắt đầu bệnh được đặc trưng bởi các khu vực kính mờ nhìn thấy hai bên ở vùng tiếp giáp với màng phổi, chủ yếu ở vùng giữa và dưới [24 -27]. Khi bệnh tiến triển, một số bệnh nhân cho thấy mật độ tăng theo nghĩa các vùng phổi đông đặc, được đo bằng phương pháp X quang, dẫn đến tăng trọng lượng phổi [28]. Không thể loại trừ rằng những thay đổi này là do viêm phổi bệnh viện bổ sung.
Về mặt sinh lý bệnh, suy hô hấp chủ yếu được đặc trưng bởi suy hô hấp thiếu oxy từ nhẹ đến nặng. Tuy nhiên, trong quá trình bệnh, một số bệnh nhân có CO2 trong máu tăng đáng kể. Bệnh nhân được đặt nội khí quản và thở máy trong giai đoạn này của bệnh có độ chênh oxy động mạch – phế nang tăng (cũng có tính đến FiO2 cao và giả sử chỉ số hô hấp là 0,85) và sự khác biệt lớn đáng kể giữa CO2 động mạch và end-tidal. Phù hợp với những thay đổi được quan sát trong hình ảnh và dựa trên dữ liệu của Gattinoni và cộng sự [29], 2 biểu hiện CT theo trình tự thời gian có thể được phân biệt, cái gọi là viêm phổi COVID-19 loại L và loại H (xem bên dưới).
Định nghĩa của hội chứng suy hô hấp cấp tính (ARDS) theo định nghĩa của Berlin có thể được đáp ứng trong cả hai biểu hiện; tuy nhiên, người ta đã chứng minh rằng viêm phổi COVID- 19, đặc biệt là ở giai đoạn đầu (loại L), nhưng cũng ở giai đoạn muộn (loại H), khác biệt đáng kể với những thay đổi quen thuộc đi kèm với ARDS, như những gì được quan sát thấy trong sốc nhiễm trùng hoặc viêm phổi do vi khuẩn. Dưới đây mô tả một mô hình được phát triển dựa trên quét CT chưa được xác nhận lâm sàng hoặc mô bệnh học tại thời điểm này.
1.3 Viêm phổi COVID-19, Loại L
Giai đoạn đầu này, có thể được bù bởi bệnh nhân có hỗ trợ oxy, được mô tả là viêm phổi COVID-19, loại L, bởi Gattinoni và cộng sự [29], trong đó L là viết tắt của “thấp”:
- Độ đàn hồi thấp (tức là, độ giãn nở cao)
- Không phù hợp thông khí/tưới máu thấp
- Trọng lượng phổi thấp với mức độ ứ dịch viêm thấp, mối tương quan X quang của hình kính mờ, và không có hoặc ít đông đặc. Loại này, do đó, cũng có tiềm năng huy động thấp.
Trong khi, theo định nghĩa của Berlin, ARDS có mặt, từ quan điểm chức năng và X quang, giai đoạn này khác với ARDS về mặt tổn thương phế nang lan tỏa (DAD, diffuse alveolar damage). Trong DAD, đơn vị chức năng phế nang sẽ bị suy yếu, cùng với việc mất sự ổn định của phế nang và sự phát triển của phù phế nang và mô kẽ. Cho đến nay không có nghiên cứu có hệ thống nào về bệnh nhân COVID-19 đã chết trong giai đoạn này, trong đó kết quả giải phẫu bệnh lý sẽ tương quan với kết quả chẩn đoán hình ảnh. Tuy nhiên, từ quan điểm sinh lý bệnh học, viêm phổi COVID-19 loại L phải được phân biệt với ARDS. Chúng tôi tin rằng điều này có ý nghĩa quan trọng đối với chỉ định hỗ trợ hô hấp trong suy hô hấp cấp tính liên quan đến COVID-19.
Trong giai đoạn đầu của nhiễm trùng phổi, thiếu oxy là triệu chứng chính. Sự khác biệt chính đối với ARDS như chúng ta biết, trong đó giảm đáng kể độ giãn nở do tổn thương phổi, là độ đàn hồi của phổi được bảo tồn trong viêm phổi COVID-19 [29]. Dữ liệu được trình bày bởi Dreher và cộng sự [30] cũng cho thấy độ giãn nở trung bình khá tốt ở bệnh nhân thở máy, nhấn mạnh sự khác biệt so với ARDS bình thường. Về mặt chức năng, hiện tượng thiếu oxy đáng kể này với độ giãn nở duy trì ở phổi rất có thể được giải thích bằng một rối loạn phân phối thông khí-tưới máu rõ rệt. Trong giai đoạn đầu, nhiễm virus dẫn đến viêm cục bộ, viêm dưới màng phổi vừa phải, khu trú với sự tích tụ dịch mô kẽ (hình thái tương ứng với hình kính mờ nhìn thấy trên CT). Phần lớn hơn của phổi không bị ảnh hưởng, điều này giải thích độ co giãn phổi bình thường được bảo tồn [31]. Ở các khu vực bị ảnh hưởng, các mạch bị giãn tối đa [31-33] với sự mất hiện tượng co mạch do thiếu oxy (cơ chế Euler- Liljestrand) và do đó tăng thể tích shunt. Không rõ liệu đây là kết quả của tổn thương nội mô hoặc thư giãn cơ trơn mạch máu chủ động được điều chỉnh bởi các chất trung gian viêm. Phản ứng sinh lý đối với tình trạng thiếu oxy là tăng thông khí. Do độ giãn nở phổi được bảo tồn, tuy nhiên, bệnh nhân không cảm thấy điều này là khó thở. Điều này giải thích rằng không có/chỉ có các triệu chứng khó thở nhỏ được cảm nhận, mặc dù giảm CO2 máu rõ rệt <22 mm Hg và giảm oxy máu đáng kể đồng thời.
Ngoài việc ghi lại các thông số trao đổi khí và khí máu, thông số lâm sàng hàng đầu là nhịp thở đo được và sự thay đổi của nó theo thời gian, có thể được hiểu là thông số thay thế của nỗ lực hô hấp. Mặc dù rất mong muốn và hữu ích để xác định nỗ lực hô hấp cũng như thay đổi áp lực trong lồng ngực bằng phương pháp đo áp lực thực quản [29, 34], phương pháp này không thể được áp dụng trong môi trường lâm sàng, đặc biệt là vì công nghệ và kinh nghiệm cần thiết để đo thực quản áp lực thường không có sẵn trong các đơn vị chăm sóc đặc biệt (ICU). Tần số hô hấp tăng và thông khí tăng có thể dẫn đến tổn thương phổi nặng hơn do stress cơ học liên quan (lực cắt – shear forces và biên độ áp lực màng phổi cao). Hiện tượng này lần đầu tiên được mô tả bằng thực nghiệm bởi Barach và cộng sự [35, 36] và Mascheroni và cộng sự [37] và được gọi là bệnh nhân tự gây tổn thương phổi (P-SILI, patient self- inflicted lung injury) [38]. Việc cung cấp oxy trong giai đoạn này có thể, ở một mức độ nhất định, cung cấp cứu hộ cho thông khí. Do một shunt giả định, tuy nhiên, hiệu quả của việc cung cấp oxy ngày càng bị hạn chế.
Từ quan điểm sinh lý bệnh học, hỗ trợ cơ học bằng phương pháp thông khí không xâm lấn (NIV, non-invasive ventilation) hoặc áp lực đường thở dương liên tục (CPAP, continuous positive airway pressure) thông qua hệ thống mặt nạ hoặc mũ bảo hiểm (helmet) có thể hữu ích trong giai đoạn này để ngăn ngừa P-SILI có thể (xem tuyên bố 3). Tuy nhiên, điều này nên được xem xét thận trọng nếu hỗ trợ, cho phép tải trọng cơ học thấp nhất có thể lên phổi, cũng không làm giảm nhịp hô hấp xuống < 30 lần/phút. Trong tình huống này, với các mô dễ bị tổn thương trong nhu mô phổi, sự thiếu đồng bộ giữa bệnh nhân và máy thở hoặc biên độ áp lực quá mức sẽ góp phần gây ra tổn thương tiến triển. Liệu stress như vậy có thể được giảm bằng cách sử dụng morphin liều thấp cần phải được xác minh lâm sàng. Tuy nhiên, câu hỏi vẫn còn, và trong trường hợp thất bại trong liệu pháp oxy hoặc NIV (hoặc CPAP), trong từng trường hợp cụ thể, cần đánh giá xem có nên thực hiện đặt nội khí quản có kiểm soát và thông khí xâm lấn để giảm stress cơ học gây ra bởi nỗ lực thở tăng lên. Cuối cùng, do tổn thương phổi bổ sung được dự kiến từ thông khí xâm lấn, oxy hóa màng ngoài cơ thể (ECMO, extra-corporeal membrane oxygenation) cũng cần được xem xét; nó chắc chắn là bảo vệ phổi nhiều hơn, nhưng mang lại rủi ro bổ sung của riêng nó (xem tuyên bố 5).
1.4 Viêm phổi COVID-19, Loại H
Theo các nghiên cứu hiện tại, khoảng 15 – 20% bệnh nhân nhập viện bị tổn thương phổi nặng. Theo đó, mật độ rộng, tương tự như đã thấy trong các loại viêm phổi nặng khác và bệnh nhân mắc ARDS ngoài phổi, được nhìn thấy trên CT. Mô hình hình ảnh như vậy cũng có thể được gây ra bởi nhiễm trùng bệnh viện.
Nhóm làm việc của Gattinoni và cộng sự [29] mô tả trạng thái tiến triển, nguy kịch là viêm phổi COVID-19, loại H, có nghĩa là “cao”:
- Độ đàn hồi cao (tức là, độ giãn nở thấp) là kết quả của sự gia tăng phù nề
- Shunt trái phải cao
- Trọng lượng phổi cao và một phần lớn khối lượng phổi có thể huy động.
Tình trạng này phản ánh sinh lý bệnh của ARDS viêm phổi nặng với các dấu hiệu của DAD [39]. Những thay đổi rất giống nhau đã được nhìn thấy ở những bệnh nhân tử vong vì SARS [40] và MERS [41].
Mô hình của Gattinoni và cộng sự [29] đã được chứng minh là cung cấp một cơ sở tốt để hiểu rõ hơn về sinh lý bệnh của viêm phổi COVID-19. Tuy nhiên, nhiều câu hỏi vẫn chưa được trả lời. Từ quan điểm lâm sàng, bắt buộc phải có các thủ tục chẩn đoán toàn diện cho cả bệnh nhân thở tự nhiên và đặc biệt là cho bệnh nhân sau đặt nội khí quản.
Ngoài ra, việc đánh giá tình trạng bệnh tim mạch của bệnh nhân là rất quan trọng. Dữ liệu đầu tiên từ Trung Quốc cho thấy tỷ lệ bệnh nhân tim cao (20-30% bệnh nhân nhập viện) ở giai đoạn đầu của đại dịch. Những con số này đã được xác nhận trong các tập thể bệnh nhân châu Âu [6, 42]. Nồng độ troponin tăng cao được mô tả thường xuyên trong các nghiên cứu và liên quan đến tiên lượng xấu phải được coi là một chỉ số về tổn thương tim [21, 43]. Phân tích các bệnh nhân đã chết trong đoàn hệ Vũ Hán cho thấy tổn thương tim ở 34% và suy tim ở 40%, là nguyên nhân duy nhất hoặc kết hợp với suy hô hấp [21, 44-46]. Trong bối cảnh này, nguy cơ tử vong liên quan đến tổn thương tim cấp tính cao hơn ở người có tuổi, đái tháo đường, bệnh phổi tắc nghẽn mạn tính (COPD) và bệnh tim mạch từ trước. Một số yếu tố phải được thảo luận là nguyên nhân và, do sử dụng nhiều loại thuốc, tác dụng độc hại liên quan đến thuốc có thể được loại trừ; điều này thường được mô tả stress tim mạch tăng, đặc biệt là bắt đầu sớm với sự phát triển của thiếu oxy máu, phải được giả định.
1.5 Ý nghĩa của stress tim mạch
Giảm oxy máu với việc giảm nồng độ oxy đòi hỏi phải tăng cung lượng tim để duy trì sự vận chuyển oxy đầy đủ vì việc cung cấp oxy được tính bằng cách nhân cung lượng tim cho độ bão hòa oxy. Đồng thời, tim có thể bị căng thẳng thêm do hậu quả của tăng thông khí làm tăng hậu tải thất phải (RV, right ventricular). Nỗ lực hô hấp lớn hơn gây ra sự gia tăng áp lực trong lồng ngực âm tính, dẫn đến sự gia tăng áp lực xuyên thành thất trái (LV, left ventricular). Từ quan điểm sinh lý bệnh học, sự phát triển của thiếu oxy máu có thể gây ra tình trạng quá tải RV, nhưng hiện tại không có bằng chứng nào cho thấy đây là nguyên nhân sinh lý bệnh trong giai đoạn đầu của bệnh. Mức độ mà một sự tiến triển nặng đi cùng với việc tăng quá tải RV, như đã thấy trong ARDS nặng, vẫn cần phải điều tra thêm.
Như trong viêm phổi mắc phải tại cộng đồng (CAP, community-acquired pneumonia), phản ứng viêm toàn thân có thể thúc đẩy các biến chứng về tim như rối loạn nhịp tim, suy tim và biến cố mạch vành. Tuy nhiên, tỷ lệ biểu hiện của tim cao hơn so với CAP (khoảng 25%).
Một nguyên nhân khác của tổn thương tim có thể là viêm cơ tim. Tuy nhiên, cho đến nay, chỉ có một vài nghiên cứu trường hợp quan trọng có sẵn.
Ở mức độ nào, tăng D-dimers được xác định thường xuyên phản ánh hoạt động đông máu tăng lên vẫn chưa được thiết lập. Thật vậy, căn bệnh này dường như có liên quan đến việc tăng nguy cơ biến cố huyết khối và rối loạn hệ thống đông máu. Ví dụ, thuyên tắc phổi được phát hiện ở 25% trong số 81 bệnh nhân mắc COVID-19 bị bệnh nặng [47]. Tuy nhiên, vẫn chưa rõ liệu đây là những sự kiện huyết khối hay huyết khối tại chỗ.
| Tuyên bố chính 1.1 |
| Có thể phân biệt hai loại viêm phổi COVID-19, với các bệnh lý khác nhau (loại L và loại H) tương ứng với viêm phổi giai đoạn sớm và giai đoạn cuối.
Sự khác biệt này có thể được xem xét trong hỗ trợ hô hấp của ARF. |
| Tuyên bố chính 1.2 |
| Bệnh tim kèm theo, dù có từ trước hay liên quan đến COVID-19, đều có tác động đáng kể đến cả tiến triển và tiên lượng của bệnh, do đó, nên luôn luôn được xem xét trong mỗi giai đoạn điều trị. |
Phát hiện 1.1: Giai đoạn đầu không phải là điển hình của ARDS tại phổi (pneumogenic ARDS). Các giai đoạn muộn có thể tương ứng với ARDS tại phổi; nhiễm trùng bệnh viện và các biến chứng về tim và huyết khối phải được xem xét trong chẩn đoán phân biệt.
Tuyên bố 2: Trình tự thời gian và tiên lượng của ARF trong quá trình điều trị bệnh
W.J. Randerath và T. Bauer.
2.1 Giới thiệu
Bệnh phổi COVID-19, do virus SARS CoV-2 gây ra, là một bệnh viêm phổi đặc trưng bởi sự thiếu miễn dịch trong tình hình đại dịch. Các bệnh có thể so sánh là các bệnh nhiễm trùng do virut cúm tái tổ hợp và khả năng miễn dịch không có hoặc thấp trong dân số (ví dụ, cúm A/H1N1) [48]. Theo định nghĩa dịch tễ học, đây là đại dịch loại 3 với số lượng người nhiễm bệnh cao nhưng tỷ lệ tử vong tương đối thấp. Trên toàn thế giới, 6,1% bệnh nhân bị nhiễm xác nhận đã chết. Tuy nhiên, tỷ lệ tử vong có lẽ được đánh giá thấp hiện nay, vì ước tính số lượng các trường hợp không được ghi nhận là cao. Giả định này cũng được hỗ trợ bởi sự khác biệt lớn trong khu vực về tỷ lệ tử vong chung, từ 0,9% ở Hàn Quốc đến 7,2% ở Ý [49, 50].
Trong trường hợp không điều trị nguyên nhân, COVID-19 gây hại cho sinh vật thông qua 2 cơ chế, thứ nhất là tác dụng gây độc tế bào trực tiếp của sự xâm nhập, sao chép nội bào, trục xuất và làm chết tế bào chủ; và thứ hai, thông qua cơ thể, thất bại trong việc phát triển khả năng miễn dịch đủ để kiểm soát nhiễm trùng. Trong đại dịch loại 3, người ta cho rằng tác dụng gây độc tế bào trực tiếp chỉ ảnh hưởng đến tỷ lệ tử vong trong các trường hợp ngoại lệ do tỷ lệ tử vong trong giai đoạn đầu của nhiễm trùng sẽ phải cao hơn, và tuổi tác và bệnh đi kèm sẽ đóng vai trò phụ. Chu và cộng sự [22] đã nghiên cứu hồi cứu 191 bệnh nhân nhập viện với bệnh COVID-19 đã được xác nhận; 54 người trong số họ đã chết (28%). Các bệnh đi kèm thường gặp nhất là tăng huyết áp động mạch (30%), đái tháo đường (19%) và bệnh tim mạch vành (8%). Các phân tích đa biến cho thấy tỷ lệ tử vong tăng đáng kể với tuổi ngày càng tăng (tỷ lệ chênh lệch [OR] 1,10, KTC 95% 1,03-1,17, mỗi năm trong cuộc đời; p = 0 0043), điểm SOFA cao hơn (5,65, 2,61- 12,23; p <0,0001) và D-dimers > 1 g/mL (18,42, 2,64-128,55; p = 0,0033). Virus có thể được phát hiện cho đến lúc chết (tối đa 37 ngày) [22].
Theo trình tự thời gian của bệnh, khó thở xảy ra ở thời gian trung bình là 13 ngày (khoảng 9-16,5 ngày) và không khác biệt ở những người sống sót và không sống sót. Hệ thống phân loại 3 giai đoạn của bệnh, theo đề xuất của Siddiqi và Mehra [15], do đó dường như có ý nghĩa lâm sàng (Hình 1).
2.2 Giai đoạn I: Nhiễm trùng sớm
SARS-CoV-2 được giới thiệu thông qua ACE2, hiện diện với mật độ khác nhau trong niêm mạc của cổ họng, phổi và ruột non. Các triệu chứng lâm sàng bao gồm suy giảm vị giác, đau họng, ho và hiếm gặp hơn là tiêu chảy. Phết họng được lấy từ vòm họng để xét nghiệm PCR nhằm phát hiện virus. Tuy nhiên, dữ liệu gần đây cho thấy phết mũi có thể âm tính ở 27% và phết họng trong 68% trường hợp, mặc dù bệnh nhân mắc COVID-19 [51]. Do đó, Viện Robert Koch (RKI) khuyến nghị rằng, nếu COVID-19 tiếp tục bị nghi ngờ và các mẫu từ đường hô hấp trên cung cấp kết quả âm tính, các mẫu từ đường hô hấp sâu, cũng nên được phân tích. Từ quan điểm lâm sàng, sự khởi đầu của bệnh được xác định tốt nhất bằng sự khởi phát của sốt hoặc các triệu chứng giống như cúm [20]. Tất cả 3 dạng lâm sàng (nhẹ, nặng và nguy kịch) có thể phát triển từ giai đoạn I, tùy thuộc vào khả năng miễn dịch và độ hấp thụ.
2.3 Giai đoạn II: Liên quan đến phổi
Bằng chứng về virus trong cổ họng cao vào những ngày đầu tiên của bệnh, trong khi sự liên quan đến phổi chỉ bắt đầu bằng sự nhân lên của virus trong phổi, đánh dấu sự khởi phát của viêm phổi do virus [52, 53]. Các triệu chứng lâm sàng hiện nay cũng bao gồm khó thở và ho và tăng mật độ trong phổi thấy trên X-quang ngực hoặc CT ngực dưới dạng kính mờ [54]. Phân loại mức độ nặng khác nhau trong ấn phẩm này của giai đoạn II là giai đoạn IIa không bị thiếu oxy (PaO2/FiO2 ≥ 300 mm Hg, tương ứng với PaO2 động mạch hoặc mao mạch ≥ 63 mm Hg với không khí phòng) và pha IIb với giảm oxy máu (PaO2/FiO2 < 300 mm Hg, tương ứng với PaO2 động mạch hoặc mao mạch < 63 mm Hg với không khí phòng) dường như hợp lý đối với quyết định ban đầu liên quan đến hỗ trợ hô hấp và nơi chăm sóc bệnh nhân COVID-19 [15]. Đánh giá ban đầu về giảm oxy máu dưới oxy bổ sung bằng cách sử dụng các bảng chuyển đổi là không đáng tin cậy và chưa được xác nhận ở những bệnh nhân không điều trị.
Liên quan đến việc triển khai thực tế hỗ trợ hô hấp trong ARF, xem khuyến nghị 3 của bản thảo này cho giai đoạn IIa và khuyến nghị 4 và 5 cho giai đoạn IIb và các giai đoạn tiếp theo.
Bệnh nhân COVID-19 trong giai đoạn II chủ yếu được điều trị tại bệnh viện và hiện tại thuốc chắc chắn không thể ảnh hưởng đến sự tiến triển của bệnh. Do đó, việc điều trị đầy đủ bệnh đi kèm và theo dõi chức năng cơ quan là rất quan trọng. Hình 1 cung cấp một ví dụ về tiến triển lâm sàng. Các thông số sau nên được đo theo các khoảng đều đặn trong giai đoạn II để có thể phát hiện các chỉ số của các quá trình quan trọng càng sớm càng tốt (theo dõi trị liệu).
2.4 Theo dõi trị liệu
Điểm số SOFA là một yếu tố dự báo đáng kể về tỷ lệ tử vong trong phân tích đa biến (tuổi cao hơn, điểm SOFA cao hơn và D-dimer > 1 μg/mL khi nhập viện) [22]. Trong so sánh đơn biến, điểm số SOFA (không sống sót 4,5 [phạm vi 4-6] so với người sống sót 1.0 [phạm vi 1-2]) và điểm số qSOFA (không sống sót 1.0 [phạm vi 1-1] so với người sống sót 0 [phạm vi 0 – 2]) cung cấp một sự khác biệt có hiệu quả tương tự. Điểm số SOFA bao gồm đánh giá phổi (PaO2/FiO2), hệ thống thần kinh (Thang điểm hôn mê Glasgow, GCS), hệ thống tim mạch (liều catecholamine), chức năng gan (bilirubin), đông máu (huyết khối) và chức năng thận (creatinin). COVID-19 bên ngoài ICU thường không liên quan đến tình trạng nhiễm trùng, điều đó có nghĩa là theo dõi nhịp thở, mức độ suy giảm ý thức, huyết áp và SaO2 là đủ (qSOFA) [55].
Công thức máu được khuyến cáo khi nhập viện và trong suốt quá trình điều trị vì sức mạnh dự đoán của nồng độ tế bào lympho. Trong phân tích của Zhou và cộng sự [22], số lượng tế bào lympho < 800/μL phổ biến hơn ở những người không sống sót (76 so với 26%, p <0,0001). Nồng độ tế bào lympho thấp liên tục được mô tả thường xuyên hơn trong người không sống sót trong ấn phẩm của Wang và cộng sự [20].
Tổn thương cơ tim (chấn thương tim) được định nghĩa là nồng độ troponin tăng cao (troponin I độ nhạy cao [hs-TnI]> 28 ng/L, tương ứng với giới hạn trên của tỷ lệ phần trăm 99% của hệ thống phân tích được sử dụng) được quan sát ít thường xuyên hơn ở những người sống sót hơn ở những người không sống sót (15 so với 28%) [6]. Trong một phân tích đa biến của 416 bệnh nhân, tổn thương cơ tim và sự phát triển của ARDS là các yếu tố nguy cơ độc lập đối với người không sống sót (Kaplan-Meier, xét nghiệm log-rank test) [56, 57].
D-Dimers
Rối loạn đông máu là một yếu tố quan trọng để đánh giá mức độ nặng của bệnh ở những bệnh nhân bị nhiễm trùng nặng trong bối cảnh nhiễm trùng huyết [58]. Trong 3 nghiên cứu hồi cứu, tăng D-dimers, đặc biệt nếu chúng vẫn tăng trong suốt quá trình bệnh, có liên quan đến xác suất tử vong cao hơn [20, 22, 59]. Yin và cộng sự. [60] so sánh thời gian thromboplastin một phần (PTT), số lượng tiểu cầu và D-dimers ở bệnh nhân COVID-19 với những bệnh nhân bị viêm phổi nặng do các nguyên nhân khác. Họ không tìm thấy sự khác biệt về mức độ D-dimer (COVID-19: 1.94 μg/mL [phạm vi 0,90-9,44] so với không phải COVID-19 2,25 μg/mL [phạm vi 1.40–5.81]). Tuy nhiên, trong tất cả các trường hợp, các giá trị D-dimer tuyệt đối trong cả hai nhóm đều vượt quá giới hạn trên 0,5 μg/mL. Mặc dù số lượng tiểu cầu tăng nhẹ ở bệnh nhân COVID-19, nhưng nó vẫn trong phạm vi tham chiếu. Hiện tại, liệu các rối loạn đông máu quan sát được ở bệnh nhân COVID-19 có đặc hiệu với nhiễm SARS-CoV-2 hay không nên được giải thích trong bối cảnh nhiễm trùng huyết (bệnh nhân) hiện tại.
Các thông số trong phòng thí nghiệm bổ sung sau đây cũng có thể chỉ ra tiến triển bệnh nặng: men gan tăng cao, lactate dehydrogenase (LDH) và creatinine. Các thông số viêm cao như CRP, IL-6 và ferritin cũng là các chỉ số tiên lượng không thuận lợi [20].
2.5 Giai đoạn III: Viêm quá mức
Đáp ứng miễn dịch thể dịch không đủ, do đó không đủ bất hoạt và loại bỏ SARS-CoV-2 dẫn đến giai đoạn III bị viêm quá mức, với tỷ lệ suy cơ quan tăng và đặc biệt là khả năng tổn thương phổi ở dạng ARDS. Sự phát triển của ARDS phần lớn độc lập với mầm bệnh gây hại và có thể xảy ra trong viêm phổi cũng như tổn thương đơn hoặc đa cơ quan ngoài phổi. Từ quan điểm sinh lý bệnh học, tình trạng viêm quá mức trong COVID-19 do thiếu đáp ứng miễn dịch là rất quan trọng [61]. Dựa trên định nghĩa ARDS hiện tại của Berlin, sự khởi phát của rối loạn có thể trong vòng 1 tuần kể từ khi xuất hiện các yếu tố nguy cơ hoặc các triệu chứng hô hấp mới hoặc tăng và do đó có liên quan đến đặc điểm của viêm phổi COVID-19 [62]. Tuy nhiên, trong các khía cạnh về mặt khoa học, định nghĩa ARDS không thể chuyển hoàn toàn sang COVID-19 (xem tuyên bố 1). Nó cũng bao gồm 3 mức độ nặng chưa được phân biệt trong tất cả các ấn phẩm:
- Nhẹ: PaO2/FiO2 = 201-300 mm Hg với PEEP hoặc CPAP 5 cmH2O
- Vừa phải: PaO2/FiO2 = 101-200 mm Hg với PEEP ≥ 5 cmH2O
- Nặng: PaO2/FiO2 < 100 mm Hg với PEEP ≥ 5 cmH2O.
Trong bối cảnh viêm phổi COVID-19, định nghĩa Berlin không được áp dụng nhất quán trong các ấn phẩm được mô tả dưới đây, điều đó có nghĩa là việc so sánh các kết quả lâm sàng có thể được bảo lưu. Tuy nhiên, chúng tôi muốn trình bày những kết quả này cho mục đích định hướng.
Phân tích tạm thời dữ liệu của bệnh nhân COVID-19 trong ICU cho thấy rằng khởi phát khó thở trung bình ở nhóm bệnh nhân này là 6,5 ngày sau khi xuất hiện các triệu chứng đầu tiên. Tuy nhiên, ARDS từ trung bình đến nặng sau đó đã phát triển nhanh chóng, trong vòng trung bình 2,5 ngày sau khi bắt đầu khó thở [22, 63, 64]. Wang và cộng sự. [20] đã mô tả các đặc điểm và sự phát triển của 138 bệnh nhân COVID nhập viện. Tổng cộng 26% đã phải chuyển sang ICU do các biến chứng, 61% trong số đó là do ARDS. PaO2/FiO2 trung bình là 136 mm Hg (khoảng 103 -234 mm Hg), có nghĩa là hầu hết bệnh nhân có ARDS từ trung bình đến nặng. Các lý do khác là rối loạn nhịp tim (44%) và sốc (31%). Thời gian trung bình từ khi nhập viện đến ARDS vừa đến nặng trong nhóm này là 8 ngày. Bệnh nhân cần được chăm sóc đặc biệt đã nhận được hỗ trợ hô hấp sau đây cho ARF: điều trị lưu lượng cao qua mũi (NHF; 11%), NIV (42%) và thông khí xâm lấn (47%) [20].
Nghiên cứu của Wu và cộng sự [65], không chứa định nghĩa về ARDS hoặc mức độ nặng của nó, phải được xem xét nghiêm túc trong bối cảnh này. Thành phần của các liệu pháp hỗ trợ hô hấp trong đoàn hệ ARDS (n = 84) trong nghiên cứu này (NHF 20%, NIV 73% và thông khí xâm lấn ± ECMO 7%) cho thấy đây là những trường hợp chủ yếu nhẹ.
Một nhóm khác nhau đã được nghiên cứu bởi Yang và cộng sự [64], bao gồm 52 người trưởng thành bị bệnh nặng trong một đoàn hệ gồm 710 bệnh nhân bị viêm phổi do SARS-CoV-2. Sau 28 ngày, 32 bệnh nhân đã chết, trung bình 7 ngày sau khi được chuyển đến ICU. Ở những bệnh nhân nguy kịch, suy hô hấp do thiếu oxy rõ rệt và ARDS là những đặc điểm nổi trội, trong khi tăng CO2 máu chỉ xảy ra trong những trường hợp hiếm gặp. Thông khí cơ học (MV) được yêu cầu trong 42-100% [6, 20, 64].
Các yếu tố nguy cơ phát triển ARDS được mô tả cho đến nay bao gồm tuổi, bệnh đồng thời, sốt cao > 39°C, tiền sử hút thuốc và các thông số trong phòng thí nghiệm (giảm bạch cầu và nồng độ procalcitonin tăng) [63, 66].
Theo báo cáo ban đầu, thời gian chăm sóc tích cực được mô tả là kéo dài và cai máy bị trì hoãn. Thời gian phục hồi được báo cáo lên tới 6 tuần. Các biến chứng điển hình liên quan đến ARDS liên quan đến COVID-19 bao gồm suy thận cấp (29%), tăng men gan (29%) và tổn thương tim (23-33%) như bệnh cơ tim, viêm màng ngoài tim, rối loạn nhịp tim và tử vong do tim đột ngột. Tuy nhiên, những điều này thường chỉ xảy ra khi các triệu chứng phổi đã giảm [63, 64]. Suy đa cơ quan, sốc nhiễm trùng (13%) và viêm phổi thứ phát được mô tả ít thường xuyên hơn (12%).
| Tuyên bố chính 2.1 |
| Đánh giá mức độ ARF trong viêm phổi COVID-19 nên dựa trên phân tích khí máu động mạch hoặc mao mạch trên không khí phòng. Nó phải bao gồm việc tính toán lượng oxy cung cấp (được đo từ các thông số về độ bão hòa oxy, huyết sắc tố, giá trị hiệu chỉnh của yếu tố Hüfner và cung lượng tim). |
| Tuyên bố chính 2.2 |
| Đánh giá lâm sàng về sự tiến triển của bệnh nhân viêm phổi COVID-19 nên bao gồm theo dõi lâm sàng (ví dụ: qSOFA) cũng như theo dõi dựa trên thông số trong phòng thí nghiệm (ít nhất là D-dimers, CRP, PCT, tiểu cầu, LDH, troponin, ferritin và NT-proBNP) để phát hiện suy đa cơ quan, kết hợp với một thông số khác về suy hô hấp (ví dụ SaO2). |
Phát hiện 2.1. COVID-19 tiến triển theo 3 giai đoạn bệnh liên tiếp (nhiễm trùng sớm, bệnh phổi và viêm quá mức).
Tuyên bố 3: Thở oxy, NHF, NIV và thông khí xâm lấn với sự cân nhắc đặc biệt về sự hình thành của khí dung lây nhiễm
J. Geiseler và D. Dellweg.
3.1 Nguyên tắc vật lý của việc tạo khí dung và lây truyền phần tử hạt nhiễm trùng
Sars-CoV-2 có đường kính trong khoảng từ 60 đến 140nm [67]. Con đường lây truyền chính của virus là lây lan qua đường khí dung. Virus có thể được phát hiện trên bề mặt bằng PCR nhưng không thể nuôi cấy ở đó. Các virus được vận chuyển qua các hạt khí dung được tạo ra trong đường hô hấp của những người bị nhiễm bệnh [68]. Một khía cạnh quan trọng khác là sự lây nhiễm của virus giảm dần trong hạt khí dung. Khi số lượng RNA virus và chất lượng virus sống, và do đó liên quan khả năng lây nhiễm, như virus cúm A đã được kiểm tra đồng thời trong một thí nghiệm, số lượng virus sống và do đó khả năng lây nhiễm đã giảm xuống với hệ số là 102 sau 90 phút – mặc dù cùng một lượng RNA virus [69].
3.2 Tính chất vật lý của hạt khí dung
Các khía cạnh sau đây rất quan trọng đối với sự lan truyền của các hạt khí dung từ phổi của con người: sự hình thành, giải phóng và hành vi của khí dung trong một căn phòng cũng như sự lắng đọng hạt khí dung sau khi tái hít vào bởi một người khác.
3.2.1. Hình thành và giải phóng
Việc giải phóng các hạt khí dung đòi hỏi năng lượng, theo đó năng lượng của hơi thở nghỉ ngơi bình thường đã đủ [68, 70-72]. Ho hoặc hắt hơi làm tăng tốc độ thoát ra theo hệ số xấp xỉ 4 lần so với nhịp thở khi nghỉ ngơi [73]. Phạm vi tối đa của đám mây khí dung trước mặt một người không khác biệt đáng kể và là 0,6 m khi thở bình thường, 0,6 m khi hắt hơi và 0,8 m khi ho [73]. Tuy nhiên, nhìn vào số lượng hoặc khối lượng hạt là không đủ để đánh giá mức độ lây nhiễm. Nồng độ virus trong các hạt cũng có vấn đề. Nó có thể khác nhau gấp 32 lần ở bệnh nhân nhiễm virus cấp tính [74].
3.2.2. Hành vi của hạt khí dung trong phòng
Hạt khí dung là các hạt rắn hoặc lỏng lơ lửng trong khí (trong trường hợp này là không khí) có đường kính khoảng 0,001-100 μm. Đường kính khí động học (dae) là một tham số quan trọng cho các cơ chế phân tán thiết yếu của lắng đọng và va chạm. Nó được tính bằng tỷ lệ kích thước hạt (do) và mật độ hạt (p) (dae = do/p). Đường kính khí động học trung bình theo khối lượng (MMAD, mass median aerodynamic diameter) thường được sử dụng để phân loại các hạt khí dung. Tuy nhiên, khả năng của một hạt hạt khí dung để vận chuyển virus phụ thuộc vào khối lượng hạt. Điều quan trọng cần lưu ý là khối lượng phụ thuộc vào đường kính lũy thừa 3. Một hạt có đường kính 10 μm có cùng khối lượng với 1.000 hạt 1 μm [75].
Các hạt khí dung thở ra thay đổi kích thước hạt của chúng tùy thuộc vào độ ẩm tương đối của môi trường. Các hạt co lại ở độ ẩm thấp nhưng có thể tăng kích thước ở độ ẩm cao và do đó thay đổi tính chất vật lý của chúng [76].
Trong một không gian không bị giới hạn, lực hấp dẫn làm cho các hạt lắng đọng. Theo luật của Stoke, lực ma sát của không khí ngăn chặn sự lắng đọng dưới kích thước hạt 0,5-1 μm. Do đó, hạt khí dung có kích thước này duy trì ở mức gần như không đổi trong phòng và có thể hít vào. Khi các hạt khí dung có khối lượng lớn hơn rơi xuống nhanh hơn, nguy cơ gặp phải những thứ này sẽ lớn nhất gần nguồn tạo ra hạt khí dung (tức là, bệnh nhân) (Bảng 1). Nhìn chung, câu hỏi đặt ra là liệu các hạt hạt khí dung nhỏ hơn không chìm ngay lập tức cũng có trong không khí của phòng bệnh nhân ở nồng độ có thể gây nhiễm trùng hay không. Vì những dữ liệu này không có sẵn cho coronavirus, nên các tuyên bố sau chủ yếu dựa trên các thí nghiệm và đo lường với virus cúm. Blachere và cộng sự [77] đã có thể đo các mẫu không khí trong phòng và phát hiện ra rằng 46% các hạt virus đã được nhìn thấy trong các hạt khí dung > 4 μm. Tuy nhiên, 49% virus đã được tìm thấy trong các hạt có kích thước 1-4 μm và 4% trong các hạt < 1 μm. Fabian và cộng sự [72] thậm chí đã tìm thấy 99% DNA virus trong các hạt < 5 μm. Do đó, cả hai nghiên cứu đều phát hiện ra rằng 99% virus nằm trong phần khí dung hô hấp và có thể duy trì không khí trong vài giờ.
Trong các mẫu lấy từ không khí trong phòng tại các cơ sở chăm sóc sức khỏe cũng như trung tâm chăm sóc ban ngày và khoang máy bay trong mùa cúm, đã tìm thấy 5,8 × 103 đến 3,7 × 104 bản sao của virus trên một mét khối không khí trong phòng [78] Gấp 2 đến 20 lần số lượng hạt virus cần thiết để gây nhiễm trùng [79]. Điều này có nghĩa là, giả sử thông gió 10 L/phút, ngưỡng này sẽ đạt được sau 5 phút trong trường hợp xấu nhất và sau 50 phút trong trường hợp tốt nhất. Ngoài ra để được xem xét là sức sống (thời gian sống sót) của virus trong hạt khí dung. Dữ liệu thực nghiệm mới về coronavirus đã chỉ ra rằng Sars-CoV-2 trong hạt khí dung có chu kỳ bán rã 1,1 giờ [80]. Việc có thể tập trung virus ở trạng thái ổn định còn sống trong phòng bệnh nhân hay không tùy thuộc vào tải lượng virus của bệnh nhân (thấp hoặc siêu lây lan), thể tích phút hô hấp, và kích thước và độ thông thoáng của phòng. Nhìn chung, việc truyền vi-rút hạt khí dung dường như là hoàn toàn có thể. Các mô hình tính toán giả định, ví dụ, khoảng 50% tất cả các trường hợp cúm được truyền theo cách này [81].
| Bảng 1. Tỷ lệ lắng đọng/khuếch tán như là một hàm của đường kính hạt [75] | ||
| Particle diameter, μm | Sedimentation, μm/s | Diffusion, μm/s |
| 0.01 | 0.07 | 340 |
| 0.1 | 0.7 | 38 |
| 1 | 38 | 8 |
| 5 | 740 | 3 |
| 10 | 2.910 | 2 |
| 100 | 72.000 | 1 |
Bình phương đường kính hạt, mật độ hạt và độ nhớt của khí (trong trường hợp này là không khí trong phòng) cũng ảnh hưởng đến tốc độ lắng. Ngoài ra, các hạt < 1 μm phải chịu chuyển động và khuếch tán của Brown.
Các hạt do đó tồn tại trong không khí trong các khoảng thời gian khác nhau trước khi chúng lắng đọng. Mặc dù nguy cơ nhiễm trùng gia tăng vẫn chưa được chứng minh, cần đảm bảo thông gió phòng có hệ thống và nên đeo khẩu trang theo các khuyến nghị RKI hiện tại. Một số tác giả cho rằng việc phân loại tùy ý trong hạt khí dung và không phải hạt khí dung dựa trên kích thước tạo điều kiện cho việc xử lý thực tế [82], nhưng điều này không phản ánh đầy đủ vật lý hạt khí dung như vậy.
3.2.3. Lắng đọng hạt khí dung sau khi hít
Các hạt hạt khí dung có kích thước xấp xỉ 3-4 μm theo khí mang của nó. Ngoài ra, quán tính khối lượng làm cho các hạt cố gắng và di chuyển thẳng về phía trước khi hướng của luồng khí thay đổi. Khi một bề mặt bị va chạm, điều này được gọi là xung lực. Vùng thanh môn ở đường hô hấp trên là nơi lưu lượng hít vào thay đổi hướng lớn nhất. Do đó, các hạt nhỏ hơn có xác suất cao hơn được hít vào đường hô hấp dưới và đến các tế bào biểu mô phế nang, mặc dù các hạt có MMAD xấp xỉ 10 μm vẫn có xác suất lắng đọng ít nhất 50% trong phế quản [83].
3.3 Hạt khí dung trong trị liệu hỗ trợ hô hấp
Áp lực hoặc lưu lượng bên ngoài bổ sung được áp dụng cho hệ hô hấp bằng NHF, CPAP, NIV hoặc thông khí xâm lấn. Một nghiên cứu về thông khí xâm lấn đã có thể chỉ ra rằng số lượng các hạt thở ra tăng lên cùng với áp lực dương thì thở ra (EPAP) cao hơn (trong trường hợp này > 5 cm H2O) [84]. Vì các hạt khí dung có thể hít thở vào được sản xuất ở mức độ phế nang, nên có vẻ như việc huy động phế nang tăng lên có thể dẫn đến sự hình thành hạt khí dung tăng lên.
3.3.1. Thông khí không xâm lấn
Simonds và cộng sự [82] đã có thể chứng minh rằng, ở những bệnh nhân có triệu chứng cảm lạnh được thở bằng NIV, số lượng hạt > 3 μm tăng đáng kể ở 1 m từ đầu bệnh nhân. Ở khoảng cách gần (20 cm từ đầu bệnh nhân), mặt khác, chỉ có số lượng hạt > 10 μm tăng lên, mặc dù điều này đề cập đến những bệnh nhân có triệu chứng cảm lạnh thông thường hoặc tăng tiết. Không có sự gia tăng của các hạt có kích thước bất kỳ được tìm thấy ở những đối tượng khỏe mạnh. Ngược lại, khi sử dụng mặt nạ không có lỗ thông hơi (nonvented mask) với bộ lọc (filter), số lượng hạt phát ra giảm ở mức 20 cm và ở mức 1 m ở tất cả các đối tượng, mặc dù không đáng kể. Một mô hình mô phỏng sử dụng các hạt khói làm proxy cho các giọt cho thấy luồng không khí từ hệ thống thông hơi bao phủ khoảng cách tối đa lần lượt là 0,6 [85] và 0,85 m [86]. Đối với rò rỉ mặt nạ (mask leakage), phạm vi của dòng rò là < 10 cm [87]. Chúng tôi không tìm thấy dữ liệu nào về sự hình thành hạt khí dung trong NIV bằng hệ thống ống kép (dual-hose systems) trong quá trình tìm kiếm tài liệu của chúng tôi. Vì các hệ thống này hoạt động với mặt nạ không có lỗ thông hơi và các hạt khí dung truyền nhiễm có thể được loại bỏ khỏi không khí thở ra bằng cách lắp đặt bộ lọc vi rút, nên nguy cơ tạo ra các hạt khí dung có khả năng lây nhiễm thấp như khi sử dụng các hệ thống ống đơn (single-hose systems) với mặt nạ không có lỗ thông hơi.
Trong một phân tích hồi cứu của 9 bệnh nhân SARS, Fowler và cộng sự [88] đã tính toán rủi ro tương đối (RR) của lây truyền nhiễm trùng là 2,33 (95% CI 0,25-21,76; p = 0,5) cho nhân viên y tế đến bệnh nhân điều trị NIV. Tuy nhiên, rủi ro trong những trường hợp này không tăng đáng kể và nghiên cứu không cung cấp bất kỳ thông tin nào về các hệ thống mặt nạ được sử dụng. Một phân tích hồi cứu về việc truyền virut cho nhân viên bệnh viện trong dịch SARS năm 2003 cho thấy nguy cơ lây nhiễm cho các nhân viên liên quan đến việc áp dụng NIV [89]. Tuy nhiên, nghiên cứu đó cũng cho thấy rằng chỉ cần kỹ thuật đơn giản như ghi ECG cho bệnh nhân cũng có liên quan đến nguy cơ nhiễm trùng cao, bất kể tình trạng thông khí.
3.3.2. Thông khí xâm lấn
Thông khí xâm lấn trước tiên cần đặt nội khí quản. Trong dịch SARS ở Canada, Fowler và cộng sự [88] đã mô tả RR của lây nhiễm là 13,3 cho quy trình đặt nội khí quản. Thompson và cộng sự [90] đã nghiên cứu hàm lượng RNA virus của các hạt khí dung trong các quy trình khác nhau trong bối cảnh dịch cúm ở Anh. Họ đã tìm thấy mức độ phơi nhiễm cao hơn đáng kể với RNA virus từ các hạt có kích thước < 7,3 μm trong khi bệnh nhân được đặt nội khí quản. Phạm vi ô nhiễm hạt khí dung trong mô hình mô phỏng lên tới 2 m quanh đầu bệnh nhân [91]. Mặc thiết bị bảo vệ thích hợp là rất cần thiết. Ngoài ra, bài báo cuối cùng này đề xuất đặt một hộp trên đầu bệnh nhân để ngăn ngừa ô nhiễm khí dung, mặc dù điều này có nhược điểm là khả năng di chuyển của tay trong quá trình thao tác bị hạn chế. OR của sản xuất khí dung trong khi đặt nội khí quản là 2.3. Hút đàm qua nội khí quản của một bệnh nhân thở máy trong cùng một nghiên cứu đã cho kết quả OR là 4,11 đối với việc sản xuất các hạt khí dung chứa virus. Không có dữ liệu về lây truyền virus ở bệnh nhân thở máy xâm lấn ngoài các thủ tục đã được công bố cho đến nay. Nếu, ví dụ, một bóng chèn bị xì hoặc không đủ chặn có thể dẫn đến sự hình thành hạt khí dung không được biết đến. Hơn nữa, không phải tất cả các máy thở đều có bộ lọc virus ở nhánh thở ra. Không có dữ liệu về điều này có sẵn trong tài liệu xuất bản.
3.3.3. Trị liệu bằng ống thông mũi lưu lượng cao (Nasal High-Flow Therapy)
Dòng chảy xuyên qua mũi lên tới 80 L/phút được tạo ra trong NHF. Không khí làm sạch khoảng chết và tạo ra một áp lực đường thở dương. Bräunlich và cộng sự [92] đã có thể chứng minh rằng hiệu ứng thanh thải CO2 và áp lực dương cũng có thể được phát hiện trong các đường dẫn khí nhỏ. Luồng khí xuyên qua ngày càng tăng dẫn đến luồng không khí tăng từ mũi và miệng. Sự phân tán không khí thở ra, được đánh dấu bằng các hạt khói để dễ hình dung, tăng từ 6,5 đến 17,2 cm với sự gia tăng lưu lượng mũi từ 10 đến 60 L/phút [93]. Trong một nghiên cứu của Kotoda và cộng sự [94], không có hạt truyền nhiễm nào được phân tán qua NHF từ đường dẫn khí đầy nấm men của một manikin đào tạo y tế. Leung và cộng sự [95] điều tra sự bài tiết vi khuẩn ở 0,4 và 1,5 m từ đầu bệnh nhân ở bệnh nhân viêm phổi do vi khuẩn. Họ so sánh việc sử dụng NHF so với mặt nạ oxy đơn giản trong phòng với 6-12 trao đổi không khí mỗi giờ. Họ không tìm thấy sự khác biệt về mặt định lượng về sự phát tán mầm bệnh giữa hai loại điều trị, mặc dù có thể giả định rằng mặt nạ oxy làm giảm đáng kể lưu lượng thở ra. Một nghiên cứu gần đây từ Trung Quốc khuyến cáo nên đeo khẩu trang phẫu thuật cho bệnh nhân đang điều trị bằng NHF, nhưng không cung cấp bất kỳ dữ liệu nào về mức độ bảo vệ nhiễm trùng đạt được hoặc những hạn chế có thể có đối với hiệu quả của NHF [96].
3.3.4. Hệ thống máy phun khí dung
Simonds và cộng sự [82] đã mô tả sự tăng mạnh về thể tích khí dung ở gần bệnh nhân sau khi hít i bằng máy phun khí dung. Tuy nhiên, nghiên cứu được tiến hành tốt của họ có một lỗ hổng hệ thống về mặt này, vì các hạt khí dung từ máy phun khí dung thậm chí không đến được với bệnh nhân được đưa vào phép đo. Hai phân tích hồi cứu về rủi ro của các ứng dụng máy phun khí dung được thực hiện trong đại dịch SARS năm 2003 ở Canada [89, 97]. Không nghiên cứu nào có thể xác nhận tăng nguy cơ nhiễm trùng cho các nhân viên y tế thực hiện điều trị bằng máy phun khí dung. Tuy nhiên, cần nhấn mạnh rằng việc hít nước muối đẳng trương đơn giản làm giảm sự giải phóng hạt khí dung sinh học từ phổi trung bình 72% trong tối đa 6 giờ [98]. Lý do cho điều này dường như là sức căng bề mặt được sửa đổi của màng dịch bao phủ biểu mô đường hô hấp.
3.3.5. Liệu pháp oxy
Trong nghiên cứu được thực hiện bởi Simonds và cộng sự [82], quản lý oxy thông qua mặt nạ Venturi không dẫn đến sự hình thành khí dung tăng gần bệnh nhân. Nếu không khí thở ra của một manikin thở nhân tạo được đánh dấu bằng các hạt khói để hình dung, thì không khí thở ra có thể được hình dung lên đến 0,2, 0,22, 0,3 và 0,4 m từ mặt của manikin khi oxy được cung cấp ở 4, 6, 8 và 10 L/phút thông qua mặt nạ Venturi [86]. Trong cùng một thí nghiệm, việc áp dụng 1 hoặc 5 L O2 thông qua trị liệu oxy đã tạo ra một đám mây có thể thở ra là 0,66 m hoặc 1 m.
Thao tác liên quan đến liệu pháp oxy đã được chứng minh là một yếu tố nguy cơ lây truyền virus cho nhân viên y tế trong một nghiên cứu [97], nhưng trong một nghiên cứu khác thì không phải [89].
3.3.6. Tóm lược
Vật lý hạt khí dung cho thấy việc truyền các hạt truyền nhiễm, chứa virus thông qua hạt khí dung là một khả năng lý thuyết. Đặc biệt, nhân viên y tế lo ngại về sự gia tăng hoạt động tại giường bệnh nhân, đặc biệt là liên quan đến NIV, và do đó có thể tiếp xúc với các hạt khí dung có khả năng lây nhiễm.
Bằng chứng liên quan đến việc sử dụng liệu pháp oxy, NHF, CPAP và NIV bị hạn chế về khả năng so sánh do các phương pháp khác nhau được thực hiện để chứng minh khí dung, nhưng cũng do điều kiện phòng khác nhau (có/không có trao đổi không khí thường xuyên). Để đánh giá tình hình điều trị, chủ yếu so sánh việc sản xuất khí dung của hơi thở tự nhiên và bệnh nhân ho. Ở đây, một sự gia tăng nhỏ trong phạm vi hạt khí dung được quan sát là kết quả của các thao tác kỹ thuật. Tuy nhiên, nó ít hơn so với thông khí xâm lấn, đôi khi được khuyến cáo là đặt nội khí quản bảo vệ trực tiếp để bảo vệ nhân viên y tế chống lại các hạt khí dung truyền nhiễm. Dựa trên một so sánh với dữ liệu về đặt nội khí quản và hút đàm qua nội khí quản, các tác giả nhận thấy rằng kỹ thuật sau đi kèm với nguy cơ tiếp xúc với khí dung cao hơn đáng kể.
| Tuyên bố chính 3.1 |
| Các hệ thống mở hoặc hệ thống có lỗ thông hơi (được gọi là mặt nạ có lỗ thông hơi) có thể làm tăng sự giải phóng các hạt có thể hít vào. Rò rỉ mặt nạ đóng một vai trò khá phụ thuộc trong sự hình thành hạt khí dung. Các hệ thống kín (được gọi là mặt nạ có lỗ thông hơi) với bộ lọc khử virus ngược dòng trong hệ thống hô hấp là an toàn và không dẫn đến tăng sự hình thành hạt khí dung. Bằng cách tương tự, các hệ thống ống kép với bộ lọc khử vi rút trong ống thở cũng an toàn và không dẫn đến sự hình thành hạt khí dung tăng. |
| Tuyên bố chính 3.2 |
| Hệ thống hút kín phải được sử dụng để hút thông qua ống nội khí quản hoặc ống thông mở khí quản. Trong quá trình thông khí xâm lấn, điều quan trọng là phải đảm bảo rằng không khí thở ra được lọc phù hợp. Trong trường hợp không có bộ lọc thích hợp trong máy thở, nên sử dụng bộ lọc khử vi-rút ở nhánh thở ra. |
| Tuyên bố chính 3.3 |
| Dựa trên kiến thức hiện tại, liệu pháp khí dung, NHF, CPAP hoặc NIV có thể được thực hiện bởi nhân viên đeo PPE (kính bảo hộ, mặt nạ FFP2 hoặc FFP3 và áo choàng) mà không tăng nguy cơ nhiễm trùng. |
Phát hiện 3.1. Đặt nội khí quản có nguy cơ lây nhiễm cao. Các thủ tục trong đó hệ thống thông khí xâm lấn cần phải được mở có liên quan đến tăng nguy cơ nhiễm trùng.
Phát hiện 3.2. NHF mở rộng phạm vi khí dung thở ra thêm vài cm. Cho đến nay, một sự giải phóng gia tăng của các hạt khí dung truyền nhiễm so với bệnh nhân thở tự phát không thể được chứng minh trong môi trường in vitro hoặc in vivo.
Phát hiện 3.3. Mặc dù máy phun khí dung có vòi phun làm tăng lượng khí dung trong không khí trong phòng, nhưng chúng không làm tăng nguy cơ nhiễm trùng cho nhân viên y tế. Hít phải dung dịch muối đẳng trương làm giảm đáng kể sự phóng thích khí dung từ phổi.
Phát hiện 3.4. Oxygen thông qua mặt nạ hoặc ống mũi không dẫn đến tăng sự hình thành hạt khí dung. Các hệ thống oxy khác nhau (ống mũi, mặt nạ oxy và mặt nạ Venturi) có thể làm chệch hướng không khí trong quá trình thở ra theo nhiều cách khác nhau. Chỉ các ống mũi có lưu lượng oxy cao có phạm vi xa hơn so với những ống được sử dụng dưới nhịp thở tự nhiên.
Tuyên bố 4: NIV trong suy hô hấp cấp
M. Westhoff, W. Windisch và B. Schönhofer.
4.1 Giới thiệu
Trong bối cảnh đại dịch COVID-19, có khoảng 5-6% bệnh nhân bị thiếu oxy nặng cần điều trị chăm sóc tích cực, nhiều bệnh nhân phải thở máy xâm lấn hoặc NIV [9, 64]. Suy hô hấp do thiếu oxy gây ra do viêm phổi nặng hoặc tình trạng giống ARDS sau đó. Viêm phổi nặng được xác định bởi sự hiện diện của sốt hoặc nghi ngờ nhiễm trùng đường hô hấp và nhịp thở > 30 lần/phút, khó thở nặng hoặc SpO2 < 90% trong không khí phòng. Chẩn đoán ARDS dựa trên các hướng dẫn hoặc khuyến nghị có sẵn cho đến nay, với phân loại thích hợp thành ARDS nhẹ, trung bình và nặng dựa trên tỷ lệ PaO2/FiO2 [5, 62, 99- 104]. Phần sau đây giải thích các tùy chọn và giới hạn của NIV trong ARF. Bất kỳ sự leo thang trị liệu nào cũng đòi hỏi định nghĩa về mục tiêu trị liệu dựa trên ý kiến của bệnh nhân, điều này sẽ được thảo luận tại lần tiếp xúc giữa bác sĩ và bệnh nhân ban đầu và sau đó được xác minh hàng ngày [3, 105].
4.2 Sinh lý bệnh
Suy hô hấp nặng ở ARDS được cho là do không phù hợp thông khí/tưới máu hoặc shunt [106]. Dữ liệu gần đây về ARDS trong COVID-19 cho thấy những thay đổi sinh lý bệnh tiềm ẩn có thể rất đa dạng. Ví dụ, Gattinoni và cộng sự [29, 34], trong các nghiên cứu của họ về các bệnh nhân thở máy xâm lấn đã đáp ứng định nghĩa ARDS của Berlin, đã phát hiện ra rằng, trái ngược với ARDS điển hình, có thể thấy cái gọi là ARDS không điển hình. Điều này được đặc trưng bởi sự mất điều hòa tưới máu phổi và co mạch máu thiếu oxy với chức năng cơ học được duy trì của phổi. Hơn nữa, nó đã được tìm thấy ở một số bệnh nhân, việc cải thiện oxy trong PEEP không phải lúc nào cũng là kết quả của việc cải thiện khả năng phục hồi mô phổi [29, 34, 107]. Điều này dẫn đến các cài đặt khác nhau của áp lực thông khí, đặc biệt là PEEP và hiệu quả của tư thế nằm sấp [29, 34, 107]. Tuy nhiên, do các tuyên bố của các tác giả chỉ đề cập đến các bệnh nhân thở máy xâm lấn đã được điều trị bằng NIV và thông khí xâm lấn trong các khoảng thời gian khác nhau, nên khả năng chuyển sang điều trị NIV cho ARF trong COVID-19 hiện bị hạn chế.
4.3 Thuật toán chỉ định
Liệu pháp ban đầu của giảm oxy máu và suy hô hấp tập trung vào quản lý oxy thông qua ống mũi, mặt nạ Venturi và NHF. Khi quá trình trao đổi khí xấu đi dần dần và nhu cầu oxy tăng lên, cần xem xét lại chỉ định CPAP hoặc thông khí. Ngoài chỉ định, cả thời gian và loại thông khí thích hợp, có thể xâm lấn hoặc không xâm lấn, cần phải được xác định. Trong trường hợp một người không đặt nội khí quản (DNI, do not intubate), thì nên thiết lập cho dù ít nhất là NIV, như được mô tả trong hướng dẫn S3 [tiếng Đức] hiện tại của NIV cho ARF, mong muốn [5].
Nếu áp dụng chỉ định thông khí, trọng tâm trong ARDS truyền thống là tăng áp lực xuyên phổi và cải thiện hoặc bình thường hóa dung tích cặn chức năng để cải thiện rối loạn trao đổi khí. Một PEEP cao và liên tục được áp dụng có thể ngăn ngừa sự xẹp của phế nang và được sử dụng để đạt được việc huy động các vùng phế nang bị xẹp. Do rò rỉ mặt nạ hoặc không dung nạp, khiến cho việc duy trì PEEP lâu dài chỉ có thể ở một mức độ hạn chế, và do đó, gây ra sự tái phát nhanh chóng và suy giảm trao đổi khí liên tiếp, tính hữu ích của NIV bị hạn chế khi mức độ nặng của ARDS tăng lên [5, 99].
Sử dụng NIV trong ARDS vừa và nặng dẫn đến thất bại điều trị trong > 50% trường hợp. Điều này có liên quan đến tỷ lệ tử vong gần 50% trong ARDS nặng [5, 99]. Bên cạnh mức độ nặng của tình trạng lâm sàng hiện tại (Điểm SAPS > 37), mức độ của rối loạn oxy hóa là một yếu tố dự báo về thất bại NIV; tỷ lệ PaO2/FiO2 < 150 mm Hg được mô tả là giới hạn tới hạn để tăng tỷ lệ tử vong [108].
Thể tích khí lưu thông cao (> 9,2 hoặc 9,5 mL/kg) theo NIV có liên quan đến tỷ lệ tử vong tăng [108-11]. Điều này dẫn đến kết luận rằng NIV chỉ có tác động tích cực đến kết quả nếu nó có thể được sử dụng để cung cấp thông khí bảo vệ phổi với PEEP cao tương ứng trong ARDS bình thường [109]. Bệnh nhân thở tự nhiên bị ARF thiếu oxy biểu hiện tăng hoạt trung khu hô hấp cao với nhịp thở cao, và do đó có thể gây biến đổi áp lực xuyên phổi có thể gây tổn hại [34, 38]. Vì trung khu hô hấp của bệnh nhân được duy trì dưới NIV, nên việc hỗ trợ áp lực hít vào quá cao và (đặc biệt) trong bối cảnh NIV có thể đòi hỏi tăng thể tích và do đó có khả năng gây ra nguy cơ tổn hại đến phổi. Trong những tình huống như vậy, NIV không còn bảo vệ phổi nữa, vì thể tích khí lưu thông được coi là bảo vệ phổi không thể được áp dụng [112]. Kết nối này cũng được gạch chân bởi Gattinoni và cộng sự [34] trong nghiên cứu về ARDS không điển hình trong COVID-19. Với sự tham khảo nghiên cứu của Brochard và cộng sự [38], họ khuyên nên đặt nội khí quản để tránh áp lực âm quá mức và P-SILI ở những bệnh nhân có dấu hiệu lâm sàng về nỗ lực hô hấp quá mức theo CPAP hoặc NIV.
Một nỗ lực trị liệu với các thủ tục không xâm lấn dưới dạng NIV hoặc, chủ yếu là CPAP với sự leo thang đến NIV, có thể được thực hiện trong các trường hợp suy hô hấp thiếu oxy và đáp ứng không đủ với thở oxy hoặc ARDS nhẹ, đặc biệt trong các trường hợp suy hô hấp chủ yếu là tăng CO2 máu (ví dụ, bệnh đi kèm tim, COPD, giảm thông khí do béo phì và bệnh thần kinh cơ) [5, 99]. Các khuyến nghị hiện tại ở Ý, ví dụ, chủ yếu kêu gọi áp lực CPAP cao, leo thang NIV chỉ sau đó [113]. Mặt khác, chỉ có 11% bệnh nhân ICU ở Lombardy được điều trị bằng NIV [49]. Bệnh nhân được đặt nội khí quản ở mức trung bình PaO2/FiO2 là 160 mm Hg, với các yêu cầu PEEP cao tiếp theo. Một khuyến nghị tương tự về CPAP/NIV được cung cấp trong các khuyến nghị NHS ở Anh [114], nhưng với lời khuyên quan trọng là ngưỡng đặt nội khí quản phải thấp, và trong trường hợp suy giảm lâm sàng (yêu cầu tăng dần, đều đặn hoặc SaO2 giảm nhanh, và/hoặc tăng tần số thở và nỗ lực hít vào; xem tuyên bố 5), nên đặt nội khí quản ngay lập tức và thở máy (MV). Trong nghiên cứu hiện tại của họ về việc điều trị các bệnh nhiễm trùng đường hô hấp nặng do cộng đồng mắc phải, Arabi và cộng sự [115] kết luận tương tự như bằng chứng trước đây rằng NIV có thể được sử dụng ở những bệnh nhân được chọn trong giai đoạn đầu và trong các loại suy hô hấp thiếu oxy cấp tính nhẹ hơn. Đồng thời, họ chỉ ra rằng, ở những bệnh nhân không được cải thiện sớm, NIV chỉ trì hoãn đặt nội khí quản hơn là ngăn chặn nó. Một kết luận tương tự có thể được rút ra từ các ấn phẩm hiện có về thông khí trong COVID-19.
Sự phát triển từ khi xuất hiện các triệu chứng hô hấp đầu tiên sang ARDS và đặt nội khí quản sau đó, đặc biệt ở bệnh nhân COVID-19, có thể tiến triển nhanh chóng trong vài ngày, do đó cần đưa ra quyết định thở máy kịp thời [20, 113, 116]. Sự hiện diện của viêm phổi 2 bên và tiến triển xấu đi của CT ngực là những chỉ số tiên lượng không thuận lợi cho sự phát triển như vậy [44, 117].
Về nguyên tắc, cần có sự giám sát chặt chẽ để xác định các tiêu chí cho sự thất bại của NIV, với tùy chọn chuyển nhanh sang thông khí xâm lấn [5, 49, 110, 113, 118, 119]. Do đó, điều trị lý tưởng nên diễn ra trong một môi trường chăm sóc tích cực. Giám sát bao gồm độ bão hòa oxy, nồng độ khí trong máu và thể tích khí lưu thông, nhưng cũng đánh giá tình trạng lâm sàng của bệnh nhân. Cung cấp oxy xấu đi với PaO2/FiO2 <150 hoặc 175 mm Hg sau 1 giờ NIV, nhịp thở > 30 lần/phút, điểm APACHE cao và điểm số HACOR > 5 có liên quan đến tiên lượng xấu hơn đáng kể [120- 123]. Điều này dẫn đến thuật toán trị liệu được đề xuất trong Hình 2. Tuy nhiên, quyết định hoặc không thực hiện từng bước này phải dựa trên tình huống lâm sàng cụ thể, PaCO2, mức độ diễn tiến nhanh của suy hô hấp và kinh nghiệm của bác sĩ lâm sàng.
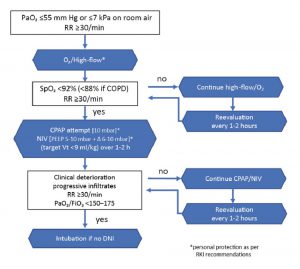
4.4 Lời khuyên thiết thực từ góc độ vệ sinh
Tùy thuộc vào áp lực thông khí áp dụng hoặc tăng lưu lượng, cả việc sử dụng NIV và NHF ngắt quãng đều dẫn đến sự hình thành hạt khí dung tăng lên [88, 93, 101, 124], có nguy cơ tiềm ẩn nguy cơ nhiễm virus trong nhiễm trùng COVID-19 (xem vị trí tuyên bố 3). Tuy nhiên, nỗi sợ bị nhiễm COVID-19 từ phía nhân viên y tế không phải là lý do chính để đặt nội khí quản. Do đó, việc bảo vệ nhân viên phải là ưu tiên hàng đầu. NIV thất bại nên được xác định sớm để đặt nội khí quản có thể được chuẩn bị và thực hiện đúng. Điều này ngăn ngừa đặt nội khí quản cấp cứu, được chứng minh là có liên quan đến kết cục bệnh nhân kém hơn và do thời gian đáp ứng kéo dài và các biện pháp bảo vệ không đầy đủ, có thể khiến nhóm cấp cứu gặp nguy hiểm do tăng nồng độ virus [2].
Vì những lý do trên, rò rỉ cần phải giảm đến mức tối thiểu khi sử dụng NIV. Do đó, mặt nạ mũi-miệng, mặt nạ toàn mặt hoặc mũ bảo hiểm hô hấp nên được sử dụng cho các trường hợp COVID-19. Ngoài ra, mặt nạ không có lỗ thông hơi phải được sử dụng. Các máy thở được sử dụng cho bệnh nhân COVID-19 tốt nhất nên là hệ thống ống kép. Khi sử dụng hệ thống ống đơn, nên chèn bộ lọc vi rút giữa giao diện và lỗ rò rỉ dự định (whisper swivel) hoặc van thở ra [104, 112].
Khi sử dụng thiết bị và cài đặt áp lực cho bệnh nhân, phù hợp với tình huống khẩn cấp, bệnh nhân đang thở CPAP hoặc NIV trước đó yêu cầu thay đổi mặt nạ và ống thích hợp, bao gồm cả việc gắn thêm bộ lọc virus [125].
Tóm tắt 4.5
Tóm lại, các bằng chứng hiện có [49, 13, 118, 126, 127] về cơ bản xác nhận các khuyến nghị và hướng dẫn [4, 5, 99, 101, 126] để điều trị ARF. Theo các hướng dẫn này, ARDS vừa và nặng vừa phải liên quan đến COVID-19 không tạo thành một chỉ định phù hợp cho CPAP hoặc NIV.
| Tuyên bố chính 4.1 |
| Liệu pháp oxy bao gồm NHF và NIV/CPAP sử dụng mặt nạ mũi-miệng hoặc mũ bảo hiểm là những lựa chọn điều trị leo thang khi điều trị oxy thông thường không đủ và miễn là không đáp ứng được các tiêu chí đặt nội khí quản. Vui lòng tham khảo hướng dẫn S3 hiện tại về việc sử dụng CPAP/NIV [5]. |
| Tuyên bố chính 4.2 |
| Sinh lý bệnh của suy hô hấp do thiếu oxy trong COVID-19 rất phức tạp và theo cách hiểu hiện tại, khác với các tình trạng khác kèm theo thiếu oxy. Trong bối cảnh đó, tình trạng thiếu oxy cấp tính, cũng như tăng khó thở nhanh chóng và suy giảm lâm sàng nhanh chóng theo CPAP/NIV, có thể xảy ra. Vì lý do này, việc theo dõi liên tục với sự sẵn sàng để tiến hành đặt nội khí quản phải được đảm bảo mọi lúc. |
| Tuyên bố chính 4.3 |
| Bảo vệ nhân viên bằng PPE nên được ưu tiên hàng đầu. Sợ lây nhiễm không phải là một lý do chính cho đặt nội khí quản. Vì lý do này, rò rỉ nên được giảm đến mức tối thiểu. Các hệ thống kín (được gọi là mặt nạ không được bảo vệ) với bộ lọc khử virus ngược dòng trong hệ thống hô hấp là an toàn và không dẫn đến tăng sự hình thành hạt khí dung.
Bằng cách tương tự, các hệ thống ống kép với bộ lọc khử vi rút trong ống thở cũng an toàn và không dẫn đến sự hình thành hạt khí dung tăng. Mặt nạ mũi miệng không có lỗ thông hơi, mặt nạ toàn mặt hoặc mũ bảo hiểm nên được sử dụng làm giao diện. Nên đặt bộ lọc khử vi-rút giữa giao diện và thiết bị thở ra (van rò rỉ hoặc van thở ra cho các hệ thống ống đơn). |
Tuyên bố 5: Sự liên tục của việc chăm sóc trong điều trị ARF
S. Kluge và P. Lepper.
5.1 Giới thiệu
Có tính đến các phát hiện được mô tả trong các tuyên bố trên, phần này dự định cung cấp các khuyến nghị điều trị dựa trên bằng chứng với sự xem xét thích đáng về các khía cạnh y học cá nhân hóa. Trái ngược với y học thảm họa, phương pháp y học cá nhân hóa có nghĩa là từng bệnh nhân có thể được điều trị như thể có quyền truy cập không hạn chế vào tài nguyên. Tuy nhiên, điều này không có nghĩa là các liệu pháp thử nghiệm có thể hoặc nên được sử dụng một cách bừa bãi chỉ vì tất cả các khía cạnh y tế của COVID-19 chưa được biết đến. Điều đó cũng không có nghĩa là các liệu pháp không được chỉ định cũng như không hợp lý về mặt sinh lý bệnh nên được thực hiện.
Việc sử dụng chăm sóc y tế chuyên sâu phải dựa trên các nguyên tắc thực hành lâm sàng tốt. Do không có phương pháp điều trị nguyên nhân nào cho đến nay, điều trị bổ trợ cho bệnh nhân COVID-19 cần tập trung vào việc duy trì hoặc khôi phục cân bằng nội môi.
5.2 Chỉ định nhập ICU
Bệnh nhân cần được chăm sóc đặc biệt hơn nên nhanh chóng được xác định trong phòng cấp cứu bệnh viện. Nhiễm trùng huyết cấp tính hoặc rối loạn chức năng cơ quan liên quan sẽ được đánh giá trong bối cảnh này. Đánh giá này, tương tự như đánh giá viêm phổi mắc phải tại cộng đồng, nhằm xác định cái gọi là tiêu chí phụ của Hiệp hội lồng ngực Hoa Kỳ và Hiệp hội bệnh truyền nhiễm Hoa Kỳ (ATS/IDSA) và bao gồm các bệnh kèm theo có khả năng không ổn định [3, 128]. Bệnh nhân cần điều trị bằng MV và/hoặc thuốc vận mạch (tiêu chí chính) phải luôn được điều trị trong ICU. Ở những bệnh nhân bị giảm tưới máu biểu hiện lâm sàng, nên đo lượng lactate ban đầu. Đánh giá lại thường xuyên, điều chỉnh theo mức độ nặng ban đầu của rối loạn chức năng cơ quan, nên được thực hiện cho đến khi đạt được sự ổn định lâm sàng.
Tiêu chí chính:
- Cần đặt nội khí quản và MV
- Cần thiết phải dùng thuốc vận mạch (sốc nhiễm trùng)
Nhiều điểm số đã được phát triển trong những năm gần đây và được đánh giá trong các nghiên cứu để dự đoán những bệnh nhân có nguy cơ cao cần được chăm sóc y tế chuyên sâu hoặc điều trị bằng MV, và/hoặc điều trị catecholamine, mà không cần phải bắt đầu điều trị thay thế cơ quan (tức là không có tiêu chí chính). Tất cả các điểm số đều có điểm chung là, các thông số lâm sàng, sinh hóa trong phòng thí nghiệm và X quang của rối loạn chức năng cơ quan cấp tính được xác định, khi kết hợp trong các cách xử trí khác nhau, tạo ra các dự đoán tương tự nhau. Trong các phân tích tổng hợp, các điểm số này được phát hiện là vượt trội so với chỉ số CRB-65 về mặt dự đoán rủi ro. Do đó, cái sau không được áp dụng cho COVID-19.
Tiêu chí phụ:
Nguy cơ cao cần được chăm sóc y tế chuyên sâu tồn tại nếu > 2 trong số 9 tiêu chí phụ được đáp ứng.
- Suy hô hấp cấp tính nặng (PaO2 ≤ 55 mm Hg hoặc ≤ 7 kPa trên không khí phòng)
- Nhịp thở ≥ 30 lần/phút.
- Tổn thương thâm nhiễm nhiều thùy trên phim X-quang ngực
- Rối loạn ý thức mới xảy ra
- Hạ huyết áp hệ thống cần điều trị bằng liệu pháp dịch truyền tích cực
- Suy thận cấp (nitơ urê ≥ 20 mg/dL)
- Giảm bạch cầu (giảm bạch cầu < 4.000 tế bào/mm3)
- Giảm tiểu cầu (giảm tiểu cầu < 100.000 tế bào/mm3)
- Hạ thân nhiệt (nhiệt độ cơ thể <36 ° C)
5.3 Diễn tiến của bệnh nhân COVID-19 trong môi trường chăm sóc đặc biệt
Một tỷ lệ đáng kể bệnh nhân bị suy hô hấp có tình trạng thiếu oxy liên quan, thường không thể điều chỉnh hoàn toàn, ngay cả với FiO2 cao, bao gồm NHF. Độ giãn nở phổi tương đối cao trong phần lớn các trường hợp (> 50 mL/cm H2O) [34]. Do thiếu oxy, những bệnh nhân này có tần số thở và thể tích hô hấp tăng đáng kể > 15 L/phút. Xác định chỉ số Horovitz thường cung cấp các giá trị thấp hơn đáng kể vào khoảng 120. Những thay đổi 2 bên trong hình ảnh X quang hoặc CT ngực thường không đủ để giải thích rối loạn oxy hóa nặng của những bệnh nhân này.
Khi sử dụng ống thông động mạch phổi, các phép đo cho thấy một số bệnh nhân ban đầu có áp lực động mạch phổi bình thường và sức cản mạch máu bình thường giảm kết hợp với cung lượng tim tăng bình thường/vừa phải (khoảng 6 -9 L/phút). Do đó, rối loạn oxy hóa có thể được giải thích bằng một shunt phải/trái có liên quan với sự suy yếu điều hòa mạch máu phổi (suy giảm hoặc không có “co thắt mạch máu phổi do thiếu oxy”) và rối loạn phân bố nặng (xem khuyến nghị 1). Những bệnh nhân này trước tiên nên được điều trị thiếu oxy máu, ví dụ, bằng NHF, oxy mũi hoặc NIV, có thể ổn định chúng.
5.3.1. Chỉ định của NIV
Với tham chiếu đến hướng dẫn S3 hiện tại của NIV cho ARF [5], cần lưu ý những điều sau đây.
NIV có thể cải thiện oxygen hóa trong hầu hết các bệnh nhân bị viêm phổi mắc phải cộng đồng nặng, nhưng tỷ lệ thất bại tương đối cao [20, 64]. Ngoài mức độ nặng của biểu hiện lâm sàng, mức độ của rối loạn oxygen hóa có thể là một yếu tố dự báo về sự thành công hay thất bại của NIV. Nói chung, một nỗ lực điều trị với NIV là hợp lý trong các trường hợp nặng của COVID-19, đặc biệt ở những bệnh nhân mắc COPD, với sự cân nhắc thích hợp của các chống chỉ định và tiêu chí chấm dứt. Về nguyên tắc, cần có sự giám sát chặt chẽ để xác định các tiêu chí của thất bại NIV, với khả năng chuyển nhanh sang thông khí xâm lấn [5]. Do đó, điều trị lý tưởng nên diễn ra trong một ICU. Các lý lẽ chính cho việc chọn ICU là nơi thực hiện NIV thay thế cho thông khí xâm lấn là: khả năng theo dõi liên tục bệnh nhân và bắt đầu các phương pháp điều trị cứu mạng có khả năng được chỉ định mà không trì hoãn. Liên quan đến trình độ của nhân viên y tế và điều dưỡng, NIV đặt ra yêu cầu cao đối với nhân viên như thông khí xâm lấn. Do đó, các điều kiện tiên quyết về cấu trúc phải được đáp ứng.
Trường hợp ngoại lệ là những bệnh nhân bị suy hô hấp, ví dụ, trong bối cảnh đợt cấp của COPD. Trong các trường hợp cụ thể, thông khí cũng có thể được thực hiện trong một ICU trung gian chuyên về thông khí. Ở những bệnh nhân mắc NIV từ trước, sự chuyển đổi giữa suy hô hấp mạn tính ổn định lâm sàng và mất bù thường xuyên bị mờ. Ở đây, NIV có thể, trong một số trường hợp, cũng được thực hiện trong phòng bệnh tổng quát, với điều kiện phải đáp ứng các điều kiện kỹ thuật và cấu trúc.
5.3.2. Đánh giá diễn tiến lâm sàng và quản lý tại ICU
Việc đánh giá bệnh nhân nên được định hướng xung quanh các thông số sinh lý (thời gian đổ đầy mao mạch, lactate máu, lượng nước tiểu và bình thường hóa nhịp thở) thay vì các thông số mục tiêu bằng số để ước tính cung cấp đủ oxy. Nếu bệnh nhân có truy cập tĩnh mạch trung tâm hoặc ống thông động mạch phổi, rất hữu ích để xác định độ bão hòa oxy tĩnh mạch trung tâm hoặc hỗn hợp.
Suy giảm độ bão hòa oxy với PaO2/FiO2 < 150 hoặc 175 mm Hg sau 1 giờ NIV, nhịp thở > 30 lần/phút, điểm APACHE cao và điểm số HACOR > 5 là chỉ định đặt nội khí quản ở bệnh nhân mục tiêu điều trị [120-123].
Ở những bệnh nhân đã được đặt nội khí quản và thở máy, tư thế nằm sấp và PEEP cao có liên quan đến tỷ lệ thành công khác nhau. Những bệnh nhân này nên được thở máy theo khuyến nghị theo khuyến nghị hướng dẫn S3 [4]. Do tỷ lệ rủi ro/lợi ích thuận lợi, nên cố gắng cải thiện tình trạng của bệnh nhân bằng các biện pháp đó. Mức độ PEEP cao ở những bệnh nhân này cũng có nguy cơ bị tâm phế cấp tính nếu có thể loại trừ tắc mạch phổi. Thao tác huy động thường không hứa hẹn khi độ giãn nở tốt. Nhu cầu an thần có thể cao trong giai đoạn này của bệnh. Quản lý thể tích nên được hạn chế trong khi tính đến việc bệnh nhân bị mất dịch cao không cân xứng do nhịp thở nhanh và sốt cao.
Trong quá trình bệnh, đôi khi có thể kéo dài trong nhiều tuần, độ giãn nở thường giảm và tình trạng phổi ngày càng giống với viêm phổi COVID-19 loại H [4, 34].
Ở những bệnh nhân COVID-19 bị suy hô hấp trong đó thông khí xâm lấn bằng các biện pháp được mô tả ở trên là không đủ để đảm bảo hấp thu oxy và loại bỏ CO2 đầy đủ, nên xem xét ECMO. Đây là điều kiện được chỉ định về mặt y tế và bệnh nhân đã đồng ý sử dụng. Liên quan đến việc quản lý thêm, vui lòng xem hướng dẫn S3 hiện tại về thông khí xâm lấn và sử dụng các thủ thuật hỗ trợ ngoài cơ thể trong ARF [4].
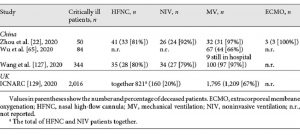
Thật khó để so sánh dữ liệu về kết quả của các loại hỗ trợ hô hấp khác nhau vì không có cài đặt và thông số chính xác nào được báo cáo. Bảng 2 cung cấp tổng quan về các đánh giá từ Trung Quốc và Vương quốc Anh. Cho dù các số liệu này cũng phản ánh tình hình ở Đức không thể được đánh giá ở giai đoạn này, vì các số liệu cụ thể chưa có sẵn. Tổng quan về hỗ trợ hô hấp trong suy hô hấp cấp tính cho thấy sự không đồng nhất của tình trạng trong các đợt nặng của bệnh (Bảng 2).
| Tuyên bố quan trọng 5.1 |
| Ở bệnh nhân COVID- 19, NIV trong ARF thiếu oxy nên được thực hiện trong ICU hoặc tương đương bởi đội ngũ nhân viên có kinh nghiệm đầy đủ. |
| Tuyên bố chính 5.2 |
| Vui lòng tham khảo hướng dẫn S3 áp dụng [4] để thực hiện thông khí xâm lấn. |
| Tuyên bố chính 5.3 |
| Trong bệnh nhân COVID-19 bị suy hô hấp trong đó thông khí xâm lấn sử dụng các biện pháp được mô tả ở trên là không đủ để đảm bảo hấp thu oxy và loại bỏ CO2 đầy đủ, nên xem xét ECMO. Điều này dựa trên điều kiện được chỉ định về mặt y tế và đã nhận được sự đồng ý của bệnh nhân. |
Phát hiện 5.1. Bệnh nhân COVID-19 mắc ARF đưa ra một bức tranh không đồng nhất, ngay cả trong khi điều trị ở ICU, và không thể phân loại bừa bãi thành một trong các loại theo định nghĩa ARDS của Berlin.





